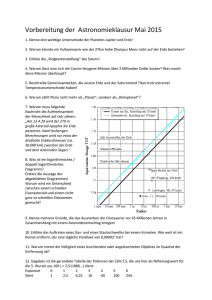
Unsichtbares wird sichtbar gemacht
Werbung

Unsichtbares wird sichtbar gemacht S. 7-10 1. Erkläre, wie man die minimale Durchbiegung eines Tisches sichtbar machen kann. 2. Erkläre die Funktionsweise eines Rasterkraftmikroskops anhand der Abbildung auf Seite 10. 3. Nenne Eigenschaften von Atomen. S. 11-13 4. Wie groß sind Atome ungefähr? 5. Was versteht man unter einem Mol? 6. Schreibe die Zahl 0,97*10-5 ohne Potenz und die Zahl 0,0000045 als Potenz möglichst kurz. 7. Was haben die Gase Wasserstoff, Stickstoff und Sauerstoff gemeinsam? 8. Nenne Beispiele, in denen Nanotechnologie eine Rolle spielt. 9. Beschreibe, wie man herausbekommen könnte, wie viele Salzkörner in einer 500 g Packung Salz enthalten sind. 10. Eine Leiterbahn in einem Computerchip ist 80 nm breit. Wie viele Atome liegen etwa nebeneinander? Aufbau des Atoms S.14-16 11. Erkläre, wie man heute den Aufbau von Atomen untersucht. 12. Beschreibe das Streuexperiment von Rutherford. Erkläre, wie er aus dem Versuchsergebnis den Aufbau eines Atoms ableitete. a. Wie ist der Versuch aufgebaut? b. Welche Teilchen werden geschossen? c. Warum werden die Teilchen abgelenkt? d. Warum werden nur wenige Teilchen abgelenkt und was kann man darauf schließen? 13. Zwei Luftballons, die an einem Faden hängen, werden mit einem Wolltuch gerieben. Was stellt man fest, wenn man die Luftballons einander nähert? Erkläre. 14. Erkläre, wie man ein Elektroskop aus Aluminiumstreifen herstellen kann und erkläre die Wirkungsweise. 15. Worin unterscheiden sich a) positiv, b) negativ geladene bzw. c) neutrale Gegenstände? 16. Wie verändert sich die Kraft zwischen ungleichnamig geladenen Gegenständen mit der Entfernung? 17. Erkläre, wie MILLIKAN in seinem Versuch herausfand, dass jede Ladung ein Vielfaches der Elementarladung ist, die ein Elektron trägt. (->S.16 mitte) 18. Welche Eigenschaften hat ein Elektron? (->S. 16 mitte). S.17-19 19. Beschreibe den Aufbau eines Atoms im Allgemeinen, und den Aufbau von Wasserstoff- bzw. Heliumatom (Atomkern, Protonen, Neutronen, Elektronen, Größenvergleich, Masse) 20. Beschreibe das Bohr’sche Atommodell (einige Stichworte: Kreisbahnen, Bahnwechsel eines Elektrons, Bahnwechsel erfolgt mit Energieauf- bzw. abgabe, Energiequantisierung) 21. Beschreibe das Orbitalmodell des Atoms (Stichworte: Aufenthaltswahrscheinlichkeit) 22. Erkläre anhand eines alltäglichen Beispiels, was man unter Aufenthaltswahrscheinlichkeit versteht. S. 20-21 23. Erkläre den Aufbau des Atomkerns von a) Wasserstoff bzw. von b) Helium. 24. Was bezeichnet die Ordnungszahl Z im Periodensystem der Elemente? 25. Woraus bestehen Protonen und Neutronen? 26. Bei welchem Zerfallsprozess entstehen die so genannten Neutrinos? 27. Der Atomkern von Eisen besteht aus 26 Protonen und 30 Neutronen. Wie lautet die Ordnungszahl? Berechne die Masse von einem Eisenatomkern (mProton=1,67 * 10-27 kg) S. 22-23 28. Erläutere die berühmte Formel von Albert Einstein: E = m c². Welche Größen sind beteiligt? 29. Wie lautet das Antiteilchen des Elektrons und welche Eigenschaften hat es? 30. Was geschieht, wenn Elektron und Positron aufeinander treffen? 31. Welche Quarks gibt es und welche Ladungen tragen sie? 32. Aus welchen Quarks sind Proton bzw. Neutron aufgebaut? 33. Welche Teilchen gehören zu den Leptonen? 34. Welche Teilchen nennt man Hadronen? S. 24-25 35. Es gibt vier verschiedene Kraftarten: a) die starke Kraft, b) die schwache Kraft, c) die elektromagnetische Kraft und d) die Gravitationskraft. Erkläre, zwischen welchen Teilchen bzw. Körpern diese Kräfte wie (abstoßend oder anziehend?) wirken und in welchen Entfernungen. 36. Zwei Luftballons werden mit einem Wolltuch aufgeladen. Sie stoßen sich daraufhin ab. Um welche Kraftart handelt es sich? 37. Ein Apfel fällt vom Baum. Welche Kraftart ist dafür verantwortlich? 38. Protonen bestehen aus Quarks. Protonen sind stabil, weil zwischen den Quarks Kräfte wirken. Zu welcher Kraftart gehören diese Kräfte und wie wirken sie?