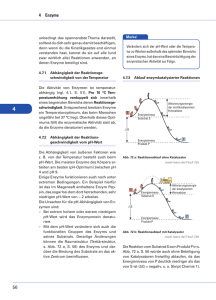
Das Aquarium im Chemieunterricht
Werbung

Philipps Universität Marburg Fachbereich Chemie Lehramt Wintersemester 2006/2007 Seminar: Übungen im Experimentalvortrag (AC) Chemie der Aquaristik Hinweis: Dieses Protokoll stammt von der Seite www.chids.de (Chemie in der Schule). Dort können unterschiedliche Materialien für den Schulunterricht heruntergeladen werden, unter anderem hunderte von Experimentalvorträgen so wie der vorliegende: http://www.chids.de/veranstaltungen/uebungen_experimentalvortrag.html Astrid Höhle Willinger Str. 9 34497 Korbach 1. Das Aquarium im Chemieunterricht ...................................................................................... 3 2. Grundlagen der Aquaristik ..................................................................................................... 3 3. Das Aquarienwasser ............................................................................................................... 5 4. Die Wassertemperatur .......................................................................................................... 30 5. Wasserpflanzen im Aquarium .............................................................................................. 31 6. Der Bodengrund des Aquariums .......................................................................................... 36 7. Schulrelevanz ....................................................................................................................... 37 8. Literatur- und Bildnachweise ............................................................................................... 38 2 1. Das Aquarium im Chemieunterricht Bislang fand das Thema Aquarium nahezu keinen Eingang in den Chemieunterricht. Im Biologieunterricht oder aber im Rahmen einer Arbeitsgemeinschaft zum Aufbau und zur Pflege eines Schulaquariums hat die Aquaristik allerdings schon an vielen Schulen einen Platz im Unterrichtsgeschehen gefunden. Aber auch im Chemieunterricht lässt sich die Thematik gut integrieren. So können an einem Aquarium viele chemische Zusammenhänge anschaulich und lebendig verdeutlicht werden. Hier wären die verschiedenen Stoffkreisläufe, wie z.B. der Kohlenstoffdioxidkreislauf oder aber der Stickstoffkreislauf, sowie viele andere grundlegende chemische Begriffe, wie der pH-Wert, Säure-Base-Reaktionen usw. zu nennen. Auch können die Schüler selbst erfahren, wie viel Chemie in der Umwelt zu erforschen ist. Hierbei werden komplexe Zusammenhänge auf den abgegrenzten, wenn auch immer noch sehr umfangreichen, Bereich des Aquariums eingeschränkt. Viele altbekannte Unterrichtsinhalte lassen sich in der Thematik des Aquariums motivieren, verknüpfen und von einer anderen Seite beleuchten, so z.B. die Wasseranalyse, der pH-Wert, Gleichgewichtsreaktionen oder aber auch Säure-Base-Reaktionen. Je nach Klasse und Unterrichtsziel kann ein Schwerpunkt auf Analytik sowohl im qualitativen als auch im quantitativen Zusammenhang gelegt werden. Natürlich bietet sich hierbei ebenso eine Fächerübergreifende Projektphase zum Thema Aquaristik an. Hierbei können besonders gut Verbindungen zwischen Chemie und Biologie hergestellt werden. 2. Grundlagen der Aquaristik Was ist eigentlich ein Aquarium? Als Aquarium bezeichnet man ein wassergefülltes Becken, in der Regel mit Glaswänden, in dem Wasserpflanzen und Wassertiere, insbesondere Fische, gehalten werden. (nach: Encarta) In der Praxis unterscheidet man meist, ob es sich um ein Süßwasser oder Salzwasser (bzw. Meereswasser) Aquarium handelt. Während Meereswasseraquarien zumeist nur als Warmwasseraquarien mit Wassertemperaturen über 20°C vorkommen, unterscheidet man bei Süßwasseraquarien zwischen Kaltwasser- und Warmwasseraquarien. Da die meisten Zierfische allerdings aus warmen Regionen der Erde stammen, handelt es sich bei den meisten Aquarien um Warmwasseraquarien. Es gibt aber auch Kaltwasseraquarien, in denen 3 zumeist Goldfische gehalten werden. Da die Thematik Aquaristik sehr umfangreich ist, möchte ich mich im Rahmen dieser Ausarbeitung auf Süßwasseraquarien beschränken und die Salzwasseraquarien ausklammern. Aquarium Süßwasser Kaltwasser Meerwasser Warmwasser Aufbau eines Aquariums Möchte man sich ein Aquarium anschaffen, so wird schnell klar, dass es hierfür einer gewissen Grundausstattung bedarf. Zunächst benötigt man neben einem Glasbecken und einem stabilen Unterschrank einige technische Geräte. So sollten ein Filter, eine Sauerstoffmembranpumpe, sowie ein Tauchheizstab und ein Thermometer nicht fehlen. Für das Pflanzenwachstum benötigt man eine entsprechende Beleuchtung, sowie Bodengrund (z.B. in Form von Kies oder Sand). Filter Glasbecken Thermometer Heizstab Bodengrund Abbildung 1 Neben der technischen Basisausstattung braucht man des Weiteren Pflanzen, Versteckmöglichkeiten für die Fische (wie Steine oder Wurzeln) und natürlich artgerechtes Aquarienwasser. Zwar gibt es auch reine Pflanzenaquarien, aber generell gehören natürlich Tiere (wie Fische, kleine Frösche, Schnecken, Garnelen oder aber auch Krebse) in das Aquarium. Pflanzen Wasser Steine, Wurzeln, Verstecke und natürlich Fische! Abbildung 2 4 Im Folgenden sollen nun die wichtigsten Faktoren eines artgerechten Aquariums unter chemischen Gesichtspunkten näher untersucht werden. Zunächst also zum wichtigsten Faktor, dem Aquarienwasser. 3. Das Aquarienwasser Das Aquarienwasser ist der wichtigste Faktor eines funktionierenden Aquariums. Die hier ablaufenden chemischen Prozesse sind komplex und stehen zueinander in Bezug. Die Qualität des Aquarienwassers ist entscheidend, da Fische im Vergleich zu jedem anderen Tier mit diesem in engstem Kontakt stehen. Das Wasser bildet ihren Lebensraum. Dadurch, dass Fische über Kiemen atmen, nehmen sie über diese eine Vielzahl an im Wasser gelösten Stoffen auf. Hierunter können auch Schadstoffe sein. Um eine unnötige Belastung der Tiere zu vermeiden, sollte das Aquarienwasser daher möglichst dem natürlichen Lebensraum der Fische (meist tropische Gewässer) nachempfunden sein. Damit dies gelingt, muss man sich zunächst im Klaren darüber sein, was die Wasserqualität in der Natur von der des Leitungswassers unterscheidet. Betrachtet man zunächst den natürlichen Lebensraum der Fische. Hier stehen die, die Wasserqualität prägenden Faktoren im natürlichen Gleichgewicht. Sowohl Tiere, als auch Pflanzen und Bakterien halten die wichtigen Stoffkreisläufe in Gang und sorgen so z.B. für einen natürlichen und zuverlässigen Abbau von gefährlichen Giftstoffen. Man kann sagen: "Das Wasser lebt". Nun im Kontrast dazu unser Leitungswasser. Dieses ist biologisch tot. Es sind keine Bakterien oder anderen Lebewesen enthalten, da es uns als sauberes, keimfreies und steriles Trinkwasser dient. Auch haben wir im Aquarium, anders als in der Natur, ein abgeschlossenes System. Dieses kann sich nicht völlig eigenständig regulieren. Daher bedarf es des Eingriffs des Menschen, der die Natur best möglich nachahmen sollte. Einer der wichtigsten Parameter für "fischgerechtes" Aquarienwasser ist der pH-Wert. Der pH-Wert im Aquarium Im tropischen Süßwasseraquarium sollte der pH-Wert möglichst an den des natürlichen Lebensraumes der Fische angelehnt sein. In den meisten tropischen Seen, Tümpeln oder Flussarmen herrscht ein leicht saurer pH-Wert im Bereich von 6-7. Der pH-Wert ist besonders wichtig für ein gut funktionierendes Aquarium, da er einerseits entscheidenden Einfluss auf 5 die Löslichkeit von Stoffen hat, sich aber auch entscheidend auf die Lage von vielen Gleichgewichtsprozessen auswirkt (z.B. NH3/NH4+ (aq)). Versuch 1: Zusammenhang Kohlenstoffdioxidgehalt und pH-Wert Chemikalien: • Calciumcarbonat • 10 M Salzsäure • gesättigte Calciumhydroxidlösung • Bromthymolblau • Phenolphthalein Geräte: Durchbohrter Gummistopfen 250 mL Becherglas 100 mL Weithalserlenmeyerkolben pH-Elektrode 20 mL Einwegspritze zweifach gewinkeltes Glasrohr Durchführung: 10 M Salzsäure pH-Elektrode Calciumhydroxidlsg. gesättigt + Indikatorlösung Calciumcarbonat 6 Zunächst wird eine gesättigte Calciumhydroxidlösung hergestellt. Von dieser füllt man ca. 150 mL in ein 250 mL Becherglas und gibt tropfenweise die Indikatoren hinzu, bis ein intensiv violetter Farbton erreicht wird. In den Weithalserlenmeyerkolben füllt man nun ca. 10 g festes Calciumhydroxid und baut anschließend die Apparatur wie oben gezeigt auf. Auf den Erlenmeyerkolben wird ein einfach durchbohrter Stopfen aufgesetzt, durch den man ein Glasrohr steckt, welches zweifachgewinkelt den Erlenmeyerkolben mit dem Becherglas verbindet. Hierbei ist darauf zu achten, dass das eine Ende des Glasrohres in die Calciumhydroxidlösung eintaucht, aber nicht auf dem Boden des Becherglases aufsteht. Anschließend zieht man mit einer Spritze 10 mL der zehn molaren Salzsäure auf und setzt diese auf eine Kanüle auf, welche zuvor durch den Gummistopfen gestochen wurde. Zum Schluss taucht man vorsichtig die pH-Messelektrode in das mit Calciumhydroxidlösung gefüllte Becherglas. Jetzt kann mit dem eigentlichen Versuch begonnen werden. Dazu gibt man mit Hilfe der Einwegspritze kleine Portionen Salzsäure auf das Calciumcarbonat und beobachtet die Calciumhydroxidlösung, sowie den pH-Wert mittels der pH-Elektrode. Beobachtung: Gibt man Salzsäure auf Calciumcarbonat so kann man schon bald eine heftige Gasentwicklung beobachten. Das entstehende Gas wird über das Glasrohr in die Calciumhydroxidlösung geleitet, dieses lässt sich ebenfalls in Form von Gasbläschen beobachten. In oben stehender Tabelle sind die wichtigsten Beobachtungen in Bezug auf Färbung der Lösung, Aussehen dieser und pH-Wert zusammengefasst. Man sieht, dass je mehr Salzsäure 7 zugegeben wird und je mehr Gas in die Calciumhydroxidlösung eingeleitet wird, desto stärker fällt der pH-Wert. Dementsprechend verändert sich auch die Farbe der Indikatoren und damit verknüpft die Farbe der Calciumhydroxidlösung, der diese zugesetzt wurden. Bei einem pHWert von ca. zehn kann man eine deutliche Trübung der Lösung feststellen, die aber bei einem pH-Wert von sieben wieder verschwindet, sodass eine klare Lösung verbleibt. Entsorgung: Die Lösungen werden neutralisiert und im anorganischen Schwermetallabfall entsorgt. Erklärung: Zunächst reagieren die im Calciumcarbonat vorliegenden Carbonationen mit den Protonen der Salzsäure. Hierdurch entwickelt sich Kohlenstoffdioxidgas und als Nebenprodukt entsteht Wasser. CO32(aq ) 2 H (aq ) CO2 ( g ) H 2 O(l ) Das so entstandene, in die Calciumhydroxidlösung eingeleitete Kohlendioxid reagiert mit dieser zu Calciumcarbonat, was in Form von weißem Niederschlag beobachtet werden kann, da Calciumcarbonat in Wasser nur schwer löslich ist. Dies erfolgt solange, bis ein pH-Wert von ca. zehn erreicht ist, da der pKs-Wert des Paares Hydrogencarbonat/Cabonat bei 10,4 liegt. Ca (OH ) 2 ( aq ) CO2 ( g ) CaCO3 ( s ) H 2 O(l ) Leitet man nun weiter Kohlendioxid in die Lösung ein, so wird das entstandene Calciumcarbonat weiter mit Wasser und Kohlendioxid zu Calciumhydrogencarbonat umgesetzt. Dies ist damit zu erklären, dass eine weitere Senkung des pH-Wertes erfolgt, was auch durch das Umschlagen der Indikatoren sichtbar wird. Dadurch wird das untenstehende Gleichgewicht zur Seite der Hydrogencarbonationen verschoben. Hierbei werden auch die Ionen an der Oberfläche des Niederschlags protoniert. Das vorliegende Calciumhydrogencarbonat ist jedoch in Wasser löslich, wodurch die Lösung wieder klar wird. Dies ist dadurch bedingt, dass das nur einfach geladene Hydrogencarbonation nur halb 8 so stark durch das Calciumkation angezogen wird, wie das zwei negativ geladene Carbonation. CaCO3 ( s ) CO2 ( g ) H 2 O(l ) Ca ( HCO3 ) 2 ( aq ) Wie in vorherigem Versuch exemplarisch demonstriert, besteht ein direkter Zusammenhang zwischen den drei Größen pH-Wert, Carbonathärte und Kohlenstoffdioxidgehalt: 2 H 2 O(l ) CO2 ( aq ) H 3 O(aq ) HCO3( aq ) Bereits in der Reaktionsgleichung wird deutliche, welche Auswirkungen Veränderungen der jeweiligen Konzentrationen haben. Explizit lässt sich dies aber auch mit dem Massenwirkungsgesetz begründen: c ( H O ) c ( HCO ) 3 3 K 2 c( H O ) c ( CO ) 2 2 Wobei ebenfalls direkt der Zusammenhang mit dem pH-Wert deutlich wird. pH lg c (H O ) 3 Durch diese Betrachtung ist leicht ersichtlich, dass der pH-Wert umso niedriger ist, je höher der Gehalt an Kohlenstoffdioxid und je niedriger die Konzentration an HydrogencarbonatIonen ist. Da das Leitungswasser normalerweise schwach basisch bis neutral ist, muss der pHWert meist nachträglich gesenkt werden. Dies kann entweder durch eine spezielle Kohlenstoffdioxid-Düngung oder aber durch Torffilterung erfolgen. Hierbei sorgt die Huminsäure des Torfs für die Absenkung des pH-Werts. Müssen höhere pH-Werte gesenkt werden, können auch anorganische Säuren wie z.B. Schwefel- und Salzsäure hinzugefügt werden. Die Wasserhärte Die Gesamtwasserhärte (kurz Gesamthärte) entspricht der Menge an im Wasser vorliegender Konzentration an Erdalkaliionen. Die Wasserhärte unterscheidet sich hierbei von Region zu Region oft deutlich, da sie von der Herkunft des Leitungswassers abhängt. Ist das aus der Leitung entnommene Trinkwasser z.B. durch ein Kalkgestein gesickert, so ist dieses sehr hart. Die Gewässer im tropischen Regenwald weisen allerdings zumeist eine sehr geringe 9 Wasserhärte auf. Das Wasser ist somit deutlich "weicher" als hier in Europa. Möchte man die Wasserhärte im Aquarium bestimmen, so kann man im Handel spezielle Testreagenzien erwerben, welche zumeist nach dem Prinzip der Komplexometrie funktionieren. Mit folgender Tabelle lassen sich die erhaltenen Werte grob klassifizieren: Wasser mit einem hohen Gehalt an Erdalkaliionen bezeichnet man im allgemeinen als sehr hart, während Wasser mit einer sehr geringen Erdalkaliionenkonzentration als sehr weich bezeichnet wird. Härtebereich Härtegrad in Härte in Charakterisierung °dH mmol/L 1 <7 <1,3 Weich 2 7-14 1,3-2,5 Mittelhart 3 14-21 2,5-3,8 Hart 4 >21 >3,8 Sehr hart Möchte man nun die Gesamthärte im Aquarium senken, so bieten sich hierzu zwei Möglichkeiten an, die beide das Wasser entsalzen: Die Umkehrosmose und der Einsatz von Ionenaustauschern. Bei der Umkehrosmose leitet man mit hohem Druck Leitungswasser an einer semipermeablen Membran vorbei. Durch diese können die Wassermoleküle hindurch diffundieren, während größere Teilchen diese nicht passieren können. Wozu dient nun aber der hohe Druck? Dies hängt damit zusammen, dass an der Membran osmotischer Druck aufgebaut wird. Der hohe Druck wirkt diesem entgegen und sorgt dafür, dass die Wassermoleküle, die die Membran einmal passiert haben, nicht wieder auf die andere Seite gelangen. Auch beim Einsatz eines Ionenaustausches werden die Kationen entfernt. Am Ionenaustauscher werden hierbei diese gegen Protonen ausgetauscht. Ionenaustauscher gibt es sowohl als anorganische, die zumeist aus Aluminiumsilikaten aufgebaut sind, aber auch als organische. Diese sind aus makromolekularen Gerüstbausteinen aufgebaut. Die Wirkung eines solchen natürlichen, organischen Ionenaustauschers lässt sich gut exemplarisch am Beispiel des Torfs zeigen. Demonstration 1: Torf als Ionenaustauscher Chemikalien: 40g Aquarienfiltertorf Leitungswasser 10 entionisiertes Wasser Kupfer(II)-sulfat-Pentahydrat 4 M Salzsäure Ammoniak-Lösung (w = 25%) Wasserhärtetest (Stäbchen oder aus dem Zoofachhandel) Geräte: 2 500 mL Bechergläser 3 500 mL Erlenmeyerkolben Glastrichter Faltenfilter Demoreagenzglas Magnetrührer mit Rührfisch pH-Papier Spatel Durchführung: Teil 1: Torf als Wasserenthärter Ein Becherglas wird zur Hälfte mit Leitungswasser gefüllt. Nun rührt man ca. 20 g Aquarienfiltertorf in das Wasser ein. Die so hergestellte Suspension lässt man etwa eine halbe Stunde stehen und filtriert dann ab. Anschließend misst man den pH-Wert und die Wasserhärte. Teil 2: Torf als Ionenaustauscher Zuerst muss der Filtertorf aktiviert werden. Dazu rührt man 20 g Filtertorf in einem Becherglas in ca. 200 mL vier molare Salzsäure ein. Dann wird das ganze zehn Minuten lang kräftig mit dem Magnetrührer gerührt. Anschließend wird die Salzsäure abfiltriert und der Torf solange mit Wasser gewaschen, bis der pH-Wert dem des zum Waschen verwendeten Wassers entspricht. Jetzt kann mit dem eigentlichen Ionenaustauschversuch begonnen werden. Hierzu gibt man den aktivierten Torf in ein weiteres Becherglas und schlämmt diesen mit einer wässrigen Kupfersulfatlösung (6,25 g Kupfersulfat in 300 mL entionisiertem Wasser gelöst) auf und gibt noch 200 mL entionisiertes Wasser hinzu. Nun rührt man mit Hilfe eines Magnetrührers etwa 11 eine viertel Stunde bis pH-Wert-Konstanz erreicht ist. Der so erreichte pH-Wert wird gemessen und mit dem von einer reinen wässrigen Kupfersulfatlösung verglichen. Schließlich filtriert man ab und wäscht den Torfrückstand mit Wasser bis mittels Ammoniak keine Kupferionen mehr im Waschwasser nachgewiesen werden können. Danach gibt man zum Rückstand ca. 60 mL Salzsäure und nimmt von der Lösung ca. 2 mL ab, welche man zu 5 mL Ammoniaklösung zum Nachweis von Kupferionen gibt. Beobachtung: Teil 1: Torf als Wasserenthärter Der pH-Wert sinkt von etwa 7 auf einen Wert von 4,5 ab. Außerdem ist eine deutliche Reduktion der Wasserhärte des Leitungswassers um ca. 40% zu beobachten. Teil 2: Der pH-Wert der Kupfersulfat-Lösung sinkt von 4,2 auf 2,5 nach Zugabe von Filtertorf und 15 minütigem Rühren. Die blaue Farbe der Kupfersulfatlösung schwächt sich außerdem merklich ab. Gibt man Kupferionen zu einer Ammoniaklösung so färbt sich diese blau. Entsorgung: Die Lösungen werden neutral im Schwermetallabfall entsorgt. Erklärung: Teil 1: Torf als Wasserenthärter Die Wasserhärte wird durch den Gehalt an Calcium- und Magnesiumionen im Wasser bestimmt. Im Torf sind Huminsäuren enthalten, welche die vorliegenden Erdalkalimetallionen komplexieren. Im Gegenzug werden hierfür Protonen ausgetauscht. Daher erniedrigt sich die Wasserhärte. Dementsprechend ist Moorwasser zumeist sehr weich, aber auch sauer. Teil 2: Torf als Ionenaustauscher Durch die in der Huminsäure enthaltenen Carboxylgruppen und phenolischen OH-Gruppen fungiert Huminsäure als schwach saurer Kationenaustauscher. In diesem Versuch wird gezeigt, wie Huminsäure bzw. Torf als Kationenaustauscher in der Lage, ist Kuperkationen 12 gegen Protonen auszutauschen. Dieser Prozess ist allerdings reversibel, sodass durch Zufügen einer starken mineralischen Säure die Kupferkationen wieder freigesetzt werden können. Beispiel für eine Strukturformel einer Huminsäure: Abbildung 3 Die Carbonathärte Die Carbonathärte entspricht der zu den Erdalkalimetallionen äquivalente Menge an Carbonat- oder Hydrogencarbonationen, welche im Wasser gelöst sind. Wie bereits angesprochen, liegt der pH-Wert im Aquarium meist in einem sehr schwach sauren bis neutralen Bereich. Daher liegen im Aquarienwasser zu einem deutlich größeren Anteil Hydrogencarbonationen vor. 2 H O CO H O HCO 2 ( l ) 2 3 ( aq ) 3 ( aq ) ( aq ) Auch hier wird noch einmal der direkte Zusammenhang zwischen pH-Wert, Carbonathärte und gelöstem Kohlenstoffdioxid deutlich. So führt eine Zugabe von Kohlenstoffdioxid z.B. 13 zwar zu einer Senkung des pH-Wertes, gleichzeitig wird aber auch die Carbonathärte erhöht. Gibt man jedoch Säuren hinzu, so werden pH-Wert und Carbonathärte gesenkt. Bei nicht eingestelltem Gleichgewicht und im Wasser im Überschuss enthaltenem Kohlenstoffdioxid kann es dazu kommen, dass zur Dekoration gedachte oder im Kies verwendete carbonathaltige Steine gelöst werden, was einen sprunghaften Anstieg der Gesamthärte des Aquarienwassers zur Folge hat. 2 CaCO CO H O Ca 2 HCO 3 2 ( l ) ( aq ) 3 ( aq ) 2 ( s ) ( aq ) Für den Laien kann der Zusammenhang zwischen Carbonathärte, pH-Wert und Kohlenstoffdioxidgehalt mit Hilfe von Tabellen leicht nachvollzogen und eingeschätzt werden. CO2-Gehalt (mg/L) in Abhängigkeit von Carbonathärte (°d) und pH-Wert Abbildung 4 Der Sauerstoff im Aquarium Da Fische über Kiemen unter Wasser atmen, ist es für sie besonders wichtig, dass immer ausreichend Sauerstoff in gelöster Form im Aquarienwasser vorliegt. Aber nicht nur für Fische ist eine möglichst hohe Konzentration an gelöstem Sauerstoff entscheidend. Diese ist auch maßgeblich für einen funktionierenden aeroben Schadstoffabbau und die Lage von Gleichgewichtsprozessen. Hier kann exemplarisch das Vorliegen von Eisen(II)- bzw. Eisen(III)-Ionen im Aquarienwasser genannt werden. 14 Sauerstoff kann über verschiedene Wege in das Aquarium gelangen. Ein großer Teil löst sich über die Wasseroberfläche im Wasser. In einem funktionierenden Aquarium sorgen aber auch eine ausreichende Anzahl an Wasserpflanzen, welche Fotosynthese betreiben, für die Umwandlung von Kohlenstoffdioxid in Sauerstoff. Da dies meist jedoch noch nicht ausreichend ist, verwendet man oft Sauerstoffmembranpumpen. Die Menge des gelösten Sauerstoffs ist daher im Allgemeinen abhängig von der Größe der Wasseroberfläche und deren Oberflächenbewegung (diese kann durch Pumpen oder Filter verstärkt werden), sowie Anzahl und Größe der im Aquarium vorhandenen Wasserpflanzen. Zwei nicht zu vernachlässigende Faktoren sind zudem Druck und vor allem Temperatur. +15°C Temperatur O2(aq) in mg/L in °C (p=1bar) 10 11,2 25 -25% 8,35 Hierbei wird deutlich, dass bei steigender Temperatur der Sauerstoffgehalt stark abnimmt. Eine leichte Temperaturerhöhung kann daher schon fatale Auswirkungen auf die Menge des im Wasser gelösten Sauerstoffs haben. Der maximale Gehalt an gelöstem Sauerstoff in einem Liter Wasser bei Standarddruck und einer für Aquarien üblichen Wassertemperatur von 25°C liegt bei 8,35 mg. Die große Bedeutung des gelösten Sauerstoffs wird bei der Klassifizierung von Gewässern deutlich: Diese werden je nach Sauerstoffgehalt in folgende fünf Güteklassen unterteilt: Güte- Grad der organischen O2-Gehalt in klasse Belastung mg/L I unbelastet >8 II mäßig belastet 6-8 ertragreiche Fischgewässer III kritisch belastet 4-6 Fischsterben möglich IV stark verschmutzt 2-4 periodisches Fischsterben Eignung als Fischgewässer Laichgewässer für Edelfische 15 V übermäßig verschmutzt <2 Fische nur örtlich, nicht auf Dauer Versuch 2: Sauerstoffgehalt im Aquarium Chemikalien: Mangan(II)chloridlösung (80 g gelöst in 100 mL H2O (bidest.)) Alkalische Iodid-Lösung Natriumthiosulfatlösung (c = 0,01 mol/L) Stärkelösung Schwefelsäure Geräte: Klarglasflaschen mit abgeschrägtem Stopfen (100 mL) Injektionsspritzen Vollpipette 50 mL Messpipette 10 mL Tropfpipette Peleusball Messkolben 100 mL Messkolben 1 L Bürette Stativmaterial Magnetrührer mit Rührfisch Durchführung: Eine Probe Aquarienwasser wird unter Luftausschluss direkt in eine Klarglasflasche, deren Volumen zuvor bestimmt wurde, abgefüllt. Unmittelbar nach dem das Wasser entnommen wurde, gibt man zu diesem langsam mit Hilfe einer Injektionsspritze, welche tief in die Wasserprobe eintaucht, jeweils 0,5 mL Manganchloridlösung und Fällungsreagenz. Anschließend verschließt man die Klarglasflasche mit einem abgeschrägten Stopfen und schüttelt gut durch. Nun wartet man etwa drei Stunden, sodass der erhaltene, braune 16 Niederschlag absitzen kann. Danach nimmt man mittels einer Pipette die Hälfte der klaren Lösung vorsichtig ab. Der zurückbleibende Niederschlag wird unter Zugabe von 2 mL Schwefelsäure gelöst. Anschließend wird in die Flasche ein Rührfisch gegeben und man lässt die Klarglasflasche für zehn Minuten im Dunkeln. Danach kann mit der Titration begonnen werden: Hierzu titriert man mit Natriumthiosulfatlösung bis sich die Lösung hellgelb verfärbt hat und fügt nun Stärkelösung als Indikator hinzu. Im Anschluss titrierte man weiter, bis die Lösung farblos ist. Beobachtung: Unmittelbar nach Zugabe des Fällungsreagenz zur entnommenen Wasserprobe kann man das Ausfallen eines hellbraunen Niederschlages beobachten. Diesen kann man in Phosphorsäure lösen. Hierbei erhält man eine tiefbraune Lösung. Titriert man diese Lösung nun mit Natriumthiosulfatlösung, so kommt es zum Farbumschlag von dem vorher beschriebenen intensiven braun Ton nach hellgelb. Fügt man jedoch Stärkelösung hinzu, so verfärbt sich die Lösung schmutzig blau. Diese Blaufärbung verschwindet allerdings bei Titration mit weiterer Natriumthiosulfatlösung wieder, die Lösung wird farblos. Entsorgung: Um wirklich alles Iod umzusetzen gibt man nach der Titration noch einige Tropfen Na2S2O3Lösung im Überschuss zu. Danach wird die Lösung neutralisiert und im anorganischen Schwermetallabfall entsorgt. Auch alle weiteren anfallenden Abfälle werden in den Schwermetallabfällen entsorgt. Erklärung: Fügt man zur Aquarienwasserprobe Manganchloridlösung und das Fällungsreagenz zu, so bildet sich zuerst ein weißer und anschließende ein brauner Niederschlag von Manganhydroxid. 17 2 Mn 2 OH Mn ( OH ) weiß ) ( aq ) ( aq ) 2 ( s ) ( 1 2 Mn ( OH ) O H O 2 Mn ( OH ) braun )oder 2 ( s ) 2 ( aq ) 2 3 ( s ) ( 2 1 2 Mn ( OH ) O H O 2 MnO ( OH ) ( braun ) 2 H O 2 ( s ) 2 ( aq ) 2 ( s ) 2 2 Gibt man nach dem Ausfällen zum erhaltenen Niederschlag Schwefelsäure hinzu, so löst sich dieser und es bilden sich in einer Redoxreaktion I3—Ionen. Diese sind für die tiefbrauner Farbe der erhaltenen Lösung verantwortlich. 4 1 2 0 Mn( SO4 ) 2 ( aq ) 2 K I ( aq ) Mn SO4 ( aq ) K 2 SO4 ( aq ) I 2 ( aq ) 1 2 1 / 3 2 3 ( aq ) ( aq ) ( aq )3 ( aq ) 2 tiefbraun 3 2 Mn ( OH ) 6 H O 3 I 2 Mn I 12 H O 3 ( s ) I I I 3 ( aq ) 2 ( aq ) ( aq ) Titriert man diese Lösung nun mit Natriumthiosulfatlösung, so reagiert das vorliegende Iod mit Thiosulfat-Ionen und es werden Iodid- und Tetrathionat-Ionen gebildet. Auch hierbei handelt es sich wiederum eine Redoxreaktion. 0 2 1 2 , 5 2 2 I 2 S O 2 I S O 2 ( aq ) 2 3 ( aq ) ( aq ) 4 6 ( aq ) Rechnung zur Bestimmung des Sauerstoffgehaltes: Aus dem Verbrauch an Natriumthiosulfatlösung lässt sich rechnerisch der Sauerstoffgehalt in der Aquarienwasserprobe wie folgt bestimmen: 1 mL Verbrauch an Natriumthiosulfatlösung entspricht in diesem Fall 0,08 mg Sauerstoff. Dementsprechend ergibt sich für die Sauerstoffmassenkonzentration in der Probe des Aquarienwassers: (O2 ) V ( Na 2 S 2 O3 ) 0,08 t 10 3 mg VFl . VRe . L 18 Der mikrobielle Stickstoffkreislauf im Aquarium Der mikrobielle Stickstoffkreislauf ist im Aquarium ein sehr wichtiger Kreisprozess, da er maßgeblich für den Abbau von Schadstoffen verantwortlich ist. Abbildung 5 Ammonifizierung Durch abgestorbene Pflanzen, tote Fische, Fischausscheidungen usw. liegt eine große Menge an organische Stickstoffverbindungen im Aquarienwasser vor. Diese werden von Bakterien und Pilzen mit Hilfe eines Enzyms, der Urease, hydrolysiert. Es bilden sich Ammoniak und Ammonium-Ionen. Dieser Prozess ist in der folgenden Reaktionsgleichung exemplarisch am Beispiel des Harnstoffs dargestellt. Urease CO ( NH ) 2 H O NH NH HCO 2 2 ( aq ) 2 ( l ) 4 ( aq ) 3 ( aq ) 3 ( aq ) Das Entstehen von Ammoniak bringt jedoch einige Probleme mit sich. Ammoniak ist sehr gut in Wasser löslich; es können sich bei 20°C bis zu 500 g Ammoniak in einem Liter Wasser lösen. Der in Wasser gelöste Ammoniak ist jedoch äußerst giftig für Fische. Die tödliche Dosis liegt bereits bei 0,05-3 mg. Wie in unterer Reaktionsgleichung jedoch ersichtlich, stehen Ammoniak und Ammonium-Ionen allerdings im Aquarienwasser im Gleichgewicht. NH 2 H O NH OH 500 g NH / L H O bei 20 C ) 3 ( g ) 2 ( l ) 4 ( aq ) ( aq ) ( 3 2 19 Der entsprechende pKB-Wert liegt bei ca. 4,8. Daraus wird ersichtlich, dass bei niedrigen pHWerten das Gleichgewicht der Reaktion nahezu vollständig auf der rechten Seite liegt und nur eine verschwindend geringe Menge an Ammoniak im Wasser vorliegt. Erhöht man jedoch den pH-Wert bis ins Basische, so steigt der Gehalt an Ammoniak rapide an. (s. auch Abbildung 6) Abbildung 6 Bei einem pH-Wert von ca. 9,25 stehen Ammoniak und Ammonium-Ionen schon im Verhältnis 1:1. Daher ist es wichtig im Aquarium auf einen niedrigen pH-Wert zu achten. Zudem sind Teilwasserwechsel, bei denen Ammonium-Ionen und Ammoniak teilweise entfernt werden, unverzichtbar. Zur Löslichkeit von Ammoniak in Wasser und zur Gleichgewichtsreaktion zwischen Ammoniak und Ammonium-Ionen: Versuch 3: Löslichkeit von Ammoniak im Aquarienwasser Chemikalien: konzentrierte Ammoniaklösung entionisertes Wasser (ca. 3 x 600 mL) Phenolphtalein 20 Thymolphthalein Methylrot Geräte: 3 Glasrohre ca. 30 cm Länge mit ausgezogener Spitze 3 undurchbohrte Stopfen 3 einfachdurchbohrte Gummistopfen 3 20 mL Einwegspritzen 3 1L Bechergläser 3 1L Rundkolben 3 Hebebühnen Abzug Wasserbad Stativmaterial Durchführung: 21 Eine große Plastikschüssel füllt man mit heißem Leitungswasser. Anschließend gibt man in einen der 1 L Rundkolben im Abzug ca. 50 mL Ammoniaklösung. Den Kolben verschließt man nun mit einem undurchbohrten Stopfen und schwenkt ihn einige Minuten im Wasserbad, sodass sich eine ausreichende Menge Ammoniakgas entwickeln kann. Dann entfernt man die noch vorhandene Ammoniak-Lösung aus dem Kolben und verschließt diesen erneut zur Aufbewahrung. Mit den anderen zwei Kolben verfährt man genauso. Nun füllt man die 1L Bechergläser jeweils mit ca. 600 mL entionisiertem Wasser und gibt einige Tropfen des entsprechenden Indikators hinzu. Im Anschluss wird die Apparatur wie oben gezeigt aufgebaut. Für die eigentliche Versuchsdurchführung tauscht man zügig die undurchbohrten Stopfen, gegen Stopfen aus, welche einfachdurchbohrt sind und in denen ein Glasrohr mit ausgezogener Spitze steckt. Ebenfalls ist der Stopfen mit einer Spritze durchbohrt, in welcher sich etwas entionisiertes Wasser befindet. Nach dem Austausch der Stopfen werden die Bechergläser mit Hilfe der Hebebühne erhöht, sodass die Glasstäbe tief in die Lösungen tauchen. Jetzt spritzt man mittels der Spritze einige Milliliter Flüssigkeit in den oberen Rundkolben. Beobachtung: 22 Unmittelbar nach Einspritzen einer kleinen Flüssigkeitsmenge beginnt sich die Flüssigkeit aus dem Becherglas durch das Glasrohr nach oben in den Kolben zu saugen. Dies hat den Anschein, als würde ein Springbrunnen entstehen. Die Flüssigkeiten aus den Bechergläsern verfärben sich, sobald sie in den oberen Rundkolben gelangen. Bei Phenolphthalein erfolgt ein Farbumschlag von farblos zu pink, bei Methylrot von rot zu gelb und bei Thymolphthalein von farblos zu blau. Entsorgung: Die Lösungen werden neutralisiert und im anorganischen Schwermetallabfall entsorgt. Erklärung: Bei diesem Versuch ist die Wasserlöslichkeit von Ammoniak zentral. Ammoniak weist eine gute Löslichkeit in Wasser auf. So lösen sich bei Zimmertemperatur in einem Volumenteil Wasser etwa 700 Volumenteile gasförmiges Ammoniak. Durch die Volumenabnahme entsteht beim Springbrunnenversuch ein Unterdruck, welcher das Wassers aus dem Becherglas in den oberen Kolben steigen lässt. NH 2 H O NH OH 500 g NH / L H O bei 20 C ) 3 ( g ) 2 ( l ) 4 ( aq ) ( aq ) ( 3 2 Wie obige Reaktionsgleichung zeigt bilden sich durch das Lösen von gasförmigem Ammoniak in Wasser Hydroxidionen. Der pH-Wert der Lösung im Rundkolben ist also stark basisch, was durch den Farbumschlag des Indikators angezeigt wird. Die Nitrifikation Als Nitrifikation bezeichnet man die aerobe (also unter Beteiligung von Sauerstoff) Umwandlung von Ammonium- zunächst zu Nitrit- und schließlich zu Nitrat-Ionen. Dies erfolgt unter Einwirken von nitrifizierenden Bakterien. Im ersten Schritt erfolgt die Nitritation von Ammonium-Ionen zu Nitrit-Ionen: Nitritatio n 2 NH 3 O 2 NO 2 H O 4 H 4 ( aq ) 2 ( g ) ( aq ) 2 ( l ) ( aq ) 2 23 Im zweiten Schritt werden die Nitrit-Ionen zu Nitrat-Ionen oxidiert, hierbei spricht man von Nitratation: Nitratatio n 2 NO 3 O 2 NO 2 ( aq ) 2 ( g ) 3 ( aq ) Die eben dargestellte Nitrifikation ist der wichtigste Vorgang zum Schadstoffabbau im Aquarium. Er erfolgt zumeist im Filter, oder aber im Aquarienboden, da hier die entsprechenden Bakterien großflächig siedeln. Das durch die Nitritation entstehende Nitrit ist für Fische ebenso wie Ammoniak äußerst schädlich. Aber auch Nitrat, als Endprodukt des Schadstoffabbaus, ist nicht unbedenklich. Zwar wird dieses von den Pflanzen als Nährstoff aufgenommen, doch sind diese im Aquarium zumeist nicht in der Lage, alles anfallende Nitrat umzusetzen, sodass dieses die Fische schädigen kann und für ein verstärktes Algenwachstum verantwortlich sein kein. Da man als Laie oft nicht ohne weiteres feststellen kann, wie hoch Nitrit- und Nitratwerte im Aquarienwasser sind, gibt es im Zoofachhandel Tests. Diese setzen sich zumeist aus Azofarbstoffen (ähnlich Lunges I und II) zusammen und sind halbquantitativ (s. Versuch 3). Versuch 3: Halbquantitative Bestimmung des Nitratgehalts Chemikalien: Aquarienwasser Test Set Nitrat der Fa. Tetra (Enthält drei Testreagenzien, ein Pulver, Testküvette und eine Vergleichsfarbkarte) Durchführung: In die skalierte Testküvette füllt man 5 mL Aquarienwasser. Zu diesem gibt man nun 14 Tropfen von Testreagenz 1 und schüttelt leicht. Danach tropft man 7 Tropfen Testreagenz 2 hinzu und schüttelt wiederum leicht. Anschließend fügt man mit dem mitgelieferten Spatel einen Spatel des Pulvers hinzu und verschließt danach die Küvette mit dem im Set enthaltenen passenden Deckel. Nun wird für ca. 20 Sekunden kräftig geschüttelt. Abschließend werden noch sieben Tropfen Testreagenz 3 zugefügt und die Probe wird ca. 24 zehn Minuten stehen gelassen. Anschließend kann mittels Vergleich mit der beigefügten Farbkarte der Nitratgehalt bestimmt werden. Beobachtung: Die Lösung verfärbt sich je nach Nitratkonzentration gelb(0-12,5 mg Nitrat), orange (12,5-25 mg Nitrat) oder aber rot (über 25 mg Nitrat). Entsorgung: Die Lösungen werden im Abfluss entsorgt. Erklärung: Der im Zoofachhandel erhältliche Nitrattest basiert, ähnlich wie der Nachweis mit Lunges I und II, auf den Prinzipien der Diazotierung und Azokupplung. Bei Testreagenz 1 handelt es sich um Essigsäure, bei Testreagenz 2 um ein primäres aromatisches Amin und bei Testreagenz 3 um die Kupplungskomponente, ein weiteres aromatisches System. Das Pulver ist feiner Zinkstaub. Im ersten Schritt werden bei diesem Test nach Zugabe von elementarem Zink und Säure die Nitrationen zu Nitritionen reduziert. Dabei bilden sich auch Wasser und Zink(II)kationen. 0 5 3 2 Zn( s ) N O3( aq ) 2 H (aq ) N O2( aq ) Zn(2aq ) H 2 O(l ) Die so entstandenen Nitrit-Ionen reagieren mit weiteren Protonen unter Wasserabspaltung zu Nitrosonium-Ionen, bei denen es sich um gute Elektrophile handelt. Nun erfolgt die Diazotierung. Hierbei greifen die Nitrosonium-Ionen (nach Zugabe von Testreagenz 2) das in der Lösung vorhandene primäre Amin an. Unter Abgabe und anschließender Wiederaufnahme eines Protons wird ein Wassermolekül vorgebildet, welches 25 abschließend abgespalten wird. Dadurch erhält man ein Diazoniumion. Dieses ist Mesomerie stabilisiert. Im abschließenden, farbgebenden Schritt erfolgt die Azokupplung des Diazoniumions mit dem in Testreagenz 3 enthaltenen aromatischen System. Hierbei wird zunächst ein sigmaKomplex gebildet. Für diesen sind verschiedene mesomere Grenzstrukturen formulierbar. Durch Abspaltung eines Protons bildet sich der Azofarbstoff aus. Insgesamt handelt es sich bei der Azokupplung um eine elektrophile Substitution. 26 Schwermetalle im Aquarienwasser Wechselt man das Aquarienwasser und ersetzt es teilweise durch Leitungswasser, so können Schwermetallionen zum Problem werden. Heutzutage sind die meisten Wasserleitungen der Häuser aus Kupfer, es gibt aber vereinzelt auch noch Bleileitungen. Steht das Wasser nun längere Zeit in den Leitungen, oder wird an diesen gearbeitet, können erhöhte Konzentrationen der Schwermetallionen in das Aquarium gelangen. Aber auch in verschiedenen Medikamenten gegen Fischkrankheiten sind Kupferionen enthalten. In sehr hohen Konzentrationen sind die auf diese Weise in das Aquarium gelangenden Kupferionen für Fische giftig. Ein größeres Problem stellt aber die Toxität von Kupferionen für Bakterien dar. Durch zu hohe Kupferionenkonzentrationen können nämlich die positiv auf die Wasserqualität einwirkenden Bakterien in Filter und Bodengrund absterben; der Schadstoffabbau würde stark beeinträchtigt und das Gleichgewicht des Aquariums empfindlich gestört. Auch die Kupferionenkonzentration kann mit Test-Sets aus dem Zoohandel ermittelt werden (s. auch Modell eines Teststreifens in Versuch 6). Stellt man dabei eine erhöhte Kupferionenkonzentration fest, so empfehlen sich ein Wasserwechsel mit geeignetem Wasser oder aber der Zusatz eines so genannten Wasseraufbereiters. Dieser enthält unter anderem den Komplexbildner EDTA, welcher dafür sorgt, dass die im Wasser enthaltenen Schwermetallionen komplexifiziert und somit unschädlich werden. Versuch 4: Kupfernachweis mit Indikatorstäbchen Chemikalien: 27 • 0,1 M Kaliumiodidlösung • Stärkelösung • Leitungswasserproben Geräte: Schere Filterpapier (mittel) weiße Plastikfolie Klebestift 2 100mL Erlenmeyerkolben Messpipette Glaskapillare Fön Durchführung: Herstellung der Indikatorteststäbchen: Zunächst werden aus einem Filterpapier mehrere Streifen (etwa 10 cm x 1 cm) zurecht geschnitten. Von der weißen Plastikfolie werden ebenfalls drei weiße Streifen entsprechender Größe (etwa 10 cm x 1 cm, 8 cm x 1 cm und 1 cm x 1cm) zugeschnitten und so mit dem Klebestift aufgeklebt, dass die Rückseite des Teststäbchens vollkommen abgedeckt ist und auf der Vorderseite ein ca. 1 cm x 1cm Streifen frei bleibt. Hier verbleibt eine kleine sichtbare Filterpapierlücke. Beim Verkleben der Streifen sollte man darauf achten, dass der Kleber nicht direkt auf das Filterpapier aufgetragen wird, sondern auf die Plastikfolie, da ansonsten die Filterpapierporen verkleben könnten. Die Kapillarwirkung des Filterpapiers würde somit gestört und der Nachweis unmöglich gemacht. 28 Präparieren des Teststäbchens für den Kupfernachweis: Zunächst wird die Stärkelösung hergestellt. Dazu stellt man eine gesättigte Lösung von Stärke und entionisiertem Wasser her, lässt diese aufkochen und schließlich abkühlen. Ebenfalls stellt man eine 0,1 molare Kaliumiodid her. Nun hält man die Glaskapillare in die Stärkelösung, wodurch die Lösung in dieser empor steigt. Anschließend setzt man die Spitze der Kapillare auf die freie Zone des Filterstäbchens auf und trägt Tropfen weise die Lösung auf. Hierbei sollte man darauf achten, dass keine Stärkelösung unter die Folie wandert, da sonst die Nachweisreaktion nicht im sichtbaren Bereich des Teststäbchens erfolgen würde. Nach gleichmäßigem Auftragen der Stärkelösung legt man den Teststreifen entweder zum Trocknen beiseite. Der Trockenvorgang kann aber auch durch den vorsichtigen Einsatz eines Föns beschleunigt werden. Nach dem Trocknen der Reaktionszone trägt man auf gleiche Weise mit Hilfe einer weiteren Glaskapillare die Kaliumiodidlösung auf und lässt wiederum trocknen. Den soeben beschriebenen Vorgang wiederholt man für die Stärkelösung und die Kaliumiodidlösung jeweils noch drei Mal. Auf diese Weise stellt man am besten gleich mehrere Teststreifen her. Nachweis von Kupferionen im Leitungswasser: In zwei Erlenmeyerkolben füllt man jeweils ca. 50 mL einer Leitungswasserprobe ab. In das eine Gefäß gibt man frisch aus der Leitung etwas Wasser. In den zweiten Kolben füllt man Leitungswasser welches potentiell Kupferionen enthält. Die besten Resultate lassen sich hierbei erzielen, verwendet man Wasser, welches längere Zeit in der Leitung gestanden hat, oder Wasser aus Leitungen, an denen Arbeiten vorgenommen wurden. In die beiden Erlenmeyerkolben hält man nun zugleich je ein Teststäbchen und lässt die Flüssigkeit zur Reaktionszone emporsteigen. Anschließend nimmt man die Teststeifen heraus und vergleicht die Reaktionszonen. 29 Beobachtung: Taucht man das Teststäbchen in die Flüssigkeit, so steigt dieses das Filterpapier empor. Bei der Probe mit dem Leitungswasser, welches länger in der Leitung gestanden hat, lässt sich im Bereich der Reaktionszone eine Blaufärbung beobachten. Bei der Probe mit frischem Leitungswasser bleibt eine Färbung der Reaktionszone aus. Entsorgung: Die Wasserproben werden in den Abguss gegeben. Die Teststäbchen können im Feststoffabfall entsorgt werden. Erklärung: Die im Wasser enthaltenen Kupferionen reagieren mit der auf die Teststreifen aufgetragenen Kaliumiodid Lösung, genauer gesagt mit den Iodidionen, zu Kupferiodid und Iod. Das so entstandene Iod reagiert mit den noch vorhandenen Iodidionen zu Polyiodidionen. Diese lagern sich in die Helix der Stärke (genauer der Amylose) ein und es entstehen Einschlussverbindung, welche man als Clathrate bezeichnet. Hierbei handelt es sich um einen Charge-Transfer-Komplex, der für die charakteristische blaue Farbe sorgt. 2 2 1 1 0 2 Cu ( aq ) 4 I (aq ) 2 Cu I I 2 ( aq ) I 2 ( aq ) I (aq ) I 3( aq ) 4. Die Wassertemperatur Wie bereits an einigen Stellen angesprochen, ist auch die Wassertemperatur im Aquarium entscheidend. Dies liegt zum einen daran, dass Fische nicht in der Lage sind, ihre Körpertemperatur selbst zu regulieren, aber auch zum anderen daran, dass die Wassertemperatur viele chemische Prozesse im Aquarium entscheidend beeinflusst. So führt eine Temperaturerhöhung um 10 K beispielsweise zu einer Verdoppelung bis Verdreifachung 30 der Reaktionsgeschwindigkeit. Somit ist die Temperatur entscheidend für die Lage chemischer Gleichgewichte und damit verbunden die Löslichkeit verschiedener Stoffe. Wie bereits weiter oben angesprochen, löst sich im wärmeren Wasser weniger Sauerstoff. Außerdem erhöht sich der Stoffwechsel der Fische bei höherer Temperatur und Wasserverunreinigungen und Sauerstoffverbrauch nehmen zu. Es empfiehlt sich daher, die Temperatur im Aquarium ständig mit einem geeigneten Thermometer zu kontrollieren. Da die meisten Fische aus ihren tropischen Herkunftsregionen Wassertemperaturen zwischen 20-28 °C bevorzugen, muss das Aquarium mit einem gut regulierbaren Tauchheizstab beheizt werden. 5. Wasserpflanzen im Aquarium Ein Aquarium ohne Wasserpflanzen ist nahezu undenkbar. Sie sind entscheidend für die Produktion von Sauerstoff im Aquarium mittels Photosynthese und tragen zur Reduktion der Schadstoffkonzentration mit bei. Außerdem bieten sie Versteck- und Brutmöglichkeiten für Fische. Nicht zu vernachlässigen ist auch der ästhetische Aspekt. Ein Aquarium mit gesunden Wasserpflanzen sieht schön aus. Dies geht sogar soweit, dass es reine Pflanzenaquarien gänzlich ohne, oder nur mit sehr wenigen kleinen, Fischarten gibt. Nährstoffe der Wasserpflanzen Genauso wie für ganz normale Pflanzen ist auch für Wasserpflanzen eine Versorgung mit den notwendigen Nährstoffen essentiell. Nur so bleiben sie gesund und wachsen. Im Folgenden soll nun ein kurzer Überblick darüber gegeben werden, welche Nährstoffe die Wasserpflanzen benötigen, wie diese in das Aquarium gelangen und in welcher Form sie aufgenommen werden. Zunächst sei als Element Kohlenstoff erwähnt, dieses wird von den Pflanzen als Kohlenstoffdioxid aufgenommen, welches durch Gasaustausch mit der Luft, die Atmung der Fische oder aber eine Kohlenstoffdioxiddüngeanlage in das Aquarium gelangt. Des Weiteren benötigen die Wasserpflanzen Stickstoff. Dieser findet sich im Aquarium in Ammonium- und Nitrat-Ionen wieder, welche als Abbauprodukte des Stickstoffkreislaufs übrig bleiben oder aber bei der Atmung der Fische entstehen. Außerdem brauchen die Pflanzen des Aquariums Kalium und Phosphor. Kalium wird von den Pflanzen in Form von Kalium-Ionen, Phosphor als Phosphat-Ionen aufgenommen. Beide Ionen gelangen beim Wasserwechsel, durch Fischfutter oder aber durch den Zusatz von Aquarienpflanzendünger in das Aquarium. Für die 31 Wasserpflanzen essentiell ist außerdem Eisen. Dieses kann jedoch nur in Form von Eisen(II)Ionen von den Wasserpflanzen aufgenommen werden. Diese kommen wiederum durch Wasserwechsel, Fischfutter oder Zugabe von speziellen Düngemitteln in das Aquarium. Notwendiges Element Aufgenommen als… Kommt in das Aquarium durch… Kohlenstoff Kohlenstoffdioxid Gasaustausch mit Luft, Atmung der Fische, CO2Düngung Stickstoff Kalium Ammonium-Ionen, Abbauprodukte, Atmung Nitrat-Ionen der Fische Kalium-Ionen Wasserwechsel, Fischfutter, Düngung Phosphor Phosphat-Ionen Wasserwechsel, Fischfutter Eisen Eisen-(II)-Ionen Wasserwechsel, Fischfutter, Dünger Zur Aufnahme von Eisen(II)-Ionen Versuch 5: Eisen(II)-Ionen im Aquarienwasser Chemikalien: • Eisen(II)-sulfat-heptahydrat • entionisiertes Wasser • verdünnte Natronlauge • verdünnte Salzsäure • Leitungswasser Geräte: 4 Demoreagenzgläser Demoreagenzglasständer 32 Tropfpipette pH-Elektrode Durchführung: Zunächst wird aus 2 g Eisen(II)-sulfat-heptahydrat und 200 mL entionisiertem Wasser eine Lösung hergestellt. Anschließend gibt man jeweils in ein Demoreagenzglas wässrige Lösungen mit den pH-Werten 5, 6.5, 7.5 und 9. Dazu verwendet man Leitungswasser und stellt den pH-Wert durch Zugabe von entsprechenden Mengen Natronlauge bzw. Salzsäure unter Kontrolle über eine pH-Elektrode ein. Anschließend gibt man zu allen vier Proben je zwei Tropfpipetten Eisen(II)-sulfatheptahydratlösung hinzu und beobachtet die Veränderung mehrere Minuten. Beobachtung: Die Eisen(II)-sulfat-heptahydratlösung weist einen gelb-braunen Farbton auf. Daher verfärben sich alle vier Proben etwas. Bei der Probe mit pH-Wert 5 ist jedoch auch nach mehreren Minuten keine Farbveränderung oder Trübung zu beobachten. Sie verbleibt schwach gelblich und klar. Auch bei der Probe mit pH-Wert 6,5 kann zunächst keine Veränderung beobachtet werden. Nach ca. zwei Minuten kann jedoch ein wenn auch geringes Ausflocken eines grüngelben Niederschlags festgestellt werden. Die Bildung eines Niederschlags erfolgt bei einem pH-Wert von 7,5 schon binnen einiger Sekunden. Bei einem pH-Wert von 9 bildet sich sofort nach Zugabe der Lösung ein voluminöser intensiv moosgrüner Niederschlag. Entsorgung: Die Wasserproben werden neutralisiert und im anorganischen Schwermetallabfall entsorgt. Erklärung: Die in das Wasser gelangenden Eisen(II)-Ionen, welche leicht löslich sind, werden bei entsprechendem pH-Wert unter Gegenwart von Sauerstoff unmittelbar zu Eisen(III)-Ionen 33 oxidiert. Diese bilden mit den in den Wasserproben vorhandenen Hydroxidionen einen schwerlöslichen Niederschlag von Eisen(III)-hydroxid. 2 2 3 4 Fe ( aq ) O2 ( g ) 8 OH (aq ) 2 H 2 O 4 Fe(OH ) 3( s ) Wie man der Reaktionsgleichung entnehmen kann, ist die Lage des Gleichgewichts stark abhängig vom pH-Wert und vom Sauerstoffgehalt des Wassers. Schon eine geringe Erhöhung des pH-Werts führt zu einer immensen Erhöhung der Reaktionsgeschwindigkeit, sodass die Oxidation ab einem pH-Wert von ca. 8 vollständig diffusionskontrolliert wird. Untenstehende Abbildungen zeigt die Stabilitätfelder von Eisenionen und Eisenverbindungen unter Standardbedingungen in Abhängigkeit des pH-Wertes (also der Wasserstoffionenkonzentration) und dem Redoxpotential. Sowohl aus der Abbildung als auch aus obiger Reaktionsgleichung kann man entnehmen, dass hohe Sauerstoffgehalte das Redoxpotential mehr zu positiven Werten hin verschieben. Es bilden sich daher bei hohen Sauerstoffkonzentrationen Eisen(III)-Ionen bzw. Eisen(III)oxidhydroxid. 34 Abbildung 7 Wie bereits erwähnt können Pflanzen nur Eisen(II)-Ionen aufnehmen. Das Vorliegen von entweder Eisen(II)- oder Eisen(III)-Ionen ist jedoch stark vom pH-Wert (wie im Versuch gezeigt) und vom Sauerstoffgehalt abhängig. Im Aquarium herrscht in den meisten Zonen ein aerobes Milieu. Hier ist also eine ausreichende Menge an Sauerstoff vorhanden, sodass die Eisen(II)-Ionen direkt zu einem Niederschlag von Eisen(III)-Ionen reagieren, welcher sich dann in Bodengrund und Filter festsetzt. Diesen Betrachtungen zu Folge wären also für die Aufnahme von Eisen(II)-Ionen durch die Pflanzen ein niedriger pH-Wert und ein anaerobes (also sauerstoffarmes) Milieu förderlich. Leider ist der pH-Wert jedoch überall im Aquarium nahezu konstant, jedoch der Sauerstoffgehalt ist unterschiedlich. Während in den meisten Zonen des Aquariums ein aerobes Milieu herrscht, bilden die unteren Schichten des Bodengrundes ein anaerobes Milieu. Hier kann eine Reduktion von Eisen(III)- zu Eisen(II)Ionen erfolgen. Um eine für die Pflanzen möglichst hohe Konzentration an Eisen(II)-Ionen zu erhalten, eignet sich aber auch der Einsatz von speziellen Aquarienpflanzendüngern. In diesen ist neben allen wichtigen Nährstoffen und Spurenelementen wiederum der Komplexbildner EDTA enthalten. Dieser komplexifiziert die Eisen(II)-Ionen in einem Chelatkomplex, sodass 35 diese ohne oxidiert zu werden, bis zu den Wurzeln der Wasserpflanzen transportiert werden können. 6. Der Bodengrund des Aquariums Der Bodengrund eines Aquariums erfüllt mehre Funktionen gleichzeitig. Er bietet Halt für die Wurzeln der Aquarienpflanzen und versorgt diese mit Nährstoffen. Außerdem findet sich im Bodengrund eine Menge an Futter für die Fische. Wie bereits angesprochen bildet er neben dem Aquarienfilter einen weiteren großen Lebensraum für Schadstoff abbauende Mikroorganismen. Spezielles Pflanzensubstrat (Nährstoffdepot) (anaerobe Schicht, sauerstoffarm) Aquarienkies oder Sand (5cm) (aerobe Schicht) Als Bodengrund eignen sich, je nach Fischbesatz, Kies (dieser sollte jedoch nicht scharfkantig sein) oder aber Sand. Oft kommt auch ein spezielles Pflanzsubstrat als unterste Bodenschicht zum Einsatz, welches im Zoohandel gekauft werden kann und alle wichtigen Nährstoffe enthält. Es dient als Nährstoffdepot und kann die Aquarienpfanzen über einen langen Zeitraum kontinuierlich versorgen. Die Schicht an Kies und Pflanzsubstrat sollte mindesten fünf Zentimeter betragen. Wie in der Abbildung schematisch dargestellt, bildet der obere Teil des Bodengrundes eine aerobe Schicht, der untere Bereich jedoch eine anaerobe. Die Wahl des Bodengrundes sollte sorgfältig bedacht werden, da sich nicht jeder Kies (z.B. aus der Kiesgrube) als Aquarienkies eignet. Dies liegt daran, dass viele Gesteine je nach Rahmenbedingungen im Aquarium, verwittern können und somit zahlreiche auch unerwünschte gelöste Stoffe ins Aquarium gelangen können. Folgende Tabelle fasst die wichtigsten Gesteinsarten zusammen und welche gelösten Substanzen durch sie in das Aquarium gelangen. 36 Gesteinsart gelöste Substanzen Kalkstein (CaCO3) Ca2+- und HCO3--Ionen Dolomit (CaMg(CO3)2) Mg2+-, Ca2+- und HCO3--Ionen Quarz (SiO2) Kieselsäuren (SiO2 · n H2O) Anhydrid (CaSO4) Ca2+- und SO42--Ionen Feldspat (NaAISi3O8) Na+-,HCO3--Ionen, Kieselsäuren (SiO2 · n H2O) Tonmineralien z.B. Kaolinit (AI2Si2O5(OH4)) Der wichtigste dieser Verwitterungsprozesse, der von Kalkstein, kann durch folgende Reaktionsgleichung dargestellt werden. 2 CaCO H O Ca HCO OH 3 ( l ) ( aq ) 3 ( aq ) ( s ) 2 ( aq ) Aus Unwissen oder Unachtsamkeit gelangt häufig Kalkstein in Form von Kies oder Dekorationssteinen in das Aquarium. Wie aus obiger Gleichung ersichtlich wird, führt dies unter anderem zu einem drastischen Anstieg der Carbonathärte im Aquarium. Besser als Bodengrund eignet sich der etwas kostspieligere Kies aus dem Aquarienhandel. Hierbei handelt es sich um Quarz-Kies, welcher bei Verwitterung nicht zu einer Aufhärtung des Aquarienwassers führt: SiO n H O SiO n H O 2 2 ( l ) 2 ( s ) 2 7. Schulrelevanz Das Thema Aquaristik ist nicht explizit im Lehrplan vorgesehen, jedoch lässt sich ein breites Spektrum an chemischen Zusammenhängen am Beispiel des Aquariums konkretisieren. Man kann z.B. einen Beitrag zur ökologischen Bildung und Umwelterziehung erbringen, in dem man das Thema Wasserverschmutzung behandelt. Betrachtet man etwa den Aquarienfilter so kann man exemplarisch im kleinen überschaubaren Maßstab hieran die Aufbereitung von Abwässern, Trink- und Flusswasser nachvollziehen. Sehr gut eignet sich ein Projekt zum Aquarium aber auch, um sinnvoll das im Lehrplan vorgeschriebene Thema Wasseruntersuchungen mit analytischen Schnelltestverfahren in den Unterricht zu integrieren. Hierbei kann man auf die im Zoofachhandel erhältlichen Schnelltestverfahren zurückgreifen. Ebenso lassen sich Themen aus der 10. Jahrgangsstufe mit dem Aquarium verbinden. Leicht lassen sich hierbei konkrete Motivationen für Probleme im Zusammenhang mit 37 Stoffmengenkonzentrationen finden. Auch können praktische Verfahren der Maßanalyse wie Titrationen von den Schülern mit Wasserproben eines Aquariums leicht nachvollzogen und selbst durchgeführt werden. In Klasse 10 sollen ebenfalls Stoffkreisläufe behandelt werden. Das Aquarium als noch relativ überschaubares System liefert wiederum zahlreiche konkrete Beispiele, wie den Stickstoffkreislauf oder aber den Kohlenstoffdioxidkreislauf. Selbst im Oberstufenunterricht in der Klasse 13 kann das Aquarium als Bezug zum Alltag dienen. Hier lassen sich zahlreiche konkrete Beispiele für das chemische Gleichgewicht und die Umkehrbarkeit verschiedener Reaktionen zeigen. In diesem Zusammenhang ist ebenso eine Thematisierung des Prinzips vom Zwang möglich. Auch das Massenwirkungsgesetz kann auf reale Problemstellungen angewendet werden. Als reales Beispiel ist im Lehrplan ausdrücklich die Sauerstofflöslichkeit in Wasser vorgesehen. Zudem lässt sich mit Bezug zur Aquaristik das Feld der Umweltchemie und Umweltanalytik mit stark experimentellem Bezug unterrichten. Besonders gut eignet sich das Thema Aquarium, um es in einer Projekteinheit zu behandeln. Dies kann entweder als Unterrichtseinheit (auch fächerübergreifend mit der Biologie) erfolgen oder aber im Rahmen einer Projektwoche. 8. Literatur- und Bildnachweise Bildnachweise: Titel: http://ahandler.safen.at/pod/add/stereo/beispiele/aquarium512.jpg1 Abbildung 1: http://www.bleyenberg.de/aquarium/aqua01.gif Abbildung 2: http://www.bleyenberg.de/aquarium/aqua02.gif Abbildung 3: Huminsäuren in Oberflächensedimenten der Nordsee : Indikatoren für terrestrischen Eintrag?, Ummo Fooken, Oldenburg, Univ., Diss., 1999 Abbildung 4: http://www.dennerle.de/Co2Unten.jpg Abbildung 5: http://upload.wikimedia.org/wikipedia/commons/thumb/4/4d/AquariumNitrogenCycle.png/300px-Aquarium-NitrogenCycle.png Abbildung 6: http://www.zoo-hoefler.de/Chemie/images/nh2.gif Abbildung 7: http://dc2.uni-bielefeld.de/dc2/wasser/images/feoxid1.gif Abbildung 8: Staatsexamensarbeit Chemie im Aquarium, 2004-2005, Volker Zimnol 38 Literaturnachweise: Chemie in unserer Zeit, 31. Jahrg. 1997, Nr.1 Chem. Exp. Technol. 3, S. 331-336, 1977 Praxis der Naturwissenschaften, 6/45, Jg. 1996 Praxis der Naturwissenschaften, 1/44, Jg. 1995 Naturwissenschaften im Unterricht 1, Nr.4, 1990 Naturwissenschaften im Unterricht 3, Nr.15, 1992 Staatsexamensarbeit Chemie im Aquarium, 2004-2005, Volker Zimnol http://www.drak.de/ Lehrplan Chemie Gymnasialer Bildungsgang, Hessisches Kultusministerium, Huminsäuren in Oberflächensedimenten der Nordsee : Indikatoren für terrestrischen Eintrag?, Ummo Fooken, Oldenburg, Univ., Diss., 1999 39