- 1 - Schema einer Lipiddoppelschicht Membranpermeabilität 6.2
Werbung
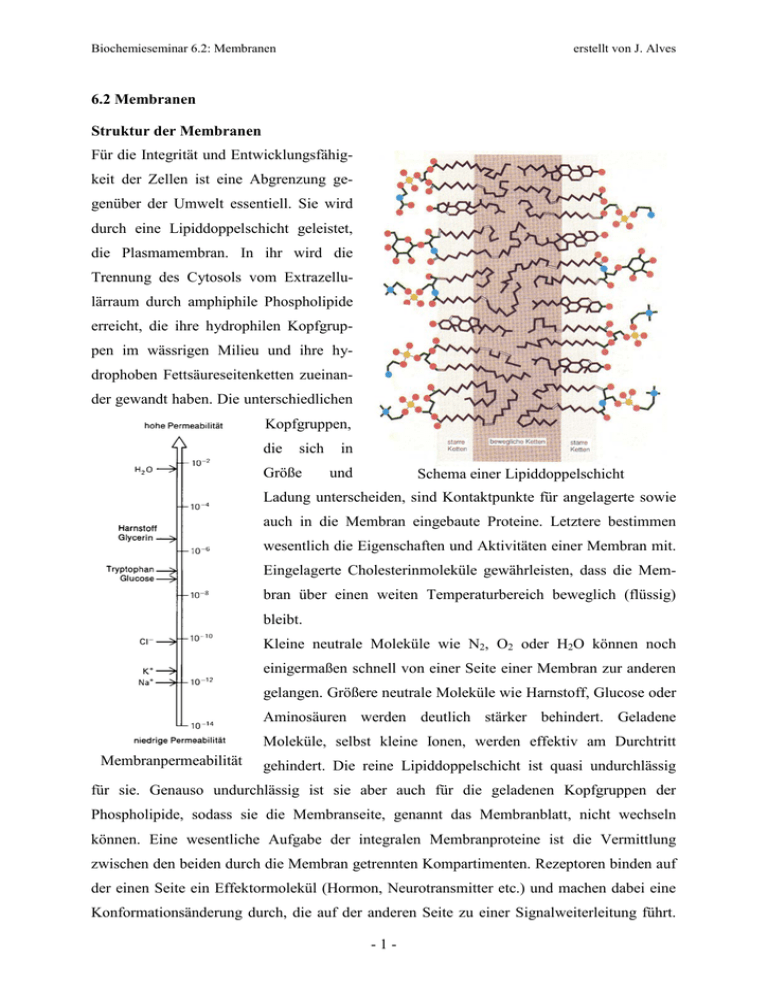
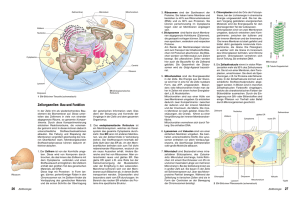
Biochemieseminar 6.2: Membranen erstellt von J. Alves 6.2 Membranen Struktur der Membranen Für die Integrität und Entwicklungsfähigkeit der Zellen ist eine Abgrenzung gegenüber der Umwelt essentiell. Sie wird durch eine Lipiddoppelschicht geleistet, die Plasmamembran. In ihr wird die Trennung des Cytosols vom Extrazellulärraum durch amphiphile Phospholipide erreicht, die ihre hydrophilen Kopfgruppen im wässrigen Milieu und ihre hydrophoben Fettsäureseitenketten zueinander gewandt haben. Die unterschiedlichen Kopfgruppen, die sich Größe in und Schema einer Lipiddoppelschicht Ladung unterscheiden, sind Kontaktpunkte für angelagerte sowie auch in die Membran eingebaute Proteine. Letztere bestimmen wesentlich die Eigenschaften und Aktivitäten einer Membran mit. Eingelagerte Cholesterinmoleküle gewährleisten, dass die Membran über einen weiten Temperaturbereich beweglich (flüssig) bleibt. Kleine neutrale Moleküle wie N2, O2 oder H2O können noch einigermaßen schnell von einer Seite einer Membran zur anderen gelangen. Größere neutrale Moleküle wie Harnstoff, Glucose oder Aminosäuren werden deutlich stärker behindert. Geladene Moleküle, selbst kleine Ionen, werden effektiv am Durchtritt Membranpermeabilität gehindert. Die reine Lipiddoppelschicht ist quasi undurchlässig für sie. Genauso undurchlässig ist sie aber auch für die geladenen Kopfgruppen der Phospholipide, sodass sie die Membranseite, genannt das Membranblatt, nicht wechseln können. Eine wesentliche Aufgabe der integralen Membranproteine ist die Vermittlung zwischen den beiden durch die Membran getrennten Kompartimenten. Rezeptoren binden auf der einen Seite ein Effektormolekül (Hormon, Neurotransmitter etc.) und machen dabei eine Konformationsänderung durch, die auf der anderen Seite zu einer Signalweiterleitung führt. -1- Biochemieseminar 6.2: Membranen erstellt von J. Alves Kanäle und Transporter kontrollieren den Durchtritt von definierten Molekülen, zu denen sie in der Regel eine hohe Affinität aufweisen, durch die Membran. Verankerungsmoleküle binden extrazellulär oder intrazellulär meist netzwerkartig angeordnete Strukturen, sodass die Zelle mit ihrem Cytoskelett in die Extrazellulärmatrix eingelagert wird und sich Zug- und Scherkräfte nicht nachteilig auf die Zelle auswirken. Aufbau und Synthese der Membranen Die Phospholipide werden am glatten endoplasmatischen Retikulum (ER) synthetisiert, die Glycerophospholipide sowie Cholesterin an der cytosolischen Seite und Ceramid, das erst im Golgi-Apparat in Sphingomyelin und Glycolipide umgewandelt wird, an der luminalen Seite der Membran. Die dafür verantwortlichen Enzyme sind membranständig und haben ihr katalytisches Zentrum zum wässrigen Milieu geöffnet, da alle Vorstufen noch löslich sind. Sobald aber zwei lange hydrophobe Ketten miteinander verknüpft sind, bleiben sie in die Membran eingelagert und sind bereit, mit verschiedenen Kopfgruppen beladen zu werden. Eine intensive Synthese auf einer Seite der Membran würde dazu führen, dass dieses Membranblatt zu stark aufgefüllt würde und die Integrität der Doppelschicht gefährdet wäre. Deshalb gibt es am glatten ER eine Scramblase, die einen Lipidaustausch zwischen den beiden Membranblättern ermöglicht. Dieses Enzym ist allerdings unspezifisch und würde letztendlich zu einer Gleichverteilung aller gebildeten Lipide über beide Membranseiten führen. Man findet aber eine extreme Ungleichverteilung vor allem der Membranen außerhalb des ER. Diese wird durch ATP-abhängige, Lipid-spezifische Verteilung der Phospholipide auf die beiden Blätter der Plasmamembran Transportprozesse hervorgerufen. Man unterscheidet Flippasen (Transport vom äußeren zum cytosolischen Membranblatt) und Floppasen (Transport vom cytosolischen zum äußeren Membranblatt). Eine Flippase sorgt zum Beispiel für einen Rücktransport von Aminophospholipiden wie Phosphatidylserin auf die Innenseite. Dies ist notwendig, da dessen Auftreten an der Außenseite als Erkennungssignal für das Andocken von Makrophagen dient, die die Zelle dann eliminieren, und bei Blutplättchen zur Aktivierung von Prothrombinase und damit zu Koagulation und Thrombose führt. In diesen Zellen ist das Gleichgewicht zwischen den Enzymaktivitäten an der Membran durch Ca2+ reguliert. Bei niedrigen Konzentrationen wird die Asymmetrie der Lipidverteilung auf die -2- Biochemieseminar 6.2: Membranen erstellt von J. Alves Membranblätter aufrechterhalten. Bei einem starken Ca2+-Einstrom wird die Scramblase aktiviert und die Flippase gehemmt. So kommt es zur Umverteilung von Phosphatidylserin an die Außenseite der Zelle mit den genannten Effekten. Verteilung der Mambranlipide Es gibt zwei Wege, über die zelluläre Membranen vom glatten ER mit neuen Phospholipiden versorgt werden. Als erstes gibt es einen Vesikeltransport zwischen dem ER und den Peroxiso- Gleichgewicht der ungerichteten und gerichteten Lipidaustauschaktivitäten in der Membran von Thrombozyten. men, zwischen dem ER, dem GolgiApparat, den endo- und exocytotischen Vesikeln und der Plasmamembran sowie zwischen diesen Vesikeln und den Lysosomen. Durch die Fluidität der Membranen wird ihr Gehalt an Phospholipiden dabei deutlich durchmischt. Die beiden Membranblätter bleiben allerdings erhalten, sodass das innere Blatt der Vesikel sowie die luminale Seite von ER und Golgi der Außenseite der Plasmamembran entspricht. So erklärt sich zwanglos die Lokalisation der Sphingolipide in diesem Membranblatt, da sie erst im Golgi synthetisiert werden, in dem keine Scramblase mehr arbeitet. Ein Abbau von Membranbestandteilen erfolgt in den Lysosomen, nachdem sie als intraluminale Vesikel nach innen eingestülpt wurden. Über den Vorgang der Autophagie werden dort auch Zellorganellen die wie Mitochondrien Verteilungswege der Lipidvesikel in der Zelle -3- Biochemieseminar 6.2: Membranen erstellt von J. Alves einschließlich ihrer Membranen abgebaut. Bei diesem Vesikeltransport scheinen die Mitochondrien ausgenommen zu sein. Hier wird deshalb der zweite Weg bedeutsam, bei dem Phospholipidtransferproteine, auch Phospholipidaustauschproteine genannt, arbeiten. Sie extrahieren vor allem Phosphatidylcholin und Phosphatidylserin aus einer Membran, diffundieren damit durchs Cytosol und liefern es an einer anderen Membran ab. Dabei scheint es keine definierte Richtung zu geben, sie arbeiten Arbeit eines Phospholipidtransferproteins also zufällig. Insgesamt findet so aber ein Ausgleich über die Membranen statt, sodass „lipidreiche“ Membranen wie das glatte ER Phospholipide an „lipidarme“ Membranen wie sich vergrößernde Mitochondrien abgeben. Dabei könnte es eine Rolle spielen, dass in elektronenmikroskopischen Bildern Mitochondrien häufig in der Nähe des ER gefunden werden, sodass die Lipide gleich „weitergereicht“ werden können. 2009 ist gefunden worden, dass der MDM-Komplex (MDM = mitochondrial distribution and morphology, also Gene, deren Defekt Verteilung und Morphologie der Mitochondrien beeinflusst) eine Verbindung der äußeren Mitochondrienmembran mit der ERMembran herstellt. Eine andere Arbeitsgruppe hatte schon gefunden, dass der genetische Defekt einzelner Komponenten dieses Komplexes zu einer Verringerung des Anteils von Phosphatidylethanolamin und Cardiolipin in der Mitochondrienmembran führt. Eine direkte Übertragung einzelner Lipidmoleküle zwischen den beiden Membranen würde natürlich wieder das cytosolische Membranblatt der äußeren Mitochondrienmembran auffüllen. Man postuliert deshalb ein Austauschprotein, das diese Phospholipide auf das andere Membranblatt überführt, sowie einen weiteren Transport zur inneren Mitochondrienmembran. Die so eingebauten Phospholipide können in den Mitochondrien noch nachträglich umgebaut werden, wodurch eine deutlich unterschiedliche Lipidzusammensetzung zu anderen Membranen in der Zelle resultiert. Membranproteine werden am rauen ER synthetisiert, so dass ihre Transmembrandomänen direkt in die Membran eingefügt werden. Über den Vesikeltransport werden sie dann auf die verschiedenen Membranen verteilt, wobei Sortierungsmechanismen dafür sorgen, dass sie in den Zwischenstationen (zum Beispiel dem Golgi-Apparat) in die Transportvesikel gelangen -4- Biochemieseminar 6.2: Membranen erstellt von J. Alves und in dem Zielorganell erhalten bleiben. Proteine der Mitochondrienmembran werden im Cytosol synthetisiert und dann anschließend in die mitochondriellen Membranen eingebaut. Grundlegende Literatur: Löffler, Basiswissen Biochemie, 7. Auflage S. 295-302, 310-314 Löffler Petrides Heinrich, Biochemie & Pathobiochemie, 8. Auflage S. 41-44, 174178, 562-564 Rassow Hauser Netzker Deutzmann, Biochemie, 3. Auflage S. 328-332, 350-351 Themen, die im Vortrag angesprochen werden sollten: Glattes und raues Endoplasmatisches Retikulum Phospholipide der beiden Membranblätter Ungleichverteilung • Scramblase • Flippase • Floppase Phospholipidtransport • Vesikeltransport • Phospholipidaustauschproteine Mitochondrielle Besonderheiten -5-