• Lehre der Energie, ihrer Erscheinungsform und Fähigkeit, Arbeit zu
Werbung

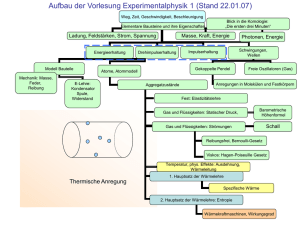
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 Vladimir Dyakonov Raum E143, Tel. 888-5875, eMail: [email protected] 10 Wärmelehre/Thermodynamik • Lehre der Energie, ihrer Erscheinungsform und Fähigkeit, Arbeit zu verrichten. 1 10 Wärmelehre/Thermodynamik Literatur: Skript dieser Vorlesung: http://physik.uni-wuerzburg.de/ep6/teaching Bergmann Schaefer (de Gruyter) Band I: Mechanik, Akustik, Wärme Douglas Giancoli (Pearson Studium Verlag, 2006) Physik, Kap. 17-20 Gerthsen (Springer Verlag) Physik Tipler (Spektrum Verlag) Physik G. von Oppen, F. Melchert (Pearson Studium Verlag 2006) Physik für Ingenieure 10 Wärmelehre/Thermodynamik Was ist Wärmelehre ? • eine unbeliebte Thematik ? • undurchschaubare Physik ? Maxwell‘scher Dämon Perpetuum mobile 2 10 Wärmelehre/Thermodynamik Teilgebiet der Physik : Im 19. Jhd. entwickelt durch: Temperatur, Wärme und Umwandlung von Energie Maxwell, Boltzmann, Kelvin, Clausius*, Nernst Heutige Forschungs- und Anwendungsgebiet: Energietechnik, Physik der Phasenumwandlung, Biophysik (Membranphysik), Nichtgleichgewichts-Thermodynamik Phänomenologische Thermodynamik: Einführung von 2 neuen physikalischen Größen: Temperatur, Wärmemenge Kinetische (molekulare) Gastheorie: Auf Prinzipien der klassischen Mechanik aufgebaut 1822-1888 * Rudolf Clausius, ein Begründer der Thermodynamik, war an der Universität Würzburg 10 Wärmelehre/Thermodynamik Historie: 1760: -Joseph Black „kalorische Theorie“: - Wärme ist eine unzersetzbare Flüssigkeit - Flüssigkeit hat das innere Bestreben, von Systemen hoher Temperatur zu den tieferer Temperatur zu fließen 1799: - Benjamin Thompson (Graf Rumford) - kinetische Theorie der Wärme - „Kanonenrohre“- Ende der „Wärmesubstanz“ 1738: - Daniel Bernoulli - der von einem Gas ausgeübte Druck rührt von den Impulsen seiner sich bewegenden Moleküle her, wenn diese auf die Behälterwände prallen 1728-1799 1753-1814 1700-1782 3 10 Wärmelehre/Thermodynamik Historie: 1765: -James Watt „Dampfmaschine“: - Umwandlung von Wärme in mechan. Energie - Einleitung der Industriellen Revolution 1736-1819 Newcomen‘sche Dampfmaschine 4 Watt‘sche Dampfmaschine 10 Kinetische Theorie der Wärme Hintergrund: - Mikroskopische Betrachtung des Vielteilchensystems - Mechanisches Modell für die Bestandteile des Systems - Berechnung von Zustandsvariablen durch Mittelung - statistische Mechanik ist Weiterentwicklung der kinetischen Theorie der Wärme - L. Boltzmann 1844-1906 J. C. Maxwell 1831-1879 J. W. Gibbs 1839-1903 5 10.1 Thermodynamischer Gleichgewichtszustand • TD befaßt sich mit Systemen, die aus sehr vielen Massenpunkten bestehen • Studium der Bewegungsabläufe aller Einzelteilchen ist praktisch nicht möglich • Interessant: statistische Mittelwerte über Geschwindigkeiten, kinetische und potentielle Energien der Teilchen, Druck, Temperatur, Volumen, innere Energie des Gesamtsystems • Systembeschreibung mittels Mittelwerte nur im thermodynamischen Gleichgewichtszustand sinnvoll Heliumflasche Kein Gleichgewichtszustand des Ausströmenden Gases Heliumballon: Thermisches Gleichgewicht 10.1 Thermodynamischer Gleichgewichtszustand • Zustand eines Systems = Gesamtheit seiner Eigenschaften, die durch äußere Bedingungen festgelegt sind • Zustandsgrößen Im thermodynamischen Gleichgewicht ist eine Reduktion der Parameter zur Kennzeichnung eines Systems auf wenige, der Messung allein zugängliche Größen möglich = Zustandsgrößen, die unabhängig sind von: - der sonstigen Beschaffenheit eines Körper - der Vorgeschichte: Druck p Volumen V Temperatur T Innere Energie U Entropie S • Zustandsgrößen sind im thermodynamischen Gleichgewicht konstant • Thermodynamische Wärmemenge und Arbeit sind kein Zustandsgrößen, weil sie vom Prozess abhängen !!! 6 10.1 Thermodynamischer Gleichgewichtszustand • stationärer Zustand = Ändern sich die Eigenschaften eines Systems nicht mit der Zeit = Gleichgewichtszustand (bestimmt durch Angabe von p, V, T) • Zustandsgleichungen: -Beschreiben den Zustand eines Gases (Substanz), nicht Prozesse - Liefern funktionelle Abhängigkeiten von Zustandsgrößen f(p,V,T)=0 In der Thermodynamik kommt die Zeit nicht explizit vor!!! 10.2 Temperatur • Temperatur (i) Temperatur ist aus der Sinnesempfindung warm/kalt entstanden; Nervensystem nur in der Lage Temperaturunterschiede subjektiv einzuschätzen: Physiker brauchen aber objektive Zahlen! (ii) Temperatur T ist ein skalare Zustandsgröße, die in einem thermodynamischen Gleichgewicht einen festen Wert hat und den Wärmezustand eines Systems beschreibt (iii) 2 Realisierungsmöglichkeiten des Gleichgewichts - thermische Isolation - Verbindung zu einem Wärmereservoir TRes T Thermische Isolation T=TRes Verbindung zu einem Wärmereservoir 7 10.2 Temperatur und Bewegung Temperatur T ist nur ein anderes Maß für die mittlere kinetische Energie der Moleküle im betreffenden Körper !!! Definition der Temperatur (nur Translationsenergie): Definitionsgleichung Wtrans = 1 2 3 mv = kT 2 2 m = Masse der Moleküle v2 = quadratisch gemittelte Geschwindigkeit der Moleküle k = Boltzmannkonstante; k = 1.381·10-23 J/K T = Temperatur in K (Kelvin) Aus Definitionsgleichung folgt: Existenz eines absoluten Nullpunkts der Temperatur, d.h. W und T sind Null Kelvin-Temperatur/Skala 10.2 Temperatur Thermisches Gleichgewicht & 0. Hauptsatz der Thermodynamik: Bringt man zwei Körper mit unterschiedlicher Temperatur in Kontakt, so nehmen sie nach einiger Zeit die gleiche Temperatur an. Der anfangs wärmere Körper kühlt sich ab und der anfangs kältere Körper wärmt sich auf. Beide Körper sind dann im thermischen Gleichgewicht. Körper A Körper 1 T1 Körper C Körper 2 T2 Körper B Sind zwei Körper A und B jeder für sich mit einem dritten Körper C (z.B. Thermometer) im thermischen Gleichgewicht, so sind A und B auch untereinander im thermischen Gleichgewicht. 8 10.2 Temperatur • Temperaturskala wird willkürlich festgelegt (i) 2 Fixpunkte (ii) lineare Skala zwischen den Fixpunkten • Celsius-Skala: Bei „Normaldruck“, d.h. Luftdruck: 1013.25 hPa (=760 mmHg) (i) Fixpunkte: 1. Eis-Wasser Gemisch („Eiswasser“): 0º C 2. Siedendes Wasser: 100º C (ii) Zwischen den Fixpunkten wird die Temperaturskala in 100 gleiche Teile zerlegt und zu kleineren (negativen) und größeren Temperaturen hin linear extrapoliert (Nach schwedischen Mathematiker Celsius, 1742) • Fahrenheit-Skala (vorwiegend USA): (i) Fixpunkte: 1. Salmiak-Schnee-Gemisch: 0º F 2. Menschliches Blut: 100º F (ii) Zwischen den Fixpunkten wird die Temperaturskala in 100 gleiche Teile zerlegt und zu kleineren (negativen) und größeren Temperaturen hin linear extrapoliert 10.2 Temperatur-Skalen Kelvinskala: TC=TK-273.15º 9 10.2 Temperatur Umrechnung: Beispiele: T (°C ) = 5 / 9 {T (° F ) − 32)}°C 32 º F= 0 ºC 100 º F= 37.7 ºC 212 º F= 100 ºC Problem: Temperaturdefinition ist abhängig vom Stoff (Wasser,Eis, Blut etc.) Gesucht: Temperaturfestlegung, die ohne Angabe eines bestimmten Stoffes auskommt 10.2 Temperaturmessung • Zur Temperaturmessung sind im Prinzip alle (physikalischen) Eigenschaften geeignet, die in reproduzierbarer Weise von der Temperatur abhängen (thermometrische Eigenschaft): -------- Volumen, Länge von Festkörpern Volumen von Flüssigkeiten, Gasen Elektrischer Widerstand Kontaktspannung zwischen Metallen Wärmestrahlung Magnetische Suszeptibilität etc. • Mit der quantitativen Messung dieser physikalischen Größen und geeigneter Eichmethoden ergeben sich Verfahren (Messgeräte, Thermometer) zur Temperaturmessung 10 10.2 Temperaturmessung Versuch: Wärmeausdehnung eines Gases: 10.2 Temperaturmessung Wärmeausdehnung fester und flüssiger Stoffe*: Ausdehnung von Festkörpern: a) Lineare (eindimensionale) Ausdehnung l: l (T ) = l0 (1 + αT ) α = linearer Ausdehnungskoeffizient, [α] =1 K-1 l0 = Länge bei Bezugstemperatur T0 Relative Längenänderung Beispiele α20 °C Quarzglas 0,5 · 10-6 Glas 8 α= ∆l l0 ⋅ T [°K-1] · 10-6 Kupfer 17 · 10-6 Nylon 80 · 10-6 α Quarz : α Glas : α Metall :α Polymer ≈ 1:10 : 20 :100 . *In begrenztem Temperaturbereich beobachtet man eine lineare Erhöhung der Ausdehnung von Festkörpern und Flüssigkeiten mit steigender Temperatur T 11 10.2 Temperaturmessung Versuch: Wärmeausdehnung eines Festkörpers: 10.2 Temperaturmessung Wärmeausdehnung fester und flüssiger Stoffe*: Ausdehnung von Festkörpern/Flüssigkeiten: V (T ) = l (T ) 3 = l0 (1 + αT ) 3 3 αT << 1 ≈ l0 (1 + 3αT ) 3 = V0 (1 + γT ) γ= 3α , Volumenausdehnungskoeffizient oder kubischer Ausdehnungskoeffizient V0 = Volumen bei Bezugstemperatur T0 Achtung: - Ausdehnung nichtisotroper Stoffe kann in allen 3 Raumrichtungen unterschiedlich groß sein. - Für die Messung muss berücksichtigt werden, dass sich die Flüssigkeit in einem Gefäß befindet, das sich ebenfalls ausdehnt. 12 10.2 Temperaturmessung Versuch: Wärmeausdehnung einer Flüssigkeit: 10.2 Temperaturmessung Versuch: Wärmeausdehnung eines Festkörpers: 13