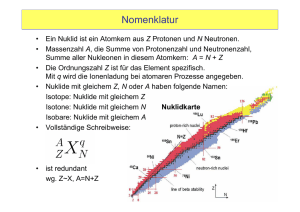
1 Atomphysik Kernphysik 27 10 08
Werbung

Atomphysik & Kernphysik Prof Dr. Prof. Dr Sabine Mahling Naturwissenschaftliche Grundlagen EEB, CEB und SSB @designed by ms Inhalte 1. Grundbegriffe 1 2. Materiebegriff 3. Atommodelle 1. DALTONsche Atomhypothese 2. THOMSONsches Atommodell 3. RUTHERFORDsches Atommodell 4. BOHRsches Atommodell 5. Wellenmechanisches Atommodell 6. Das Standardmodell 4. 4 5. 6. 7. 8. Periodensystem Nuklidkarte Antimaterie Radioaktivität Kernphysik 1. Nukleonenmassen 2. Massendefekt 3. Die 4 fundamentalen Kräfte 4. Kernspaltung 5. Kernreaktionen 1 1 Einige Grundbegriffe ... Masse m Atommasse M Molzahl n Druck p Temperatur T Energie E Wärme Q Arbeit W Entropie S Wirkungsgrad η ... 1.1 Physikalische Einheiten Volumen Druck Energie Temperatur Zeit Stoffmengen V p E T t n m3 N/m2 = Pa J = Nm K s mol 2 1.1.1 Das SI-System SI = Système y International d' Unités IS = International System of Units Basisgröße Basiseinheit Abkürzung Länge Masse Stromstärke Zeit Temperatur Lichtstärke Stoffmenge Ebener Winkel Raumwinkel Meter Kilogramm Ampere Sekunde Kelvin Candela Mol Radiant Steradiant m kg A s K cd mol rad sr http://www.chemie.fu-berlin.de/chemistry/general/si.html 1.1.1.1 Der Raumwinkel A • Der Raumwinkel Ω einer beliebigen Fläche A entspricht dem Quotienten aus der Fläche S (die sich ergibt, wenn A auf eine Kugel vom Radius r projiziert wird) und dem Kugelradius r2: Ω= S r2 http://de.wikipedia.org 3 1.1.1.2 Die Einheit des Raumwinkels Raumwinkel: Verhältnis zweier Flächen Æ SI Æ 1 m²/m²; SI-Name: Steradiant Einheit-Zeichen sr 1 sr = 1 m²/m² = 1 das Einheit-Zeichen sr kann auch weggelassen werden (nicht jedoch bei Anwendungsfeldern, bei denen intensiv mit Raumwinkeln gerechnet wird, z.B. in der Lichttechnik). Die SI-Einheiten für Lichtstärke und Lichtstrom unterscheiden sich nur durch Steradiant. Übungsaufgabe ? Wi groß Wie ß ist i t der d Raumwinkel R i k ld der vollen ll Kugeloberfläche ? 4 1.1.1.3 Polarkoordinaten der Ebene Die Polarkoordinaten ((Kreiskoordinaten)) eines Punktes in der euklidischen Ebene werden in Bezug zu einem Koordinatenursprung (einem Punkt der Ebene) und einer Polarkoordinatenrichtung (ein im Koordinatenursprung beginnender Strahl) angegeben http://de.wikipedia.org 1.1.1.4 Polarkoordinatenumrechnung Polar zu kartesisch lässt sich folgendermaßen umrechnen: x = r cos ( φ ) y = r sin ( φ ) Für kartesisch zu polar gelten die folgenden Formeln: r = x2 + y 2 ⎛ x⎞ für y ≥ 0 ⎝r⎠ ⎛ x⎞ ϕ = − arccos⎜ ⎟ für y < 0 ⎝r⎠ ϕ = arccos⎜ ⎟ 5 1.1.1.5 Raumwinkel und Polarkoordinaten Ein Punkt in der Ebene lässt sich in Polarkoordinaten durch (Flächen-) Winkel und Radius angeben. Auch im Raum gibt es ein solches Koordinatensystem. Der Raumwinkel ist dafür jedoch nicht ausreichend. Neben dem Radius sind immer die zwei Flächenwinkel Meridianwinkel φ und Breitenwinkel γ nötig. Allerdings besteht ein Zusammenhang zwischen dem Raumwinkel Ω und den beiden Winkeln der Raumpolarkoordinaten: Ω= ϕ2 γ 2 ∫ ∫ sin γ ⋅ dγ ⋅ dϕ ϕ1 γ 1 http://de.wikipedia.org 1.1.1.6 Polarkoordinaten des Raumes In räumlichen Polarkoordinaten wird ein Punkt durch seinen Abstand vom Ursprung r , sowie durch zwei Winkel θ und ϕ angegeben. Wenn der Abstand vom Ursprung konstant ist (auf einer Sphäre), benötigt man nur die zwei Winkel, um einen Punkt eindeutig zu bezeichnen, und spricht dann von sphärischen Koordinaten. Der Begriff Kugelkoordinaten kann als Oberbegriff für diese beiden Fälle angesehen werden. http://de.wikipedia.org 6 1.1.2 Vorsilben Vorsilbe Abkürzung Zehnerpotenz Dezimalzahl FemtoPicoNanoMikroMilliKil Kilo Mega Giga Tera Peta f p n µ m k M G T P 10 E-15 10 E-12 10 E-09 10 E-06 10 E-03 10 E+03 E 03 10 E+06 10 E+09 10 E+12 10 E+15 0.000 000 000 000 001 0.000 000 000 001 0.000 000 001 0.000 001 0.001 1000 1000000 1000000000 1000000000000 1000000000000000 http://physics.nist.gov/cuu/Units/prefixes.html 1.1.3 Griechische Buchstaben Α Β Γ Δ Ε Ζ Η Θ Ι Κ Λ Μ α β γ δ ε ζ η θ ϑ θ, ι κ λ μ = = = = = = = = = = = = Alpha Beta Gamma Delta Epsilon Zeta Eta Th t Theta Jota Kappa Lambda My Ν Ξ Ο Π Ρ Σ Τ Υ Φ Χ Ψ Ω υ ξ ο π ρ σ τ υ φ, ϕ χ ψ ω = = = = = = = = = = = = Ny Xi Omikron Pi Rho Sigma Tau Y il Ypsilon Phi Chi Psi Omega 7 1.1.4 Avogadrozahl und Mol Avogadrozahl: g Anzahl der Atome in 12 g des Kohlenstoff-Isotops p C-12,, gleichzeitig: Anzahl von Atomen oder Molekülen in der Stoffmenge von einem Mol und hat nach der CODATA-Empfehlung aus dem Jahr 2002 den Zahlenwert Ein Mol eines Stoffes enthält stets NA = NL = 6,0221415(10) 1023 mol − 1 Molekulargewicht, angegeben in Gramm = 1 Mol 1 Mol He = 4,003 g 1 Mol N2 = 14,007 x 2 = 28,014 g 1 Mol NaCl = 22,990 + 35,453 = 58,443 g http://physics.nist.gov/cuu/Constants/index.html http://de.wikipedia.org/ 1.1.5 Atomic Unit u 12 g C ≡ 6,0221415(10) 1023 C-Atome 12 6,022 ⋅ 1023 = 12u [ g] 1 6,022 ⋅ 1023 [ g] 1 C ≅ 1 u = http://physics.nist.gov/cuu/Constants/index.html 8 1.1.6 Druck p= F A Druck = Kraft / Fläche Pascal: Pa = N/m2 = kg/m s2 1b = 100 000 P 1bar Pa ~ atmosphärischer t hä i h L Luftdruck ftd k Normaldruck Standarddruck p = 1 atm = 101,325 kPa = 1013,25 mbar p = 1 atm = 101,325 kPa = 1013,25 mbar http://www.ebgymhollabrunn.ac.at/ipin/ph-druck.htm http://cicum92.cup.uni-muenchen.de/puchinger/glossar/glossarB2.html 1.1.7 Abgeleitete Größen Geschwindigkeit g v v= l t l t D= = Weg = Zeit ⎡m⎤ ⎢⎣ s ⎥⎦ Strahlungsdosis g D [m] [s] E m E = Energie m = Masse [J] [kg] ⎡ J ⎤ ⎢ Sv = kg ⎥ ⎦ ⎣ http://www.chemie.fu-berlin.de/chemistry/general/si.html 9 2 Was ist Materie ? Was ist Materie ? Was ist ein Stoff ? Materieaggregationen 2.1 Masse-Energie Das Weltall besteht aus Materie und strahlender Energie. Materie ist jegliche Art von Masse -Energie, die sich langsamer als Licht fortbewegt, strahlende Energie dagegen, ist jegliche Art von Masse-Energie, die sich mit Lichtgeschwindigkeit bewegt Linus Pauling E = m.c2 10 2.2 Das Universum Universum: Gesamtheit aller Objekte im Kosmos, Weltall Beschreibung durch die allgemeine Relaltivitätstheorie Entstehung durch „Urknall“ Alter: 13,7 Milliarden Jahre Kosmos: Weltraum, Weltordnung Weltraum: Beginnt in 80 - 100 km Höhe http://de.wikipedia.org/ 2.2.1 Der Urknall Urknall = Beginn des Universums nach kosmologischem Modell gemeinsame Entstehung von Materie, Raum und Zeit aus einem Ursprung ständige Expansion nach den Gesetzen der allgemeinen Relativitätstheorie „Beweise“ für die Urknalltheorie: • Die Rotverschiebung der Galaxien und damit die derzeitige Expansion des Universums • Das D S Spektrum kt d der Hi Hintergrundstrahlung t d t hl d des U Universums i • Die Grenze in der Altersverteilung der Sterne bei etwa 13 Milliarden Jahren • Die Häufigkeit der Elemente im Weltraum (insbesondere Wasserstoff, Deuterium und die Isotope des Helium) 11 2.2.2 Frühgeschichte des Universums 1 Billion = 1 Milliarde ! http://www.raumfahrer.net/astronomie/kosmologie/urknall.shtml 2.3 Der Aufbau der Erde Anteile der Elemente an der Erdkruste in g / t Metalloxide, Silikate T = 2000 °C Fe, Ni Fe Ni, S (flüssig) T = 2900 °C Æ Erdmagnetfeld Fe, Ni, (fest) p = 4 . 106 bar T = 4000 –5000 °C O Si Al Fe Ca Na K Mg Ti H P Mn F S 466.000 277.200 81.300 50.000 36.300 28.300 25 900 25.900 20.900 4.400 1.400 1.180 1.000 700 520 http://de.wikipedia.org/wiki/Innerer_Aufbau_der_Erde 12 2.4 Elemente und Verbindungen Chemisches Element Unter einem chemischen Element versteht man einen Stoff, der sich chemisch nicht mehr weiter in andere Stoffe zerlegen lässt. Chemische Ch i h Verbindung V bi d Unter einer chemischen Verbindung versteht man einen Stoff, der aus Atomen mehrerer verschiedener Elemente besteht und einheitliche physikalisch-chemische Eigenschaften wie z.B. Schmelz- und Siedepunkt aufweist. 2.4.1 Der Atombegriff • Atome sind die -einst als unteilbar geglaubten- kleinsten Bestandteile der der chemischen Elemente, die dessen Ei Eigenschaften h ft aufweisen f i • Unter einem chemischen Element versteht man einen Stoff, der aus Atomen mit gleichen chemischen Eigenschaften aufgebaut ist. 13 3 Atommodelle Vordenker: • Demokrit (ca. 500 v.Chr.): Alle Stoffe bestehen aus definierten kleinsten Teilchen den Atomen von Atomos Teilchen des Unteilbaren • Daniel Sennert (1618): Gesetz der Erhaltung der Elemente. Bei einer chemischen Reaktion gehen Elemente weder verloren, noch werden Elemente neu geschaffen. • Robert Boyle (1661): Elemente sind bestimmte primitive und einfache, völlig unvermischte Körper, sie enthalten keine anderen Körper, sie sind Zutaten, aus denen alle perfekt gemischten Körper zusammengesetzt sind und in welche diese letztlich zerlegt werden. • Antoine Laurent de Lavoisier (1785): Gesetz der Erhaltung der Masse. Die Summe der Massen der Edukte ist stets gleich der Summe der Massen der Produkte. • Jeremias Benjamin Richter (1791/92): Gesetz der äquivalenten Proportionen. http://de.wikipedia.org 3.1 Die DALTONsche Atomhypothese Daltons Atomhypothese (1808) • • • • • Materie besteht aus kleinsten kugelförmigen Teilchen oder Atomen. Diese Atome sind unteilbar und können weder geschaffen noch zerstört werden. Alle Atome eines chemischen Elements sind untereinander gleich, sie unterscheiden sich jedoch nur in der Masse von denen anderer. Diese Atome können chemische Bindungen eingehen und aus diesen auch wieder gelöst werden. Das Teilchen einer Verbindung wird aus einer bestimmten, stets gleichen Anzahl von Atomen der Elemente gebildet, aus denen die Verbindung besteht http://de.wikipedia.org 14 3.2 Das THOMSONsche Atommodell Rosinenkuchenmodell Atom hat gleich viele positive und negative Bestandteile Atom ist in der Summe elektrisch neutral Negative Ladung Positive Ladung 3.3 Das RUTHERFORDsche Atommodell At k Atomkernmodell: d ll winziger i i K Kern = M Massepunkt kt Planetenmodell: Elektronen bewegen sich auf Kreisbahnen um den Kern Kreisbahn entsteht durch Gleichgewicht von Coulomb- und Zentrifugalkraft Negative Ladung Positive Ladung Widerspruch zu den Gesetzen der Elektrodynamik ! Æ instabile Elektronenbahnen 15 3.3.1 Das RUTHERFORD-Experiment α Goldfolie Film Streuung von Alphateilchen an Goldfolie erklärbar Berechnung einfacher Atomspektren möglich 3.4 Das BOHRsche Atommodell φ = 10-7 - 10-10 m Kern: Protonen Neutronen (+) (n) Elektronenhülle: Elektronen (-) Widerspruch zu den Gesetzen der Elektrodynamik ! Æ Bremsstrahlung erwartet ! 16 3.4.1 Stabile Elektronenbahnen 1. BOHRsche Quantenbedingung: stabile Bahnen wenn das Produkt aus Kreisumfang und Elektronenimpuls ein Vielfaches des PLANCKschen Wirkungsquantums h ist (2 ⋅ π ⋅ rn ) ⋅ (me ⋅ vn ) = n ⋅ h n = Schalennummer, rn = Radius Schale n, me = Elektronenmasse, vn = Impuls Schale n 2. BOHRsche Frequenzbedingung: g g Durch Energiezufuhr ist ein Übergang zwischen den Bahnen möglich, wenn absorbierte Energie genau der Energiedifferenz ΔE zwischen den Bahnen entspricht: ΔE = h ⋅ν = E2 − E1 E1 = Energie Schale 1, E2 = Energie Schale 2, ν = Frequenz 3.4.2 Elektronen Schalen 2n2 Elektronen pro Schale E n = 4 N-Schale n = 3 M-Schale n = 2 L-Schale n = 1 K-Schale 1 Z ⋅ e 2 me ⋅ Z 2 ⋅ e 4 En = − ⋅ = 2 rn 2 ⋅ n2 ⋅ h2 En n Z e rn me = = = = = = h = Schalenenergie Schalennummer Ordnungszahl Elementarladung Orbitalradius Elektronenmasse h / 2π 17 3.4.3 Die Wasserstoffspektrallinien Spektrum p des Wasserstoffatoms P O N M L PFUND BRACKETT PASCHEN BALMER K LYMAN Spektralserien 3.4.4 Das Wasserstoffspektrum http://www.physics.utoledo.edu/ 18 3.4.5 Relativer Atomdurchmesser Haselnuss 100 m 1 cm 3.5 Wellenmechanisches Atommodell Elektron = stehende Welle Wellenfunktion eines Elektrons Ψ (r,E) Aufenthaltsbereich eines Elektrons Ψ 2(r,E) SCHRÖDINGER Gleichung SCHRÖDINGER-Gleichung HΨ = EΨ Energiezustände eines Elektrons E Kernabstand r 19 3.5.1 Stehende Welle l = n⋅ λ 2 n = 1,2,3,4,... http://uni-ka.lanable.de/html/exphys1/exse18.htm 3.5.2 Wellenmechanikprinzipien Quantenmechanik • Welle – Teilchen Dualismus λ= h p • Wellenmechanik: Teilchen Æ Wellenfunktion Ψ 1. 1 2. 3. 4. komplexwertig keine Messgröße Ψ2 (Betragsquadrat) Aufenthaltswahrscheinlichkeit des Teilchens Ψ (r,θ,ϕ,t) Æ SCHRÖDINGER-Gleichung 20 3.5.2.1 Klassische Teilchen klassische Teilchen sind Bausteine der Materie, wie in der klassischen Physik verstanden, wird mit folgenden Eigenschaften: • Ort: • Impuls: • Masse: x p = m⋅v = m E h ⋅ν = c c • keine Unschärferelation (Ort und Impuls können beliebig genau bestimmt werden) 3.5.2.2 DE BROGLIE-Wellenlänge • DE BROGLIE: auch massereiche Teilchen haben Wellencharakter – 1923 "Dualität von Welle und Korpuskel" – 1927 Bestätigung durch Doppelspaltexperiment von Clinton Davisson und Lester Germer • Hat das Teilchen einen Impuls p, so ist seine Wellenlänge λ : λ= h p p= h ⋅ν c λ= c ν c = Lichtgeschwindigkeit (299792458 ms-1) h = PLANCKsches Wirkungsquantum ν = Frequenz der Lichtwelle 21 3.5.2.3 Welle-Teilchen-Dualismus • Wellen haben auch Teilchencharakter • Teilchen haben auch Wellencharakter. • Es sind stets beide Eigenschaften vorhanden • Art der Beobachtung bedingt die Art der Erscheinung: mikroskopische ik k i h W Wellenperspektive ll kti oder d makroskopische k k i h (und somit unscharfen) Teilchenperspektive 3.5.2.4 Natur von Wellen und Teilchen Wellennatur Teilchennatur • • • • • • • • • • • • • Wellenlänge, Amplitude Wellenfunktion Ψ O bit l Ψ2 Orbitale Interferenzen Stehende Wellen Ausbreitungsgeschwindigkeit Energie: E = h.ν Masse, Impuls Flugbahnen I i ti Ionisationsvermögen ö Geometrische Optik (Newton) Geschwindigkeit Energie: E = ½ m.v2 22 3.5.2.5 Interferenzen http://de.wikipedia.org/ 3.5.2.6 Makroskopische Gegenstände Wellencharakter der Teilchen zeigt sich nicht bei makroskopischen Gegenständen (Körpern), was zwei prinzipielle Ursachen hat: – bei langsamer Bewegung haben Körper aufgrund großer Masse eine Wellenlänge, die erheblich kleiner ist als ihre Abmessungen Æ separate Beschreibung der Bestandteile. – IIn makroskopischen k k i h G Gegenständen tä d llaufen f permanentt thermodynamisch irreversible Prozesse ab Æ Photonenaustausch, Wärmestrahlung Æ Dekohärenz des Systems Æ nicht interferenzfähige Zustände Æ klassisches Teilchen http://de.wikipedia.org 23 3.5.3 Die Unschärferelation • Für ein q quantenmechanisches Teilchen ist es unmöglich g Ort x und Impuls p gleichzeitig beliebig genau zu messen Δx ⋅ Δp = h 2 • Der Zeitpunkt t eines Vorganges und die dabei übertragene Energie E lassen sich nicht gleichzeitig messen Δt ⋅ ΔE = h 2 • Je genauer eine dieser Größen bestimmt wird, desto ungenauer erscheint die andere ! Quantenmechanische Aussagen sind Wahrscheinlichkeitsaussagen ! 3.5.3.1 PLANCKsches Wirkungsquantum • Definition der Energie E: E = h⋅ c λ h = 6,626 068 76 ⋅10 −34 Js c = Lichtgeschwindigkeit, λ = Wellenlänge • h hat die Dimension einer Wirkung ! 24 3.5.4 Die Wellenfunktion des Elektrons All Allgemeine i W Wellenfunktion ll f kti fü für monochromatische h ti h W Welle ll iin r-Richtung Ri ht Ψ (r , t ) = c ⋅ ei (ϖt + kr ) Realer Anteil der Wellenfunktion Ψ (r , t ) = c ⋅ cos(ϖ ⋅ t + k ⋅ r ) Zustandsfunktion 3.5.5 Stehende Wellen Stehende Wellen • sind Wellen, bei denen die räumliche Lage der Schwingungsbzw. Wellenbäuche und –knoten sich zeitlich nicht ändert; • sind Wellen, die keine Energie transportieren Für die Strecke l, auf der die Schwingung stattfindet, muss gelten, dass sie ein Vielfaches n der Wellenlänge λ ist. l = n⋅ λ 2 n = 1,2,3,4,... d l 25 3.5.5.1 Stehende Wellen (a) l = n⋅ λ 2 n = 1,2,3,4,... d l d n = 1 Grundschwingung n = 2 1. Oberschwingung d d n = 3 2. Oberschwingung n = 4 3. Oberschwingung 3.5.5.2 Stehende Wellen (b) d d n = 1 Grundschwingung d n = 2 1. Oberschwingung d n = 3 2. Oberschwingung n = 4 3. Oberschwingung Balkendiagrammdarstellung 26 3.5.5.3 Stehende Wellen (c) 325,00 40,00 320,00 45,00 315 315,00 00 50 50,00 00 310 310,00 00 55 55,00 00 305,00 60,00 300,00 65,00 295,00 70,00 290,00 75,00 285,00 80,00 280,00 85,00 275,00 90,00 270,00 95,00 265,00 100,00 260,00 105,00 255,00 110,00 250,00 115,00 245,00 120,00 240,00 125,00 235,00 130,00 230,00 135,00 225,00 140,00 220,00 145,00 215,00 150,00 210,00 155,00 205,00 160,00 200,00 165,00 195,00 170,00 190,00 185,00 180,00 175,00 n = 1 Grundschwingung , , 335,00 30,00 330,00 35,00 325,00 40,00 320,00 45,00 315,00 50,00 310,00 55,00 305,00 60,00 300 300,00 00 65 65,00 00 295 295,00 00 70 70,00 00 290,00 75,00 80,00 285,00 280,00 85,00 275,00 90,00 270,00 95,00 265,00 100,00 260,00 105,00 255,00 110,00 250,00 115,00 245,00 120,00 240,00 125,00 235,00 130,00 230,00 135,00 225,00 140,00 220,00 145,00 215,00 150,00 210,00 155,00 205,00 160,00 200,00 165,00 195,00 170,00 190,00 185,00 180,00 175,00 n = 3 2. Oberschwingung 360,00 5,00 355,00 10,00 350,00 15,00 345,00 20,00 340,00 25,00 335 335,00 00 30,00 30 00 330 330,00 00 35 35,00 00 325,00 40,00 320,00 45,00 315,00 50,00 310,00 55,00 305,00 60,00 300,00 65,00 295,00 70,00 290,00 75,00 285,00 80,00 280,00 85,00 275,00 90,00 270,00 95,00 265,00 100,00 260,00 105,00 255,00 110,00 250,00 115,00 245,00 120,00 240,00 125,00 235,00 130,00 230,00 135,00 225,00 140,00 220,00 145,00 215,00 150,00 210,00 155,00 205,00 160,00 200,00 165,00 195,00 170,00 190,00 185,00 180,00 175,00 n = 2 1. Oberschwingung 360,00 5,00 355,00 10,00 350,00 15,00 345,00 20,00 340,00 25,00 335,00 30,00 330,00 35,00 325,00 40,00 320,00 , , 00 45,00 315 315,00 00 50 50,00 310 310,00 00 55 55,00 00 305,00 60,00 300,00 65,00 295,00 70,00 290,00 75,00 285,00 80,00 280,00 85,00 275,00 90,00 270,00 95,00 265,00 100,00 260,00 105,00 255,00 110,00 250,00 115,00 245,00 120,00 240,00 125,00 235,00 130,00 230,00 135,00 225,00 140,00 220,00 145,00 215,00 150,00 210,00 155,00 205,00 160,00 200,00 165,00 195,00 170,00 190,00 185,00 180,00 175,00 n = 4 3. Oberschwingung Polarkoordinatendarstellung 3.5.7 Der Drehimpuls des Elektrons • Ein Elektron mit der Masse m und der Ladung e, das sich mit der r Geschwindigkeit v auf einem Kreis r mit dem Radius r bewegt hat ein r magnetisches Dipolmoment μ und r einen Drehimpuls L von: r r r L=r×p r r p = m⋅v r L r r m -e m,-e Bahndrehimpuls r v r μ Linearer Impuls ( 2 ⋅ π ⋅ r ) ⋅ ( m ⋅ v) = n ⋅ h r r L ,μ gekoppelt 27 3.5.8 Der Spin des Elektrons Elektronen weisen eine Drehung um die eigene Achse auf, damit verbinden ist ein Eigendrehimpuls, den man auch als Spin bezeichnet r S Der Betrag des Spins kann die Werte annehmen: S = s⋅h Für das Elektron kann der Betrag des Spins nur sein: s = ±1 2 3.5.9 Materiewellen Materiewelle L = l ⋅h • Die Forderung im Bohrschen Atommodell, dass der Drehimpuls L ein ganzzahliges Vielfaches von h = h / 2π ist, kann anschaulich damit erklärt werden, dass eine Elektronenwelle um den Kern "herumgewickelt" herumgewickelt wird (l = Bahndrehimpulsquantenzahl). Bahndrehimpulsquantenzahl) Wellen mit einer Wellenlänge, die nicht Teiler des Umfangs ist, überlagern sich bei mehrmaligem Wickeln destruktiv. Möglich - "erlaubt" - sind also nur Wellen mit einer Wellenlänge, die den Umfang teilt. Dadurch ergeben sich nach Bohr die diskreten Orbitale der Elektronen. http://de.wikipedia.org 28 3.5.10 Quantenzahlen Quantenzahlen sind einfache Zahlen, die den Zustand eines quantenphysikalischen Systems beschreiben. Durch einen vollständigen Satz von Quantenzahlen ist der Zustand des Systems eindeutig festgelegt 3.5.10.1 Elektronenquantenzahlen Quantenzahl Hauptquantenzahl Nebenquantenzahl Magnetquantenzahl Symbol n l m erlaubte Werte 1,2,3,4,5,... 0,1,2, ... (n-1) 0,±1,±2, ... ,± l Bedeutung Kernabstand, Energie Bahndrehimpuls Drehimpulsorientierung Spinquantenzahl s ±½ Eigendrehimpuls der Bahndrehimpuls gibt den Orbitaltyp (s,p,d,f..) an; die Drehimpulsorientierung gibt die Orbitallage .(bei p: x,y,z, etc) an 29 3.5.10.2 „Elektronenschalen“ • Alle Zustände mit demselben Wert für n bilden eine Schale, – es gibt 2n2 Zustände in einer Hauptschale; • Alle Zustände mit den selben Werten für n und l bilden eine Unterschale, – Alle Zustände in einer Unterschale haben dieselbe Energie – Es gibt 2(2l+1) Zustände in einer Unterschale. 3.5.11 Atomorbitale • Atomorbitale AO sind 3-dimensionale stehende Materiewellen, die den Aufenthaltsbereich (keine klar definierte Bahn !) der Elektronen darstellen. Das energieärmste Orbital entspricht dem Grundzustand (Grundschwingung), energiereichere Orbitale entsprechen angeregten Zuständen (Oberschwingungen) z z x y s-AO: Drehimpuls l = 0 x y p-AO: Drehimpuls l = 1 30 3.5.12 Zustandsfunktionen Quantenmechanische Zustände Q ΨΑ = ΨΑ(r,θ,φ) . ΨΑ(t) ΨΒ = ΨΒ(r,θ,φ) . ΨΒ(t) ΨC = ΨC(r,θ,φ) . ΨC(t) Linearkombination der Zustände (Überlagerung) Ψ = a . ΨΑ(r,θ,φ) + b .ΨΒ(r,θ,φ) + c .ΨC(r,θ,φ) Aufenthaltswahrscheinlichkeit Ψ2 = A2.sin2(ω.t + ϕ0) 68 67 66 65 64 63 62 61 60 59 58 57 56 55 54 53 52 51 50 49 48 47 4645 44 7 89 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 3.5.13 Phänomene der Wellenmechanik • Unschärferelation Æ fundamentale Grenze der Genauigkeit der Erfassung physikalischer Eigenschaften • Zustandsüberlagerung (Superposition) ohne gegenseitige Beeinflussung Æ Linearkombinationen von Wellenfunktionen • Quantenverschränkung: räumlich getrennte Teile eines quantenmechanischen Systems (z.B. Einzelteilchen im Zweiteilchensystem) können unabhängig von der Entfernung korrelierte Messwerte besitzen Quantenmechanische Aussagen sind Wahrscheinlichkeitsaussagen ! 31 3.5.14 SCHRÖDINGER Gleichung • • Grundgleichung g g der nichtrelativistischen Quantenmechanik zeitliche Entwicklung des Zustands eines Quantensystems i⋅h⋅ Ψ(r,t) m V(r,t) ∇ • h2 ∂ Ψ (r , t ) = − ⋅ ∇ 2 Ψ (r , t ) + V (r , t ) ⋅ Ψ (r , t ) ∂t 2m = Wellenfunktion z.B. des Elektrons = Masse z.B. des Elektrons = Potentielle Energie z.B. des Elektrons = Nabla-Operator Lösung der zeitunabhängigen SCHRÖDINGERgleichung: Energiezustände E 3.5.14.1 SCHRÖDINGERs Katze http://de.wikipedia.org 32 3.5.15 Die Struktur der Elektronenschalen Hauptschalen H t h l nb bestehen t h aus U Unterschalen t h l l Die Besetzung erfolgt nach strengen Regeln n=4 n=3 n=2 n=1 s p d f 3.5.16 Die Besetzung von Elektronenschalen Schreibweise: nlx n l = Schalennummer = Unterschale s,p,d,f.. x = Zahl e- pro Orbital Besetzungszahl, kein Exponennt ! H He Li Be B C N 1 s1 1 s2 1 s2 1 s2 1 s2 1 s2 1 s2 2 s1 2 s2 2 s2 2 s2 2 s2 Valenzelektronen 2p1 2p2 2p3 33 3.5.16.1 Das Pauli – Prinzip • In einem Atom können keine zwei Elektronen in allen vier Quantenzahlen (Hauptquantenzahl, Drehimpulsquantenzahl, Magnetquantenzahl und Spinquantenzahl), Spinquantenzahl) die zu seiner Zustandsbeschreibung im Atommodell notwendig sind, übereinstimmen. • Als Folge des Pauliprinzips werden die Orbitale immer mit Elektronenpaaren besetzt, die entgegengesetzten Spin aufweisen. 3.5.16.2 Die HUNDsche Regel • Energiegleiche Orbitale einer Unterschale werden zunächst einfach besetzt 34 3.5.16.3 Elektronenkonfiguration von N PAULI Prinzip - HUNDsche Regel E n=3 n=2 n=1 s p d Elektron mit positiver Spinrichtung Elektron mit negativer Spinrichtung 3.5.16.4 Elektronenkonfiguration von Na 30 11 Schreibweisen Na 1s2 2s2 2p6 3s1 n=4 n=3 n=2 n=1 35 3.5.16.5 Das Energieprinzip Grundzustand: werden stets zunächst energieärmste Orbitale Orbitalenergien näherungsweise Elektroneneinbauschema 3.5.16.6 Elektronenkonfiguration von K Energieprinzip E n=4 n=3 4s n=2 n=1 s p Elektron mit positiver Spinrichtung d Elektron mit negativer Spinrichtung 36 Welches Element ist das ? [Ar] 3d10 4s2 4p6 = ? ? n=4 n=3 n=2 n=1 s p d f 4 Das Periodensystem der chemischen Elemente At Atome sind i d di die -einst i t als l unteilbar t ilb geglaubtenl bt kl i t kleinsten Bestandteile der der chemischen Elemente, die dessen Eigenschaften aufweisen Entwicklung 1829 DÖBEREINER ordnet Elemente nach Eigenschaften 1864 MEYER führt Tabellensystem ein 1869 MENDELEJEFF erstellt Urform des heutigen PS Voraussagen über fehlende Elemente möglich 114 chemische Elemente konnte man identifizieren. Oberhalb der Ordnungszahl 82 sind sie alle radioaktiv ! 37 4.1 Systematik der Elektronenkonfiguration Elektronenkonfiguration A Anzahl hl d der Bi Bindungselektronen d l kt ablesbar bl b Wertigkeit in Molekülen erkennbar Eigenschaften vorhersagbar 4.2 Perioden und Gruppen Perioden Hauptgruppen I II III IIII V VI VII VIII 1 2 1H 3Li 2He 4Be 5B 6C 7N 8O 9F 10Ne 3 11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar 4 19K 20Ca 31Ga 32Ge 33As 34Se 35Br 36Kr 5 37Rb 38Sr 49In 50Sn 51Sb 52Te 53I 54Xe 6 55Cs 56Ba 81Tl 82Pb 83Bi 84Po 85At 86Rn 7 87Fr 88Ra 113 114 115 116 117 118 38 4.2.1 Hauptgruppenelemente (s,p) I Alkalimetalle Li, Na, K, Rb, Cs, Fr sehr reaktive Metalle Erdalkalimetalle Be, Mg, Ca, Ba, Sr, Ra weniger reaktive Metalle Erdmetalle B, Al, Ga, In, Tl Leichtmetalle Kohlenstoffgruppe C, Si, Ge, Sn, Pb zunehmend metallisch II III IIII V Stickstoffgruppe N, P, As, Sb, Bi zunehmend metallisch Chalkogene O, S, Se, Te, Po Erzbildner Halogene g F, Cl, Br, I, At Salzbildner Edelgase He, Ne, Ar, Kr,Xe, Rn innerte Gase VI VII VIII 4.2.2 Nebengruppenelemente (d) Scandium--Gruppe IIIb Sc s2p6d1 Scandium Sc 1s2 2s2 p6 3s2 p6 d1 4s2 Y 1s2 2s2 p6 3s2 p6 d10 4s2 p6 d1 L La 1s2 2 1 2s2 p6 3s2 p6 d10 3 4s2 p6 d10 4 5s2 p6 d1 5 Ac 1s2 2s2 p6 3s2 p6 d10 4s2 p6 d10 5s2 p6 d10 5s2 6s2 6 6s2 p6 d1 7s2 Valenzelektronen: s, d 39 4.2.3 Lanthanoide und Actinoide (f) 5d1 6s2 57La [Xe] 58Ce [Xe] 4f2 6s2 59Pr [Xe] 4f3 6s2 60Nd [Xe] 4f4 6s2 89Ac [Rn] 6d1 7s2 90Th [Rn] 6d2 7s2 91Pa [Rn] 5f2 6d1 7s2 92U [Rn] 5f3 6d1 7s2 Valenzelektronen: s, d, f 4.2.3.1 Webelements (1) http://www.webelements.com 40 4.2.3.2 Webelements (2) http://www.webelements.com 4.3 Die periodischen Eigenschaften der Elemente • • • • Atomdurchmesser Ionisierungsenergie Elektronenaffinität Elektronegativität • Gasförmige Elemente • Flüssige Elemente • Feste Elemente • Radioaktive Elemente • Metallcharakter • Halbleitereigenschaften 41 4.3.1 Atomdurchmesser I II III IIII V VI VII VIII 1 2 1H 2He 3Li 4Be 5B 6C 7N 8O 9F 10Ne 3 11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar 4 19K 20Ca 31Ga 32Ge 33As 34Se 35Br 36Kr 5 37Rb 38Sr 49In 50Sn 51Sb 52Te 53I 54Xe 6 55Cs 56Ba 81Tl 82Pb 83Bi 84Po 85At 86Rn 7 87Fr 88Ra 113 114 115 116 117 118 4.3.2 Ionisierungsenergie Na ΔEI ΔEI Na+ + eKation . -19 = Ionisierungsenergie = 8,3 10 J (pro Atom) wächst mit Z sinkt, wenn rAtom wächst nimmt ab wie folgt: s>p>d>f Ö Die Ionisierungsenergie ist die Energie, die benötigt wird, um ein Atom oder Molekül zu ionisieren, d. h. um ein Elektron vom Atom oder Molekül zu trennen 42 4.3.2.1 Ionisierungsenergie Diagramm http://www.chemgapedia.de 4.3.2.2 Ionisierungsenergie im PS I II III IIII V VI VII VIII 1 2 1H 2He 3Li 4Be 5B 6C 7N 8O 9F 10Ne 3 11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar 4 19K 20Ca 31Ga 32Ge 33As 34Se 35Br 36Kr 5 37Rb 38Sr 49In 50Sn 51Sb 52Te 53I 54Xe 6 55Cs 56Ba 81Tl 82Pb 83Bi 84Po 85At 86Rn 7 87Fr 88Ra 113 114 115 116 117 118 43 4.3.2.3 Höhere Ionisierungsenergien Ionisierungsenergien der Elemente Z = 1, ..12 Z Element Ionisierungsenergie in eV zur Abtrennung des x-ten Elektrons 1 2 3 4 5 6 7 1 2 3 4 5 6 7 8 9 10 11 12 H He Li Be B C N O F Ne Na Mg 13,6 24,6 5,4 9,3 8,3 11,3 14,5 13,6 17,4 21,6 5,1 7,6 54,4 75,6 18,2 25,1 24,4 29,6 35,2 35,0 41,0 47,3 15,0 122,4 153,9 37,9 47,9 47,4 54,9 62,6 64,0 71,6 80,1 217,7 259,3 64,5 77,5 77,4 87,2 97,1 98,9 109,3 340,1 391,9 97,9 113,9 114,2 126,4 138,6 141,2 489,8 551,9 138,1 157,1 157,9 172,4 186,7 666,8 739,1 185,1 207,0 208,4 225,3 4.3.3 Elektronenaffinität ΔEE Cl. + e- Ö Cl- H F Cl Br I (kJ / mol) - 72 -333 -364 -342 -295 Anion ΔEE = Elektronenaffinität = - 6,0 . 10-19 J (pro Atom) bei Halogenen besonders groß ! Die Energiedifferenz zwischen dem Grundzustand eines neutralen Atoms und dem Grundzustand des zugehörigen Anions wird als Elektronenaffinität bezeichnet 44 4.3.4 Elektronegativität - Bedeutung Maßzahl: Atom 1 EN Bindungselektronen Atom 2 Anziehungskraft auf Bindungselektronen bei F am größten, bei Fr am kleinsten ! H Fr F Cl Br I EN 2,1 0,7 4,0 3,0 2,8 2,4 4.3.4.1 Elektronegativität Berechnung Maßzahl: EN Berechnung nach Mulliken, 1966 X + eX Æ Æ EN ~ XX+ + e- ΔEE ΔEI 1 [ΔEE + ΔEI ] 2 45 4.3.4.2 Elektronegativität im PS I II III IIII V VI VII VIII 1 2 1H 3Li 4Be 5B 6C 7N 8O 9F 2He 10Ne 3 11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar 4 19K C 20Ca G 31Ga G 32Ge A 33As S 34Se B 35Br K 36Kr 5 37Rb 38Sr 49In 50Sn 51Sb 52Te 53I 54Xe 6 55Cs 56Ba 81Tl 82Pb 83Bi 84Po 85At 86Rn 7 87Fr 88Ra 113 114 115 116 117 118 4.3.4.3 Elektronegativität Diagramm F 4,5 , Cl 4 Br I Ele ektronegativit 3,5 3 2,5 2 15 1,5 1 0,5 0 1 21 41 61 81 101 Ordnungszahl 46 4.3.4.4 Die Elektronegativitätsskala H 2,1 Li 1,0 Na 0,9 Be 1,5 Mg 1,2 K Ca 0,8 1,0 Rb Sr 0,8 1,0 Al 1,5 Sc 1,3 B 2,0 Si 1,8 C 2,5 P 2,1 Ti Ge As 1,6 1,7 2,0 Y Zr Sn Sb Te 1,3 1,6 1,7 1,8 2,1 N 3,0 S 2,5 Se 2,4 O 3,5 F 4,0 Cl 3,0 Br 2,8 I 2,4 Cs Ba 0,7 0,9 1 EN 2 3 4 4.3.5 Metallische Eigenschaften plastisch verformbar elektrische Leiter Leitfähigkeit sinkt mit steigender Temperatur relativ große Atomradien Atomgitter geringe Ionisierungsenergie Wärmeleiter Supraleiter ca. 30 metallische Elemente Metallglanz 47 4.3.5.1 Metallcharakter im PS Metallcharakter I Nichtmetallcharakter II III IIII V VI VII VIII 1 2 1H 3Li 4Be 5B 6C 7N 8O 9F 2He 10Ne 3 11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar 4 19K 20Ca 31Ga 32Ge 33As 34Se 35Br 36Kr 5 37Rb 38Sr 49In 50Sn 51Sb 52Te 53I 54Xe 6 55Cs 56Ba 81Tl 82Pb 83Bi 84Po 85At 86Rn 7 87Fr 88Ra 113 114 115 116 117 118 Metalle Halbmetalle Nichtmetalle 4.3.6 Halbmetalleigenschaften I 1 2 3 4 5 6 7 II III IIII V VI VII 1H VIII 2He 3Li 4Be 5B 6C 7N 8O 9F 10Ne 11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar 19K 20Ca 31Ga 32Ge 33As 34Se 35Br 36Kr 37Rb 38Sr 49In 50Sn 51Sb 52Te 53I 54Xe 55Cs 56Ba 81Tl 82Pb 83Bi 84Po 85At 86Rn 87Fr 88Ra 113 114 115 116 117 118 B, Si, Ge, As, Te Leitfähigkeit steigt mit der Temperatur mehrere Modifikationen z.B. kristallines und amorphes Si Halbleitereigenschaften Elektronenleitung Defektelektronenleitung 48 4.3.7 Dotiermittel I II III IIII V VI VII VIII 1 2 1H 3Li 4Be 5B 6C 7N 8O 9F 2He 10Ne 3 11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar 4 19K 20Ca 31Ga 32Ge 33As 34Se 35Br 36Kr 5 37Rb 38Sr 49In 50Sn 51Sb 52Te 53I 54Xe 6 55Cs 56Ba 81Tl 82Pb 83Bi 84Po 85At 86Rn 7 87Fr 88Ra 113 114 115 116 117 118 p-type Dotiermittel Akzeptor Atome n-type Dotiermittel Donator Atome 5 Das Standardmodell 49 5.1.1 Elementarteilchen und Quarks Elementarteilchen Leptonen leichte Teilchen Mesonen gerade Anzahl von Quarks Neutrinos ... Baryonen schwere Teilchen Hyperonen El kt Elektronen ... Bosonen "Kraftteilchen" Nukleonen Photonen Neutronen Protonen Quarks Quarks ... ... 5.1.2 Leptonen - leichte Teilchen Name Symbol Elektron Müon Tau eµτ- e+ µ+ τ+ Ruhemasse [MeV] 0,511 105,6 1784 LadungSpin -1 +1 -1 +1 -1 +1 mittlere Lebensdauer [s] 1/2 1/2 1/2 stabil 2. 10-6 3. 10-13 El k ElektronN Neutrino i νe⎯νe ? 0 0 1/2 stabil bil ? Müon-Neutrino νµ⎯νµ ? 0 0 1/2 stabil ? Tau-Neutrino ντ ⎯ντ ? 0 0 1/2 stabil ? Leptonen + Quarks = Grundbausteine der Materie + Antimaterie 50 5.1.3 Mesonen - Teilchen aus 2 Quarks Name Symbol Pionen π0 π+ π− K0⎯K0 135 Kaonen Pionen Ruhemasse [MeV] Ladung 0 Quarkaufbau Spin mittlere Lebensdauer [s] u⎯u d⎯d 0 8.10-17 u⎯d d⎯u 0 2,6 .10-8 d⎯s ⎯d s 0 10-10 -5.10- u⎯s 0 1,2.10-8 140 +1 -1 498 0 0 K+ K− 494 +1 -1 J / Psi J/Ψ 3098 0 c⎯c 1 1.10-20 D-Null D0 1863 0 c⎯u 0 1.10-12 D-Plus D+ 1863 1 c⎯d 0 4.10-13 Ypsilon Y 9460 0 b⎯b 1 1.10-20 Kaonen 8 5.1.4 Baryonen Name Symbol y Ruhemasse [MeV] Proton p ⎯p 938,3 Neutron n ⎯n 939,6 Lambda Λ ⎯Λ 1115 Sigma-Plus Σ+ ⎯Σ+ 1189 Sigma-Minus Σ− ⎯Σ− 1197 Sigma-Null Σ0 ⎯Σ0 1192 Xi-Minus Ξ− ⎯Ξ− 1321 Xi-Null Ξ0 ⎯Ξ0 1315 − − Omega-Minus Ω ⎯Ω 1672 Charm-Lambda Λc ⎯Λc 2280 - schwere Teilchen Ladung g +1 0 0 +1 -1 0 -1 0 -1 +1 s⎯u -1 0 0 +1 -1 0 1 0 -1 +1 Quarkaufbau Spin Q p mittlere Lebensdauer [s] u u d ⎯u⎯u⎯d ½ stabil d d u ⎯d⎯d⎯u ½ ca. 900 u d s ⎯u⎯d⎯s ½ 2,6.10-10 u u s ⎯u⎯u⎯s ½ 8.10-11 d d s ⎯d⎯d⎯s ½ 1,5.10-10 u d s ⎯u⎯d⎯s ½ 6.10-20 d s s ⎯d⎯s⎯s ½ 1,6.10-10 u s s ⎯u⎯s⎯s ½ 3.10-10 s s s ⎯s⎯s⎯s ½ 8.10-11 u d c ⎯u⎯d⎯c ½ 2.10-13 51 5.1.5 Eichbosonen Name Symbol Photon W-Teilchen Z-Teilchen Gluon γ W + W− Z g Ruhemasse [MeV] - Austauschteilchen Ladung ? ~83 000 ~93 000 0 Spin 0 1 0 0 mittlere Lebensdauer [s] 1 -1 1 1 stabil 10-25 10-25 stabil Austauschteilchen, übertragen Kräfte 5.1.6 Quarks - Bausteine für Elementarteilchen Name Symbol up down strange charm bottom (beauty) top (truth) u ⎯u d ⎯d s ⎯s c ⎯cc b ⎯b t ⎯t Ruhe Ruhemasse [MeV] ~5 ~10 ~100 ~1500 1500 ~4700 ? Ladung 2/3 - 2/3 -1/3 -1/3 1/3 2/3 -2/3 1/3 -1/3 1/3 2/3 -2/3 Spin mittlere Lebensdauer [s] ½ ½ ½ ½ ½ ½ stabil verschieden verschieden verschieden verschieden verschieden Elementarteilchen aus Quarktripletts : Baryonen Elementarteilchen aus Quarkdubletts: Mesonen 52 5.1.6.1 „Visual“- Quarks top up down bottom strange charm 6 Nuklidkarte In der Nuklidkarte werden alle Atomarten (Nuklide) nach Protonenund Neutronenzahl geordnet. Aus der Nuklidkarte lassen sich Eigenschaften der Nuklide ablesen, z.B. Stabilität oder radioaktive Zerfallsarten 53 6.1 Nuklidbegriff Atome Die stoffliche Welt um uns herum lässt sich zerlegen in kleine einst als unteilbar geglaubte - Teilchen, die als Atome bezeichnet werden. Nuklide Zur Zeit sind ca. 2500 Atomsorten - sogenannte Nuklide - bekannt, die sich auf 115 verschiedene chemische Elemente verteilen verteilen. Davon sind nur 274 Nuklide stabil ! Chemische Elemente Unter einem chemischen Element versteht man einen Stoff, der aus Atomen mit gleichen chemischen Eigenschaften aufgebaut ist. 6.1.1 Schreibweisen Nukleonenzahl Ordnungszahl Schreibweise: Neutron Proton Nukleonenzahl Element Ordnungszahl Element 1 1 1 H 1 4 2 4 He 2 12 6 12 C 6 54 6.1.2 Bekannte Nuklide radioaktiv • C-14 • I-131 • Tc-99 • Cs-137 • U-235 • U-238 aus der Radiocarbonmethode aus der Radiojodtherapie aus aus der Radiologie / Szintigraphie aus dem Reaktorunfall von Tschernobyl aus dem Kernbrennstoff aus dem Kernbrennstoff stabil • C-12 • B-10 • H-2 aus der Radiocarbonmethode aus der Nukleartechnik aus der Nukleartechnik 6.2 Nuklidkarte Isotope p Nuklide weisen die gleiche Ordnungszahl auf und gehören damit zum selben chemischen Element. He He-3 He-4 He-5 He-6 4,002602 0,000137 99,99986 99,99986 806,7 ms 3β− 0,02 n σabs < 0,05 σ 0,00005 H H-1 H-2 H-3 1,00794 99,985 0,015 12,323 a σ 0,332 σ 0,332 σ 0,00052 β- 3,5 Z β− 0,02 n1 10,25 m β− 0,8 N 55 6.2.1 Nuklidkarte FZ Karlsruhe 6.2.1.1 Nuklidkarte Erläuterungen Karlsruher Nuklidkarte: alle bekannten Nuklide X - Achse: Neutronenzahl Y - Achse: Protonenzahl Farben und Symbole: stabile Nuklide Positronzerfall β+ Elektroneneinfang ε Negatronzerfall β- Alphazerfall α Spontanspaltung sf Protonzerfall p Isomerenzerfall Iγ 56 6.2.2 Nuklidkarte TOICD (1) 6.2.2.1 Nuklidkarte TOICD (2) 57 6.3 Zerfallsreihen • Zerfallsreihe: Abfolge g des radioaktiven Zerfalls, die entsteht, wenn ein radioaktives Nuklid seinerseits in ein anderes radioaktives zerfällt (Isotopenfolge). Da die natürlichen Zerfallsarten die Massenzahl des Nuklids entweder unverändert lassen, wie die Gamma- und Betastrahlung oder um vier vermindern, wie die Alphastrahlung, gibt es für schwere natürliche Radionuklide vier verschiedene Zerfallsreihen: Uran-Radium-Reihe: Uran-Actinium-Reihe: Uran Actinium Reihe: Thorium-Reihe: Neptunium-Reihe: • Ausgangsnuklid U-238 Ausgangsnuklid U U-235 235 Ausgangsnuklid Th-232 Ausgangsnuklid Np-237 Endnuklid Pb-206 Endnuklid Pb Pb-207 207 Endnuklid Pb-208 Endnuklid Bi-209 Die 4. Zerfallsreihe kommt in der Natur nicht vor, da das langlebigste Glied 237Np dieser Reihe praktisch vollständig zerfallen ist. http://de.wikipedia.org 6.3.1 Die Uran-Radium-Zerfallsreihe U-238 Th-234 Pa-234 U-234 Th-230 Ra-226 Rn-222 Po-218 α β− α Pb-214 β− Bi-214 α Tl-210 β− α Pb-210 α Hg-206 β− Tl-206 β− Pb-206 α β− β− α α α α β− α β− α At-218 Rn-218 β− Po-214 α Bi-210 β− Po-210 58 6.3.2 Die Uran-Actinium-Zerfallsreihe Th-227 Pb-211 Po-211 U-235 U 235 Th-231 Pa-231 β− Ac-227 α α α α β− β− α Ra-223 Rn-219 Po-215 Bi-211 Pb-207 α β− α α β− β− β− β− α α β− Fr-223 α At-219 α Bi-215 At-215 Tl-207 6.3.3 Die Thorium-Zerfallsreihe β− Po-212 α Th 232 Th-232 Ra-228 Ac-228 Th-228 Ra-224 Rn-220 Po-216 Pb-212 Bi-212 Pb-208 α β− β− α α α α α β− β− Tl-208 59 6.3.4 Die Plutonium-NeptuniumZerfallsreihe β− α Pu-241 Pu 241 Am-241 Np-237 Pa-233 U-233 Th-229 Ra-225 Ac-225 Fr-221 At-217 Bi-213 Tl-209 β− Pb-209 Bi-209 α U-237 α α β− α α β− α α β− α Rn-217 α Po-213 β− 6.4 Nuklidgruppen Isotope Nuklide weisen die gleiche Ordnungszahl auf und gehören damit zum selben chemischen Element Isobare Nuklide haben gleiche Massen, jedoch unterschiedliche Kernladungszahlen. Sie finden sich in den Diagonalreihen der Nuklidkarte. Isotone Nuklide sind Nuklide mit gleicher Neutronenzahl Neutronenzahl. Sie stehen in den senkrechten Reihen der Nuklidkarte. Isomere Nuklide haben zwar gleiche Anzahl von Protonen und Neutronen, besitzen aber unterschiedliche Energien im Atomkern. 60 6.5 Wasserstoffisotope 1 1 2 1 3 1 T 7 Anti-Materie • Zu jedem Teilchen gibt es ein Anti-Teilchen (gleiche Masse, aber entgegengesetzte Ladung) Anti Teilchen in • Tritt ein Teilchen mit seinem Anti-Teilchen Wechselwirkung, so werden beide vernichtet, es entstehen Photonen oder Mesonen • Das Photon ist mit seinem Anti-Teilchen identisch 61 8 Radioaktivität Eigenschaft bestimmter Stoffe, sich ohne äußere Einwirkung umzuwandeln und dabei charakteristische Strahlung auszusenden Alpha-Zerfälle Beta-Zerfälle Gamma Zerfälle Gamma-Zerfälle Röntgenstrahlung Spontanspaltung Spallation u.a. Aussenden von He2+ - Teilchen Aussenden von e-,e+ aus dem Kern Aussenden von Photonen aus dem Kern Aussenden von Photonen aus inneren Elektronenschalen Spaltung eines Atomkernes Zertrümmerung eines Atomkernes 8.1 Aktivität Aktivität = Anzahl der Zerfälle pro Sekunde 1 Becquerel = 1 Zerfall pro Sekunde Symbol : Bq 1 Gramm Radium-226: 37 Milliarden Zerfälle pro Sekunde 37 Milliarden Bq = 1 Curie (Ci) 62 8.1.1 Die natürliche Aktivität eines Standardmenschen Radionuklid Aktivität in Bq K - 40 4 500 C -14 3 800 Rb - 87 650 Pb - 210, Bi - 210, Po - 210 60 Daughters g Rn - 220 30 H-3 25 Be - 7 25 Daughters Rn - 222 15 Sonstige 7 Summe 9 112 (ca. 130 Bq / kg) Quelle: Volkmer – Radiaoaktivität und Strahlenschutz 8.1.2 Spezifische Aktivität in Nahrungsmitteln Stoff Aktivität in Bq / kg KCl vegetarische Nahrungsmittel Rentierleber (Po (Po-210) 210) Paranüsse (Ra- 226) 15 944 40* 222 132 * Mittelwert Quelle: Volkmer – Radiaoaktivität und Strahlenschutz 63 8.1.3 Aktivität eines Frühstücks Nahrungsmittel 120 g Mischbrot 25 g Camenbert 25 g Corned Beef (Jugoslawien) 20 g Nuß-Nougat-Creme 125 ml schwarzer Tee (Türkei) Aktivität in Bq 2,0 0,9 1,2 3,2 6,5 Ni ht Nicht verkehrsfähig ! 100 g Quark 25 g Blaubeeren 0,2 2,4 Quelle: Volkmer – Radiaoaktivität und Strahlenschutz 8.1.4 Aktivität eines Mittagessens Nahrungsmittel 150 g Wildfleisch (Niedersachsen) 60 g Nudeln, gekocht 200 g Maronen (Niedersachsen) Aktivität in Bq 87,2 0,6 210,6 Nicht verkehrsfähig ! 20 g Pfirsich (Konserve, Griechenland) 10 g Preisselbeermus (Skandinavien) 150 g Vanilleeis 50 g Kirschen 1,0 0,0 3,0 16,7 Quelle: Volkmer – Radiaoaktivität und Strahlenschutz 64 8.2 Der radioaktive Zerfall A A t½ t Aktivität Halbwertszeit vergangene Zeit exponentieller Zerfall t t½ Unter Halbwertszeit eines Radionuklids versteht man die Zeit, in der seine Aktivität auf die Hälfte abgeklungen ist 8.2.1 Das Zerfallsgesetz A(t )= A0 ⋅ e A(t) t A0 t½ − ln 2 . t t1 / 2 = Aktivität nach einer Zeit t = vergangene Zeit = Aktivität am Anfang ( t = t0) = Halbwertszeit 65 Übung zum J-131- Zerfall Iod-131 hat eine Halbwertszeit von 8 Tagen Wieviel Bq sind nach 16 Tagen messbar, wenn zum Zeitpunkt t0 die Aktivität 100 000 Bq betrug ? ? Übung zum Cs-137 - Zerfall Beispiel p Cs-137 t1/2 = 30 y A(0) = 1 GBq für t= 0 A(30 y) = ? ? 66 8.2.2 Alpha-Zerfall 226 88 Ra → 222 86 Rn + 4 2 He (4,601 MeV ) + γ (0,186 MeV ) 5,5 % 226 88 Ra → 222 86 Rn + 4 2 He (4,784 MeV ) 94,4% 8.2.2.a Alpha-Zerfall Äußere Bestrahlung unbedeutend Abschirmung durch Papier Inkorporation gefährlich 67 8.2.2.1 Alpha-Strahlung • Teilchenart • Radionuklide • Energie • Reichweite • Energieabgabe • Wechselwirkung • Gefahren • Schutz He- 4 Kerne Z> 80: Pu - 239, Ra - 226, Rn - 222, Am - 241, Po - 210, U - 235 MeV bei 5 MeV ca. 3,5 cm (Luft) der größte Anteil wird auf einmal abgegeben Ionisation, Anregung Inkorporation, Schleimhäute Abschirmung mit Papier, Abstand > 10 cm 8.2.2.2 Alpha-Zerfallsschema http://atom.kaeri.re.kr/cgi-bin/decay?Ra-226%20A 68 8.2.2.3 Absorption von αStrahlung Ionenpaaare pro cm 2000 4000 6000 Ionisation umgebender g Materie Streuung bei kleinen Teilchenenergien um kleine Winkel Reichweite schwergeladener Teilchen ≈ Länge der Teilchenbahn 1 2 3 4 5 6 Wegstrecke [cm] 7 8 He + + + 2e − → He 8.2.3 Beta-Zerfall +υ +υ 137 55 Cs → 137 56 Ba + 0 −1 e 69 8.2.3a Beta-Zerfall Äußere Bestrahlung von untergeordneter Bedeutung Abschirmung durch Plexiglas, Aluminium 8.2.3.1 Beta-Strahlung • Teilchenart • Radionuklide • • • • Energie Reichweite Energieabgabe Wechselwirkungen • Gefahren • Schutz Negatronen, Positronen Negatronen H - 3, C - 14, Sr - 90, Cs - 137 Tl - 204, Co - 60 keV ... MeV bei 1 MeV ca. 4 m (Luft) kontinuierlich Ionisation, Anregung, Bremsstrahlung Streustrahlung, Hautexposition, Schleimhäute Inkorporation Abschirmung mit Al, PMMA 70 8.2.3.2 Beta- Zerfallsschema http://atom.kaeri.re.kr/cgi-bin/decay?Cs-137%20B- 8.2.3.3 Energie von Beta-Strahlung Betateilchen besitzen ein Energiespektrum g p beim Betazerfall entstehen Neutrinos (ν) Zerfallsenergie verteilt sich auf Betateilchen und Neutrinos E Relative Häufigkeit 20 40 60 80 100 Häufigste Energie 1 E ≈ Emax 3 MaximaleEEnergie max 0 0,2 0,4 0,6 0,8 1,0 1,2 1,4 1,6 1,8 Energie [MeV] 71 8.2.3.4 Absorption von β Strahlung Ionisation und Anregung umgebender Materie Streuung Bremsstrahlung Ionenpaare pro cm (β) = 10-2 – 10-3 • Ionenpaare pro cm (α) Reichweite (α) in Luft: cm Reichweite (β) in Luft: cm – m α-Strahlung: dicht ionisierend β-Strahlung locker ionisierend 8.2.4 Gamma-Zerfall 137 m 56 Ba → 137 56 Ba + γ 72 8.2.4.a Gamma-Zerfall Äußere Bestrahlung maßgeblich Abschirmung durch Blei 8.2.4.1 Gamma-Strahlung • Teilchenart • Quellen • • • • Energie Reichweite Energieabgabe Wechselwirkungen • Gefahren • Schutz Photonen Am - 241, Co - 60, I - 131, Ba - 133, Ba - 137m, Tc - 99m keV ... MeV theoretisch ∞ paketweise Streuung, Photoeffekt, Comptoneffekt, Paarbildungseffekt Körper-Exposition, Inkorporporation Abschirmung mit Pb 73 8.2.4.2 Gamma-Zerfallsschema http://atom.kaeri.re.kr/cgi-bin/decay?Cs-137%20B- 8.2.4.3 Absorption von γ -Strahlung Mechanismen zur Absorption von Photonen: Photoeffekt bei kleinen Photonen-Energien (vollständige Absorption in der Atomhülle) Comptoneffekt bei mittleren Photonen-Energien (inkohärente Streuung in der Atomhülle) Paarbildungseffekt bei großen Photonen-Energien (vollständige Absorption im COULOMB-Feld des Atomkerns) Abhängig von der Dichte des Mediums ! 74 8.2.4.4 Photo-, Compton- und Paarbildungseffekt 8.2.4.5 Photoeffekt Einfallendes Photon Photoelektron σ Photo ~ Z5 E7/2 σ Wirkungsquerschnitt Z Ordnungszahl E Photonenenergie 75 8.2.4.5.a Photoeffekt - animiert 8.2.4.6 COMPTON effekt Gestreutes Ph t Photon Einfallendes Photon COMPTON elektron E << me ⋅ c 2 σ COMPTON ( E , Θ) ~ const E >> me ⋅ c 2 σ COMPTON ( E , Θ) ~ 1 E σ Wirkungsquerschnitt Z Ordnungszahl E Photonenenergie θ Einfallswinkel 76 8.2.4.6.a COMPTON effekt animiert 8.2.4.7 Paarbildungseffekt Einfallendes Photon Positron Elektron E > 1,022 MeV σ Paar ~ Z 2 σ Wirkungsquerschnitt Z Ordnungszahl E Photonenenergie 77 8.2.4.7.a Paarbildungseffekt animiert 8.2.5 Beispiele für Zerfälle Radionuklid Häufigkeit Zerfallsart Halbwertzeit t1/2 Tritium Ra - 226 I - 131 Cs - 134 0,00013 % βα/γ β- / γ β/γ U - 235 U - 238 0,720 % 99,28 % 12,346 1,6 . 103 8,04 2,06 2,09 7,030 . 108 4,468 . 109 α, γ, sf * α, γ, sf a a d a h a a * sf bedeutet spontaneous fission = Spontanspaltung Quelle: Volkmer – Radiaoaktivität und Strahlenschutz 78 8.3 Strahlungsenergie 1 J = 1 Nm = 1 Ws 1 eV ist die Energie, die ein Elektron aufnimmt, wenn es beim f i D freien Durchlaufen hl f einer i S Spannung von 1 V b beschleunigt hl i t wird id 1 eV = 1,602 •10-19 J 8.3.1 Energieeinheiten Energieeinheiten J eV kWh cal erg kg u Joule 1 J = 1 N.m Elektronenvolt Kilowattstunde 1 W = 1 kg.m2/s3 = 1 J/s Kalorie Energieeinheit Kilogramm atomare Masseneinheit 79 8.3.2 Umrechnungsfaktoren 1J J MeV kWh cal erg kg 1 6,250E+12 2,778E-07 2,389E-01 1,000E+07 1,113E-17 1 MeV 1,600E-13 1 4,450E-20 3,827E-14 1,602E-06 1,783E-30 1 kWh 3,600E+06 2,247E+19 1 8,600E+05 3,600E+13 4,007E-11 1 cal 4,186E+00 2,613E+13 1,163E-06 1 4,168E+07 4,660E-17 1 erg 1,000E-07 6,242E+05 2,778E-14 2,389E-08 1 1,113E-24 1 kg 8,985E+16 5,610E+29 2,497E+10 2,146E+16 8,987E+23 1 1u 1,492E-10 9,320E+02 4,146E-17 3,546E-11 1,492E-03 1,661E-27 Quelle: Halliday, Resnik, Walker - Physik, Wiley-VCH Verlag 8.4 Strahlendosis: Energiedosis Energiedosis D = absorbierte Energie Definition: Energiemenge, die durch die Strahlung auf eine Masseneinheit 1J übertragen 1 Gray = wird kg Symbol: Gy Alte Einheit: rad (1 Gy = 100 rad) 80 8.5 Strahlendosis: Personendosis Äquivalentdosis Ä i l td i H = Z Zellschädigung ll hädi durch absorbierte Energie H = D ⋅Q Definition: Sievert Energiemenge die auf einen Menschen übertragen wird Energiemenge, wird, abhängig von der Strahlenart Symbol: Sv Alte Einheit: rem (1 Sv=100 rem) H = Personendosis D = Energiedosis Q = Qualitätsfaktoren für Strahlungs- und Gewebeart 8.6 Dosisleistung Unter der Dosisleistung DL versteht man die mit der Zeit aufgenommene (Strahlen)dosis DL = dD • =D dt DL = • dH =H dt DL = Dosisleistung D = Energiedosis H = Äquivalentdosis t = Zeit 81 8.6.1 Das Abstandsgesetz Dosisleistung g einer p punktförmigen g γγ-Strahlungsquelle g q dH A H& = = ΓH ⋅ 2 dt r dH/dt ΓH A r Nuklid ΓH Co-60 Cs-137 I-131 351 88 59 ⎡ µSv ⋅ m 2 ⎤ ⎢ ⎥ ⎣ GBq ⋅ h ⎦ = Gammadosisleistung = Gammadosisleistungskonstante (tabelliert) = Aktivität = Abstand zur Strahlungsquelle Dosisleistung eines Cs-137 Strahlers Beispiel p Cs-137 A = 1 GBq r = 10 m Dosisleistung = ? ? 82 8.7 Strahlenschutz Abstand Abschirmen Aufenthalt Quelle: Volkmer – Rad diaoaktivität und Strahlenschu utz 8.8 Strahlenbelastungen Mean Effective Dose Rate [mSv/a] cosmic radiation terrestric radiation internal natural exposure total natural medical application industrial activities Tschernobyl nuclear weapon tests flights working environment fossile energy nuclear energy industrial products total civilisation Total 0,3 0,4 1,4 2,1 2 0,01 0,01 0 005 0,005 0,005 0,002 0,002 0,001 0,001 2,036 4,136 83 8.8.1 Terrestrische Strahlung Area Anual Dose Mean Anual Dose Maximum [mSv/a] 0,4 [mSv/a] 5 4 55 6 6 175 860 Germany Kerala, Tamil, Nadu (India) Espirito Santo (Brasilia) Ramsar (Iran) Quelle: Volkmer – Radiaoaktivität und Strahlenschutz Dosisleistung [mSv/a] 0,5 1,0 1,5 2 8.8.2 Kosmische Strahlung f e cd 1 2 3 4 5 Höhe über Meeresspiegel [km] c Hamburg d München e Zugspitze f Großglockner Quelle: Volkmer – Radiaoaktivität und Strahlenschutz 84 8.8.3 Natürliche Strahlenexposition Effective Dose Rate [mSv/a] external internal total cosmic 1000 m above sea level 0 m above sea level radio nuclides 0,4 0,27 0,02 0,4 0,27 0,02 0,35 0,006 1,29 0,22 1,89 terrestric K-40 Rb-87 U-nat Th-nat 0,12 0,14 0,17 0,006 1,17 0,08 Σ 0,71 1,45 0,18 Total 2,16 Quelle: Volkmer – Radiaoaktivität und Strahlenschutz 8.8.4 Beispiele für Äquivalentdosen 7000 4000 1000 250 200 0,01 20 6 0,3 2,0 mSv mSv mSv mSv mSv/a mSv mSv/a mSv/a mSv/a mSv/a 2,1 mSv/a <3 mSv/a Strahlentod LD100 Schwere Strahlenkrankheit LD50 "Strahlenkater„ Schwellendosis (erste klinische Effekte) Maximale natürliche Strahlenbelastung (Brasilien, Monazit) 3 h Flug 10 km Höhe Grenzwert für berufliche Strahlenbelastung (Kategorie A) Grenzwert für berufliche Strahlenbelastung g ((Kategorie g B)) Grenzwert für Belastung aus kerntechnischen Anlagen Mittlere Strahlenbelastung durch medizinische Anwendungen Mittlere natürliche Strahlenbelastung D Zusätzliche natürliche Strahlendosis (Beton-, Granitbauten) Quelle: Volkmer – Radiaoaktivität und Strahlenschutz 85 8.8.5 Strahlenbelastung beim Fliegen Effektive Dosis durch Höhenstrahlung g auf ausgewählten g Flugrouten g Abflug Ankunft Dosisbereich* [µSv] Frankfurt Frankfurt Frankfurt Frankfurt Frankfurt Frankfurt Frankfurt Gran Canaria Johannesburg New York Rio de Janeiro Rom San Francisco Singapur 10 - 18 18 - 30 32 - 75 17 - 28 3-6 45 - 110 28 - 50 * Die Schwankungsbreite geht hauptsächlich auf die Einflüsse von Sonnenzyklus und Flughöhe zurück. Quelle: Volkmer – Radiaoaktivität und Strahlenschutz 8.8.6 Strahlenbelastung bei der Raumfahrt Flug Erdumkreisung Erdumkreisung Mondumkreisung Mondlandung Mondlandung APOLLO VII SALJUT 6 / IV APOLLO XI APOLLO XI APOLLO XIV Flugdauer [h] Dosis [mSv] 260 4 200 147 195 209 3,6 55 5,7 6 15 Quelle: Volkmer – Radiaoaktivität und Strahlenschutz 86 9 Kernphysik H-2 + He-3 Æ He-4 + p + 18,35 MeV Energieerzeugung durch Kernfusion (fusion) n + U-235 Æ Cs-137 + Rb-96 + 3n + 210 MeV Energieerzeugung durch Kernspaltung (fission) Bildquelle: Forschungszentrum Karlsruhe 9.1 Nukleonenmassen Nukleon Masse [g] Proton 1,672 x 10-24 24 N Neutron 1 6 4 x 10-24 1,674 Relative Ladung Spin t1/2 Atommasse Betazerfall [u] 1,00728 1,00867 1 0086 +e 0 ½ ½ stabil 12 min i 1 u = 1,660 x 10-24 g = 931,5 MeV 87 9.2 Massendefekt Als Massendefekt bezeichnet man die Differenz zwischen den Ruhemassen gebundener Nukleonen und den Ruhemassen ungebundener Nukleonen. Der Massendefekt ist ein Maß für die Kernbindungsenergie. Massendefekt eines Alphateilchens: Δm = malpha Δm = 4,00151 = 0,0307u ≅ 28 MeV - (2 x mproton + 2 x mneutron) - (2 x 1,00782 + 2 x 1,00866) 9.3 Kernbindungsenergien Mittlere tt e e Kernbindungsenergie e b du gse e g e p pro o Nukleon u eo Massenzahl 88 9.4 Kernfusion Unsere Sonne wandelt in 1 s ca. 600 Millionen Tonnen Wasserstoff in 596 Millionen Tonnen He um Æ 4 Millionen Tonnen Materie werden in Energie umgewandelt ! 9.6 Die 4 fundamentalen Kräfte • Elektromagnetische Kraft Anziehung/Abstoßung von Ladungsträgern (Reichweite: ∞) • Gravitationskraft Anziehung von Massen (Reichweite: ∞) • Starke Kernkraft bindet Nukleonen (ca. 2,0 x 10-13 cm Reichweite) • Schwache Kernkraft bindet Quarks verursacht radioaktiven Beta-Zerfall (ca. 0,5 x 10-13 cm Reichweite) 89 9.7 Kernspaltung Kernspaltung 9.7.1 Nukleare Kettenreaktion 90 9.7.2 Spaltproduktausbeute Ausbeute bei Spaltung von U-235 Massenzahl 9.8 Kernreaktionen Einfang von e-, He++ 0 −1 e + → 40 19 K 40 18 Ar Einfang von Neutronen 1 0 n + B → 10 5 Li + 7 3 He + γ 4 2 91 9.8.1 Künstliche Kernreaktion Reaktion von α-Strahlen mit Stickstoff 14N(α,p)17O 4 2 He + 14 7 N → 18 9 F → O + 17 8 1 1 p 9.8.2 Der Bethe-Weizäcker-Zyklus Kohlenstoff-Stickstoff-Zyklus Bethe-Weizsäcker-Zyklus 12C + 1H 13N 13C 14N + 1H + 1H 15O 15N + 1H → → → → → → 13N +γ 13C + e+ + ν e 14N + γ 15O + γ 15N + e+ + ν e 12C + 4He + 1,95 MeV + 1,37 MeV + 7,54 MeV + 7,35 MeV +1 1,86 86 MeV + 4,96 MeV Lebensdauer 1,3·107 Jahre 7 Minuten 2,7·106 Jahre 3,2·108 Jahre 82 Sekunden 1,12·105 Jahre Energiequelle der schwereren Sterne ! Durchlauf des Zyklus: 3,4·108 Jahren Die Energieerzeugungsrate ist beim Bethe-Weizsäcker-Zyklus proportional zur 15. Potenz der Temperatur http://de.wikipedia.org 92 9.8.3 Die Proton-Proton-Reaktion 1H + 1H e+ + e2H + 1H 3He +3He → → → → 2H + e+ + νe 2γ 2 3He + γ 4He + 1H + 1H 3He + 4He → + e→ 7Li + 1H → 7Be 7Be 7Li 3He 7Be 7Be 8B + 4He → + 1H → 8B → 8Be ↔ + 0,42 MeV + 1,02 1 02 MeV M V + 5,49 MeV + 12,86 MeV +γ + νe 4He + 4He +γ +γ 8Be + e+ + ν e 4He + 4He 10–14 Millionen Kelvin 14–23 Millionen Kelvin >23 Millionen Kelvin Die „Asche“ des Wasserstoffbrennens ist Helium 4He bei Sternen mit Größen bis zur Masse der Sonne http://de.wikipedia.org 10 Kernreaktoren • Leistungsreaktoren – Druckwasserreaktoren – Siedewasserreaktoren – Schneller Brüter – Thorium Hochtemperatur Reaktor • Forschungsreaktoren – Neutronenquellen – Unterrichtsreaktoren – .... 93 10.1 Druckwasserreaktor http://www.kernenergie.de 10.2 Siedewasserreaktor http://www.kernenergie.de 94 10.3 RBMK Reaktor http://www.kernenergie.de 10.4 Sicherheit im KKW http://www.kernenergie.de 95 10.5 Brennelemente Ein Brennelement eines Druckwasserreaktors 530 kg Uran Ein Brennelement eines Siedewasserreaktors 190 kg Uran. Druckwasserreaktor des Kernkraftwerks Emsland 193 Brennelemente Siedewasserreaktor des Kernkraftwerks Krümmel 840 Brennelemente http://www.kernenergie.de 10.6 Brennelementzyklus http://www.kernenergie.de 96 10.7 SUR-100 Reaktor 10.8 Actinidenelemente http://www.kernenergie-wissen.de/transmutation.html jährlich von einem typischen Druckwasserreaktor bei 3.0 GW produziert Nuklide kg/Jahr Halbwertszeit/in Jahren Pu-238 4.52 88 Pu-239 166 2.4 x 104 Pu-240 76.7 6.6 x 103 Pu-241 25.4 14.4 Pu-242 15.5 3.8 x 105 Np-237 14.5 2.1 x 106 Am-241 16.6 432 Am-242m 0.022 141 Am-243 2.99 7.4 x 103 Cm-243 0.011 28.5 Cm-244 0.58 18.1 ber. nach 10 a Lagerung u. typischen Abbrand von 33'000 MWtagen per Tonne Uran 97 10.9 Transmutation Umwandlung g von langlebigen g g Radionukliden in kurzlebige g Np-237, Pu-238, Pu-239, Pu-240, Am-241, Am-243, Cm-243, Cm-244 in abgebrannten Brennelementen erfordern den Nachweis der Sicherheit der Lagerung über sehr lange Zeiträume • die Anregung des Nuklids mit anschließenden Betazerfällen (Umwandlung von Neutronen in Protonen oder umgekehrt) • die Anregung des Nuklids mit anschließendem Abdampfen von Neutronen, Protonen, Alpha-Teilchen usw. • die Spaltung des Nuklids in zwei oder drei große Tochternuklide • die Zertrümmerung des Nuklids (Spallation) in viele kleine Nuklide 11 Radioaktive Abfälle • Entstehung • Klassifizierung nach Aktivität • Klassifizierung nach Wärmeentwicklung • Zwischenlagerung • Endlagerung • Wiederaufbereitung von Kernbrennstoff www.kernenergie.de 98 11.1 Entstehung Nukleare Prozesse • Aktivierung • Spaltprodukte Medizin, Forschung, Industrie • Prüfstrahler • Kontaminierte Gegenstände Uranbergbau Militär 11.2 Klassifizierung nach Bq • schwachaktiv (LAW: low active waste) > 1010 Bq/m3 • mittelaktiv (MAW: medium active waste) 1010 Bq/m3 - 1014 Bq/m3 • hochaktiv (HAW: high active waste) > 1014 Bq/m3 90 % 270 000 m3 10 % 24 000 m3 www.kernenergie.de 99 11.3 Klassifizierung nach Wärmeentwicklung Abfälle mit nicht vernachlässigbarer g Wärmeentwicklung g > 3 Kelvin Abfälle mit vernachlässigbarer Wärmeentwicklung < 3 Kelvin 31.12.2005 waren insgesamt ca. 117.350 m³ radioaktive Reststoffe mit vernachlässigbarer Wärmeentwicklung und ca. 1.850 m³ wärmeentwickelnde radioaktive Reststoffe vorhanden. In dem o. g. B t d am 31.12.2005 Bestand 31 12 2005 an wärmeentwickelnden ä t i k l d Abfäll Abfällen sind i d außer den ausgedienten Brennelementkugeln des ThoriumHochtemperaturreaktors (THTR) keine abgebrannten Brennelemente aus Leistungsreaktoren enthalten. Die THTRBrennelementkugeln wurden vom Betreiber als Abfall deklariert und erscheinen deshalb in der Abfallstatistik. www.kernenergie.de 11.4 Zwischenlager Zur Zeit werden abgebrannte Brennelemente entweder in die beiden zentralen Zwischenlager nach Ahaus (Nordrhein-Westfalen) und Gorleben (Niedersachsen) oder zur Wiederaufarbeitung in ausländische Anlagen transportiert. Um diese Transporte zu minimieren, soll nun auf Wunsch der Bundesregierung zusätzlich die Möglichkeit geschaffen werden, abgebrannte Brennelemente am Kraftwerksstandort zwischen zu lagern. Hierzu sollen Standortzwischenlager errichtet werden, die die Brennelemente bis zu ihrer Einlagerung im Endlager in 30 bis 40 Jahren aufnehmen können. Von den Betreibern der Kernkraftwerke wurden beim Bundesamt für Strahlenschutz Genehmigungsanträge zur Errichtung von Standortzwischenlagern gestellt. Für die Zwischenlagerung werden die Brennelemente in spezielle Transport/Lager-Behälter (Castor®-Behälter) verpackt, die sowohl zum Transport vom Kernkraftwerk zum Zwischenlager als auch als Lagerbehälter dienen. Die 40 cm starke Wandung schirmt die Strahlung ab, an der Außenseite des Behälters angebrachte Kühlrippen gewährleisten eine sichere Wärmeabgabe der durch den Zerfall der Spaltprodukte entstehenden Wärme an die Umgebungsluft. www.kernenergie.de 100 11.5 Endlager Wartungsfreie, zeitlich unbefristete und sichere Beseitigung von radioaktivem Abfall ohne beabsichtigte Rückholbarkeit. In Deutschland wird die Lagerung radioaktiver Abfälle in tiefen geologischen Formationen als die beste Lösung angesehen. Folgende Endlager sind genehmigt, werden untersucht oder waren in Betrieb: Schachtanlage Konrad Salzstock Gorleben Salzbergwerk Asse Morsleben (ERAM) www.kernenergie.de 11.5.1 Schachtanlage Konrad Die am 5. Juni 2002 für die Schachtanlage Konrad erteilte Genehmigung zur Endlagerung von radioaktiven Abfällen (ca. 300.000 Kubikmeter), die eine vernachlässigbare thermische Einwirkung auf das umgebende Gestein haben, ist mit der am 03.04.2007 erfolgten Beschlussfassung des Bundesverwaltungsgerichts in Leipzig rechtskräftig. rechtskräftig Jetzt kann das bisherige Bergwerk zu einem Endlager umgerüstet und schwach- bzw. mittelradioaktive Abfälle ab ca. 2012 sicher endgelagert werden. 101 11.5.2 Salzstock Gorleben Der Salzstock Gorleben wird seit 1979 auf seine Eignung für die Endlagerung aller Arten fester radioaktiver Abfälle untersucht, also auch für die Endlagerung wärmeentwickelnder Abfälle. Eine endgültige Eignungsaussage für den Salzstock Gorleben wird erst nach der untertägigen Erkundung mögli h sein. lich i Di Die B Bewertung t aller ll bisherigen Erkundungsergebnisse bestätigt seine Eignungshöffigkeit. Dennoch hat der Bund die weitere Erkundung seit Ende 2000 zur Klärung standortunabhängiger Endlagerfragen unterbrochen. www.kernenergie.de 11.5.3 Salzbergwerk Asse Im stillgelegten ehemaligen Salzbergwerk Asse bei Wolfenbüttel wurden Verfahren und Techniken zur Endlagerung radioaktiver Abfälle entwickelt und erprobt p und bis 1978 schwachund mittelaktive Abfälle eingelagert. Die Schachtanlage Asse soll 2013 vollständig und sicher verschlossen sein. www.kernenergie.de 102 11.5.4 Morsleben (ERAM) Das Endlager für radioaktive Ab Abfälle Morsleben (ERAM) war bis 1998 das einzige in Betrieb befindliche Endlager für schwachund mittelradioaktive Abfälle in Deutschland. Danach wurde die Einlagerung eingestellt. Bis 1998 waren 36.752 m3 radioaktive Abfälle eingelagert worden. Nach Entscheidung der Bundesregierung wird die Endlagerung nicht wieder aufgenommen. Derzeit wird die Stilllegung des Endlagers vorbereitet, ein entsprechendes Planfeststellungsverfahren ist eingeleitet. www.kernenergie.de 11.6 Wiederaufbereitung Anwendung chemischer Verfahren, um aus dem Kernbrennstoff nach seiner Nutzung im Reaktor (abgebrannter Kernbrennstoff) die Wertstoffe - das noch vorhandene Uran und den neu entstandenen Spaltstoff Plutonium - von den Spaltprodukten, den radioaktiven Abfällen, zu trennen. Großtechnisch mehrjährig erprobt ist zur Wiederaufarbeitung das PUREX-Verfahren. Ein abgebranntes Brennelement hat - wenn man vom Strukturmaterial absieht folgende Zusammensetzung: ca. 96% Uran, 3% Spaltprodukte (Abfall), 1% Plutonium und geringe Anteile von Transuran-Elementen. Das zurückgewonnene Uran und das Plutonium können nach entsprechender chemischer Bearbeitung wieder als Brennstoff in einem Kernkraftwerk eingeset t werden. eingesetzt erden Die in einer Wiedera Wiederaufarbeitungsanlage farbeit ngsanlage mit einem Jahresdurchsatz von 350 t jährlich zurückgewinnbaren Kernbrennstoffe entsprechen bei Einsatz in den heute üblichen Leichtwasserreaktoren der Energiemenge von ca. 10 Mio. t Steinkohle. Durch den Wiederaufarbeitungsprozeß wird der hochaktive Abfall (Spaltprodukte) abgetrennt und durch Verglasung in eine Form gebracht, die eine sichere Endlagerung gewährleistet. www.kernenergie.de 103 12.1 Atomphysiker Hans Bethe Niels Bohr John Chadwick Marie Curie Pierre Curie Paul Dirac Albert Einstein Otto Hahn Liese Meitner Max Planck Robert Oppenheimer Ernest Rutherford Snyder Arnold Sommerfeld Fritz Straßner Carl Friedrich von Weizäcker 12.2 Historisches... ...manchmal musste ich einen ganzen Tag lang eine siedende Masse mit einer Eisenstange umrühren, die fast ebenso groß war wie ich. Abends war ich zum umfallen müde...In das Laboratorium kamen nur sehr wenige Leute: der eine oder der andere Physiker oder Chemiker besuchte uns von Zeit zu Zeit, entweder um unsere Experimente zu sehen, oder um Pierre Curie...um Curie um einen Rat zu bitten. bitten Dann gab es vor der schwarzen Tafel jene Gespräche, an die man so gerne zurückdenkt, weil sie auf das wissenschaftliche Interesse und die Arbeitsintensität stimulierend wirken... Marie Curie um 1900 104 Übungsfragen 1 11. 2. 3. 4. 5. 6. 7. 8 8. 9. 10. 11. 12. Wie kann man Energie definieren ? Was ist die physikalische Einheit der Energie ? Welches Grundprinzip ist bei allen Energieumwandlungen zu berücksichtigen ? Was versteht man unter einem Raumwinkel (EEB1) ? Was versteht man unter einem Mol ? Was ist ein u ? Was ist das SI-System ? Wie kann man Materie definieren ? Welche Erkenntnis gewann man aus d. Experiment von RUTHERFORD ? (EEB1,SSB1) Beschreiben Sie das BOHRsche Atommodell, wo sind die Schwächen ? (EEB1) Wie viele Elektronen können sich maximal in der L-Schale aufhalten ? Erläutern Sie den Welle-Teilchen Dualismus ! (EEB1,SSB1) Übungsfragen 2 13. 13 14. 15. 16. 17. 18. 19. 20. 21. 22. 23. 24. Was versteht man unter der HEISENBERGschen Unschärferelation ? (EEB 1) Was ist eine „stehende Welle“ ? (EEB1) Was versteht man unter einem Orbital ? Was versteht man unter Quantenzahlen, welche kennen Sie und welche Bedeutung haben diese ? (EEB1,SSB1) Nach welchen Prinzipien werden die Elektronenschalen besetzt (Erläuterungen) ? Was sind die Elektronenkonfigurationen von Silizium, Zinn und Blei ? Was sind Nukleonen, welche gibt es ? Woraus bestehen Protonen ? Was sind Quarks ? Zu welchen Elementarteilchengruppen gehören Elektronen, Protonen bzw. Neutronen ? Welche Spektrallinien (Serien) kennt man beim Wasserstoff ? (EEB1,SSB1) Unterscheiden sich die H-Isotope in den Spektralserien ? (EEB1,SSB1) 105 Übungsfragen 3 25. 26. 27. 28. 29. 30. 31. 32. 33. 34. 35. 36. Was versteht man unter der Ordnungszahl g eines Atoms ? Was versteht man unter der Massezahl eines Atoms ? Wodurch unterscheiden sich Haupt- und Nebengruppen im PS ? (SSB1) Was sind Salzbildner ? (SSB1) Welche Elemente sind Erzbildner ? (SSB1) In welcher Gruppe befinden sich Uran und Plutonium ? (SSB1) Was ist das chemische Kurzzeichen für Eisen ? g g ? ((EEB1,SSB1) , ) Was versteht man unter Ionisierungsenergie Was versteht man unter Elektronenaffinität ? (EEB1,SSB1) Was versteht man unter Elektronegativität ? (EEB1,SSB1) Welches Element hat die größte Elektronegativität ? (EEB1,SSB1) Wie viele Nuklide sind bekannt ? Wie viele davon sind stabil ? Übungsfragen 4 37. 38. 39. 40. 41. 42. 43. 44. 45 45. 46. 47. 48. 49. 50. Wo in der Nuklidkarte findet man die stabilen Nuklide ? Nennen Sie die drei Isotope des Wasserstoffs ? Besitzen die Isotope des Wasserstoff unterschiedliche physikalische Eigenschaften? Warum ? Besitzen die Isotope des Kohlenstoff unterschiedliche chemische Eigenschaften ? Warum ? Wie ist das Anti-Photon beschaffen (EEB1,SSB1) Wie ist das Anti-Wasserstoff-Atom aufgebaut ? (EEB1,SSB1) Was versteht man unter isomeren Nukliden ? (EEB1,SSB1) Was versteht man unter Radioaktivität, was ist in diesem Zusammenhang Aktivität ? Welche physikalische Einheit hat die Aktivität ? Was versteht man unter einer nuklearen Kettenreaktion ? Was ist Alpha-Strahlung ? Woher kommen die Elektronen bei Beta-Strahlung ? Was ist die physikalische Dimension für den radioaktiven Zerfall ? Was für Strahlendosen kennen Sie? 106 Übungsfragen 5 51. 52. 53. 54. 55. 56. 57. 58. 59. 60. 61. 62. 63. Wie ist die Einheit für die Äquivalentdosis q definiert ? Wie ist die Einheit für die Energiedosis definiert ? In welchen Einheiten kann man Strahlungsenergie angeben ? Was versteht man unter Dosisleistung Wie groß ist die Dosisleistung in 2 m Abstand eines punktförmigen Cs-137 Strahlers, der eine Aktivität von 20 000 Ci aufweist ? Was ist die mittle Jahresdosis in Deutschland ? Wie hoch ist die tödliche Dosis ? Wie groß ist die Aktivität eines Standardmenschen ? (EEB1,SSB1) Was versteht man unter dem Massendefekt ? Welche 4 fundamentalen Kräfte kennen Sie (Erläuterungen) ? Was ist Kernfusion, bei welchen Nukliden kann man damit Energie gewinnen ? Was ist Kernspaltung, bei welchen Nukliden kann man damit Energie gewinnen ? Was sagt die „Kamelhöckerkurve“ aus ? Literatur 1 1. Chemie für Ingenieure - von Hoinkis Hoinkis, Jan; Lindner Lindner, Eberhard; 2007 Wiley WileyVCH - ISBN 3-527-31798-8 2. Hering - Martin - Stohrer ; Physik für Ingenieure; Springer Verlag Berlin 2002, ISBN 3-540-429-64-6 3. Dobrinski - Krakau – Vogel; Physik für Ingenieure 4. Haliday – Resnick - Walker; Physik; Viley VCH 2001, ISBN 3-527-40366-3 5. Schülerduden Physik, Duden Verlag Mannheim, 2004, ISBN 3-411-05375-5 6. De Pree; Physics made simple; Broadway Books; 2004, ISBN 0-7679-17014 7. Browne; Physics for Engineering and Science; McGraw Hill, 1998, ISBN 007-008498-X B. Bröcker; DTV-Atlas zur Atomphysik; DTV-Verlag, 1993 8. S. Hawking; CD: Eine kurze Geschichte der Zeit; Navigo, 1997 B. Bröcker; DTV-Atlas zur Atomphysik; DTV Verlag 1993 9. Volkmer – Kernenergie Basiswissen; Volkmer – Radiaoaktivität und Strahlenschutz 10. Koelzer, Lexikon der Kernenergie 107 Web-Links http://www.kernenergie.de http://www.kernenergie.de/r2/de/Gut_zu_wissen/Materialien/D ownloads/?navanchor=1010023 http://de.wikipedia.org/wiki/Erde htt // t http://atom.kaeri.re.kr/ k i k/ http://de.wikipedia.org/wiki/Atomphysik#Moderne_Atomphysik http://de.wikipedia.org/wiki/Kernphysik 108