CERTIFECT- Fipronil, (S)-Methoprene, Amitraz
Werbung

ANHANG I
ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS
1
1.
BEZEICHNUNG DES TIERARZNEIMITTELS
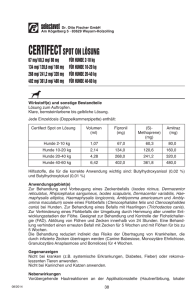
CERTIFECT 67 mg/ 60,3 mg/ 80 mg Spot on Lösung für Hunde 2-10 kg
CERTIFECT 134 mg/ 120,6 mg/ 160 mg Spot on Lösung für Hunde 10-20 kg
CERTIFECT 268 mg/ 241,2 mg/ 320 mg Spot on Lösung für Hunde 20-40 kg
CERTIFECT 402 mg/ 361,8 mg/ 480 mg Spot on Lösung für Hunde 40-60 kg
2.
QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Arzneilich wirksame Bestandteile:
Jede Einzeldosis (Doppelkammerpipette) enthält:
CERTIFECT Spot on
Lösung
Volumen
(ml)
Fipronil
(mg)
(S)-Methoprene
(mg)
Amitraz
(mg)
Hunde 2-10 kg
1,07
67
60,3
80
Hunde 10-20 kg
2,14
134
120,6
160
Hunde 20-40 kg
4,28
268
241,2
320
Hunde 40-60 kg
6,42
402
361,8
480
Hilfsstoffe:
Butylhydroxyanisol (0,02 %)
Butylhydroxytoluol (0,01 %)
Sonstige Bestandteile:
Eine vollständige Auflistung der sonstigen Bestandteile finden Sie unter Abschnitt 6.1.
3. DARREICHUNGSFORM
Lösung zum Auftropfen auf die Haut.
Klare, bernsteinfarbene bis gelbliche Lösung.
4. KLINISCHE
4.1 Z
ANGABEN
ieltierart
Hund
4.2
Anwendungsgebiete unter Angabe der Zieltierart
Zur Behandlung und Vorbeugung eines Zeckenbefalls (Ixodes ricinus, Dermacentor reticulatus,
Rhipicephalus sanguineus, Ixodes scapularis, Dermacentor variabilis, Haemaphysalis elliptica,
Haemaphysalis longicornis, Amblyomma americanum und Amblyomma maculatum) sowie eines
Flohbefalls (Ctenocephalides felis und Ctenocephalides canis) bei Hunden. Zur Behandlung eines
Befalls mit Haarlingen (Trichodectes canis). Zur Verhinderung eines Flohbefalls der Umgebung durch
Hemmung aller unreifer Entwicklungsstadien der Flöhe. Geeignet zur Behandlung und Kontrolle der
Flohstichallergie (FAD). Abtötung von Flöhen und Zecken innerhalb von 24 Stunden. Eine
2
Behandlung verhindert einen erneuten Befall mit Zecken für 5 Wochen und mit Flöhen für bis zu 5
Wochen.
Die Behandlung reduziert indirekt das Risiko der Übertragung von Krankheiten, die durch infizierte
Zecken übertragen werden (Canine Babesiose, Monozytäre Ehrlichiose, Granulozytäre Anaplasmose
und Borreliose) für 4 Wochen.
4.3 Gegenanz
eigen
Nicht bei kranken (z.B. systemische Erkrankungen, Diabetes, Fieber) oder rekonvaleszenten Tieren
anwenden.
Nicht bei Kaninchen und Katzen anwenden.
4.4
Besondere Warnhinweise
Das Tierarzneimittel bleibt auf dem Tier wirksam, wenn es der Sonne ausgesetzt ist oder nachdem der Hund
durch Regen, Baden oder Schwimmen nass geworden ist. Jedoch kann das Shampoonieren oder
Schwimmen im Wasser direkt nach der Behandlung oder häufiges Anwenden von Shampoos die Dauer der
Wirksamkeit vermindern. In diesen Fällen sollte nicht häufiger als alle zwei Wochen behandelt werden.
Behandelte Hunde sollten bis 48 Stunden nach der Behandlung nicht gebadet werden.
Sollte der Hund unbedingt mit Shampoo gewaschen werden müssen, ist es besser, dies vor der
Applikation des Tierarzneimittels zu tun.
Alle Entwicklungsstadien der Flöhe können Körbchen, Liegedecken und gewohnte Ruheplätze des
Hundes befallen, wie z.B. Teppiche und Polstermöbel, die mitbehandelt werden sollten, besonders bei
starkem Flohbefall und zu Beginn der Bekämpfung. Hierfür bieten sich geeignete Mittel zur
Umgebungsbehandlung und anschließendes regelmäßiges Staubsaugen an.
Nach der Behandlung mit CERTIFECT werden die Zecken gewöhnlich innerhalb von 24 Stunden
nach Befall abgetötet und fallen vom Hund ohne vorherige Blutmahlzeit ab. Das Ansaugen einzelner
Zecken nach Behandlung kann jedoch nicht vollkommen verhindert werden. Unter ungünstigen
Bedingungen kann daher eine Übertragung von Infektionskrankheiten nicht völlig ausgeschlossen
werden.
4.5
Besondere Vorsichtsmaßnahmen für die Anwendung
Besondere Vorsichtsmaßnahmen für die Anwendung bei Tieren
Der Kontakt mit den Augen des Hundes ist zu vermeiden.
Nur zum Auftropfen auf die Haut. Nicht oral oder anderweitig verabreichen.
Es ist wichtig, darauf zu achten, dass das Tierarzneimittel auf die trockene Haut und an einer Stelle
aufgetragen wird, die das Tier nicht ablecken kann und dass sich behandelte Tiere nicht gegenseitig
ablecken können.
Die Applikationsstelle kann nach der Behandlung nass oder ölig aussehen.
Der Mindestabstand zwischen zwei Behandlungen soll nicht weniger als 2 Wochen betragen, da die
Verträglichkeit für kürzere Behandlungsintervalle nicht geprüft wurde. Nicht anwenden bei Welpen im
Alter von unter 8 Wochen und bei Hunden mit einem Körpergewicht von weniger als 2 kg.
Innerhalb von 48 Stunden nach Behandlung sollten Hunde von fließenden Gewässern und Flüssen
ferngehalten werden (siehe auch Punkt 6.6).
Besondere Vorsichtsmaßnahmen für den Anwender
Das Tierarzneimittel kann eine Sensibiliserung der Haut, allergische Reaktionen und leichte
Augenreizung beim Menschen verursachen. Tiere oder Anwender, von denen eine
3
Überempfindlichkeit gegen die arzneilich wirksamen Bestandteile oder sonstigen Bestandteile bekannt
ist, sollten den Kontakt vermeiden, da es bei empfindlichen Individuen in sehr seltenen Fällen zu
Irritationen der Atemwege und zu Hautreaktionen kommen kann. Die Verwendung von
Schutzhandschuhen wird empfohlen.
Der direkte Kontakt mit der Applikationsstelle soll vermieden werden. Kinder sollten nicht mit
behandelten Hunden spielen, bevor die Applikationsstelle trocken ist. Deshalb empfiehlt es sich,
Hunde nicht während des Tages, sondern in den frühen Abendstunden zu behandeln. Frisch
behandelte Tiere sollten nicht in engem Kontakt mit den Besitzern, insbesondere nicht mit Kindern,
schlafen.
Dieses Tierarzneimittel enthält Amitraz, das im Einzelfall bei Personen zu neurologischen
Nebenwirkungen führen kann. Amitraz ist ein Monoamino-Oxidase-Hemmer (MAO-Hemmer); daher
sollten Anwender, die Medikamente mit MAO-Hemmern einnehmen, beim Umgang mit dem
Tierarzneimittel besonders vorsichtig sein. Um die Möglichkeit des Einatmens zu verringern, sollte die
Behandlung im Freien oder in einem gut belüfteten Raum stattfinden.
Während der Anwendung nicht rauchen, trinken oder essen.
Hände nach der Anwendung sorgfältig waschen. Gebrauchte Pipetten sind unverzüglich zu beseitigen.
Zur Aufbewahrung die Pipetten in der ungeöffneten Folienverpackung belassen.
Bei versehentlicher Hautkontamination sofort mit Wasser und Seife abwaschen.
Nach versehentlichem Kontakt mit dem Auge dieses sofort sorgfältig mit klarem Wasser ausspülen.
Bei Nebenwirkungen ist unverzüglich ein Arzt zu Rate zu ziehen und die Packungsbeilage oder die
Packung vorzuzeigen.
4.6
Nebenwirkungen (Häufigkeit und Schwere)
Vorübergehende Hautreaktionen an der Applikationsstelle (Hautverfärbung, lokaler Haarausfall,
Juckreiz, Erythem) und generalisierter Juckreiz oder Haarausfall können in seltenen Fällen auftreten.
Nach Ablecken der Applikationsstelle können vermehrtes Speicheln, Erbrechen, Hyperglykämie,
erhöhte Empfindlichkeit auf Reize, Lethargie, Bradykardie oder Bradypnoe auftreten. Diese
Symptome sind vorübergehend und klingen gewöhnlich ohne Behandlung innerhalb von 24 Stunden
wieder ab.
4.7
Anwendung während der Trächtigkeit oder Laktation
Die Unbedenklichkeit des Tierarzneimittels bei Zuchttieren, während der Trächtigkeit und Laktation
wurde durch mehrfach wiederholte Anwendung der bis zur dreifachen empfohlenen Dosis im 28 TageBehandlungsintervall nachgewiesen.
Kann während der Trächtigkeit und Laktation angewendet werden.
4.8
Wechselwirkungen mit anderen Arzneimitteln und andere Wechselwirkungen
Keine Daten verfügbar.
4.9
Dosierung und Art der Anwendung
Dosierung:
Die empfohlene Mindestdosis beträgt 6,7 mg/kg Körpergewicht für Fipronil, 6 mg/kg für (S)Methopren und 8 mg/kg für Amitraz.
4
Jede Einzeldosis (Doppelkammerpipette) enthält:
CERTIFECT Spot on
Lösung
Hunde 2-10 kg
Volumen (ml)
1,07
Fipronil
(mg)
67
(S)-Methoprene
(mg)
60,3
Amitraz
(mg)
80
Hunde 10-20 kg
2,14
134
120,6
160
Hunde 20-40 kg
4,28
268
241,2
320
Hunde 40-60 kg
6,42
402
361,8
480
Behandlungsplan:
Monatliche Anwendung in Abhängigkeit der lokalen epidemiologischen Situation während der
Zecken- und/oder Flohsaison.
Hinweis zur richtigen Anwendung:
Wählen Sie die zum Gewicht des Hundes passende Pipettengröße. Bei Hunden mit einem
Körpergewicht von über 60 kg benutzen Sie die Kombination zweier Pipettengrößen, die dem
Körpergewicht am genauesten entspricht.
Art der Anwendung:
Bei der Packung mit 3 Pipetten trennen Sie zuerst einen Blister entlang der Perforierung von den
anderen ab. Schneiden Sie den Blister entlang der gepunkteten Linie mit einer Schere auf (oder falten
Sie, wie beschrieben, die Ecke des Blisters und ziehen die Folie ab).
Entnehmen Sie die Pipette und halten Sie diese aufrecht. Schneiden Sie die Spitze der Pipette mit einer
Schere ab. Das Fell des Tieres scheiteln, bis die Haut sichtbar wird. Setzen Sie die Spitze der Pipette
auf die Haut auf und drücken Sie die Hälfte des Pipetteninhaltes am Nacken in der Mitte zwischen der
Schädelbasis und den Schulterblättern aus. Wiederholen Sie diesen Vorgang an der Basis des Nackens
vor den Schulterblättern, um die Pipette vollständig zu entleeren.
4.10 Überdosierung (Symptome, Notfallmaßnahmen, Gegenmittel), falls erforderlich
Die Verträglichkeit des Tierarzneimittels wurde bei gesunden erwachsenen Hunden, die bis zu 6 mal
in 2-wöchigem Abstand mit einer bis zur 5-fach erhöhten Dosis behandelt wurden, und bei Welpen
mit einer einmaligen Behandlung im Alter von 8 Wochen nachgewiesen.
Die Unbedenklichkeit des Tierarzneimittels bei Zuchttieren, während der Trächtigkeit und Laktation
wurde durch mehrfach wiederholte Anwendung der bis zur dreifachen empfohlenen Dosis im 28 TageBehandlungsintervall nachgewiesen.
Im Falle einer Überdosierung kann das Risiko des Auftretens von Unverträglichkeiten (siehe Punkt
4.6) steigen, sodass es wichtig ist, die Tiere immer mit der korrekten Pipettengröße gemäß ihrem
Körpergewicht zu behandeln.
Die bekannten unerwünschten Arzneimittelwirkungen von Amitraz und seinen Metaboliten beruhen
auf agonistischen Wirkungen an alpha2-Adrenorezeptoren, zu denen Hypersalivation, Erbrechen,
Lethargie, Hyperglykämie, Bradykardie oder Bradypnoe gehören können. Diese Symptome sind
vorübergehend und verschwinden gewöhnlich ohne Behandlung innerhalb von 24 Stunden.
Sollten die Symptome schwerwiegend sein oder andauern, kann als Antidot Atipamezol-Hydrochlorid
als alpha2-Adrenorezeptor-Antagonist verwendet werden.
4.11 Wartez eit
Nicht zutreffend.
5
5. PHARMAKOLOGISCHE
EIGENSCHAFTEN
Pharmakotherapeutische Gruppe: Ektoparasitika zur lokalen Anwendung, ATCvet-Code: QP53AX65
Das Tierarzneimittel ist eine insektizide und akarizide Lösung zum Auftropfen auf die Haut. Es enthält
Fipronil und Amitraz als adultizid wirksame Bestandteile in Kombination mit dem ovizid und larvizid
wirksamen Bestandteil (S)-Methopren.
5.1 Pharm
akodynamische Eigenschaften
Fipronil ist ein Insektizid und Akarizid aus der Phenylpyrazol-Familie. Die Wirkung von Fipronil und
seinem Metaboliten Fipronil-Sulfon beruht auf einer Interaktion mit Liganden-gesteuerten
Chloridionenkanälen, insbesondere mit solchen, die auf den Neurotransmitter Gamma-Aminobuttersäure (GABA) sowie auf desensitisierende (D) und nicht-desensitisierende (N) Glutamat-Kanäle
(Glu, nur bei Wirbellosen vorkommende Liganden-gesteuerte Chloridionenkanäle) ansprechen.
Hierbei kommt es zur Hemmung des prä- und postsynaptischen Chloridionenaustausches durch die
Zellmembranen. Infolge der gestörten ZNS-Aktivitäten tritt der Tod der Insekten oder Spinnentiere
ein.
(S)-Methopren ist ein Wachstumsregulator für Insekten (IGR) aus der Wirkstoffgruppe der
Juvenilhormon-Analoga, der die Entwicklung der unreifen Stadien der Insekten hemmt. Diese
Substanz imitiert die Wirkung des Juvenilhormons und führt zu einer gestörten Entwicklung und
damit zum Tod der unreifen Flohstadien. Die ovizide Wirkung von (S)-Methopren auf dem Tier
resultiert entweder daraus, dass der Wirkstoff die Eischale frisch gelegter Floheier durchdringt, oder
dass er durch die Kutikula der adulten Flöhe aufgenommen wird. (S)-Methopren verhindert ebenso die
Entwicklung von Larven und Puppen, so dass die Umgebung des behandelten Tieres von diesen
Stadien freigehalten werden kann.
Amitraz ist ein Formamidin-Akarizid, das als Agonist an Oktopaminrezeptoren wirkt und eine
Überstimulation der oktopaminergen Synapsen bewirkt und somit zu Übererregbarkeit und Krämpfen
bei Spinnentieren führt. Zusätzlich führt der Wirkstoff bei Akariden in subletalen Dosen zu Anorexie
und unterdrückt deren Reproduktionsfähigkeit. Amitraz hat spezifische Zecken-ablösende
Eigenschaften, dabei ziehen die Zecken ihre Mundwerkzeuge schnell aus dem Wirt zurück und fallen
von ihm ab. Diese Wirkung wird als expellierend bezeichnet.
Die Kombination aus Fipronil und Amitraz wirkt an verschiedenen Stellen im Nervensystem der
Zecken. Für eine niedrige Dosis Amitraz und Fipronil wurde ein synergistischer Effekt gegen Zecken
nachgewiesen. Dieser führt zu einer schnelleren Abtötung (die bereits nach 2 Stunden beginnt und
nach 24 Stunden bei mehr als 90 % liegt) sowie zu einer längeren Wirkungsdauer im Vergleich zum
einzeln angewandten Wirkstoff.
Die Behandlung mit CERTIFECT bei einem Hund mit Zeckenbefall führt zum Ablösen der Zecken,
unterbricht das Ansaugen und tötet die Zecken schnell innerhalb von 24 Stunden ab. Somit wird die
Blutmahlzeit und das damit einhergehende Risiko der Übertragung von Erregern, die durch Zecken
übertragen werden, verhindert. Das Risiko der Entstehung einer Caninen Babesiose, Monozytären
Ehrlichiose, Granulozytären Anaplasmose und Borreliose wird damit indirekt für 4 Wochen reduziert.
In Studien wurde nachgewiesen, dass es beim Säugetier keine pharmakodynamischen und
pharmakokinetischen Wechselwirkungen zwischen Fipronil, (S)-Methopren und Amitraz gibt.
5.2
Angaben zur Pharmakokinetik
Die systemische Absorption nach topischer Anwendung ist für alle drei wirksamen Bestandteile von
CERTIFECT gering.
6
Fipronil: Die absolute Bioverfügbarkeit liegt bei 9,5 %. Die durchschnittliche Höchstkonzentration
(cmax) im Plasma beträgt nach 5 Tagen 19 ng/ml (tmax). Etwa 33 Tage nach topischer Anwendung lag
die Plasmakonzentration unter 1 ng/ml (Bestimmungsgrenze).
(S)-Methopren und Amitraz: Die Resorption über die Haut ist sehr gering und Plasmakonzentrationen
lagen für (S)-Methopren unterhalb der Bestimmungsgrenze (10 ng/ml) und waren für Amitraz in den
meisten Proben nicht nachweisbar (< 0,75 ng/ml).
Metabolismus, Ausscheidung und Verteilung:
Das Hauptabbauprodukt von Fipronil auf dem Haarkleid des Hundes und im Blut ist das SulfonDerivat. Fipronilsulfon entsteht auf dem Haarkleid (durchschnittliche Konzentration < 16 % der
Fipronilkonzentration während des ersten Monats nach der Behandlung).
(S)-Methopren wird vollständig zu Kohlendioxid und Acetat abgebaut, die nachfolgend als endogene
Baustoffe Verwendung finden.
Amitraz wird im Fell des Hundes zu N-Methyl-N´-(2,4-xylyl)-Formamidin abgebaut (< 5 % der
Amitrazkonzentration). Sehr geringe, vernachlässigbare Mengen an Dimethylanilin, einem
Nebenprodukt beim Abbau von Amitraz, wurden ebenso nach der Behandlung im Haarkleid des
Hundes festgestellt.
In einer pharmakokinetischen Studie bei Hunden mit den Wirkstoffen einzeln und in Kombination
wurde gezeigt, dass keine Wechselwirkungen bestehen, die die pharmakokinetischen Eigenschaften
beeinträchtigen.
Die drei arzneilich wirksamen Bestandteile werden während der ersten Woche nach Applikation gut
über das Haarkleid des Hundes verteilt. Die Konzentrationen von Fipronil, Fipronilsulfon, Amitraz
und (S)-Methopren im Fell nehmen mit der Zeit ab und sind bis mindestens 58 Tage nach Applikation
nachweisbar. Die Hauptmetaboliten werden über das gesamte Fell des Hundes verteilt. Die
Fipronilsulfonkonzentration nahm bis Tag 58 nach topischer Applikation bis auf < 0,6 µg/g ab.
Niedrige Mengen an N-Methyl-N´-(2,4-xylyl)-Formamidin konnten bis zu 30 Tagen nach der
Anwendung festgestellt werden.
5.3 Um
weltverträglichkeit
Siehe Punkt 6.6.
6. PHARMAZ
6.1
EUTISCHE ANGABEN
Verzeichnis der sonstigen Bestandteile
Butylhydroxyanisol (E320)
Butylhydroxytoluol (E321)
Ethanol, wasserfrei
Polysorbat 80 (E433)
Povidon
Diethylenglycolmonoethylether
Octylacetat
6.2 Inkompatibilitäten
Keine bekannt.
6.3
Dauer der Haltbarkeit
Haltbarkeit des Tierarzneimittels im unversehrten Behältnis: 18 Monate.
6.4 Besondere
Lagerungshinweise
7
In der Originalverpackung aufbewahren
6.5
Art und Beschaffenheit des Behältnisses
Violette Doppelkammerpipette: Das Primärbehältnis besteht aus zwei hitzegeformten Kammern aus
Polyolefin mit einer Trennwand aus mit Polyolefin beschichtetem Aluminium in der Mitte. Die
Sekundärverpackung besteht aus einem Blister aus Plastik und Aluminium, der mit Plastik und
Aluminium ausgekleidet ist.
CERTIFECT Spot on
Lösung
Volumen (ml)
Plastikbehältnis
Karton
Hunde 2-10 kg
1,07
1 Pipette
3 Pipetten
Hunde 10-20 kg
2,14
1 Pipette
3 Pipetten
Hunde 20-40 kg
4,28
1 Pipette
3 Pipetten
Hunde 40-60 kg
6,42
1 Pipette
3 Pipetten
Es werden möglicherweise nicht alle Packungsgrößen in Verkehr gebracht.
6.6
Besondere Vorsichtsmaßnahmen für die Entsorgung nicht verwendeter Tierarzneimittel
oder bei der Anwendung entstehender Abfälle
Nicht verwendete Tierarzneimittel oder davon stammende Abfallmaterialien sind entsprechend den
nationalen Vorschriften zu entsorgen.
Das Tierarzneimittel darf nicht in Gewässer gelangen, da es eine Gefahr für Fische und andere
Wasserorganismen darstellen kann.
7. Z
ULASSUNGSINHABER
MERIAL
29, avenue Tony Garnier
F-69007 Lyon
Frankreich
8.
ZULASSUNGSNUMMER(N)
EU/0/00/000/000
9.
DATUM DER ERTEILUNG DER ERSTZULASSUNG / VERLÄNGERUNG DER
ZULASSUNG
10.
STAND DER INFORMATION
Detaillierte Angaben zu diesem Tierarzneimittel finden Sie auf der Website der Europäischen
Arzneimittel-Agentur unter http://www.ema.europa.eu/.
8
VERBOT DES VERKAUFS, DER ABGABE UND/ODER DER ANWENDUNG
Nicht zutreffend.
9
ANHANG II
A.
INHABER DER HERSTELLUNGSERLAUBNIS, DER FÜR DIE
CHARGENFREIGABE VERANTWORTLICH IST
B.
BEDINGUNGEN ODER BESCHRÄNKUNGEN DER GENEHMIGUNG FÜR
DAS INVERKEHRBRINGEN IN BEZUG AUF ABGABE UND ANWENDUNG
C.
BEDINGUNGEN ODER BESCHRÄNKUNGEN DER GENEHMIGUNG FÜR
DAS INVERKEHRBRINGEN FÜR EINE SICHERE UND WIRKSAME
ANWENDUNG DES TIERARZNEIMITTELS
D.
ANGABE DER RÜCKSTANDSHÖCHSTMENGEN (MRLs)
10
A.
INHABER DER HERSTELLUNGSERLAUBNIS, DER FÜR DIE
CHARGENFREIGABE VERANTWORTLICH IST
Name und Anschrift des für die Chargenfreigabe verantwortlichen Herstellers
MERIAL
4, Chemin du Calquet
F-31300 Toulouse Cedex
Frankreich
B.
BEDINGUNGEN ODER BESCHRÄNKUNGEN DER GENEHMIGUNG FÜR DAS
INVERKEHRBRINGEN IN BEZUG AUF ABGABE UND ANWENDUNG
Nur auf tierärztliche Verschreibung abzugeben.
C.
BEDINGUNGEN ODER BESCHRÄNKUNGEN DER GENEHMIGUNG FÜR DAS
INVERKEHRBRINGEN FÜR EINE SICHERE UND WIRKSAME ANWENDUNG DES
TIERARZNEIMITTELS
Nicht zutreffend.
D.
ANGABE DER RÜCKSTANDSHÖCHSTMENGEN (MRLs)
Nicht zutreffend.
11
ANHANG III
KENNZEICHNUNG UND PACKUNGSBEILAGE
12
A. KENNZEICHNUNG
13
ANGABEN AUF DER ÄUSSEREN UMHÜLLUNG
Packung mit 3 Pipetten
1.
BEZEICHNUNG DES TIERARZNEIMITTELS
CERTIFECT 67 mg/ 60,3 mg/ 80 mg Spot on Lösung für Hunde 2-10 kg
CERTIFECT 134 mg/ 120,6 mg/ 160 mg Spot on Lösung für Hunde 10-20 kg
CERTIFECT 268 mg/ 241,2 mg/ 320 mg Spot on Lösung für Hunde 20-40 kg
CERTIFECT 402 mg/ 361,8 mg/ 480 mg Spot on Lösung für Hunde 40-60 kg
2.
WIRKSTOFF(E) UND SONSTIGE BESTANDTEILE
Fipronil 67,0 mg, (S)-Methoprene 60,3 mg, Amitraz 80,0 mg
Fipronil 134,0 mg, (S)-Methoprene 120,6 mg, Amitraz 160,0 mg
Fipronil 268,0 mg, (S)-Methoprene 241,2 mg, Amitraz 320,0 mg
Fipronil 402,0 mg, (S)-Methoprene 361,8 mg, Amitraz 480,0 mg
3. DARREICHUNGSFORM
Spot on Lösung
4. PACKUNGSGRÖSSE(N)
3 x 1,07 ml
3 x 2,14 ml
3 x 4,28 ml
3 x 6,42 ml
5. Z
IELTIERART(EN)
Hunde (2-10 kg)
Hunde (10-20 kg)
Hunde (20-40 kg)
Hunde (40-60 kg)
6. ANWENDUNGSGEBIET(E)
Zur Behandlung und Vorbeugung eines Befalls mit Zecken und Flöhen.
Lesen Sie vor der Anwendung die Packungsbeilage.
7.
ART DER ANWENDUNG
Schneiden Sie die Pipettenspitze mit der Schere ab.
Lesen Sie vor der Anwendung die Packungsbeilage.
8. WARTEZ
EIT
14
9.
BESONDERE WARNHINWEISE, SOWEIT ERFORDERLICH
Lesen Sie vor der Anwendung die Packungsbeilage.
Nicht bei Katzen anwenden.
10. VERFALLDATUM
Verwendbar bis
11. BESONDERE
LAGERUNGSBEDINGUNGEN
Lesen Sie vor der Anwendung die Packungsbeilage.
12.
BESONDERE VORSICHTSMAßNAHMEN FÜR DIE ENTSORGUNG VON NICHT
VERWENDETEN ARZNEIMITTELN ODER VON ABFALLMATERIALIEN, SOFERN
ERFORDERLICH
Lesen Sie vor der Anwendung die Packungsbeilage.
13.
VERMERK "FÜR TIERE" SOWIE BEDINGUNGEN ODER BESCHRÄNKUNGEN
FÜR EINE SICHERE UND WIRKSAME ANWENDUNG DES TIERARZNEIMITTELS,
sofern erforderlich
Für Tiere. Verschreibungspflichtig.
14.
KINDERWARNHINWEIS "AUSSER REICH- UND SICHTWEITE VON KINDERN
AUFBEWAHREN"
Arzneimittel unzugänglich für Kinder aufbewahren.
15.
NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS
MERIAL
29, avenue Tony Garnier
F-69007 Lyon
16. Z
ULASSUNGSNUMMER(N)
EU/0/00/000/000
EU/0/00/000/000
EU/0/00/000/000
EU/0/00/000/000
17.
CHARGENBEZEICHNUNG DES HERSTELLERS
15
Ch.-B.
16
ANGABEN AUF DER ÄUSSEREN UMHÜLLUNG
Packung mit 1 Pipette
1.
BEZEICHNUNG DES TIERARZNEIMITTELS
CERTIFECT 67 mg/ 60,3 mg/ 80 mg Spot on Lösung für Hunde 2-10 kg
CERTIFECT 134 mg/ 120,6 mg/ 160 mg Spot on Lösung für Hunde 10-20 kg
CERTIFECT 268 mg/ 241,2 mg/ 320 mg Spot on Lösung für Hunde 20-40 kg
CERTIFECT 402 mg/ 361,8 mg/ 480 mg Spot on Lösung für Hunde 40-60 kg
2.
WIRKSTOFF(E) UND SONSTIGE BESTANDTEILE
Fipronil 67,0 mg, (S)-Methoprene 60,3 mg, Amitraz 80,0 mg
Fipronil 134,0 mg, (S)-Methoprene 120,6 mg, Amitraz 160,0 mg
Fipronil 268,0 mg, (S)-Methoprene 241,2 mg, Amitraz 320,0 mg
Fipronil 402,0 mg, (S)-Methoprene 361,8 mg, Amitraz 480,0 mg
3. DARREICHUNGSFORM
Spot on Lösung
4. PACKUNGSGRÖSSE(N)
1 x 1,07 ml
1 x 2,14 ml
1 x 4,28 ml
1 x 6,42 ml
5. Z
IELTIERART(EN)
Hunde (2-10 kg)
Hunde (10-20 kg)
Hunde (20-40 kg)
Hunde (40-60 kg)
6. ANWENDUNGSGEBIET(E)
Zur Behandlung und Vorbeugung eines Befalls mit Zecken und Flöhen.
Lesen Sie vor der Anwendung die Packungsbeilage.
7.
ART DER ANWENDUNG
Lesen Sie vor der Anwendung die Packungsbeilage.
Schneiden Sie die Pipettenspitze mit der Schere ab.
17
8. WARTEZ
9.
EIT
BESONDERE WARNHINWEISE, SOWEIT ERFORDERLICH
Lesen Sie vor der Anwendung die Packungsbeilage.
Nicht bei Katzen anwenden.
10. VERFALLDATUM
Verwendbar bis
11. BESONDERE
LAGERUNGSBEDINGUNGEN
Lesen Sie vor der Anwendung die Packungsbeilage.
12.
BESONDERE VORSICHTSMAßNAHMEN FÜR DIE ENTSORGUNG VON NICHT
VERWENDETEN ARZNEIMITTELN ODER VON ABFALLMATERIALIEN, SOFERN
ERFORDERLICH
Lesen Sie vor der Anwendung die Packungsbeilage.
13.
VERMERK "FÜR TIERE" SOWIE BEDINGUNGEN ODER BESCHRÄNKUNGEN
FÜR EINE SICHERE UND WIRKSAME ANWENDUNG DES TIERARZNEIMITTELS,
sofern erforderlich
Für Tiere. Verschreibungspflichtig.
14.
KINDERWARNHINWEIS "AUSSER REICH- UND SICHTWEITE VON KINDERN
AUFBEWAHREN"
Arzneimittel unzugänglich für Kinder aufbewahren.
15.
NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS
MERIAL
29, avenue Tony Garnier
F-69007 Lyon
16. Z
ULASSUNGSNUMMER(N)
EU/0/00/000/000
EU/0/00/000/000
EU/0/00/000/000
EU/0/00/000/000
18
17.
CHARGENBEZEICHNUNG DES HERSTELLERS
Ch.-B.
19
MINDESTANGABEN AUF BLISTERPACKUNGEN ODER FOLIENSTREIFEN
Für alle Handelsformen
1.
BEZEICHNUNG DES TIERARZNEIMITTELS
CERTIFECT
1,07 ml
2,14 ml
4,28 ml
6,42 ml
2. Z
ULASSUNGSINHABER
MERIAL
3. VERFALLDATUM
EXP
4. CHARGENBEZ
EICHNUNG
Lot
5.
VERMERK " FÜR TIERE"
Für Tiere
20
MINDESTANGABEN AUF DER PIPETTE
1.
BEZEICHNUNG DES TIERARZNEIMITTELS
CERTIFECT
1,07 ml
2,14 ml
4,28 ml
6,42 ml
2. Z
ULASSUNGSINHABER
MERIAL
3. VERFALLDATUM
{MM/JJJJ}
4. CHARGENBEZ
EICHNUNG
{Nummer}
21
B. PACKUNGSBEILAGE
22
GEBRAUCHSINFORMATION
(Karton mit 3 Pipetten)
CERTIFECT 67 mg/ 60,3 mg/ 80 mg Spot on Lösung für Hunde 2-10 kg
CERTIFECT 134 mg/ 120,6 mg/ 160 mg Spot on Lösung für Hunde 10-20 kg
CERTIFECT 268 mg/ 241,2 mg/ 320 mg Spot on Lösung für Hunde 20-40 kg
CERTIFECT 402 mg/ 361,8 mg/ 480 mg Spot on Lösung für Hunde 40-60 kg
1.
NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN
UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
VERANTWORTLICH IST
Zulassungsinhaber:
MERIAL
29, avenue Tony Garnier
F-69007 Lyon
Frankreich
Für die Chargenfreigabe verantwortlicher Hersteller:
MERIAL
4, Chemin du Calquet
F-31300 Toulouse-Cedex
Frankreich
2.
BEZEICHNUNG DES TIERARZNEIMITTELS
CERTIFECT 67 mg/ 60,3 mg/ 80 mg Spot on Lösung für Hunde 2-10 kg
CERTIFECT 134 mg/ 120,6 mg/ 160 mg Spot on Lösung für Hunde 10-20 kg
CERTIFECT 268 mg/ 241,2 mg/ 320 mg Spot on Lösung für Hunde 20-40 kg
CERTIFECT 402 mg/ 361,8 mg/ 480 mg Spot on Lösung für Hunde 40-60 kg
3.
WIRKSTOFF(E) UND SONSTIGE BESTANDTEILE
Lösung zum Auftropfen.
Klare, bernsteinfarbene bis gelbliche Lösung.
Jede Einzeldosis (Doppelkammerpipette) enthält:
CERTIFECT Spot on
Lösung
Volumen
(ml)
Fipronil
(mg)
(S)-Methoprene
(mg)
Amitraz
(mg)
Hunde 2 10 kg
1,07
67
60,3
80
Hunde 10-20 kg
2,14
134
120,6
160
Hunde 20-40 kg
4,28
268
241,2
320
Hunde 40-60 kg
6,42
402
361,8
480
Hilfsstoffe, die für die korrekte Anwendung wichtig sind: Butylhydroxyanisol (0,02 %) und
Butylhydroxytoluol (0,01 %)
23
4. ANWENDUNGSGEBIET(E)
Zur Behandlung und Vorbeugung eines Zeckenbefalls (Ixodes ricinus, Dermacentor reticulatus,
Rhipicephalus sanguineus, Ixodes scapularis, Dermacentor variabilis, Haemaphysalis elliptica,
Haemaphysalis longicornis, Amblyomma americanum und Amblyomma maculatum) sowie eines
Flohbefalls (Ctenocephalides felis und Ctenocephalides canis) bei Hunden. Zur Behandlung eines
Befalls mit Haarlingen (Trichodectes canis). Zur Verhinderung eines Flohbefalls der Umgebung durch
Hemmung aller unreifer Entwicklungsstadien der Flöhe. Geeignet zur Behandlung und Kontrolle der
Flohstichallergie (FAD). Abtötung von Flöhen und Zecken innerhalb von 24 Stunden. Eine
Behandlung verhindert einen erneuten Befall mit Zecken für 5 Wochen und mit Flöhen für bis zu 5
Wochen.
Die Behandlung reduziert indirekt das Risiko der Übertragung von Krankheiten, die durch infizierte
Zecken übertragen werden (Canine Babesiose, Monozytäre Ehrlichiose, Granulozytäre Anaplasmose
und Borreliose) für 4 Wochen.
5. GEGENANZ
EIGEN
Nicht bei kranken (z.B. systemische Erkrankungen, Diabetes, Fieber) oder rekonvaleszenten Tieren
anwenden.
Nicht bei Kaninchen und Katzen anwenden.
6. NEBENWIRKUNGEN
Vorübergehende Hautreaktionen an der Applikationsstelle (Hautverfärbung, lokaler Haarausfall,
Juckreiz, Erythem) und generalisierter Juckreiz oder Haarausfall können in seltenen Fällen auftreten.
Nach Ablecken der Applikationsstelle können vermehrtes Speicheln, Erbrechen, Hyperglykämie,
erhöhte Empfindlichkeit auf Reize, Lethargie, Bradykardie oder Bradypnoe auftreten. Diese
Symptome sind vorübergehend und klingen gewöhnlich ohne Behandlung innerhalb von 24 Stunden
wieder ab.
Falls Sie Nebenwirkungen, insbesondere solche, die nicht in der Packungsbeilage
aufgeführt sind, bei Ihrem Tier feststellen, teilen Sie diese Ihrem Tierarzt oder Apotheker
mit.
7. Z
IELTIERART(EN)
Hund.
8.
DOSIERUNG FÜR JEDE TIERART, ART UND DAUER DER ANWENDUNG
Dosierung:
Die empfohlene Mindestdosis beträgt 6,7 mg/kg Körpergewicht für Fipronil, 6 mg/kg für (S)Methopren und 8 mg/kg für Amitraz.
Lösung zum Auftropfen auf die Haut.
Behandlungsplan:
Monatliche Anwendung in Abhängigkeit der lokalen epidemiologischen Situation während der
Zecken- und/oder Flohsaison.
9.
HINWEISE FÜR DIE RICHTIGE ANWENDUNG
24
1.
2.
3.
4.
Trennen Sie einen Blister entlang der Perforierung von den anderen ab.
Schneiden Sie den Blister entlang der gepunkteten Linie mit einer Schere auf (oder falten Sie
die Ecke des Blisters wie beschrieben und ziehen die Folie ab).
Entnehmen Sie die Pipette und halten Sie diese aufrecht. Schneiden Sie die Pipettenspitze mit
der Schere ab.
Das Fell des Tieres scheiteln, bis die Haut sichtbar wird.
Die Spitze der Pipette auf die Haut aufsetzen. Drücken Sie die Hälfte des Pipetteninhaltes am
Nacken in der Mitte zwischen der Schädelbasis und den Schulterblättern aus. Wiederholen Sie
diesen Vorgang an der Basis des Nackens vor den Schulterblättern, um die Pipette vollständig
zu entleeren.
Die Behandlung mit CERTIFECT bei einem Hund mit Zeckenbefall führt zum Ablösen der Zecken,
unterbricht das Ansaugen und tötet die Zecken schnell innerhalb von 24 Stunden ab. Somit wird die
Blutmahlzeit und das damit einhergehende Risiko der Übertragung von Erregern, die durch Zecken
übertragen werden, verhindert. Das Risiko der Entstehung einer Caninen Babesiose, Monozytären
Ehrlichiose, Granulozytären Anaplasmose und Borreliose wird damit indirekt für 4 Wochen reduziert.
Das Tierarzneimittel bleibt auf dem Tier wirksam, wenn es der Sonne ausgesetzt ist oder nachdem der
Hund durch Regen, Baden oder Schwimmen nass geworden ist. Jedoch kann das Shampoonieren oder
Schwimmen im Wasser direkt nach der Behandlung oder häufiges Anwenden von Shampoos die
Dauer der Wirksamkeit vermindern. Behandelte Hunde sollten bis 48 Stunden nach der Behandlung
nicht gebadet werden. Sollte der Hund unbedingt mit Shampoo gewaschen werden müssen, ist es
besser, dies vor der Applikation des Tierarzneimittels zu tun.
Alle Entwicklungsstadien der Flöhe können Körbchen, Liegedecken und gewohnte Ruheplätze des
Hundes befallen, wie z.B. Teppiche und Polstermöbel, die mitbehandelt werden sollten, besonders bei
starkem Befall und zu Beginn der Bekämpfung. Hierfür bieten sich geeignete Mittel zur
Umgebungsbehandlung und anschließendes regelmäßiges Staubsaugen an.
Nach der Behandlung mit CERTIFECT werden die Zecken gewöhnlich innerhalb von 24 Stunden
nach Befall abgetötet und fallen vom Hund ohne vorherige Blutmahlzeit ab. Das Ansaugen einzelner
Zecken kann jedoch nicht vollkommen verhindert werden. Unter ungünstigen Bedingungen kann
daher eine Übertragung von Infektionskrankheiten nicht völlig ausgeschlossen werden.
10. WARTEZ
EIT
Nicht zutreffend.
11. BESONDERE
LAGERUNGSHINWEISE
Arzneimittel unzugänglich für Kinder aufbewahren.
In der Originalverpackung aufbewahren
Sie dürfen das Tierarzneimittel nach dem auf dem Karton angegebenen Verfalldatum nicht mehr
anwenden.
12. BESONDERE
WARNHINWEISE
Besondere Vorsichtsmaßnahmen für die Anwendung bei Tieren
Der Kontakt mit den Augen des Hundes ist zu vermeiden.
Nur zum Auftropfen auf die Haut. Nicht oral oder anderweitig verabreichen.
Das Tierarzneimittel auf die trockene Haut und an einer Stelle auftragen, die das Tier nicht ablecken
kann und darauf achten, dass sich behandelte Tiere nicht gegenseitig ablecken können.
25
Die Applikationsstelle kann nach der Behandlung nass oder ölig aussehen.
Der Mindestabstand zwischen zwei Behandlungen soll nicht weniger als 2 Wochen betragen, da die
Verträglichkeit für kürzere Behandlungsintervalle nicht geprüft wurde. Nicht anwenden bei Welpen im
Alter von unter 8 Wochen und bei Hunden mit einem Körpergewicht von weniger als 2 kg.
Innerhalb von 48 Stunden nach Behandlung sollten Hunde von fließenden Gewässern und Flüssen
ferngehalten werden.
Die bekannten unerwünschten Arzneimittelwirkungen von Amitraz und seinen Metaboliten beruhen
auf agonistischen Wirkungen an alpha2-Adrenorezeptoren, zu denen Hypersalivation, Erbrechen,
Lethargie, Hyperglykämie, Bradykardie oder Bradypnoe gehören können. Diese Symptome sind
vorübergehend und verschwinden gewöhnlich ohne Behandlung innerhalb von 24 Stunden.
Sollten die Symptome schwerwiegend sein oder andauern, kann als Antidot Atipamezol-Hydrochlorid
verwendet werden.
Im Falle einer Überdosierung kann das Risiko des Auftretens von Unverträglichkeiten steigen, sodass
es wichtig ist, die Tiere immer mit der korrekten Pipettengröße gemäß ihrem Körpergewicht zu
behandeln.
Weitere Informationen
Das Tierarzneimittel kann während der Trächtigkeit und Laktation angewendet werden.
Die Unbedenklichkeit des Tierarzneimittels bei Zuchttieren, während der Trächtigkeit und Laktation
wurde durch mehrfach wiederholte Anwendung der bis zur dreifachen empfohlenen Dosis im 28 TageBehandlungsintervall nachgewiesen.
Die Verträglichkeit des Tierarzneimittels wurde bei gesunden erwachsenen Hunden, die bis zu 6 mal
in 2-wöchigem Abstand mit einer bis zur 5-fach erhöhten Dosis behandelt wurden, und bei Welpen
mit einer einmaligen Behandlung im Alter von 8 Wochen nachgewiesen.
Besondere Vorsichtsmaßnahmen für den Anwender
Das Tierarzneimittel kann eine Sensibiliserung der Haut, allergische Reaktionen und leichte
Augenreizung beim Menschen verursachen. Tiere oder Anwender, von denen eine
Überempfindlichkeit gegen die arzneilich wirksamen Bestandteile oder sonstigen Bestandteile bekannt
ist, sollten den Kontakt vermeiden, da es bei empfindlichen Individuen in sehr seltenen Fällen zu
Irritationen der Atemwege und zu Hautreaktionen kommen kann. Die Verwendung von
Schutzhandschuhen wird empfohlen.
Der direkte Kontakt mit der Applikationsstelle soll vermieden werden. Kinder sollten nicht mit
behandelten Hunden spielen, bevor die Applikationsstelle trocken ist. Deshalb empfiehlt es sich,
Hunde nicht während des Tages, sondern in den frühen Abendstunden zu behandeln. Frisch
behandelte Tiere sollten nicht in engem Kontakt mit den Besitzern, insbesondere nicht mit Kindern,
schlafen.
Dieses Tierarzneimittel enthält Amitraz, das im Einzelfall bei Personen zu neurologischen
Nebenwirkungen führen kann. Amitraz ist ein Monoamino-Oxidase-Hemmer (MAO-Hemmer); daher
sollten Anwender, die Medikamente mit MAO-Hemmern einnehmen, beim Umgang mit dem
Tierarzneimittel besonders vorsichtig sein.
Um die Möglichkeit des Einatmens zu verringern, sollte die Behandlung im Freien oder in einem gut
belüfteten Raum stattfinden.
Während der Anwendung nicht rauchen, trinken oder essen.
Hände nach der Anwendung sorgfältig waschen.
Gebrauchte Pipetten sind unverzüglich zu beseitigen. Zur Aufbewahrung die Pipetten in der
ungeöffneten Folienverpackung belassen.
Bei versehentlicher Hautkontamination sofort mit Wasser und Seife abwaschen.
Nach versehentlichem Kontakt mit dem Auge dieses sofort sorgfältig mit klarem Wasser ausspülen.
Bei Nebenwirkungen ist unverzüglich ein Arzt zu Rate zu ziehen und die Packungsbeilage oder die
Packung vorzuzeigen.
26
13.
BESONDERE VORSICHTSMASSNAHMEN FÜR DIE ENTSORGUNG VON NICHT
VERWENDETEM ARZNEIMITTEL ODER VON ABFALLMATERIALIEN, SOFERN
ERFORDERLICH
Nicht verwendete Tierarzneimittel oder davon stammende Abfallmaterialien sind entsprechend den
nationalen Vorschriften zu entsorgen.
Das Tierarzneimittel darf nicht in Gewässer gelangen, da es eine Gefahr für Fische und andere
Wasserorganismen darstellen kann.
14.
GENEHMIGUNGSDATUM DER PACKUNGSBEILAGE
Detaillierte Angaben zu diesem Tierarzneimittel finden Sie auf der Website der Europäischen
Arzneimittel-Agentur unter http://www.ema.europa.eu/.
15. WEITERE
ANGABEN
Jede Stärke dieses Tierarzneimittels ist in einem Plastikbehältnis mit 1 Pipette und in einem Karton
mit 3 Pipetten erhältlich
Es werden möglicherweise nicht alle Packungsgrößen in Verkehr gebracht.
Für Tiere.
Verschreibungspflichtig.
27
GEBRAUCHSINFORMATION
(Plastikbehältnis mit 1 Pipette)
CERTIFECT 67 mg/ 60,3 mg/ 80 mg Spot on Lösung für Hunde 2-10 kg
CERTIFECT 134 mg/ 120,6 mg/ 160 mg Spot on Lösung für Hunde 10-20 kg
CERTIFECT 268 mg/ 241,2 mg/ 320 mg Spot on Lösung für Hunde 20-40 kg
CERTIFECT 402 mg/ 361,8 mg/ 480 mg Spot on Lösung für Hunde 40-60 kg
1.
NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN
UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
VERANTWORTLICH IST
Zulassungsinhaber:
MERIAL
29, avenue Tony Garnier
F-69007 Lyon
Frankreich
Für die Chargenfreigabe verantwortlicher Hersteller:
MERIAL
4, Chemin du Calquet
F-31300 Toulouse-Cedex
Frankreich
2.
BEZEICHNUNG DES TIERARZNEIMITTELS
CERTIFECT 67 mg/ 60,3 mg/ 80 mg Spot on Lösung für Hunde 2-10 kg
CERTIFECT 134 mg/ 120,6 mg/ 160 mg Spot on Lösung für Hunde 10-20 kg
CERTIFECT 268 mg/ 241,2 mg/ 320 mg Spot on Lösung für Hunde 20-40 kg
CERTIFECT 402 mg/ 361,8 mg/ 480 mg Spot on Lösung für Hunde 40-60 kg
3.
WIRKSTOFF(E) UND SONSTIGE BESTANDTEILE
Lösung zum Auftropfen.
Klare, bernsteinfarbene bis gelbliche Lösung.
Jede Einzeldosis (Doppelkammerpipette) enthält:
CERTIFECT Spot on
Lösung
Volumen
(ml)
Fipronil
(mg)
(S)-Methoprene
(mg)
Amitraz
(mg)
Hunde 2 10 kg
1,07
67
60,3
80
Hunde 10-20 kg
2,14
134
120,6
160
Hunde 20-40 kg
4,28
268
241,2
320
Hunde 40-60 kg
6,42
402
361,8
480
Hilfsstoffe, die für die korrekte Anwendung wichtig sind: Butylhydroxyanisol (0,02 %) und
Butylhydroxytoluol (0,01 %)
28
4. ANWENDUNGSGEBIET(E)
Zur Behandlung und Vorbeugung eines Zeckenbefalls (Ixodes ricinus, Dermacentor reticulatus,
Rhipicephalus sanguineus, Ixodes scapularis, Dermacentor variabilis, Haemaphysalis elliptica,
Haemaphysalis longicornis, Amblyomma americanum und Amblyomma maculatum) sowie eines
Flohbefalls (Ctenocephalides felis und Ctenocephalides canis) bei Hunden.
Zur Behandlung eines Befalls mit Haarlingen (Trichodectes canis).
Zur Verhinderung eines Flohbefalls der Umgebung durch Hemmung aller unreifer
Entwicklungsstadien der Flöhe.
Geeignet zur Behandlung und Kontrolle der Flohstichallergie (FAD).
Abtötung von Flöhen und Zecken innerhalb von 24 Stunden. Eine Behandlung verhindert einen
erneuten Befall mit Zecken für 5 Wochen und mit Flöhen für bis zu 5 Wochen.
Die Behandlung reduziert indirekt das Risiko der Übertragung von Krankheiten, die durch infizierte
Zecken übertragen werden (Canine Babesiose, Monozytäre Ehrlichiose, Granulozytäre Anaplasmose
und Borreliose) für 4 Wochen.
5. GEGENANZ
EIGEN
Nicht bei kranken (z.B. systemische Erkrankungen, Diabetes, Fieber) oder rekonvaleszenten Tieren
anwenden.
Nicht bei Kaninchen und Katzen anwenden.
6. NEBENWIRKUNGEN
Vorübergehende Hautreaktionen an der Applikationsstelle (Hautverfärbung, lokaler Haarausfall,
Juckreiz, Erythem) und generalisierter Juckreiz oder Haarausfall können auftreten. Nach Ablecken der
Applikationsstelle können vermehrtes Speicheln, Erbrechen, Hyperglykämie, erhöhte Empfindlichkeit
auf Reize, Lethargie, Bradykardie oder Bradypnoe auftreten. Diese Symptome sind vorübergehend
und klingen gewöhnlich ohne Behandlung innerhalb von 24 Stunden wieder ab.
Falls Sie Nebenwirkungen, insbesondere solche, die nicht in der Packungsbeilage
aufgeführt sind, bei Ihrem Tier feststellen, teilen Sie diese Ihrem Tierarzt oder Apotheker
mit.
7. Z
IELTIERART(EN)
Hund.
8.
DOSIERUNG FÜR JEDE TIERART, ART UND DAUER DER ANWENDUNG
Dosierung:
Die empfohlene Mindestdosis beträgt 6,7 mg/kg Körpergewicht für Fipronil, 6 mg/kg für (S)Methopren und 8 mg/kg für Amitraz.
Lösung zum Auftropfen auf die Haut.
Behandlungsplan:
29
Monatliche Anwendung in Abhängigkeit der lokalen epidemiologischen Situation während der
Zecken- und/oder Flohsaison.
9.
HINWEISE FÜR DIE RICHTIGE ANWENDUNG
1.
Schneiden Sie den Blister entlang der gepunkteten Linie mit einer Schere auf (oder falten Sie
die Ecke des Blisters wie beschrieben und ziehen die Folie ab).
Entnehmen Sie die Pipette und halten Sie diese aufrecht. Schneiden Sie die Pipettenspitze mit
der Schere ab.
Das Fell des Tieres scheiteln, bis die Haut sichtbar wird. Die Spitze der Pipette auf die Haut
aufsetzen. Drücken Sie die Hälfte des Pipetteninhaltes am Nacken in der Mitte zwischen der
Schädelbasis und den Schulterblättern aus. Wiederholen Sie diesen Vorgang an der Basis des
Nackens vor den Schulterblättern, um die Pipette vollständig zu entleeren.
2.
3.
Die Behandlung mit CERTIFECT bei einem Hund mit Zeckenbefall führt zum Ablösen der Zecken,
unterbricht das Ansaugen und tötet die Zecken schnell innerhalb von 24 Stunden ab. Somit wird die
Blutmahlzeit und das damit einhergehende Risiko der Übertragung von Erregern, die durch Zecken
übertragen werden, verhindert. Das Risiko der Entstehung einer Caninen Babesiose, Monozytären
Ehrlichiose, Granulozytären Anaplasmose und Borreliose wird damit indirekt für 4 Wochen reduziert.
Das Tierarzneimittel bleibt auf dem Tier wirksam, wenn es der Sonne ausgesetzt ist oder nachdem der
Hund durch Regen, Baden oder Schwimmen nass geworden ist. Jedoch kann das Shampoonieren oder
Schwimmen im Wasser direkt nach der Behandlung oder häufiges Anwenden von Shampoos die
Dauer der Wirksamkeit vermindern. Behandelte Hunde sollten bis 48 Stunden nach der Behandlung
nicht gebadet werden. Sollte der Hund unbedingt mit Shampoo gewaschen werden müssen, ist es
besser, dies vor der Applikation des Tierarzneimittels zu tun.
Alle Entwicklungsstadien der Flöhe können Körbchen, Liegedecken und gewohnte Ruheplätze des
Hundes befallen, wie z.B. Teppiche und Polstermöbel, die mitbehandelt werden sollten, besonders bei
starkem Befall und zu Beginn der Bekämpfung. Hierfür bieten sich geeignete Mittel zur
Umgebungsbehandlung und anschließendes regelmäßiges Staubsaugen an.
Nach der Behandlung mit CERTIFECT werden die Zecken gewöhnlich innerhalb von 24 Stunden
nach Befall abgetötet und fallen vom Hund ohne vorherige Blutmahlzeit ab. Das Ansaugen einzelner
Zecken kann jedoch nicht vollkommen verhindert werden. Unter ungünstigen Bedingungen kann
daher eine Übertragung von Infektionskrankheiten nicht völlig ausgeschlossen werden.
10. WARTEZ
EIT
Nicht zutreffend.
11. BESONDERE
LAGERUNGSHINWEISE
Arzneimittel unzugänglich für Kinder aufbewahren.
In der Originalverpackung aufbewahren.
Sie dürfen das Tierarzneimittel nach dem auf dem Karton angegebenen Verfalldatum nicht mehr
anwenden.
12. BESONDERE WARNHINWEISE
Besondere Vorsichtsmaßnahmen für die Anwendung bei Tieren
30
Der Kontakt mit den Augen des Hundes ist zu vermeiden.
Nur zum Auftropfen auf die Haut. Nicht oral oder anderweitig verabreichen.
Das Tierarzneimittel auf die trockene Haut und an einer Stelle auftragen, die das Tier nicht ablecken
kann und darauf achten, dass sich behandelte Tiere nicht gegenseitig ablecken können.
Die Applikationsstelle kann nach der Behandlung nass oder ölig aussehen.
Der Mindestabstand zwischen zwei Behandlungen soll nicht weniger als 2 Wochen betragen, da die
Verträglichkeit für kürzere Behandlungsintervalle nicht geprüft wurde. Nicht anwenden bei Welpen im
Alter von unter 8 Wochen und bei Hunden mit einem Körpergewicht von weniger als 2 kg.
Innerhalb von 48 Stunden nach Behandlung sollten Hunde von fließenden Gewässern und Flüssen
ferngehalten werden.
Die bekannten unerwünschten Arzneimittelwirkungen von Amitraz und seinen Metaboliten beruhen
auf agonistischen Wirkungen an alpha2-Adrenorezeptoren, zu denen Hypersalivation, Erbrechen,
Lethargie, Hyperglykämie, Bradykardie oder Bradypnoe gehören können. Diese Symptome sind
vorübergehend und verschwinden gewöhnlich ohne Behandlung innerhalb von 24 Stunden.
Sollten die Symptome schwerwiegend sein oder andauern, kann als Antidot Atipamezol-Hydrochlorid
verwendet werden.
Im Falle einer Überdosierung kann das Risiko des Auftretens von Unverträglichkeiten steigen, sodass
es wichtig ist, die Tiere immer mit der korrekten Pipettengröße gemäß ihrem Körpergewicht zu
behandeln.
Weitere Informationen
Das Tierarzneimittel kann während der Trächtigkeit und Laktation angewendet werden.
Die Unbedenklichkeit des Tierarzneimittels bei Zuchttieren, während der Trächtigkeit und Laktation
wurde durch mehrfach wiederholte Anwendung der bis zur dreifachen empfohlenen Dosis im 28 TageBehandlungsintervall nachgewiesen.
Die Verträglichkeit des Tierarzneimittels wurde bei gesunden erwachsenen Hunden, die bis zu 6 mal
in 2-wöchigem Abstand mit einer bis zur 5-fach erhöhten Dosis behandelt wurden, und bei Welpen
mit einer einmaligen Behandlung im Alter von 8 Wochen nachgewiesen.
Besondere Vorsichtsmaßnahmen für den Anwender
Das Tierarzneimittel kann eine Sensibiliserung der Haut, allergische Reaktionen und leichte
Augenreizung beim Menschen verursachen. Tiere oder Anwender, von denen eine
Überempfindlichkeit gegen die arzneilich wirksamen Bestandteile oder sonstigen Bestandteile bekannt
ist, sollten den Kontakt vermeiden, da es bei empfindlichen Individuen in sehr seltenen Fällen zu
Irritationen der Atemwege und zu Hautreaktionen kommen kann. Die Verwendung von
Schutzhandschuhen wird empfohlen.
Der direkte Kontakt mit der Applikationsstelle soll vermieden werden. Kinder sollten nicht mit
behandelten Hunden spielen, bevor die Applikationsstelle trocken ist. Deshalb empfiehlt es sich,
Hunde nicht während des Tages, sondern in den frühen Abendstunden zu behandeln. Frisch
behandelte Tiere sollten nicht in engem Kontakt mit den Besitzern, insbesondere nicht mit Kindern,
schlafen.
Dieses Tierarzneimittel enthält Amitraz, das im Einzelfall bei Personen zu neurologischen
Nebenwirkungen führen kann. Amitraz ist ein Monoamino-Oxidase-Hemmer (MAO-Hemmer); daher
sollten Anwender, die Medikamente mit MAO-Hemmern einnehmen, beim Umgang mit dem
Tierarzneimittel besonders vorsichtig sein.
Um die Möglichkeit des Einatmens zu verringern, sollte die Behandlung im Freien oder in einem gut
belüfteten Raum stattfinden.
Während der Anwendung nicht rauchen, trinken oder essen.
Hände nach der Anwendung sorgfältig waschen.
Gebrauchte Pipetten sind unverzüglich zu beseitigen. Zur Aufbewahrung die Pipetten in der
ungeöffneten Folienverpackung belassen.
31
Bei versehentlicher Hautkontamination sofort mit Wasser und Seife abwaschen.
Nach versehentlichem Kontakt mit dem Auge dieses sofort sorgfältig mit klarem Wasser ausspülen.
Bei Nebenwirkungen ist unverzüglich ein Arzt zu Rate zu ziehen und die Packungsbeilage oder die
Packung vorzuzeigen.
13.
BESONDERE VORSICHTSMASSNAHMEN FÜR DIE ENTSORGUNG VON NICHT
VERWENDETEM ARZNEIMITTEL ODER VON ABFALLMATERIALIEN, SOFERN
ERFORDERLICH
Nicht verwendete Tierarzneimittel oder davon stammende Abfallmaterialien sind entsprechend den
nationalen Vorschriften zu entsorgen.
Das Tierarzneimittel darf nicht in Gewässer gelangen, da es eine Gefahr für Fische und andere
Wasserorganismen darstellen kann.
14.
GENEHMIGUNGSDATUM DER PACKUNGSBEILAGE
Detaillierte Angaben zu diesem Tierarzneimittel finden Sie auf der Website der Europäischen
Arzneimittel-Agentur unter http://www.ema.europa.eu/.
15. WEITERE
ANGABEN
Jede Stärke dieses Tierarzneimittels ist in einem Plastikbehältnis mit 1 Pipette und in einem Karton
mit 3 Pipetten erhältlich
Es werden möglicherweise nicht alle Packungsgrößen in Verkehr gebracht.
Für Tiere.
Verschreibungspflichtig.
32