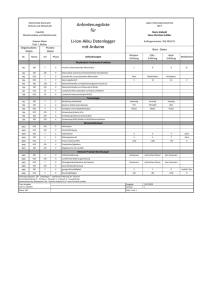
Hypophyse-NNR-Achse bei einem gesunden Hund Cushing
Werbung

Das Cushing Syndrom beim Hund V H F R C o l g Z m L a th o yp H o le ru sa T C A R N tlH re sciu fa Z H T C A A C H T Dr. med. vet. C. Rohrer Kaiser Dipl. ACVIM und ECVIM-CA (Innere Medizin) Hypophyse-NNR-Achse bei einem gesunden Hund Cushing Syndrom • Hypophysäres Cushing Syndrom (HCS) – 85% der Fälle • Adrenales Cushing Syndrom (ACS) – 15% der Fälle Hypophyse-NNR-Achse bei HCS Hypophyse-NNR-Achse bei ACS Cushing Syndrom • Chronische Erhöhung von Kortisol im Plasma • 85% HCS – Neoplasie der Hypophyse • Meist gutartig Cushing Syndrom • 15% ACS – Neoplasie der NNR • 50% gutartig • 50% bösartig – Noduläre Hyperplasie der NNR (selten) Signalement • Alter – Mittelaltrige bis alte Hunde • > 6 Jahre, Median 10 Jahre • Geschlecht – 55-65% weiblich • Rasse – Pudel, Dackel, Terrier, DSH – HCS: 75% < 20 kg Anamnese • Selten als ernsthaft krank eingestuft • Langsame Progression der Symptome • Nur selten Durchfall/Erbrechen PU/PD • 80-85% der Patienten • PD: > 100 ml/kg/Tg • Ursache der PU unbekannt – Interferenz des Cortisols mit ADH-Aktion am Sammelrohr der Niere (nephrogener DI) – Erhöhung der GFR durch Cortisol – Zentraler DI (ADH-Mangel) Polyphagie • 80-90% der Patienten • Ursachen (?) – Direkter Effekt von Glukokortikoiden – “Anti-Insulin-Effekt” von Glukokortikoiden • Subklinischer DM • Klinischer DM bei 5% der Patienten Vergrössertes Abdomen • 90-95% der Patienten • Ursachen – Umverteilung von Fett von anderen Depots ins Abdomen – Muskelschwäche (Proteinkatabolismus) – Grosse Leber – Volle Blase Haut- und Fellveränderungen • Häufig • Kein Juckreiz • Alopezie, dünne Haut, Seborrhoe, Komedonen, Calcinosis cutis, Pyodermie Lahmheit • Myopathie • KBR, Patellaluxation • Bei chronischen degenerativen Gelenkserkrankungen und Arthritis: Verdecken der klinischen Symptome durch Hypercortisolismus Respiratorische Symptome • Husten selten • Hecheln häufig – Muskelschwäche – Fettakkumulation im Abdomen – Hepatomegalie Laboranalysen • • • • Hämatologie Klinische Chemie Urinanalyse Endokrine Tests • Pulmonäre Thromboembolie Hämatologie und klin. Chemie • Hämatologie – Stressblutbild • Klinische Chemie – AP-Erhöhung bei 95% der Patienten – Cholesterinerhöhung bei 90% der Patienten – ALT-, AST-, δ GT-Erhöhungen Urinanalyse • Tiefes SG bei 85% der Patienten – Patienten können Harn konzentrieren • Häufige Proteinurie • Cystitis bei 40-50% der Patienten – Inaktives Sediment möglich Endokrine Tests Screeningtests • Screeningtests: CS ja oder nein? – LDDS – ACTH-Stim. – Urin Kortisol:Kreatinin-Quotient • Differenzierungstests: HCS oder ACS? – Erweiterter LDDS – HDDS – ACTH-Konzentration LDDS (%) ACTH-Stim. (%) Urin Kort:KreatQuotient (%) Sensitivität 85-95 60-85 98 (???) Spezifität 70-75 85-90 20-77 Screeningtests • Urin Kortisol:Kreatinin-Quotient – Ein positiver Quotient ist nicht diagnostisch für CS – Ein negativer Quotient macht CS unwahrscheinlich, jedoch nicht unmöglich Screeningtests • LDDS – Durchführung – Interpretation • 8 h Kortisol ≥ 1.4 µg/dl spricht für M. Cushing • Basale Kortisol-Konzentrationbestimmungen im Plasma sind nicht nützlich Screeningtests • ACTH-Stimulationstest – Durchführung – Interpretation Differenzierungstest • Erweiterter LDDS – Kann auch als Screeningtest gebraucht werden • 1 h Kortisol ≥ 22 µg/dl spricht für M. Cushing • HDDS – Nur bei nachgewiesenem CS sinnvoll (kein Screeningtest) LDDS vs. erweiterter LDDS • Durchführung • Interpretation – 8h Kortisolwert: CS ja oder nein? – 4h und 8h Kortisolwert: HCS oder ACS? • Es lohnt sich, den 4h und den 8h Kortisolwert zu bestimmen – Häufig kann die Lokalisation des Tumors mit nur einem Test festgestellt werden – 4h Serum aufbewahren LDDS vs. erweiterter LDDS • Interpretation des erweiterten LDDS – HCS • 4 h Kortisolwert < 1.4 µg/dl • 4 h Kortisolwert < 50% des Basalwerts • 8 h Kortisolwert < 50% des Basalwerts – 60% der Hunde mit einem HCS zeigen eine Suppression nach mindestens einem der oben genannten Kriterien LDDS vs. erweiterter LDDS Basalwert (µg/dl) 4 h Kortisol (µg/dl) 8 h Kortisol (µg/dl) 3.7 0.4 0.5 3.7 0.4 2.0 3.7 1.9 2.0 Differenzierungstest • HDDS – Durchführung – Interpretation Hunde mit ACS Hunde mit HCS Keine Supression +/- 100% 25% < 50% des Basalwerts - 60% < 1.4 µg/dl - 40% 8h Kortisolwert Bildgebende Verfahren • Röntgen – Thorax • Metastasen • Pulmonäre Thromboembolie – Abdomen • Grosse Leber • Verkalkungen bei NNR-Neoplasie Bildgebende Verfahren • Ultraschall – NN-Masse • • • • • Funktioneller Tumor Nichtfunktioneller Tumor Phäochromozytom Metastatischer Tumor Granulom, Zyste, Hämorrhagie – Lebermetastasen – Invasion der V. cava caudalis? Therapie • Chirurgie: ACS / HCS • Medikamentöse Therapie: HCS / ACS • (Bestrahlung: HCS) Chirurgie • ACS – Metastasen ausschliessen – Falls Risikopatient, zuerst medikamentell behandeln – Flüss. und Dexamethason intraop., Glukound Mineralokortikoide postop. geben – Gute Prognose, falls Tumor entfernt werden kann – Nicht jeder Patient ist Kandidat für Chirurgie Medikamentöse Therapie • (Mitotane, o,p'-DDD, Lysodren®) Lysodren® • Abkömmling von DDT • Verursacht Nekrose der NNR – Zerstörung des Tumorgewebes • Trilostan, Vetoryl® • Beste medikamentöse Therapie bei inoperablen ACS-Patienten – Gutes Ansprechen bei > 60% der Patienten Vetoryl® • Steroidanalog, welches KortisolSynthese durch NNR blockiert • Wirksamkeit von 80-90% • Anpassung der Dosierung häufig nötig Vetoryl® • Protokoll (Consensus Statement 2006) – 1xtgl 2-5 mg/kg PO • Hd <10 kg KG: Dosis im unteren Bereich wählen – ACTH-Stim. nach 1-2, 4 und 12 Wochen, danach alle 3 Monaten • ACTH-Stim. immer zur gleichen Zeit durchführen, 2-3 h nach Kapselgabe – Ziel: post-ACTH-Kortisolwert von 1.5-5 µg/dl – Anamnese und klinische Untersuchung für die Dosisanpassung berücksichtigen Prognose • HCS – Mittlere Lebensdauer nach Diagnose von 30 Monaten (Lysodren®) • Rückfälle relativ häufig (40%) – Mediane Überlebenszeit mit Vetoryl® von 660 Tagen • ACS – Mittlere Lebensdauer nach Diagnose von 16 Monaten (Lysodren®) • Rückfälle relativ häufig (63%) Prognose • …ACS – Gute Prognose bei den chirurgischen Patienten, falls sie keine Metastasen haben und die ersten 1-4 Wochen nach der Operation überstehen • Mittlere Überlebenszeit von 36 Monaten • Hunde mit Adenomen haben die bessere Prognose FALL 1: „Jango“ • Signalement – Hovawart, mk, 8 Jahre • Anamnese – Polyphagie – PU/PD – Harnwegsinfektion mit vielen Stäbchen • Therapie mit Antibiotika • Immer noch PU/PD FALL 1 • Klinische Untersuchung – Stammfettsucht – Alopezie am Bauch – Hecheln? • Differentialdiagnosen? • Plan? FALL 1 • Plan – Urinkultur – Blut und Harnuntersuchung • Resultate – Hk 52% – Cholesterin o.B. – Leberenzymen • AP o.B., ALAT 113 (N. bis 55 U/l) – UCCR 64.5 x 10-6 (N. bis < 10x10-6) • Wie weiter? Wikipedia FALL 1 Fall 2: „Casper“ • Erweiterter LDDST • Signalement Wikipedia – Bichon Frisé, mk, 13 Jahre Kortisol Basalwert 7.8 μg/dl Kortisol nach 4h 5.98 μg/dl Kortisol nach 8h 3.8 μg/dl • Wie weiter? • Anamnese/klinische Untersuchung – PU/PD, 100-166 ml/kg/Tg – Keine Polyphagie – Leicht vergrössertes Abdomen – Hecheln Fall 2 Fall 2 Parameter • Weitere Untersuchungen – Röntgen Abdomen • Grosse Leber – Zytologie Leber • Vakuoläre Hepatopathie – Harn Untersuchung • • • • SG 1.015, pH 6.5, + Protein UPCR 0.25 (N. 0.0-0.5) UCCR 14.3 x10-6 (N. < 10 x10-6) Kultur: 1000 KBE/ml Staph. und Streptokokken (Katheterharn) Resultat Einheiten Erythrozyten 9.5 6.0-9.0 (x109/μl) Hämoglobin 12.0 9.3-11.8 (mmol/l) Hämatokrit 55.3 38-55 (%) Leukozyten 8.0 6.0-12.0 (x103/μl) Neutrophile Gran. 5.24 3-10 (x103/μl) Eosinophile Gran. 0.33 0-0.6 (x103/μl) Basophile Gran. 0.01 0-0.04 (x103/μl) Monozyten 0.69 0-1.2 (x103/μl) Lymphozyten 1.74 1-4 (x103/μl) AP 201 0-81 (U/l) ALAT 109 5-125 (U/l) ASAT Cholesterin FALL 2 • ACTH-Stimulationstest Kortisol Basalwert 6.67 μg/dl Kortisol post ACTH 21.1 μg/dl • Hat er nun einen M. Cushing oder nicht? 26 0-52 (U/l) 10.0 2.9-8.5 (mmol/l)