Forschung aktuell - Max-Planck
Werbung

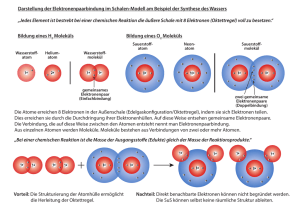
FORSCHUNG AKTUELL Sisyphos hatte ein physikalisches Problem. Denn den Stein, den er unablässig den Berg hinaufrollte, zog die Schwerkraft immer wieder zu Tal. Der Felsbrocken blieb erst am tiefsten Punkt lie6 M AX P L ANCK FO RSCHUNG 2/2007 Q UANTENOPTIK FÜR MPI S DES gen, weil seine Energie dort am kleinsten war. Physikalisch gesprochen heißt das: Er kommt am Minimum des Potenzials zur Ruhe, das die Schwerkraft aufbaut. Das Prinzip wurde der mythischen Figur zum Fluch, doch es hält auch unsere Welt, genauer gesagt die Atome, zusammen. Denn alle Teilchen zieht es zum tiefsten Punkt eines Potenzials – auch Elektronen. Die negativ geladenen Teilchen streben zum Tiefpunkt des Bindungspotenzials, das die elektrostatische Kraft des positiv geladen Atomkerns erzeugt. Da sich die Elektronen sehr schnell bewegen, stürzen sie aber nicht in den Kern, sondern umschwirren ihn in gebührendem Abstand: Sie sitzen umgeben von einem Potenzialwall in einem elektrostatischen Tal fest. Doch die Elektronen können aus dem Tal und damit ihrem Atom entkommen – was sie zum Glück für den Fortbestand der Welt nicht oft tun. Den Ausweg öffnet ihnen die Quantenmechanik: Die erlaubt ihnen, durch den Wall des Bindungspotenzials zu tunneln. Ein internationales Forscherteam um Ferenc Krausz hat die V ORLAGEN Wir müssen einen Berg erklimmen, um ihn zu überwinden – in der Quantenphysik geht das auch anders: Objekte können über einen Hügel gelangen, indem sie ihn einfach durchtunneln, anstatt mühsam hinüberzuklettern. Ein internationales Forscherteam um Ferenc Krausz vom Max-Planck-Institut für Quantenoptik hat nun erstmals Elektronen bei diesem Tunnelprozess beobachtet. Sie verfolgten, wie Elektronen der anziehenden Kraft eines Atomkerns entwischen. Mit ultrakurzen Laserpulsen haben die Wissenschaftler dabei nun diskrete Ionisationsstufen nachgewiesen, die jeweils einige 100 Attosekunden dauern, also den Bruchteil einer billiardstel Sekunde. Die Ergebnisse tragen entscheidend zu einem tieferen Verständnis bei, wie sich Elektronen in Atomen und Molekülen bewegen. (NATURE, 5. April 2007) NACH Elektronen beim Tunneln erwischt G RAFIKEN : C HRISTOPH S CHNEIDER QUANTENPHYSIK Ein Berg lässt sich auf zwei Wegen überwinden: In der klassischen Physik muss man den Berg besteigen, um auf die andere Seite zu gelangen. In der Quantenphysik geht das auch anders: Elektronen etwa können einen Berg waagerecht durchqueren – sie tunneln. Elektronen dabei nun in flagranti ertappt. Nachdem die Physiker den Elektronen mit einem Laserpuls einen Schubs gegeben hatten und mit einem andern Laserpuls den Potenzialwall ein wenig abgesenkt hatten, durchbrachen einige Elektronen den Potenzialwall. „Unser Ergebnis bestätigt zum ersten Mal in einer Echtzeitbeobachtung die theoretischen Vorhersagen der Quantenmechanik“, sagt Ferenc Krausz, Direktor am Max-Planck-Institut für Quantenoptik und Leiter des Wissenschaftlerteams. Den Gesetzen der Quantenmechanik zufolge kann ein Elektron tunneln, weil es nicht nur Teilchen ist, sondern auch Welle. Daher kann es sich mit einer gewissen Wahrscheinlichkeit auch dort aufhalten, wo es nach den Gesetzen der klassischen Physik nicht sein dürfte: zum Beispiel in einem Potenzialwall oder sogar jenseits davon. Für makroskopische Objekte wie Felsbrocken ist die Wahrscheinlichkeit, auf diese Weise über einen Berg zu gelangen, jedoch verschwindend gering. Deshalb hat auch noch niemand einen tunnelnden Felsbrocken beobachtet. Für Teilchen des Mikrokosmos wie Elektronen stehen die Chancen dagegen nicht schlecht, sich auf diese Weise durch Berge, wenn auch elektrostatische, zu mogeln. Aber nicht nur Elektronen entkommen tunnelnd der anziehenden Kraft ihres Atomkerns, auch Alpha-Teilchen lösen sich auf diese Weise aus radioaktiven Kernen, und Atomkerne tunneln bei der Fusion ebenso zueinander. Obwohl der Tunneleffekt in der Natur also nicht selten ist, konnte ihn noch niemand in Echtzeit beobachten. Dafür war er bislang schlicht zu schnell. Krausz und seine Mitarbeiter haben ihn jetzt mithilfe zweier Lichtpulse live verfolgt: einem Attosekunden-Puls von sehr kurzwelligem Ultraviolett und einem intensiven Puls aus nur wenigen Wellenzügen roten Laserlichts. Beobachtet haben die Physiker die Flucht des Elektrons nur, weil sie beide Pulse perfekt synchronisierten. Kein Instrument kann den Tunnel-Vorgang direkt auflösen. Nachweisen lassen sich nur die Endprodukte, das heißt die Ionen, die übrig bleiben, wenn ein Elektron aus einem Atom tunnelt. Die Forscher mussten sich daher eines Tricks bedienen. Sie verwendeten Neonatome als Untersuchungsobjekte. In diesem Edelgas sind die Elektronen besonders fest gebunden und widersetzen sich den Bestrebungen des Laserpulses, sie aus dem Atom zu lösen. Trifft jedoch ein sehr harter ultravioletter Attosekunden-Blitz ein Neon-Atom, regt er ein Elektron an und befördert es zur Peripherie des Atoms. Nun feuern die Forscher einen roten Laserpuls auf das Atom. In dem Puls folgen ein paar Wellenberge und -täler aufeinander. Das elektrische Feld des kräftigen roten Laserpulses drückt den Potenzialwall nach unten, der das Elektron im Atom festhält. Nun kann das angeregte Elektron < 400 Attosekunden Wahrscheinlichkeit für die Freisetzung des Elektrons durch lichtinduziertes Tunneln 1 0 t1 t2 t3 aus dem Atom tunneln. Die Kraft des roten Pulses reicht dafür aber nur, wenn Wellenberge des Lichts über dem Atom liegen. Und besonders hoch müssen sie auch sein. Das sind sie aber nur in der Mitte des Pulses. Diese Vorhersage der Theorie haben die Garchinger Physiker jetzt experimentell bestätigt, indem sie den ultravioletten und den roten Puls zueinander verschoben haben. „Mit dem nur 250 Attosekunden dauernden UV-Puls haben wir ein Elektron zu jedem beliebigen Zeitpunkt innerhalb der roten Laserwelle mit Attosekundenpräzision an die Peripherie befördert“, erklärt Krausz. Sie fuhren mit der Spitze des ultravioletten Pulses also über das Wellengebirge des roten Pulses. Gleichzeitig zählten sie die Atome, aus denen ein Elektron tunnelnd entwischt ist und die so ionisiert wurden. So stellten sie fest, dass die Elektronen nur tunneln, wenn die besonders intensiven Wellenberge des roten Pulses über das vom ultravioletten Puls angeregte Atom streifen. Zudem haben sie auf diese Weise gemessen, wie lange der Tunnelprozess dauert – nämlich weniger als 400 Attosekunden. „Die Experimente gewähren nicht nur zum ersten Mal einen Einblick in die Dynamik des Elektronen-Tunnelns“, sagt Krausz: „Wir haben zudem gezeigt, dass sich die Bewegung von Elektronen in Atomen oder Molekülen mithilfe des Laserfeld-induzierten Tunnelns in Echtzeit beobachten lässt.“ Auf der Basis dieser Erkenntnis kontrollieren die Physiker die Bewegung der Elektronen. „So können wir in Zukunft erforschen, wie sich die Grenzen der Mikroelektronik verschieben lassen“, sagt Krausz. Optische Elektronik arbeitet nämlich umso effizienter, je präziser sich das Wechselspiel zwischen Licht und Elektronen steuern lässt. Auch kompakte Röntgenlaser können Physiker möglicherweise entwickeln, wenn sie die elektronischen Prozesse in Atomen besser beeinflussen können. Mit solchen brillanten Röntgenquellen ließen sich biologische Objekte besser abbilden oder die Strahlentherapie verbessern. ● 2/2007 M AX PL A NCK F ORSCHUNG Zeit Tunneln in Stufen: Jedes Mal, wenn der Wellenberg eines infraroten Laserpulses (rote Welle) auf das Atom trifft, steigt die Wahrscheinlichkeit, dass ein Elektron aus dem Atom tunnelt (grüne Kurve, Ausschnitt). Der Schritt von einer Stufe zur nächsten dauert nur einige 100 Attosekunden – so lange, wie die Elektronen zum Tunneln brauchen. @ Kontakt: PROF. DR. FERENC KRAUSZ Max-Planck-Institut für Quantenoptik, Garching Tel.: +49 89 32905-612 Fax: +49 89 32905-649 E-Mail: ferenc.krausz@ mpq.mpg.de 7 FORSCHUNG AKTUELL 8 STEREOCHEMIE Auf den Spuren des Florigens Handschlag der Moleküle Warum blühen Krokusse im Frühling und Astern im Herbst? Und wieso befinden sich die Blüten immer an der Sprossspitze und nicht irgendwo an Blatt und Stängel? Tatsächlich besitzen Pflanzen molekulare Lichtsensoren in ihren Blättern, die jahreszeitliche Unterschiede der Tageslänge messen. Zum richtigen Zeitpunkt, meist im Frühling, senden die Blätter einen Botenstoff als Signal für die Blütenbildung aus. Die Frage, um welche Substanz es sich bei diesem Florigen handeln könnte, hat Generationen von Botanikern beschäftigt. Erste Fortschritte gab es Ende der 1990er-Jahre sowie 2005. Kontrovers diskutiert wurde die Frage, wie das Florigen in die Sprossspitze gelangt. Georg Coupland und seine Mitarbeiter vom Max-Planck-Institut für Züchtungsforschung in Köln konnten zeigen, dass das Protein selbst wandert – und stellten damit eine andere Publikation in Frage (SCIENCE, 20. April 2007). Leben ist Teamarbeit im großen Stil: Im menschlichen Körper werkeln tausendmal mehr Moleküle Hand in Hand, als Sterne im Weltall leuchten. Wie Moleküle ihre Kooperationspartner erkennen hat nun ein internationales Wissenschaftlerteam um Forscher vom Max-Planck-Institut für Festkörperforschung beobachtet. Sie verfolgten mit einem Rastertunnelmikroskop, wie sich zwei chirale Dipeptid-Moleküle zu einem Dimer verbanden. Solche Moleküle liegen wie viele Moleküle in unserem Körper in zwei spiegelbildlichen Formen vor, die sich wie die rechte und linke Hand nicht zur Deckung bringen lassen. Damit die Dipeptide stabile Paare formen und Biomoleküle die Lebensprozesse aufrechterhalten können, müssen sich die Moleküle mit passenden Formen erkennen. Wie die Forscher nun herausgefunden haben, verändern sie sich dabei leicht – wie zwei Hände, die sich umeinander schließen. (ANGEWANDTE CHEMIE, 20. April 2007) M AX P L ANCK FO RSCHUNG 2/2007 FÜR FÜR PROF. DR. GEORGE COUPLAND Max-Planck-Institut für Züchtungsforschung, Köln Tel.: +49 221 5062-205 Fax: +49 221 5062-207 E-Mail: coupland@ mpiz-koeln.mpg.de F ESTKÖRPERFORSCHUNG @ Kontakt: F OTO : MPI Die Existenz des sogenannten Florigens war bereits 1936 von dem Russen Michael Chailakhyan postuliert worden: Die Blütenpracht werde durch einen hormonellen Stimulus ausgelöst. Unklar war, ob es sich dabei um ein Eiweiß, eine Nukleinsäure oder eine andere Substanz handelte. In den 1990er-Jahren grenzten Detlef Weigel und seine Mitarbeiter am Salk Institute in La Jolla (USA) den lang gesuchten Blütentreiber auf molekularer Ebene ein: Sie hatten bei der Ackerschmalwand Arabidopsis thaliana das Gen Flowering Locus T entdeckt, kurz FT genannt (Kardailsky et al., SCIENCE 1999). Dieses muss in den Blättern aktiviert werden, damit sich an den Sprossspitzen Blüten bilden können. Die Frage blieb, wie FT jene Gene beeinflusst, die schließlich die Blüten hervorbringen. Der Durchbruch gelang Weigel und seinem Team, inzwischen am Max-Planck-Institut für Entwicklungsbiologie in Tübingen, sechs Jahre später: Sie entdeckten, dass FT an ein weiteres Protein bindet, das FD. Dieses Protein steuert direkt die Aktivität von Genen, sodass sich Gruppen von Stammzellen an der Sprossspitze zu Blüten entwickeln. FD wird erst durch Bindung an das FT-Protein aktiv und im Gegensatz zu FT an den Sprossspitzen produziert (Wigge et al., SCIENCE 2005). Da das FT-Gen nur in den Blättern aktiv ist, muss das entsprechende Protein, um an FD binden zu können, irgendwie vom Blatt in die Sprossspitze gelangen. Möglicherweise geht dabei nicht das FT-Protein selbst auf Wanderschaft, sondern die entsprechende Boten-RNA. Das zumindest glaubten Tao Huang, Postdoc an der Schwedischen Universität für Agrarwissenschaften in Umea, und seine Kollegen, als sie die mRNA von FT sowohl in den Blättern als auch in der Sprossspitze fanden (Huang et. al., SCIENCE 2005). Mitte April 2007 zogen die schwedischen Pflanzenforscher um Ove Nilsson diese Veröffentlichung jedoch wieder zurück, nachdem der Versuch, die Experimente zu wiederholen, fehlgeschlagen war. SCIENCE veröffentlichte den Widerruf in derselben Ausgabe, in der Georg Coupland und seine Mitarbeiter ihre jüngsten Ergebnisse vorstellten: In Zusammenarbeit mit Kollegen vom Imperial College in London hatten sich die MaxPlanck-Forscher mittels GFP – eines aus einer Qualle stammenden grün fluoreszierenden Proteins – an die Fersen des FT-Proteins geheftet. So verfolgten die Wissenschaftler den Weg des GFP-FT-Komplexes in Arabidopsis vom Blatt bis zur Pflanzenspitze unter dem Mikroskop und zeigten, dass das FT-Protein tatsächlich in den Blättern gebildet wird und danach durch die gesamte Pflanze bis in den Wuchskegel der Sprossspitzen wandert, wo es die Blütenbildung induziert. Einen weiteren Beleg dafür, dass das FT-Protein – und nicht die dazugehörige mRNA – wandert, lieferte ein Versuch mit Arabidopsis-Mutanten, die kein FT-Protein bilden, da ihnen das entsprechende Gen fehlt. Diese Mutanten wurden auf normale Arabidopsis-Pflanzen gepfropft. Die Forscher beobachteten nun, wie das FT-Protein aus der unteren Pflanze durch die aufgepfropfte, FT-freie Pflanze hindurchwanderte und schließlich Blüten gebildet wurden. Trotzdem: Nicht alle Wissenschaftler halten die Beweiskraft der Experimente für ausreichend. Das Schlusskapitel im Florigen-Krimi lässt also noch auf sich warten. ● Z ÜCHTUNGSFORSCHUNG PFLANZENFORSCHUNG F OTO : MPI Das FT-Protein wurde mit einem grün fluoreszierenden Protein (GFP) markiert und im Gefäßsystem eines jungen ArabidopsisKeimlings unter dem Mikroskop beobachtet. So konnte experimentell nachgewiesen werden, dass das FT-Protein aus den Blättern bis in die Sprossspitzen der Ackerschmalwand wandert. FORSCHUNG AKTUELL 1027 Moleküle mit nahezu hunderttausend unterschiedlichen Formen machen unseren Körper zu dem, was er ist. Jedes Molekül trägt eine strukturelle Information. „Diese Informationen entscheiden darüber, welche Moleküle zusammenarbeiten, damit der Körper funktioniert“, sagt Magalí Lingenfelder, eine der beteiligten Max-PlanckForscherinnen. So vermitteln Biomoleküle den Befehl, dass unsere Muskeln kontrahieren. Sie sorgen dafür, dass wir unsere Nahrung effizient verwerten. Und sie lassen Gedanken entstehen. Das internationale Forscherteam, in dem Wissenschaftler aus dem Stuttgarter Max-Planck-Institut, vom Fraunhofer Institut für Werkstoffmechanik in Freiburg und dem King‘s College in London zusammenarbeiteten, hat nun im Detail verfolgt, wie zwei Diphenylalanin-Moleküle miteinander wechselwirken, während sie sich aneinanderlagern. Die Wissenschaftler vom Max-Planck-Institut für Festkörperforschung schossen mit einem Rastertunnelmikroskop Bildsequenzen von diesem Prozess. Auf den Filmen ist zu erkennen, dass sich nur Moleküle gleicher Chiralität, also identischer Struktur, erkennen. Nur sie schließen sich also bereitwillig zu Paaren und Ketten zusammen. „Auf diese Weise nutzt die Natur Informationen, die in der Molekülgestalt stecken, um komplexe Strukturen aufzubauen“, so Magalí Lingenfelder. Ein wichtiger Teil dieser Information ist in der Chiralität gespeichert. Der Begriff der Chiralität Eine Begegnung molekularer Art: Rastertunnelmikroskopie-Aufnahmen zeigen, wie sich Diphenylalanin-Moleküle aneinanderlagern. leitet sich vom griechischen Wort für Hand ab und beschreibt Moleküle, die wie linke und rechte Hände in zwei Formen existieren: der rechtshändigen und der linkshändigen Form. Sie lassen sich räumlich nicht zur Deckung bringen – im Bild der Hand gesprochen liegen entweder die Handflächen beziehungsweise -rücken aufeinander oder die Daumen zeigen in entgegengesetzte Richtungen. Und nur zwei rechte oder zwei linke Hände greifen beim Handschlag passgenau ineinander. Genauso formen auch nur zwei Moleküle derselben chiralen Form eine stabile Struktur. Wenn sich Moleküle der rechtshändigen oder linkshändigen Form zusammenschließen, sprechen Chemiker von chiraler Erkennung. „Sie ist für alle Prozesse in unserem Körper von großer Bedeutung“, sagt Giovanni Costantini, der ebenfalls an den Arbeiten beteiligt war: „Die laufen nämlich nur ab, wenn sich rechtshändige oder linkshändige Moleküle untereinander erkennen.“ Wie beim Händeschütteln reicht es aber nicht, dass sich zwei Moleküle derselben chiralen Form finden, sie müssen sich zudem einander anpassen. Auch Hände greifen schließlich nur ineinander, wenn sie sich umeinander schließen. Während die Max-Planck-Wissenschaftler den molekularen Handschlag beobachteten, haben Theoretiker am King‘s College in London und am Fraunhofer Institut für Werkstoffmechanik in Freiburg den Prozess rechnerisch modelliert. „Der Mechanismus chiraler Molekülerkennung hilft uns, die elementaren Schritte der Evolution zu verstehen“, so Costantini. Er könne aber auch dazu beitragen, komplexe künstliche Materialien mit spezifischen Funktionen zu entwickeln. ● 2/2007 M AX PL A NCK F ORSCHUNG @ Kontakt: DR. MAGALÍ LINGENFELDER Max-Planck-Institut für Festkörperforschung, Stuttgart Tel.: +49 711 689-1620 Fax: +49 711 689-1620 E-Mail: m.lingenfelder@ fkf.mpg.de 9 FORSCHUNG AKTUELL FORSCHUNG AKTUELL ANTHROPOLGIE ASTROPHYSIK Wie lange ist ein Kind ein Kind? Licht gibt Asteroiden Spin Eine lange Kindheit hat einen hohen Preis – rein biologisch: Kinder können sich nicht selbst ernähren, sind auf die Gefahren ihrer Umwelt nicht vorbereitet und fortpflanzen können sie sich auch nicht. „Dafür können Kinder behütet und angeleitet von Erwachsenen besser lernen“, sagt Tanya Smith, die am Max-Planck-Institut für evolutionäre Anthropologie an dem Projekt mitgearbeitet hat. Da moderne Menschen mehr lernen als andere Lebewesen, dauert auch ihre Kindheit länger als die aller anderen Primaten. Die ausgedehnte Jugend bedeutet auch, dass die Zähne langsamer wachsen. Und das war auch schon so, kurz nachdem sich der Mensch aus seinen evolutionären Vorfahren entwickelt hatte. Das hat das internationale Forscherteam jetzt am Wachstumsprofil eines Menschen nachgewiesen, der vor 160 000 Jahren im heutigen Djebel F OTO : PNAS, P ROCEEDINGS OF THE N ATIONAL A CADEMY OF S CIENCES , USA Ein virtuelles Gebiss haben Wissenschaftler aus einem fossilen Kiefer rekonstruiert. Im Hintergrund ist die Maserung des Zahnschmelzes zu erkennen. 10 M AX P L ANCK FO RSCHUNG 2/2007 Irhoud in Marokko lebte. Er war mit acht Jahren gestorben und auch nicht weiter entwickelt als ein gleichaltriges Kind unserer Zeit, wie die Wissenschaftler an den fossilen Überresten seiner Zähne feststellten. Selbstverständlich ist das nicht: Die Vorgänger des Homo sapiens, Homo heidelbergensis und Homo erectus und die noch früheren Australopithecus-Arten, waren mit acht Jahren schon deutlich erwachsener. Ihre Jugend währte nur etwa so lange wie die von Schimpansen. „Den modernen Menschen charakterisiert aber ein ganz anderes Verhalten und eine ganz andere Kultur, die längeres Lernen nötig macht“, sagt Tanya Smith: „Bislang war jedoch unklar, wann sich das reproduktive Verhalten und die körperliche Entwicklung daran angepasst haben“ – ab wann die Kindheit also so lange dauerte wie beim modernen Menschen. „Unsere Ergebnisse belegen, dass der Homo sapiens schon sehr früh in seiner Entwicklungsgeschichte die kulturellen und auch biologischen Charakteristika des heutigen Menschen besaß“, sagt Smith: „Wenn wir die Entwicklung der Hominiden als Ganzes betrachten, treten diese Eigenschaften aber erst sehr spät auf, nämlich erst im Homo sapiens.“ Abgelesen haben die Wissenschaftler das biologische Alter des achtjährigen Menschen aus Djebel Irhoud an seinen Zähnen. Feine Linien zeichnen den Zahnschmelz wie Jahresringe einen Baumstamm. Aus ihnen können Wissenschaftler rekonstruieren, in welchem Alter sich die ersten Backenzähne aus dem Kiefer geschoben haben. Dieses Alter gibt wiederum einen sehr guten Orientierungspunkt, wie schnell ein Mensch gewachsen ist. Und das auch noch Millionen von Jahren nach seinem Tod. Wie lange ein Zahn gewachsen ist, lässt sich jedoch nur im Inneren des Zahnschmelzes herausfinden, weil nur dort die detaillierte Struktur der Linien zu erkennen ist. Dort hineinzublicken, ohne den Zahnschmelz zu zerstören, ist nicht einfach, aber möglich: Paul Tafforeau, Wissenschaftler an der European Synchrotron Radiation Facility in Grenoble, entwickelte dafür eine Methode der Mikrotomografie. Mit Synchrotron-Röntgenstrahlung löst er sehr feine Strukturen des Zahnschmelzes dreidimensional auf, ohne ihm zu schaden. Wie der 160 000 Jahre alte Zahnschmelz des marokkanischen Kindes strukturiert ist, verglich Tanya Smith mit dem Zahnschmelz heutiger Menschenkinder und dem anderer Menschen-Arten. „Bislang haben uns Fossilien vor allem verraten, wie Menschen anatomisch gebaut waren“, sagt Tanya Smith: „Jetzt haben wir daraus zum ersten Mal auch den Lebenslauf eines Menschen abgelesen.“ ● Dass Sonnenstrahlen einen Stein ins Rollen bringen, hat auf der Erde noch niemand beobachtet. Im All ist das anders: Dort haben Astronomen aus Europa und den USA – darunter auch Hermann Boehnhardt vom Max-PlanckInstitut für Sonnensystemforschung – jetzt erstmals nachgewiesen, dass das Licht der Sonne eine Kraft auf den erdnahen Asteroid 2000 PH5 ausübt. Diese ist zwar sehr schwach, reicht aber, um den Himmelskörper jedes Jahr um eine Millisekunde schneller rotieren zu lassen. Damit haben sie zum ersten Mal den Yarkovsky-O‘Keefe-Radzievskii-Paddack-, kurz YorpEffekt gemessen. Diesen haben Astrophysiker theoretisch schon länger vorhergesagt. (SCIENCE EXPRESS, 8. März 2007) @ Kontakt: DR. TANYA M. SMITH Max-Planck-Institut für evolutionäre Anthropologie, Leipzig Tel.: +49 341 3550-362 Fax: +49 341 3550-399 E-Mail: [email protected] F OTOS : S TEPHEN C. L OWRY Vor 160 000 Jahren dauerte die Kindheit schon genauso lange wie heute. Dies hat nun ein internationales Forscherteam vom Leipziger MaxPlanck-Institut für evolutionäre Anthropologie und der französischen European Synchrotron Radiation Facility nachgewiesen. Die Wissenschaftler fanden heraus, dass die Zähne eines fossilen Homo sapiens-Kindes nicht weiter entwickelt waren als die eines heutigen Kindes im selben Alter. Auch das frühe Homo sapiens-Kind war also noch nicht ausgewachsen. Bei Australopithecus- und frühen Homo-Arten währte die Kindheit dagegen noch kaum länger als die von Schimpansen, die in zehn bis zwölf Jahren erwachsen werden. (PNAS, 19. März 2007) Asteroiden haben mit einer Kugel meistens nicht viel Ähnlichkeit. Der Asteroid 2000 PH5 etwa saust als flacher Felsbrocken durchs All, rund 120 Meter lang wie breit und knapp 60 Meter hoch. Obendrein verzerren Beulen die Symmetrie des Himmelskörpers. Und seine Oberfläche besteht auch noch aus verschiedenen Gesteinen. Das sieht nicht hübsch aus, macht 2000 PH5 aber – zusammen mit seiner kurzen Rotationsperiode von derzeit etwa zwölf Minuten – zu einem geeigneten Kandidaten, um den Yorp-Effekt zu messen: ein Drehmoment, das die Sonne mit ihrem Licht erzeugt und den Asteroiden allmählich schneller rotieren lässt. Der Effekt beruht darauf, dass ein Körper einen winzigen Rückstoß erfährt, wenn er Lichtteilchen abstrahlt. Der Yorp-Effekt ist jedoch nur an kleinen Himmelskörpern zu beobachten, die keine Kugelgestalt und eine uneinheitliche Oberfläche besitzen. Zum Beispiel an 2000 PH5. Seine unregelmäßige Gestalt sorgt dafür, dass sich manche Partien von 2000 PH5 stärker aufheizen als andere – und auch mehr Wärme als infrarotes Licht wieder abstrahlen. Mit dem sichtbaren Licht ist es nicht anders: Manche Regionen des kosmischen Felsens reflektieren es besser als andere. So erfahren manche Regionen auch einen größeren Rück- stoß als andere. Unterm Strich ergibt sich so ein Drehmoment, das dem Asteroiden Jahr für Jahr ein bisschen mehr Spin gibt. „Das Drehmoment ist allerdings so klein, dass der Yorp-Effekt bislang noch nicht beobachtet wurde“, sagt Hermann Boehnhardt. Dem Forscherteam, in dem er mitgearbeitet hat, ist das jetzt erstmals gelungen. Die Wissenschaftler haben den Asteroiden über fünf Jahre hinweg immer wieder mit optischen Teleskopen – darunter das 8,2-Meter Very Large Telescope Array und das 3,5-Meter New Technology Telescope der Europäischen Südsternwarte in Chile und die 3,5- und 2,2-MeterTeleskope im spanischen Calar Alto – verfolgt. Die Rotationsgeschwindigkeit berechneten sie aus dem Takt, in dem 2000 PH5 ihnen mal seine hel- Der Asteroid 2000 PH5 im Visier, aufgenommen mit dem 3,5-Meter-Teleskop im spanischen Calar Alto. Aus den Schwankungen seiner Helligkeit berechnen die Forscher die Rotationsgeschwindigkeit dieses Himmelskörpers, die unter dem Einfluss der Sonnenstrahlung stetig wächst. leren und mal seine dunkleren Seiten zuwandte. „Die Beschleunigung stimmt ziemlich genau mit theoretischen Vorhersagen einer anderen Gruppe überein“, so Boehnhardt. Demnach rotiert 2000 PH5 jährlich um eine tausendstel Sekunde schneller. Auf diese Weise könnte er noch zu einem der am schnellsten rotierenden Asteroiden im Sonnensystem avancieren: Legt sein Spin weiterhin so zu, braucht 2000 PH5 in 35 Millionen Jahren nur noch etwa 20 Sekunden, um einmal um sich selbst zu wirbeln. Statt des Rekords könnte die Beschleunigung 2000 PH5 aber auch ein vorzeitiges Ende bringen – wenn nämlich der Drall ihn zerreißt. „Möglicherweise lässt der Yorp-Effekt manche Asteroiden so schnell rotieren, dass sie auseinanderbrechen“, sagt Hermann Boehnhardt. Das könnte auch der Grund sein, warum Astronomen bislang keinen Asteroiden entdeckt haben, der weniger als 80 Sekunden für eine Drehung braucht. ● 2/2007 M AX PL A NCK F ORSCHUNG @ Kontakt: DR. HERMANN BOEHNHARDT Max-Planck Institut für Sonnensystemforschung, Katlenburg-Lindau Tel.: +49 5556 979-545 Fax: +49 5556 979-219 E-Mail: boehnhardt@ mps.mpg.de 11 FORSCHUNG AKTUELL KLIMAFORSCHUNG Rückkopplung im Treibhaus 12 M AX P L ANCK FO RSCHUNG 2/2007 B IOGEOCHEMIE @ Kontakt: PROF. DR. MARTIN HEIMANN Max-Planck-Institut für Biogeochemie, Jena Tel.: +49 3641 576-350 Fax: +49 3641 576-301 E-Mail: martin.heimann@ bgc-jena.mpg.de FOTO: DEUTSCHES ENTOMOLOGISCHES INSTITUT IM ZALF Messungen also berechnen, wie viel Kohlendioxid die Senke des südlichen Ozeans aufnimmt. Und wie sich deren Kapazität im Laufe der letzten 25 Jahre verändert hat. Eigentlich sollte der südliche Ozean heute mehr Treibhausgas aufnehmen als zu Beginn der Messungen. Schließlich hat die Kohlendioxid-Konzentration in der Atmosphäre deutlich zugenommen. Stattdessen aber stagnierte die Aufnahme in den letzten 25 Jahren, wie die Messungen des Wissenschaftlerteams belegen. Schuld ist der Klimawandel, der die Winde über dem südlichen Ozean anfacht. Diese wiederum verändern die Meeresströmungen. So gelangt mehr Wasser zur Oberfläche, das bereits mit Kohlenstoff gesättigt ist. Ähnliche Phänomene sind auch andernorts zu erwarten: „Wir müssen davon ausgehen, dass solche Rückkopplungen den Klimawandel auch in anderen Teilen der Welt verstärken“, sagt Heimann. ● Verstreut über den ganzen Erdball liegen die Messstationen (Sterne), in denen die Wissenschaftler die Kohlendioxid-Konzentrationen der Luft gemessen haben. So haben sie ermittelt, wie viel Treibhausgas der südliche Ozean aufnimmt. FÜR Abbrennende Wälder, rauchende Schlote und auch manche Regionen der Weltmeere bezeichnen Geochemiker als Kohlenstoffquellen. Nimmt ein Wald oder ein Ozean dagegen mehr Kohlendioxid auf, als er abgibt, sprechen sie von einer Kohlenstoffsenke. Und zumindest in die Meere sollte die Atmosphäre desto mehr Kohlendioxid drücken, je mehr sie enthält. Der südliche Ozean wurde auf diese Weise von einer Quelle zur Senke: Noch vor einigen Jahrzehnten setzte er unterm Strich Kohlendioxid frei. Inzwischen nimmt er netto Kohlendioxid auf, weil dessen Konzentration in der Atmosphäre so drastisch gestiegen ist. Das ist eine Sache des chemischen Gleichgewichts und lässt sich im Prinzip auch bei einem Wassersprudler beobachten. Wenn sich der südliche Ozean weiterhin an dieses Prinzip hielte, könnte er den zunehmenden Klimawandel abschwächen. „Doch der Klimawandel sorgt dafür, dass die Meere weniger Kohlendioxid aufnehmen“, sagt Prof. Dr. Martin Heimann, Direktor am Max-Planck-Institut für Biogeochemie in Jena: „So bleibt mehr vom Menschen emittiertes Kohlendioxid in der Atmosphäre, was wiederum den Klimawandel verstärkt.“ Diese positive Rückkopplung hat das internationale Wissenschaftlerteam, in dem unter anderen auch Forscher von der Universität East Anglia und des British Antarctic Survey mitarbeiten, jetzt erstmals mit Messungen belegt. Theoretisch vorhergesagt haben Wissenschaftler diesen Effekt schon länger. Nun haben die Wissenschaftler vom Jenaer Max-Planck-Institut Messungen von 42 Stationen, die sich über die gesamte Erde verteilen, ausge- wertet. Die Messstationen haben teilweise seit Beginn der 1980er-Jahre die Konzentration des Treibhausgases in ihrer Umgebung registriert. Wie stark die Konzentrationen zwischen den einzelnen Stationen zu- oder abnehmen, hängt unter anderem von den Luftströmungen ab. Aber auch davon, wie viel Gas die Senken aus der Luft ziehen. Im Umkehrschluss konnten die Forscher aus ihren G RAFIK : MPI Die Ozeane nehmen fast ein Drittel des Kohlendioxids auf, das die Menschheit in die Atmosphäre bläst. Und je mehr Treibhausgas die Luft belastet, desto mehr sollte sich auch in den Meeren lösen. Tut es aber nicht. Zumindest im südlichen Ozean macht sich in den letzten 25 Jahren ein Sättigungseffekt bemerkbar. Das hat ein internationales Forscherteam unter der Führung des Max-Planck-Instituts für Biogeochemie in Jena jetzt erstmals gemessen: Obwohl die Kohlendioxid-Emmissionen seit den frühen 1980er-Jahren um 40 Prozent zugenommen haben, nahm der südliche Ozean nicht mehr Kohlendioxid auf. Schuld ist eine Rückkopplung: Der Klimawandel, den Treibhausgase zumindest mitverursachen, stört den Kohlenstoffkreislauf der Ozeane. (SCIENCE, 17. Mai 2007) Panorama FORSCHUNG AKTUELL AUF EINE NEUE ART VON FLÖHEN sind Forscher des Radolfzeller Max-Planck-Instituts für Ornithologie an Nestlingen des Kleinen Felsensittichs gestoßen, der an den Steilküsten Patagoniens brütet. Dabei handelte es sich um Sandflöhe der Gattung Hectopsylla, die den Wissenschaftlern durch ihren ungewöhnlichen, für Flöhe bislang einzigartigen Nistplatz auffielen: Sie parasitieren in den Nasenhöhlen und unter den Zungen der Sittichküken. Hectopsylla narium, so der Name der neu entdeckten Flöhe, ist mit Tunga penetrans verwandt, dem Überträger der Tropenkrankheit Tungiasis. Die Weibchen dieser Sandflohart bohren sich bevorzugt in die Haut menschlicher Füße, legen dort ihre Eier ab und verursachen schwere Entzündungen. Die übrigen 22 Sandfloharten kommen vor allem in Südamerika an verschiedenen Säugetieren und Vögeln vor. DIE ZÜCHTUNG VON ENERGIEPFLANZEN, die vermehrt Biomasse bilden, fassen Wissenschaftler des Max-Planck-Instituts für Pflanzenphysiologie und der Universität Potsdam ins Auge. Es geht dabei um die Frage, ob und wie sich Pflanzen dazu bringen lassen, vermehrt Biomasse zu bilden – also organische Substanz, die dann als Träger und Lieferant regenerativer Energie dienen kann. Um zu derart gemästeten Pflanzen zu kommen, muss deren Stoffwechsel im Detail erforscht werden: Welche ihrer Inhaltsstoffe (Zucker, Säuren oder Proteine) und welche äußeren Faktoren (Licht, Wasser und Nährstoffe) beeinflussen das Wachstum und damit die Produktion von Biomasse? Als Modellorganismus zur Klärung solcher Zusammenhänge dient den Forschern eine breite Palette von genetisch gut charakterisierten Linien der Ackerschmalwand Arabidopsis thaliana, die sich durch große Unterschiede im Wachstum auszeichnen – Unterschiede, die es nun in Bezug zu den Inhaltsstoffen der einzelnen Pflanzen zu setzen gilt, um dann weiter zu Vorhersagen des Ertrags zu kommen. DER ÄTNA LIEFERT KATALYSATOREN, die sich für die großtechnische Herstellung von Nanoröhrchen und Nanofasern aus Kohlenstoff anbieten. Das entdeckten Forscher des Berliner Fritz-HaberInstituts der Max-Planck-Gesellschaft: Sie pulverisierten zunächst Lavagestein aus dem Ätna und erhitzten es unter einer Wasserstoffatmosphäre auf 700 Grad Celsius, wodurch die in der Lava enthaltenen, fein verteilten Eisenoxide zu elementarem Eisen reduziert wurden. Dann leiteten die Forscher über dieses Pulver ein Gasgemisch aus Wasserstoff und Ethylen – und erhielten winzige Röhrchen und Fasern aus Kohlenstoff, die sich an den Lavapartikeln abgeschieden hatten. Dieses Verfahren könnte den Weg zu einer effizienten und kostengünstigen Herstellung von Kohlenstoff-Nanoröhrchen ebnen. Denn zum einen wird der vulkanische Katalysator Eine neue Flohart haben Forscher des Max-PlanckInstituts für Ornithologie entdeckt: Hectopsylla narium (hier der Kopf in einer elektronenmikroskopischen Aufnahme) lebt in den Nasenhöhlen und unter den Zungen von Küken des Kleinen Felsensittichs. vom Ätna in großen Mengen geliefert; zum andern ist das als eigentlicher Katalysator wirkende Eisen feinst verteilt an das extrem poröse Lavagestein gebunden, das damit zugleich als Katalysator und Träger dient. Und ein weiterer Vorteil des Verfahrens liegt noch darin, dass es ohne nasschemische Schritte auskommt. DAS GEHIRN IM TRAUMSCHLAF haben Wissenschaftler des Münchner Max-Planck-Instituts für Psychiatrie jetzt erstmals mit einem kombinierten Messverfahren untersucht: Zugleich mit der Registrierung von Hirnströmen mittels Elektroenzephalografie (EEG) setzten sie die bildgebende funktionelle Kernspintomografie ein, um die Aktivität des Gehirns an schlafenden und träumenden Probanden aufzuzeichnen. So konnte beispielsweise genau verfolgt werden, wie das Gehirn im Schlaf auf akustische Reize – etwa Klaviermusik – reagiert. Besonders interessante Befunde lieferten Messungen während des sogenannten REM-Schlafs, also während Traumphasen, die mit raschen Augenbewegungen (engl.: Rapid Eye Movements) einhergehen: Hier ließen sich wiederkehrende, kurzzeitige Phasen hoher Hirnaktivität nachweisen, in denen äußere Reize vom Gehirn ausgeblendet werden und der Schläfer quasi wehrlos ist; dazwischen aber lagen Phasen, in denen Außenreize rudimentär wahrgenommen und gelegentlich sogar in das Traumgeschehen einbezogen werden. ● 2/2007 M AX PL A NCK F ORSCHUNG www Mehr zu diesen Themen finden Sie unter www. maxplanck.de 13