Die Schlacht im Mund oder der Aggressivität von Bakterien
Werbung

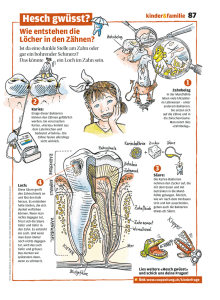
Die Schlacht im Mund oder der Aggressivität von Bakterien auf der Spur Die Mundhöhle ist ein Biotop, in dem Bakterien, mitunter auch Viren und Pilze, eine Schlacht um optimale Lebensbedingungen austragen. Doch ein Ungleichgewicht zwischen den Mikroorganismen bzw. die Besiedlung mit Krankheit auslösenden Keimen können Zähne, Zahnfleisch und damit die Gesundheit gefährden. An der Universität Leipzig will man es nun genauer wissen und erforscht, was während der mikrobiologischen Interaktionen passiert. Während über die Normalbesiedelung mit Viren noch wenig bekannt ist, weiß man über das Pilze problematisch sind. Bestimmte Bakterien seien zudem als Schutz gegen besonders aggressive Arten und gegen Viren wichtig, so Dr. Stefan Rupf, Oberarzt an der Poliklinik für konservierende Zahnheilkunde und Parodontologie an der Universität Leipzig. Nun sind die Schuldigen zwar längst ausgemacht, z. B. sind vor allem die Mutans-Streptokokken für Karies verantwortlich. Doch jede Bakterienart gliedert sich in verschiedene, unterschiedlich aggressive Stämme, die sich wiederum im Laufe der Zeit bis in die Genstruktur hinein verändern können. Bleibt also die Frage, wie man nicht nur die Anwesenheit bestimmter Bakterien registrieren, sondern so viel wie möglich über deren aktuelle Aggressivität erfahren kann. Mit kombinierten Verfahren dem Mikroklima im Mund auf der Spur Hier nutzen die Zahnmediziner zur Analyse ein besonderes Massenspektrometrie-Verfahren: MALDI-TOF (Matrix Assisted Laser Desorption/Ionisation Time of Flight) Massenspektrometrie. Ein Verfahren, welches das Biochemiker-Team um Prof. Dr. Klaus Eschrich, Institut für Biochemie der Universität Leipzig, bereits für die Feinanalyse von Bakterien-Unterarten eingesetzt hatte. Dabei werden die zu analysierenden Substanzen - in diesem Fall die Eiweißbestandteile der Bakterien mittels Laserenergie ionisiert und diese Ionen anschließend innerhalb eines Vakuums durch ein elektrisches Feld beschleunigt. Aufgrund unterschiedlicher Geschwindigkeiten werden die Teilchen so sortiert. In einer Grafik zeigen dann verschiedene Spitzen, welche Eiweiße bei einem bestimmten Bakterium besonders häufig vorkommen. "Wir können also einerseits im Labor die Säureproduktion einzelner Bakterienstämme messen und andererseits parallel dazu über MALDI-TOF Massenspektrometrie deren Eiweißstruktur und, mit anderen Methoden, auch ihr Genom charakterisieren. Dann geht es ans Vergleichen", erklärt Dr. Rupf den Fortgang der Analyse. So will man herausfinden, welche Stämme unter welchen Umständen besonders schädlich für Zähne und Zahnfleisch sind. Praxiseinsatz noch nicht anzudenken Ziel ist eine Nutzung zur Prävention Bislang zählt dieser Ansatz noch zur Grundlagenforschung, wie Dr. Rupf erläutert. "Die Impfung von Patienten gegen Karies war bislang erfolglos. Auch das kontrollierte Einbringen von Bakterien in die menschliche Mundhöhle ist nicht ohne Risiko, denn sie könnten nicht nur die aktuelle Balance unkontrolliert verändern, sondern auch die Mundhöhle verlassen und sich in anderen Körperregionen ansiedeln. Ich vermute einen Lösungsansatz vor allem in der Identifizierung von Faktoren, die bekannte Bakterienstämme besonders aggressiv machen. Wenn man dies weiß, könnte man im Vorfeld pathologischer Veränderungen neue Wege der Prävention beschreiten." Mundhygiene das wichtige Mittel für Zahngesundheit Wer nun glaubt, er könne die Zahnbürste demnächst wegstecken, der irrt allerdings. "Nach wie vor spielt die Mundhygiene eine wichtige Rolle beim Kampf gegen Karies und Parodontitis", so Dr. Rupf. Und dabei ist 1 die Zuckermenge aus zahnmedizinischer Sicht für den Schutz vor Karies weniger bedeutsam als die Häufigkeit, mit der man den Bakterien neue Nahrung zuführt und sie so zur ständigen Säureproduktion animiert. (Quelle: Pressemitteilung der Universität Leipzig über idw) 2