20Aorten- und Arterienerkrankungen
Werbung

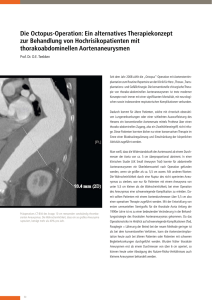
20 Aorten- und Arterienerkrankungen Messsequenzen und Fragestellung Anatomie von Aorta und Arterien inklusive Gefäßwand: DIR-TSE (Black-Blood-TSE), Flussanalyse: PC-Angiographie und -Mapping, Entzündung in der Gefäßwand: T1w-gespoilte TurboGRE-Sequenz (LE), Angiographie der Aorta und Arterien: 3D-kontrastverstärkte MRA. Messprotokoll für die CE-MRA T1-gewichtete, gespoilte 3D-Gradientenechosequenz, Flipwinkel: 20–40° (30–60°), TR 2–4 ms (kurz), TE < 2,5 ms, Messung kleiner Schichtdicken quer zum Gefäß und Addition zum Messvolumen, starke Sättigung des stationären Gewebes und des Blutes in der Messschicht durch die Gradientenechosequenz, MR-Kontrastmittelgabe als Bolus: bei Passage des gemessenen Gefäßabschnitts erfolgt eine starke T1-Verkürzung = maximales T1w-Signal (= stärkste Herabsetzung der Blutsättigung), Bildgebungsvolumen langstreckig entlang der Gefäßachse orientiert: großes FOV-3D sagittal/koronal, Messung der kontrastgebenden zentralen k-Linien (ky = 0) zu Beginn der Sequenz bei Kontrastmittelankunft (= Zentrum des Kontrastmittelbolus): dadurch Aufnahme des Arteriensignals und Unterdrückung des Venensignals, Aufnahmezeit: exakt bei Durchlauf des Maximums des Kontrastmittelbolus, alternativ schnellere Auffüllung des k-Raums durch: − Keyhole-Technik, − elliptisch-zentrische Auffüllung des k-Raums, Injektionszeit des Kontrastmittels und Länge der Messsequenz: minimal 2/3 der Messzeit, Kontrastmittelmenge: 0,2 mmol/kg Körpergewicht pro Minute, typische Untersuchungs-/Messdaten für die CE-MRA: − TR unter 6 ms, TE unter 2,5 ms, Flipwinkel 30–60°, − FOV 320 × 400 mm, Matrix 256 × 192 (256), − Schichtdicke: 1,5–3 mm mit 24 sukzessiven Schichten, − partielle k-Raum-Abtastung: 48 sukzessive Schichten in 20–30 s, − bei Anwendung von SENSE: Aufnahme von 60 Schichten à 0,9 × 0,9 × 1 mm in 12 s, − Schnittebene: 3D-Volumen frei wählbar, − Kontrastmittel: Gd-DTPA oder Gd-BOPTA: 0,2 mmol/kg Köpergewicht/min, Gesamtmenge: 20–40 ml, Injektionsgeschwindigkeit: 1,5–3,0 ml/s, injizierte Boluslänge: 60–80 % der Akquisitionszeit, − Kontrastmitteldetektion: Testbolus mit Messung der Kreislaufzeit und Start durch den Anwender, automatische Erkennung der Ankunft des Bolus und Start der Messung (Bolus-TRAK, CARE-Bolus, SMART). MR-relevante Krankheitsbilder Aneurysma dissecans, intramurale Hämatome, Aneurysma verum, Bauchaortenaneurysma, inflammatorisches Bauchaortenaneurysma, Nierenarterienstenose(n), Mesenterialarterienstenose(n), Leriche-Syndrom. Aorten- und Arterienerkrankungen Aneurysma dissecans Typ I Typ II Typ III Ätiologie Ein Aneurysma dissecans kann als Folge einer Atherosklerose oder einer arteriellen Hypertonie entstehen. Typen thorakal (nach De Bakey; Abb. 20.1): – Typ I: Aszendens bis linke A. subclavia, – Typ II: nur Aszendens, – Typ III: ab linker A. subclavia zur Deszendens (Letalität Typ I 1–2 %/h, 80 % nach 2 Wochen); thorakoabdominal (nach Crawford; Abb. 20.2): – Typ I: Deszendens thorakal bis suprarenal abdominal, – Typ II: Deszendens thorakal bis zur Bifurkation abdominal, – Typ III: knapp oberhalb des Zwerchfells beginnend bis zur Bifurkation abdominal, – Typ IV: nur abdominal unterhalb des Zwerchfells bis zur Bifurkation. MRI-Technik und -befunde Black-Blood-TSE: Aortenwanddestruktion: wahres Lumen dunkel, falsches Lumen hell, ggf. Leck paraaortal mit erhöhter SI, drohende Ruptur bei hoher SI im Perikard(erguss), 20.1 Schema der Typen von dissezierenden Aortenaneurysmen nach De Bakey: Typ I von der Aortenklappe bis zu den Iliacalarterien (links), Typ II nur im Aszendensbereich bis zum Truncus (Mitte) und Typ III in der deszendierenden thorakalen Aorta distal des Abgangs der linken A. subclavia bis in den Beckenbereich (rechts); Stanford A = Typ I + II, Stanford B = Typ III Typ I Typ II Diaphragma Truncus coeliacus A. renalis A. mesenteria superior 20.2 Schema der vier Typen von (dissezierenden) thorako-abdominalen Aortenaneurysmen nach Crawford Typ III Typ IV 161 162 Aorten- und Arterienerkrankungen 20.3 MR-Bild eines Aortenaneurysmas (Marfan-Syndrom) (links); MR-Bild einer Aortitis mit Aneurysma (Mitte) und LE: Kontrastmittelanreicherung in der Aortenwand (rechts oben) mit Thrombus im Lumen (rechts unten) (modifiziert nach Hombach et al. 2005) 3D-CE-MRA: Darstellung des falschen und des wahren Lumens sowie des Entrys und ggf. des Reentrys, Typ der Dissektion, Beteiligung von Seitenästen (Abgang innerhalb oder außerhalb der Dissektionsmembran: supraaortale Arterien, rechter Truncus, Karotiden, Subklavia), Cine-SSFP: Darstellung einer begleitenden Aortenklappeninsuffizienz, Ruptur an der Aortenbasis oder der Aortenklappe. Follow-up mit MRI Ideale Methode zur Nachsorge und Überwachung von Patienten mit konservativer oder operativer Behandlung: Durchmesser der Aorta, Ausschluss einer Restdissektion, Verdickung der Prothese, Leck an der Prothese mit Hämatom. Intramurale Hämatome Ätiologie Ein intramurales Hämatom hat die gleichen Ursachen wie eine Aortendissektion. Typen Es handelt sich um eine Vorstufe der Aortendissektion. Eine spezielle Typen-Einteilung gibt es nicht. Aneurysma verum Ätiologie Ursächlich für ein Aneurysma verum kann eine Mediadegeneration, ein Marfan-Syndrom oder eine Atherosklerose sein. Typen Man unterscheidet die fusiforme von der sakkulären Form und dem Aneurysma spurium (= »Aneurysma falsum«). MRI-Technik und -befunde Black-Blood-TSE: Aortenwanddicke, Aortendurchmesser, ggf. Leck paraaortal mit Hämatom oder Thrombus, 3D-CE-MRA: Darstellung des gesamten Aortenbogens mit Ausdehnung und Grad des Aneurysmas, ggf. begleitende Aortitis (LE der Aortenwand; Abb. 20.3), Cine-SSFP: Darstellung einer begleitenden Aortenklappeninsuffizienz. Follow-up mit MRI Im Rahmen der konservativen Therapie: Durchmesserkontrolle, Kontrolle des Grades der Aorteninsuffizienz; postoperativ: Prothesenfunktion, ggf. Leck an der Prothese mit Hämatom. Bauchaortenaneurysma MRI-Technik und -befunde Black-Blood-TSE: Aortenwand mit Hämatomausbreitung und -lokalisation, Verteilung exzentrisch oder zirkumferenziell, SI: grau bis hell. Ätiologie Ein Bauchaortenaneurysma kann als Folgeerkrankung einer Atherosklerose oder einer arteriellen Hypertonie entstehen. Follow-up mit MRI Progression bis zur Dissektion und/oder Ruptur (in 1/ der Fäl3 le). Typen Man unterscheidet das Aneurysma verum von dem inflammatorischen Aneurysma. Aorten- und Arterienerkrankungen MRI-Technik und -befunde Black-Blood-TSE: Aortenwanddicke, Aortendurchmesser, ggf. Leck paraaortal mit Hämatom oder Thrombus, 3D-CE-MRA: Darstellung des gesamten Aneurysmabereichs mit Ausdehnung und Grad des Aneurysmas, Darstellung des Aneurysmahalses und zusätzlicher Gefäßstenosen. Follow-up mit MRI Verlaufskontrolle bei konservativer Therapie (Durchmesser, Ausdehnung), Kontrolle von Stent-Grafts oder Protheseninterponat. Inflammatorisches Bauchaortenaneurysma Ätiologie Hierbei handelt es sich um eine chronische Inflammation aus weitgehend unbekannter Ursache. MRI-Technik und -befunde Black-Blood-TSE: Aortenwanddicke, Aortendurchmesser, Größe und Ausdehnung der Fibrose, Beziehung zum dorsalen parietalen Peritoneum, Miteinbeziehung der Nierenarterien, Befall anderer Bauchorgane, Planung der OP, 3D-CE-MRA: Darstellung des gesamten Aneurysmabereichs mit Ausdehnung und Grad des Aneurysmas, Planung der OP. Follow-up mit MRI Verlaufskontrolle nach Operation. Nierenarterienstenose(n) Ätiologie Eine Nierenarterienstenose ist häufig atherosklerotisch oder durch eine arterielle Hypertonie bedingt. Typen Es wird eine atherosklerotische und eine fibromuskuläre Form unterschieden. MRI-Technik und -befunde PC-Flussmessung und besonders 3D-CE-MRA: Darstellung der Lokalisation und der Länge der Stenose, der Schweregrad ist indirekt ablesbar an den signifikanten Unterschieden der Parenchymanfärbung, der Dicke des Nierenkortex und der verminderten Gd-Kontrastmittel-Ausscheidung. Merke: Die Quantifizierung des Stenosegrades mittels MRI ist unsicher, sie erfolgt ggf. besser mit transkutanem Doppler. Follow-up mit MRI Langzeitverlauf nach PTA oder operativer Beseitigung (Plastik). Mesenterialarterienstenose(n) Ätiologie Mesenterialarterienstenosen sind ebenfalls entweder atherosklerotisch oder durch eine arterielle Hypertonie bedingt. MRI-Technik und -befunde PC-Flussmessung: Messung des Mesenterialflusses in Ruhe und postprandial: normalerweise relativ rascher Anstieg der Flussgeschwindigkeit postprandial, bei Mesenterialischämie verzögerter oder fehlender Anstieg der postprandialen Flussgeschwindigkeit, 3D-CE-MRA: Darstellung von Zahl und Lokalisation der Stenose(n) bzw. eines Verschlusses einer oder mehrerer der drei Mesenterialgefäße. Merke: Bei Befall von zwei der drei Mesenterialgefäße ist die Diagnose einer Mesenterialischämie gesichert. Die Quantifizierung des Stenosegrades mittels MRI ist unsicher. Follow-up mit MRI Langzeitverlauf nach PTA oder operativer Beseitigung (Plastik). Leriche-Syndrom Ätiologie bei chronischem Verschluss: Die Genese ist meist arteriosklerotisch; selten kommt es im Zusammenhang mit einer Takayasu-Arteriitis oder einer kongenital hypo- oder dysplastischen Erkrankung zum Leriche-Syndrom. bei akutem Verschluss der infrarenalen Aorta: Ursächlich können hierfür Traumen, thromboembolische Erkrankungen, eine Aneurysmathrombose oder eine In-situThrombose einer präexistenten, ulzerierten Plaque sein. 163