Zellstoffwechsel Stoffwechsel
Werbung

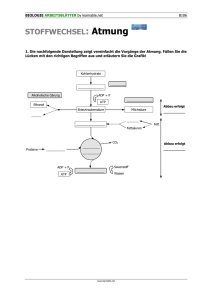
06.10.2011 Zellstoffwechsel Stoffwechsel Gesamtheit aller chemischen und energetischen g Umsetzungen g im Organismus. Der Austausch erfolgt über Oberflächen und spezielle Organe. Stoffaufnahme Stoffabgabe Fließgleichgewicht 1 06.10.2011 OXYDATION Dehydrierung - H2 CH3 – CH – COOH CH3 – C – COOH OH O + H2 REDUKTION Hydrierung Milchsäure Brenztraubensäure A – Substrat – H + Ferment A – Substrat + Ferment – H Ferment – H + B – Substrat B – Substrat – H + Ferment H2 – übertragendes Ferment als „Vermittler“ (Katalysator) entspricht der Funktion der Enzyme 2 06.10.2011 Aufbau eines Enzyms Holoenzym Proteinanteil Nichtproteinanteil Apoenzym Coenzym Wirkungsmechanismus von Enzymen 3 06.10.2011 Verdauungsenzyme: Einteilung nach Wirkungsrichtung: Kohlehydrate……………Amylasen Disaccharasen, Hexokinase, Isomerase, Aldolase, Fette………………………Lipasen Eiweiße…………………...Proteasen Polypeptidasen Dipeptidasen Pepsin 4 06.10.2011 Strukturformel von AMP, ADP ATP energiereiche Verbindung Phosphorylierung = P-Abgabe Phosphorylierung ATP überträgt üb t ä t das d endständige d tä di Ph Phosphorsäuremolekül h ä l kül auff Glucose und überführt sich selbst damit in das um 1 Phosphatgruppe ärmere ADP Mg ++ Glucose + ATP Glucose – 6 – Phosphat + ADP Hexokinase 5 06.10.2011 Vitamine Fettlösliche Vitamine: A D E K A: enge chem. chem Beziehung zum Carotin (Retinol) Schutzwirkung auf Epithelien D: Steroid, kann unter UV-Einfluss in Haut Gebildet werden (Calciferol) enth. in Leberöl, Butter verantw. Für Ca-Resorption im Darm (Rachitis) hoher Ca-Stoffw. hoher Vitaminbedarf (Wachstum) E: Tocopherol Antioxidans, wirkt toxischen Oxidationsprodukten entgegen stabilisiert oxidationsempfindliche Phospholipide K: Blutgerinnungsfaktor (Faktor VII) antihämorrhag. Vitamin Mangel: Störung in Blutgerinnung Wasserlösliche Vitamine • B-Komplex B1: C Coenzym d der D Decarboxylasen b l und dd der Ald Aldehydtransferasen h dt f wirkt i kt b beii Decarboxilierung der BTS Mangel: Störungen KH-Abbau Degeneration der Nerven und Muskelgewebe (Beri-Beri-Krankheit 19. Jh Verzehr von poliertem Reis • B2: Bestandteil von > 50 Enzymen (Riboflavin) Mangel: Hauterkrankungen, Hauterkrankungen Wachstumsstillstand • B6: Pyridoxin Coenzym in AS-Stoffwechsel Mangel: Wachstumsstörungen, Anämie Lymphknotenatrophie 6 06.10.2011 Wasserlösliche Vitamine • B12: Teil von CoA, verantwortlich mit für Stoffwechsel Mangel: Senkung der Erythrozyten (Wachstumsfaktor) • C: Ascorbinsäure Mangel: allg. Schwäche, Gelenkschmerzen, Skorbut enthalten in Zitrusfrüchten, Sauerkraut • H: Biotin verantw. Enzymaufbau Carboxylasen Mangel: Hauterkrankungen, Haarausfall Entstehung von Energie im Körper Glucose 1 Schritt 1. Glycolyse Pyruvat CO2 Gärung Acetyl CoA CO2 Ethanol NADH/H+ Citratzyklus CO2 CO2 Atmungskette O2 H2O 7 06.10.2011 Zellatmung Energiegewinnung Atmungsgleichung (Glukose) C6 H12 O6 + 6O2 6CO2 + 6H2O + 675 kcal Gl k l Glykolyse (Mil (Milchsäuregärung) h ä ä ) C6 H12 O6 2C3H6O3 + Energie Glukose Milchsäure Glykolyse: Glukose Triose Zitronensäurezyklus Atmungskette aerob Brenztraubensäure CO2 + H2 H2 + O CH3-CO-COOH CO COOH Kohlendioxid Wasser anaerob Milchsäure 8 06.10.2011 Glukose +ATP Glukose – 6 – phosphat Fruktose – 6 – phosphat ADP 6C 6C Fruktose – 1,6 – diphosphat 1 2 +ATP ADP 6C 2 Phosphoglyzerinaldehyd 3C 2 Diphosphoglyzerinsäure 3C 2 Phosphoglyzerinsäure 3 4 +2H3PO4 +2 ADP 2ATP 5 2 Phosphoglyzerinsäure – 2 6 2 Phosphoenolbrenztraubensäure 7 2 Brenztraubensäure +2 ADP 2ATP 8 CH3-CO-COOH 9 06.10.2011 Entstehung von Energie im Körper Glucose Glycolyse Pyruvat CO2 2. Schritt Gärung Acetyl CoA CO2 Ethanol CO2 Citratzyklus NADH/H+ CO2 Atmungskette O2 H2O Einschleusung der BTS in den ZSZ BTS CH3 – C – H – TPP + CO2 = CH3 – C – COOH + TPP = I I. Azetaldehyd O O Liponsäure (CH3 – C – H) - TPP + S – CH – (CH2)4 – COOH = II. Liponsre. enth. Disulfidbindung Reduzierung d. Disulfidbindung S – (CH2)2 TPP …Thiaminpyrophosphat CH3 – C – S – Liponsre. + TPP = Aldehydrest = O O HS 10 06.10.2011 Einschleusung der BTS in den ZSZ - CH3 – C - S – CoA + HS – L. = CH3 – C – S – L + CoA = III III. O HS O Die Liponsre. wird dann von NAD+ oxydiert HS – L + NAD+ HS Aktivierte Essigsäure = Acetyl-CoA S – L – NADH + H+ HS S 6 COOH H2C - COOH + H2O CH2 – C – S – CoA + C = O HO – C – COOH + CoA - SH = O CH2 H2C - COOH COOH „aktivierte Oxalessig- Essigsre. Säure 2C 4C Zitronensäure 6C 11 06.10.2011 Zitratzyklus Grundprinzip des Zitratzyklus C- Atom 12 06.10.2011 Bei der Regulation des Zellstoffwechsels beteiligte Mechanismen Vorgang Bedeutung Förderung der Synthese von Boten-RNA Förderung bzw. Ausbildung d. Synthese von Enzymen (Enzyminduktion) Hemmung der Synthese von Boten-RNA Hemmung der Synthese von Enzymen und anderen Proteinen Erhöhter Abbau von Enzymen u.a. Proteinen durch zelleigene Proteasen Abnahme der Enzymtätigkeit Aktivierung u u. Hemmung von Enzymen Regulation der Enzymaktivität Steigerung des Umsatzes und des Abbaues von Nährstoffen Erhöhte Bereitstellung von ATP für funktionelle Leistungen (Kontraktion, Sekretion usw.) Endprodukthemmung von Enzymketten, Konkurrenz um Koenzyme Enzymregulation Entstehung von Energie im Körper Glucose Glycolyse Pyruvat CO2 Gärung Acetyl CoA CO2 Ethanol 3. Schritt NADH/H+ Citratzyklus CO2 CO2 Atmungskette O2 H2O 13 06.10.2011 Atmungskette Zytochrome (enth. Fe-Ion) H2 - Transport Elektronen- Transport Succinat Ubichinon – H2 Sauerstoff O2 + Flavoenzym – H2 NAD – H2 ZSZ H2 (NADP – H2) 2 - + 2Fe+++ 2Fe++ - Phyllochinon – H2 Co-Fermente 3 Wege CO2 2 - + 2Fe+++ 2Fe++ 2Fe+++ 2H+ 2Fe+++ O- - H2O Schaffung von Reaktionsbedingungen für H2 u. O2 Flavinenzyme: enthält Riboflavin (Vit. B12) NAD….Nikotinamid – Adenin Dinukleotid Resultat: 2 CO2 – Moleküle Ausatmung 8 H – Atome Atmungskette 11 ATP + 1 energiereiche Bindung insges. 12 ATP Abbau von 1 Mol Glucose 24 gebildet 14 06.10.2011 Energiebilanz für 1 Mol Glucose Glykolyse Substratphosphorylierung……………………………2 ATP Oxydation der bis Azetyl-CoA Gebildeten 4 Mol NADH……………………………12 ATP Zitronensäurezyklus………………………………..24 ATP insges. 38 ATP Biologischer Sinn des Zellstoffwechsels • Oxydation des Substrat – H2 • Freiwerdende Energie stufenweise gewinnen, um sie für die Zelle besser nutzbar zu machen • Oxydationsenergie wird zum Aufbau energiereicher Adenosinphosphate verwendet. = oxydative Phosphorylierung 15 06.10.2011 Proteinsynthese Der genetische Code U U C A G UUU UUC UUA UUG CUU CUC CUA CUG AUU AUC UC AUA AUG GUU GUC GUA GUG C Phe Leu Leu Ile e Met Val UCU UCC UCA UCG CCU CCC CCA CCG ACU ACC CC ACA ACG GCU GCC GCA GCG A Ser Pro Thr Ala G UAU UAC UAA UAG UGU UGC ochre UGA amber UGG CAU CAC CAA CAG His AAU AAC C AAA AAG GAU GAC GAA GAG Tyr Gln Asn Lys Asp Glu CGU CGC CGA CGG AGU AGC GC AGA AGG GGU GGC GGA GGG Cys opal Trp Arg Ser Arg Gly U C A G U C A G U C A G U C A G 16 06.10.2011 Schritte von der Transkription eines Gens bis zur Proteinbildung Translation: a. Ribosom mit P- und A-Ort, kleine Untereinheiten mit m-RNA in Kontakt; b. erste Aminoacyl-t-RNA am P-Prt, Einrücken eines zweiten Moleküls in den A-Art; c. Verknüpfung der Aminosäuren; d. Entlassung der ersten t-RNA aus dem P-Ort; e. Die zweite Aminoacyl-t-RNA ist an den P-Ort gerückt 17 06.10.2011 Gengesteuerte Proteinsynthese Aufbau einer eukaryotischen Transkriptionseinheit Schematische Darstellung der drei Grundelemente einer eukariotischen Transkriptionseinheit mit Angabe der regulatorischen Sequenzen im Promotor (TATA-Box) un der 3`-Region (AATAAA- und PyGTGTTPyPy-Signal; PY = Pyrimidin). Das vorliegende Strukturgen besteht aus fünf Exons (E1 – E5), die durch vier Introns (I1 – I4) voneinander getrennt sind. 18 06.10.2011 Organisation von Genen in einem Chromosom und Beispiel für den Aufbau eines Gens bei Wirbeltieren Replikation 1. Besteht aus zwei aufeinanderfolgenden Zellteilungen der nur eine identische Replikation vorausgeht 2. Stark abgewandelte 1. Teilungsphase homologen Chromosomen 3. Bildung von Bivalenten (Tetraden) 4 4. Interchromosomale Rekombination Erbanlagen 5. Kreuzweise Umtausch homologen Chromosomen Längspaarung der zufällige Vereilung der Crossing over zwischen nicht 19 06.10.2011 Schematische Darstellung des Stoffaustausches 20 06.10.2011 Natrium-Kalium-Pumpe, ein besonderer Fall von aktivem Transport Passiver und aktiver Transport im Vergleich 21