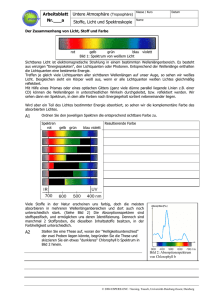
Seminar zum Praktikumsversuch: „Optische Spektroskopie“
Werbung

Seminar zum Praktikumsversuch: „Optische Spektroskopie“ Tilman Zscheckel Otto-Schott-Institut Optische Spektroskopie Definition: - qualitative oder quantitative Analyse, die auf der Wechselwirkung von Licht mit Materie beruht - Bestimmung von Parametern als Funktion der Wellenlänge oder Zeit - Materie kann tot oder lebend sein - Licht im Spektralbereich von fernen UV (ca. 200nm ) bis ins NIR (ca. 3 µm) 2 Optische Spektroskopie Elektromagnetisches Spektrum über 24 Dekaden [1] 3 Optische Spektroskopie Vorzüge der Optischen Spektroskopie: - prinzipiell alle Aggregatzustände für Proben verwendbar - auch hochstreuende Suspensionen messbar - Remotemessungen möglich - hohe zeitliche Auflösung bis zu 10-15 s (Femptosekunden bei Blitzlichtspektrophotometrie) - kleinste Stoffmengen mit Lumineszenzmethoden nachweisbar (bis 10-18 Mol) 4 Optische Spektroskopie Übersicht der Spektroskopieprinzipien [1] 5 Absorptionsspektroskopie Lichtquelle Monochromator Probe Photodetektor Prinzip der Absorptionsspektroskopie 6 Lichtquellen Art der Lichterzeugung: • Temperaturstrahler: - alle auf Glühwendeln basierenden Systeme • Lumineszenzstrahler: - basierend auf elektronisch angeregter Emission - Gasentladungslampen, Dioden, Laser Art des spektralen Strahlungsflusses: • Linienstrahler: - Konzentration der Energie auf wenige Linien • Kontinuumsstrahler: - Verteilung der Energie über breiten Spektralbereich Für die Absorptionsspektroskopie werden Kontinuumsstrahler benötigt! 7 Lichtquellen Kontinuumsgenerierung • hohe Intensitäten über großen Wellenlängenbereich erzeugbar • Deuteriumlampe für 190 < l< 390 nm • Wolframlampe für 390 < l < 3500 nm 8 Monochromatoren Dispersionsprisma nach [1] • Wellenlängenabhängige Brechung • Nachteil: - schwierige Wellenlängenkalibration (rechnergestützt durchaus bewältigbar) 9 Monochromatoren Dispersionsgitter nach [1] • winkelabhängige Beugung am Doppelspalt Interferrenz bei Phasengleichheit paralleler Strahlen funktioniert in Beugung und Reflektion • Nachteil: - Überlagerung mehrerer Ordnungen (mit zusätzlichem Filter überwindbar) 10 Monochromatoren Strahlengang durch Monochromator • Filter verhindert Überlagerung von höheren Beugungordnungen (Bsp.: 2. Ordnung von 400nm fällt zusammen mit 1. Ordnung von 800nm) • Monochromasie für beliebige Wellenlängen wegen drehbarem Dispersionsgitter 11 Strahlgang PbS Si Strahlteilung für „zeitgleiche“ Messung von Referenz und Probe • Herausrechnen der Streu- und Reflexionsanteile im Spektrum möglich • Wechselbare Halbleiterdetektoren mit Photomultiplierröhren um großes Spektrum abdecken zu können 12 Detektoren Photomultiplier • Halbleiterdetektoren mit Arbeitsbereichen Si : 0,2-1,1 µm PbS: 0,8-3,5 µm • Umwandlung von Quanten in Elektronen und Verfielfachung dieser rauscharme Signalverstärkung 13 Wechselwirkungen Wechselwirkungen zwischen elektromagnetischer Strahlung und Materie 14 Wechselwirkungen I0 = IR + IS + IA + IT I0 , Strahlintensität vor Wechselwirkung mit der Probe R= , Reflexionsvermögen der Probe S= , Streuvermögen A= , Absorptionsvermögen T= , Transmissionsvermögen 15 Wechselwirkungen Reflexionsvermögen Fresnel - Formel: - für einen einzelnen Grenzflächenübergang zwischen Luft und Glas vereinfachbar 16 Wechselwirkungen Streuung • Streuung an Inhomogenitäten (Blasen und Schlieren) • Tyndalleffekt (Streuung durch Schwebeteilchen oder Kolloide) • Miestreuung (an sphärischen Teilchen) 17 Wechselwirkungen Absorption I0 IT Gesetz nach Lambert und Beer [1] Die Intensität eines Strahlbündels nimmt exponentiell mit steigender Schichtdicke der Probe ab 18 Wechselwirkungen Absorption – Gesetz nach Lambert und Beer El = lg (I0/IT) = el∙c∙ d El/d = el∙c [cm-1] el = El/(c∙d) [cm-1∙ppm-1] El = lg (1/ti)l E l I e : Extinktion : Wellenlänge : Intensität : spezifischer Extinktionskoeffizient c : Konzentration d : Schichtdicke ti : Reintransmission ti = 10-El =10-(el∙c∙ d ) = I/I0 19 Anwendung Lambert Beer • Anwendbarkeit nur für verdünnte Lösungen • Atome/Moleküle dürfen nicht miteinander wechselwirken Abstand muss ausreichend sein sonst weitere überlagernde Effekte • für Atome nur elektronische Übergänge • zusätzliche Übergänge bei Molekülen (Rotationen, Schwingungen, auch in Kombination) • nachweisempfindlich bis wenige ppm (parts per million) 20 Anwendung Bestimmung des Extinktionskoeffizienten el • Eichung mit Konzentrationsreihe • Abweichung von der Linearität wegen Wechselwirkung bei zu geringem Abstand der Atome zueinander 21 Anwendung ElAbs=El-EB Beispielspektrogramm mit Basislinienkorrektur • stark wellenlängenabhängige Dispersion schräge oder gebogene Basislinie (Dispersionskurve verfügbar?) • Basislinie darf Meßkurve nicht überschneiden 22 Anwendung Sonderglas FP10 • Fluorid-Phosphatglas mit 10 mol% Sr(PO3)2 • Anwendung: - niedrige Brechzahl - anomale Teildispersion • Cu2+-auch als Verunreinigung Extinktionskoeffizient el für Qualitätskontrolle nützlich (Konzentrationsbestimmung) 23 Redox-Verhalten Cu in FP-Glas +0 0,01 100 0,05 500 0,10 1000 1,00 2,00 Ma% Cu’ 10.000 20.000 ppm Cu‘ Pt/Luft/ ~1000°C C/Ar/ 900°C 30‘ C/Ar/ 1000°C 30‘ C/Ar/1100°C 30‘ C/Ar/1200°C 30‘ Redox-Verhalten von Cu2+ in FP-Glas [2] Redox-Verhalten Cu in FP-Glas +10.000 20.000 ppm Cu 1 Ma% Cu2+ / Cu+ / Cu0 2 Ma% Cu Pt/Luft/ ~1000°C 80 C/Ar/ 900°C 30‘ 60 / 40 % C/Ar/ 1000°C 30‘ 25 / Cu2O / Cu0 C/Ar/1100°C 30‘ C/Ar/1200°C 30‘ Redox-Verhalten von Cu2+ in FP-Glas [2] / 20 % 1-5 / <5 / >90 % - / <1 / >99 % Quellen [1] Werner Schmidt: „Optische Spektroskopie“ 2. Auflage, Wiley-VHC [2] D.Ehrt & A.Brettschneider, ICG Peking, 1995 26