Echokardiographie in der Herzinsuffizienzdiagnostik
Werbung

óó Schwerpunkt · Herzinsuffizienz
Abklärung der Herzinsuffizienz
Mit der Echokardiographie zur
massgeschneiderten Therapie
SCHLOMO V. ASCHKENASY, ZÜRICH
Zusammenfassung
óó Die Echokardiographie erlaubt innerhalb kürzester Zeit eine nicht-invasive
eingehende Untersuchung des Herzens. Über die Beurteilung der Anatomie
und des Pumpmechanismus hinaus ist es heute möglich, durch Ausnutzung
des Doppler-Effekts, Informationen über den Schweregrad von Klappenundichtigkeiten und von Lungenhochdruck zu erhalten. Neben der genaueren Abklärung einer Herzinsuffizienz möglichst früh im Verlauf sollte die Echokardiographie wegen ihrer hohen Aussagekraft auch viel häufiger zur zielorientierten
Anpassung der medikamentösen Therapie eingesetzt werden.
Résumé
óó L’échocardiographie permet de réaliser en très peu de temps un examen
approfondi et non invasif du cœur. En plus de l’évaluation de l’anatomie et du
mécanisme de pompage il est aujourd’hui possible, en utilisant l’effet Doppler,
d’obtenir des informations sur la sévérité de défauts d’étanchéité valvulaire et
d’une hypertension pulmonaire. Outre l’investigation plus précise d’une insuffisance cardiaque, l’échocardiographie devrait, en raison de sa haute fiabilité,
être bien plus souvent mise à profit en vue d’une adaptation ciblée de la pharmacothérapie.
Riassunto
óó L’ecocardiografia consente di effettuare in breve tempo un esame accurato
e non invasivo del cuore. Oltre alla valutazione dell’anatomia e del meccanismo
di pompaggio grazie all’Effetto Doppler oggi è possibile ottenere informazioni sulla gravità delle insufficienze valvolari e sull’ipertensione polmonare.
L’ecocardiografia non solo è in grado di identificare in modo preciso e precocemente nel decorso un’insufficienza cardiaca, ma grazie alla sua elevata significatività dovrebbe essere utilizzata molto più frequentemente, anche al fine
di adattare la terapia medicamentosa in modo più mirato.
óóóó Die Echokardiographie ist das wichtigste Werkzeug des Kardiologen in der Diagnostik bei Patienten
mit Zeichen der Links- und/oder Rechtsherzinsuffizienz [1]. Kein anderes Tool erlaubt die nicht-invasive
Erhebung einer solch grossen Zahl von morphologischen und dynamischen Befunden direkt am Bett
des Patienten. Die Abklärung von Dyspnoe oder
peripheren Ödemen gehört neben der Abklärung
von Thoraxschmerzen und retrosternalem Druck zu
den häufigsten Zuweisungsgründen des Hausarztes
an einen Kardiologen. Wenn auch die koronare
Herzkrankheit die häufigste Ursache einer verminderten Auswurffraktion des linken Ventrikels ist,
gibt es doch viele andere Gründe, an die man primär
selten denkt.
Mit den hier zusammengestellten Befunden soll
die Mannigfaltigkeit der Diagnosen aufgezeigt werden, die sich hinter der landläufigen Diagnose «Herzinsuffizienz» verbergen können. Die hier gezeigten
Bilder wurden im Laufe der Jahre 2005 und 2006 im
Alltag einer kardiologischen Praxis aufgezeichnet
und sind somit durchaus repräsentativ für einen
Querschnitt durch die möglichen Diagnosen. Symptome der Linksherzinsuffizienz – Dyspnoe, Rasselgeräusche über der Lunge, eingeschränkte Leistungsfähigkeit etc. – können sowohl bei gestörter systolischer Funktion wie auch bei gestörter diastolischer
Funktion des linken Ventrikels (LV) auftreten.
Befunde bei Patienten mit
eingeschränkter LV-Funktion
Die häufigste Ursache der gestörten systolischen
LV-Funktion ist die koronare Herzkrankheit, gefolgt von der hypertensiven und der valvulären
Herzkrankheit. Im Folgenden werden anhand verschiedener Krankheitsbilder die bei diesen und
anderen Erkrankungen echokardiographisch dokumentierbaren Pathologien dargestellt.
Kombiniertes Aortenklappenvitium versus KHK:
Stellvertretend für die koronare und valvuläre Herzkrankheit als Ursache der Herzinsuffizienz soll
dieser Fall stehen. Bei einem 50-jährigen Patienten
ist seit Kindheit eine mittelschwere Aortenklappen-
8
CARDIO VASC
2006 | 5
©
Medien & Medizin Verlag MMV AG, Basel
insuffizienz bekannt, die damals mit einem Herzkatheter diagnostiziert wurde. In den vergangenen
Jahren ist der Schweregrad der Insuffizienz weitgehend unverändert geblieben, während derjenige
der Stenose von Jahr zu Jahr zugenommen hat.
Im Rahmen der jährlichen Verlaufskontrolle
wird eine Echokardiographie durchgeführt. Im parasternalen Kurzachsenschnitt (Abb. 1a) zeigt sich
eine mittelschwere Aortenklappeninsuffizienz {AI},
was sich auch in Abbildung 1b in der relativ kurzen
Dezelerationszeit, dem relativ steilen Abfall des
diastolischen Dopplerspektrums der Insuffizienz
{AIS}, zeigt. Aus dem systolischen Spektrum der
Stenose {ASS} errechnet sich ein mittlerer systolischer Gradient von 42 mmHg über der Klappe.
Die m-mode Aufnahme des basalen Anteils des
linken Ventrikels in Abbildung 1c zeigt ein sich
kaum, bzw. paradox bewegendes interventrikuläres
Septum {IVS} und eine normal kontrahierende postero-laterale Wand {PW}. Der endsystolische Cavum-Durchmesser {ESD} ist kaum kleiner als der
enddiastolische {EDD}. In Abbildung 1d zeigt sich
ein enddiastolischer parasternaler Kurzachsenschnitt und korrespondierend dazu in Abbildung 1e
die Kontrastmittel-Aufnahme, die keinen Kontrastmittelausfall im Bereich des Septums zeigt. Im Falle einer fehlenden Perfusion wäre der entsprechende
Teil des Septums vollständig schwarz. Eine hochgradige Stenose oder ein Gefässverschluss mit Perfusion über Kollateralen würde sich in einer verspäteten Anfärbung des von diesem Gefäss perfundierten Areals zeigen. Die prompte Anflutung des
Kontrastmittels kann in statischen Bildern nicht
gezeigt werden, lag hier jedoch vor. Bei Abbildung 1f
handelt es sich um eine endsystolische-4-Kammerblick-Aufnahme des aspektmässig zu grossen linken
Ventrikels {LV} und dem sich während der Systole
kaum kontrahierenden Septum {IVS}. Korrespondierend dazu sieht man in Abbildung 1g die Kontrastmittelaufnahme, welche auch hier eine normale Kontrastmittelanreicherung im Septum {IVS}
zeigt.
Das Ergebnis der echokardiographischen Untersuchung lässt sich folgendermassen zusammenfassen: Es findet sich neu eine Hypo- bis Akinesie
des interventrikulären Septums und eine nicht
mehr normale EF. Die Stenose (mittlerer Gradient
42 mmHg) ist bei eingeschränkter EF mittelschwer
bis schwer und die Insuffizienz mittelschwer. Die
Untersuchung der myokardialen Perfusion mittels
Sonovue®, einem Kontrastmittel zur Darstellung
der myokardialen Durchblutung, zeigt eine prompte Kontrastmittelanreicherung im Septum, was darauf schliessen lässt, dass hier die chronische Volumen- und Druckbelastung und nicht eine KHK
Ursache der Hypokinesie ist. Die Koronarangiographie bestätigt diesen Befund; die Koronarien
CARDIO VASC
2006 | 5
©
Medien & Medizin Verlag MMV AG, Basel
Fotos: Aschkenasy
Schwerpunkt · Herzinsuffizienz óó
Abb. 1a–g: Die Darstellung der myokardialen Durchblutung mit einem Kontrastmittel lässt eine KHK als Ursache der Herzinsuffizienz ausschliessen.
Abb. 2a–c: Die links-ventrikulären Thromben sind eine der möglichen Komplikationen der schwer eingeschränkten EF.
sind normal. Die nun nicht mehr normale EF macht
die valvuläre Herzkrankheit zu einer Operationsindikation.
Dilatative Kardiomyopathie: Eine Dilatation des
linken Ventrikels kann viele Ursachen haben; die
dilatative Kardiomyopathie im engeren Sinne, eine
schwere koronare Herzkrankheit, ein St. n. Myokarditis, eine ausgebrannte hypertensive oder valvuläre Herzkrankheit etc. Echokardiographisch
findet man der Bezeichnung entsprechend einen
dilatierten linken Ventrikel mit einer schwer eingeschränkten Auswurffraktion (EF). Da eine reduzierte EF in statischen Bildern schlecht gezeigt
werden kann, seien hier stellvertretend der so genannte «Smoke» – die Reflexion des Ultraschalls
an den sich kaum bewegenden Erythrozyten im viel
zu grossen Ventrikel – und eine der möglichen Komplikationen der schwer eingeschränkten EF, die
links-ventrikulären Thromben, gezeigt. Abbildung
2a stellt einen 4-Kammerblick eines massivst dilatierten linken Ventrikels {LV} dar, mit normalem
rechten Ventrikel {RV} und liegender Elektrode
des «Cardioverter Defibrillators» {ICD}. Im Cavum
9
óó Schwerpunkt · Herzinsuffizienz
Abb. 3a+b: M-mode Aufnahmen des linken Ventrikels.
Die verspätete Kontraktion der postero-lateralen Wand
im Vergleich zum interventrikulären Septum (D1) ist
nach Resynchronisation deutlich reduziert (D2).
Abb. 4a–g: Typischer Befund einer isolierten, linksventrikulären «non-compaction»-Kardiomyopathie.
des linken Ventrikels erkennt man spontanen Kontrast {Smoke} bedingt dadurch, dass sich das Blut
im dilatierten Ventrikel kaum bewegt. Einzig der
mitrale Einfluss {M. infl} wirbelt einige Eryhthrozyten auf, wodurch in diesem Bereich der Smoke
fehlt. Abbildung 2b zeigt einen 3-Kammerblick
{3CV} mit deutlich erkennbarem, 4 cm grossem
Thrombus {Thr} im Apex. In der kurzen Achse {SAX}
wird erkennbar, dass der Thrombus zirkulär der
Wand des linken Ventrikels entlang läuft (Abb. 2c).
In Abbildung 2 sind ausserdem die Aortenklappe
{AOV}, das Mitralklappensegel {MVL} sowie der
Papillarmuskel {PM} sichtbar.
Asynchronie: Ein weiteres häufiges Problem bei
Patienten mit schwer eingeschränkter EF ist die
asynchrone Kontraktion der verschiedenen Myokardanteile des linken Ventrikels, dies vor allem
bei Patienten mit Linksschenkelblock. Durch die
Einlage eines biventrikulären Pacers mit einer
Pacer-Elektrode im rechten Ventrikel und einer im
Sinus Coronarius kann dieses Problem bei einigen
Patienten behoben und dadurch die Symptomatik
der Herzinsuffizienz reduziert werden (siehe auch
10
Artikel von Dr. Tanner über kardiale Resynchronisation, S. 20). Meist wird in diesen Fällen auch ein
ICD implantiert, da viele dieser Patienten auch ein
erhöhtes Risiko für den plötzlichen Herztod haben.
Stellvertretend für die diversen durch eine Resynchronisation erreichten hämodynamischen Verbesserungen sei hier nur die Reduktion der verspäteten Kontraktion der postero-lateralen Wand im
Vergleich zum interventrikulären Septum gezeigt
(Abb. 3). Die maximale Kontraktion des interventrikulären Septums {S} und der Hinterwand {PW}
liegen im Bild a deutlich weiter auseinander {D1}
als im Bild b {D2}. Die vertikalen Linien markieren
den Beginn des QRS-Komplexes. In Abbildung 3b
erkennt man im EKG die Schrittmacher-Aktion
{PM} und den nun schmäleren QRS-Komplex.
Die echokardiographische Verbesserung (gemessen an der interventrikulär-mechanischen Verzögerung (IMD), am mitralen Regurgitationsindex,
am endsystolischen Volumen, an der LV-EF und
am enddiastolischen Volumen) konnte sowohl bei
ischämischer wie auch bei nicht-ischämischer Ätiologie in der CARE-HF-Extension-Studie bei 735
von 813 Patienten über eine Zeitspanne von 29 Monaten nach Beginn der Resynchronisation eindrücklich gezeigt werden [2].
Linksventrikuläre «non-compaction»-Kardiomyopathie: Diese seltene Kardiomyopathie, die erst in
der neuen Klassifikation der AHA ihren eigenen
Platz erhalten hat und nun als primäre, genetisch
bedingte Kardiomyopathie geführt wird, wurde
massgeblich in Zürich durch Prof. Jenni beschrieben. Der in seiner embryologischen Entwicklung
stehen gebliebene linke Ventrikel zeigt eine dünne
kompakte Wand und eine mindestens doppelt so
dicke, schwammförmige Innenschicht mit tiefen
Rezessi, in denen sich bei schlechter EF Thromben
bilden können. Viele Patienten leiden unter teils
gefährliche Rhythmusstörungen und einer Herzinsuffizienz.
Die in Abbildung 4 gezeigten Bilder gehören
zum Herzen eines Patienten, der viele Jahre als
Hilfsarbeiter auf Baustellen gearbeitet hat. Im Laufe der Jahre zeigten sich Zeichen der Herzinsuffizienz, die medikamentös behandelt wurden. Eine
Echokardiographie wurde nie durchgeführt. Erst
eine akute Dekompensation führte zur Zuweisung
und die Echokardiographie ergab überraschend den
typischen Befund einer isolierten, linksventrikulären «non-compaction»-Kardiomyopathie (Abb. 4).
Im 4-Kammerblick (Abb. 4a) ist die schwammförmige Muskelbeschaffenheit der Innenschicht des
linksventrikulären {LV} Apex {Pfeil} deutlich erkennbar. Im LV-Apex (Abb. 4b) zeigen sich tiefe
Rezessi {Pfeile}. Im parasternalen Querschnitt des
LV-Apex (Abb. 4c) kann gezeigt werden, dass der
CARDIO VASC
2006 | 5
©
Medien & Medizin Verlag MMV AG, Basel
Schwerpunkt · Herzinsuffizienz óó
nicht-kompakte Anteil der Wand {ncM} mehr als
doppelt so dick ist wie der kompakte Anteil {cM},
was für die Diagnose einer «non-compaction»-Kardiomyopathie verlangt wird. Die m-mode Aufnahme des linken Ventrikels (Abb. 4d) zeigt die deutlich eingeschränkte Auswurffraktion im Sinne einer
eingeschränkten diastolisch/systolischen Verkürzung der basalen Ebene des LV. Die Dopplermessung der Trikuspidalinsuffizienz erlaubt die Bestimmung der Druckdifferenz zwischen dem rechten
Vorhof und dem rechten Ventrikel (Abb. 4e). Addiert man zu diesem Wert den zentralen Venendruck (ZVD), erhält man den systolischen Pulmonalisdruck. Im Zustand der Dekompensation betrug
der Pulmonalisdruck ca. 65–70 mmHg (50,5+ZVD),
nach der medikamentösen Rekompensation noch ca.
35 mmHg. In Abbildung 4f zeigt sich eine schwere
Mitral-klappenisuffizienz {MI} vor Rekompensation, in Abbildung 4g eine mittelschwere MI nach
erfolgreicher Rekompensation.
Daraus ergab sich folgende Konsequenz für das
weitere Vorgehen: Die gestörte LV-Geometrie bewirkte bei Volumenüberlastung eine schwere Mitralinsuffizienz {MI} mit mittelschwerer, pulmonaler
Hypertonie (syst. Pulmonalisdruck ca. 70 mmHg).
Der Einsatz von Schleifendiuretika führte innert
weniger Tage zu einer Abnahme der MI und der
pulmonalen Hypertonie. In der Folge wurde auch
eine orale Antikoagulation mit Marcoumar begonnen.
Tachykardiomyopathie: Eine unterschätzte Ursache
der Herzinsuffizienz ist die Schädigung des Myokards durch eine chronisch zu hohe Herzfrequenz.
Eine 70-jährige Patientin wird von ihren Angehörigen zugewiesen, weil sie seit einigen Monaten an
Dyspnoe leidet und diese aktuell in einem Ausmass
zugenommen hat, die keinerlei körperliche Tätigkeit mehr erlaubt (NYHA III–IV). Im EKG zeigt
sich ein typisches Vorhofflattern mit einer Frequenz
von 105/min, welches anamnestisch seit über einem
Jahr besteht. Echokardiographisch findet sich eine
schwer eingeschränkte EF (30%), eine schwere
Mitralinsuffizienz sowie eine pulmonale Hypertonie
(Abb. 5). Die «m-mode»-Aufnahme des parasternalen Längsschnitts (Abb. 5a) zeigt eine eingeschränkte systolische Verkürzung {(EDD-ESD)/
EDD} der basalen Anteile des LV. In Abbildung 5b
sieht man die schwere Mitralklappeninsuffizienz
{MI}, in Abbildung 5c das EKG mit typischem Vorhofflattern (105/min). Der mitrale Einfluss zeigt die
fehlende A-Welle bei Vorhofflattern (Abb. 5d).
Nach erfolgreicher kathetertechnischer Ablation des Vorhofflatterns (Radiofrequenzablation
des Isthmus) normalisiert sich innert weniger Wochen die EF (Abb. 6a): Der Schweregrad der Mitralklappeninsuffizienz {MI} hat deutlich abgenom-
CARDIO VASC
2006 | 5
©
Medien & Medizin Verlag MMV AG, Basel
Abb. 5a–d: Tachykardiomyopathie vor Ablation
Abb. 6a–d: Normale EF nach Ablation bei Status nach Tachykardiomyopathie
LV: Lumen des linken Ventrikels, IVS: Interventrikuläres Septum, PW: Hinterwand des linken
Ventrikels, EDD: Enddiastolischer Durchmesser des LV, ESD: Endsystolischer Durchmesser des
LV, E: Frühdiastolischer mitraler Einfluss, A: Durch die Vorhofskontraktion bedingter mitraler
Einfluss.
men (Abb. 6b) und das EKG (Abb. 6c) zeigt einen
Sinusrhythmus mit AV-Block ersten Grades. Der
mitrale Einfluss zeigt nun wieder eine E- und eine
A-Welle (Abb. 6d). Da die beiden Flussspektren
fusioniert sind, kann aus diesem Spektrum keine
Aussage über die diastolische Funktion gemacht
werden.
Es verbleiben lediglich eine leichte Mitralinsuffizienz und eine leichte pulmonale Hypertonie. Der
ehemals exzentrisch-hypertrophe linke Ventrikel
11
óó Schwerpunkt · Herzinsuffizienz
Abb. 7a–j: Hypertrophe Kardiomyopathie mit schwerer Mitralinsuffizienz.
ist durch die Abnahme der Grösse nun konzentrisch
hypertroph. Die Symptomatik hat sich auf eine
NYHA I–II reduziert.
Befunde bei Patienten
mit erhaltener LV-Funktion
Herzinsuffizienzzeichen können trotz hoch-normaler EF auftreten, wenn die diastolische Funktion
des Ventrikels gestört ist. Die Erschlaffung des
Myokards ist ein grossteils aktiver, Energie-verbrauchender Prozess, der sehr früh im Verlauf einer
kardialen Erkrankung gestört sein kann. Dies oftmals lange vor dem Auftreten einer systolischen
Funktionsstörung. Die häufigsten Ursachen sind
die arterielle Hypertonie und die koronare Herzkrankheit, wesentlich seltener sind Kardiomyopathien sowie genetische, rheumatologische und Stoffwechselerkrankungen (M. Fabry, M. Gaucher etc.)
des Myokards.
12
Hypertrophe Kardiomyopathie: Eine voll ausgebildete hypertrophe Kardiomyopathie kann aus verschiedenen Gründen zu einer Herzinsuffizienz führen, dies, obwohl hier nicht selten die EF über 80%
beträgt. Die schwere linksventrikuläre Hypertrophie
führt zu einer ausgeprägten diastolischen Funktionsstörung und die Patienten sollten mit allen positiv
lusitropen (relaxationsfördernden) Medikamenten
behandelt werden. Dazu gehören in erster Linie
Betablocker und Calcium-Antagonisten. Bei der
hypertrophen obstruktiven Kardiomyopathie
(HOCM) kommt es bedingt durch die sub-aortal
gelegene Hypertrophie zu einem dynamischen Gradienten im Ausflusstrakt, der sich im Laufe der Systole aufbaut. Die dadurch entstehende sehr hohe
Flussgeschwindigkeit führt zu einem Sog, der die
Sehnenfäden des anterioren Mitralsegels nach anterior zieht (SAM, Systolic Anterior Motion), wodurch
die Mitralklappe kurz nach Beginn der Systole wieder aufgeht, was zu einer schweren Mitralinsuffizienz
führen kann. Die Mitralinsuffizienz führt zusammen
mit der diastolischen Funktionsstörung zur Ausbildung einer pulmonalen Hypertonie, welche zu Herzinsuffizienz-Symptomen führt.
In der Echokardiographie wird dabei Folgendes
sichtbar (Abb. 7a): Enddiastolischer, parasternaler
Kurzachsenschnitt auf Höhe der Mitralklappe. Die
Klappe ist offen {MV open}. Man erkennt das deutlich zu dicke interventrikuläre Septum {IVS} und
Hinterwand {PW}. Zu Beginn der Systole (Abb. 7b)
schliesst sich die Klappe {MV closed}. Nur wenige
Millisekunden später hat die Flussgeschwindigkeit
im «Left Ventricular Outflow Tract» {LVOT} bereits derart zugenommen, dass sich die Klappe wieder öffnet (Abb. 7c). In Abbildungen 7e und 7f
erkennt man die Sehnenfäden {chordae}, die kurz
nach Beginn der Systole gegen das Septum hin nach
anterior gezogen werden {SAM} und dadurch die
Mitralklappe {MV} wieder öffnen. In Abbildung 7g
ist die Vorwärts-bewegung der Chordae {SAM}
auch in der m-mode Aufnahme deutlich zu erkennen. Abbildung 7f zeigt den 3-Kammerblick mit
Flussbeschleunigung im {LVOT} und schwerer
Mitralklappeninsuffizienz {MI}. Die CV-DopplerFlussmessung zeigt in Abbildung 7h einen im Verlauf der Systole kontinuierlich zunehmenden Gradienten im LVOT, gegen Ende der Systole beträgt
der Spitzengradient 65 mmHg. Das Flussspektrum
der Trikuspidalinsuffizienz (Abb. 7j) zeigt, dass der
systolische Pulmonalisdruck 65 mmHg + ZVD beträgt, in diesem Fall ca. 75 mmHg, was die NYHA
III–IV-Symptomatik der Patientin erklärt.
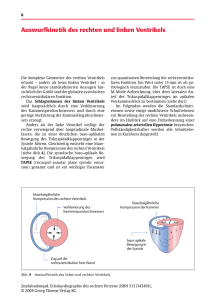
Rechtsherzinsuffizienz
Deutlich seltener als der linke Ventrikel macht sich
der rechte Ventrikel isoliert (also nicht sekundär
zur Linksherzinsuffizienz) mit Symptomen bemerk-
CARDIO VASC
2006 | 5
©
Medien & Medizin Verlag MMV AG, Basel
Schwerpunkt · Herzinsuffizienz óó
bar. Neben dem im Erwachsenenalter relativ selten
neu entdeckten, klinisch relevanten Atrium-Septum-Defekt (ASD) und dem kongenitalen oder
häufiger postmyokardinfarkt auftretenden Ventrikel-Septum-Defekt (VSD), der arrhythmogenen
rechtsventrikulären Kardiomyopathie und dem
Morbus Uhl (das Fehlen des rechtsventrikulären
Myokards) ist die primäre oder sekundäre pulmonale Hypertonie eine seltene, jedoch enorm wichtige
Ursache für eine isolierte Rechtsherzinsuffizienz.
Pulmonale Hypertonie: Eine 60-jährige Patientin
wird wegen progredienter Dyspnoe (NYHA III–IV)
und Zeichen der Rechtsherzinsuffizienz zur Echokardiographie zugewiesen. Der systolische 4-Kammerblick (Abb. 8a) zeigt, dass der rechte Ventrikel
grösser ist als der linke und die Deviation des Vorhofseptums {IASs} beweist, dass der Druck im rechten Vorhof über dem des linken Vorhofs liegt. Typisch für die Druck- und Volumenbelastung ist die
D-Form des linken Ventrikels im parasternalen
Kurzachsenschnitt (Abb. 8b). Eine diastolische
D-Form findet sich in der Regel bei Volumenbelastung, eine systolische bei Druckbelastung des rechten Ventrikels. In diesem Fall sowohl diastolisch
(Abb. 8b) wie auch systolisch (Abb. 8c). Zirkulär
um das Herz erkennt man einen kleinen Saum von
Perikarderguss {PE}. Das Flussspektrum der Trikuspidalinsuffizienz (Abb. 8d) zeigt eine Druckdifferenz zwischen dem rechten Vorhof und Ventrikel
von 81 mmHg, rechnet man den ZVD dazu, so
erhält man einen Pulmonalisdruck von ca. 90 bis
100 mmHg (Norm bis 33 mmHg). Anhand der
Flussbeschleunigung (Abb. 8e) der Trikuspidalinsuffizienz {TI}, die bereits vor der Trikuspidalklappe (Pfeil) beginnt, erkennt man, dass hier eine relevante Insuffizienz vorliegt. Die Druckdifferenz
zwischen der Pulmonalarterie und der rechten Ventrikel (Abb. 8f), gemessen am Flussspektrum der
Pulmonalklappeninsuffizienz, beträgt 25 mmHg
(normal <12 mmHg). Dieser hohe Wert lässt auf
eine partielle Fixierung der pulmonalen Hypertonie
schliessen.
Bei dieser echokardiographischen Untersuchung findet sich ein Cor Pulmonale mit mittelschwerer bis schwerer pulmonaler Hypertonie sowie
wenig Perikarderguss. Die Dyspnoe ist in diesem
Fall somit nicht durch eine Linksherzinsuffizienz,
sondern durch die pulmonale Hypertonie verursacht. Die weiteren Abklärungen ergeben, dass die
Patientin an einer Sklerodermie leidet.
CARDIO VASC
2006 | 5
©
Medien & Medizin Verlag MMV AG, Basel
Abb. 8a–f: Pulmonale Hypertonie: Der Pulmonalisdruck ist stark erhöht.
Schlussfolgerung
Die Ursachen einer Herzinsuffizienzsymptomatik
sind sehr heterogen. Mit der Echokardiographie
steht ein diagnostisches Hilfsmittel zur Verfügung,
das nicht-invasiv, praktisch überall verfügbar und
kostengünstig ist. Die aus dieser Untersuchung gewonnenen Befunde erlauben es, die medikamentöse
Therapie zielgesteuert mit den verschiedensten Medikamentenklassen anzupassen, was klinisch und
prognostisch viel mehr Erfolg verspricht, als der
alleinige Einsatz von Diuretika zur Symptomminderung. Jeder Patient mit Zeichen der Herzinsuffizienz
sollte daher möglichst früh im Verlauf der Erkrankung einer Echokardiographie zugeführt werden.
Dr. med. Schlomo V. Aschkenasy
FMH Kardiologie
Klosbachstrasse 104
8032 Zürich
E-Mail: [email protected]
Literatur:
1.
Swedberg K et al.: Eur Heart J 2005; 26: 1115-1140.
2. Tavazzi L. et al.: präsentiert am ESC 2005.
13