Musterlösung 27.2.2002 (download pdf)
Werbung

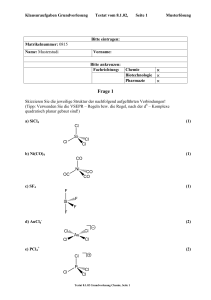
Klausuraufgaben Grundvorlesung Testat vom 27.2.02, Seite 1 Punkte Bitte eintragen: Matrikelnummer: Name: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage 1 Schreiben Sie die chemischen Symbole für nachfolgende Elemente an: a) Lanthan La (1) b) Rhodium Rh (1) c) Rhenium Re (1) c) Ruthenium Ru (1) d) Plutonium Pu (1) e) Palladium Pd (1) Frage 2 Schreiben Sie chemische Gleichungen für die nachfolgenden Umsetzungen an. a) Ausgangsstoffe Produkte Fe2O3, CO Fe, CO2 Gesamtgleichung: Fe2O3 + 3 CO → 2 Fe + 3 CO2 Testat 27.2.02 Grundvorlesung Chemie, Seite 1 (3) Klausuraufgaben Grundvorlesung b) Testat vom 27.2.02, Seite 2 Ausgangsstoffe Produkte Cu2+, I- CuI , I2 Punkte Redoxteilgleichung (Kupfer): Cu2+ + e- → Cu1+ (1) Redoxteilgleichung (Iod): I- → ½ I2 + e- (1) Gesamtgleichung: Cu2+ + 2 I- → CuI + ½ I2 c) (1) Ausgangsstoffe Produkte H2O2 , KI I2, KOH Redoxteilgleichung (H2O2): H2O2 + 2 e- → 2 OH- (2) Redoxteilgleichung (Iod): 2 I- → I2 + 2 e- (1) Gesamtgleichung: H2O2 + 2 I- → I2 + 2 OHd) (2) Ausgangsstoffe Produkte (NH4)2Cr2O7 N2, Cr2O3, H2O Redoxteilgleichung ([Cr2O7]2-): [Cr2O7]2- + 8 H+ + 6 e- → Cr2O3 + 4 H2O (2) Redoxteilgleichung (NH4+): 2 NH4+ → N2 + 8 H+ + 6 e- (2) Gesamtgleichung: (NH4)2Cr2O7 → N2 + Cr2O3 + 4 H2O Testat 27.2.02 Grundvorlesung Chemie, Seite 2 (2) Klausuraufgaben Grundvorlesung Testat vom 27.2.02, Seite 3 Punkte Frage 3 Machen Sie für die nachfolgenden Verbindungen die jeweils geforderten Angaben: a) Verbindung: Schwefelsäure Summenformel: H2SO4 (1) Valenzstrichformel: (2) O H S O H O O Koordinationsform am Schwefel: tetraedrisch (1) Oxidationsstufe des Schwefels: +VI (1) HNO3 (1) b) Verbindung: Salpetersäure Summenformel: Valenzstrichformel, Mesomerie: (2) O O N N HO HO O O Koordinationsform am Stickstoff: trigonal planar (1) Formale Ladung am Stickstoff: +1 (1) C2H4O2 (1) c) Verbindung: Essigsäure Summenformel: Valenzstrichformel: (2) O H H C H H Oxidationsstufen aller Kohlenstoffzentren: C O (2) -III, +III Testat 27.2.02 Grundvorlesung Chemie, Seite 3 Klausuraufgaben Grundvorlesung Testat vom 27.2.02, Seite 4 Punkte Frage 4 Im Diagramm ist die Elementarzelle einer Verbindung (Perowskit) gezeigt, die Sauerstoff (weiße Kugeln), Titan (schwarze Kugeln) und Calcium (graue Kugeln) enthält. a) Geben Sie die stöchiometrische Formel der Verbindung an: (3) CaTiO3 b) Welche Koordinationszahl hat Ca? (1) 12 (8) c) Welche Koordinationszahl hat Ti? (1) 6 d) Welches Koordinationspolyeder beschreibt die Koordination von Ti durch O? (1) Oktaeder e) Welche Oxidationsstufe hat Ti? +IV Testat 27.2.02 Grundvorlesung Chemie, Seite 4 (1) Klausuraufgaben Grundvorlesung Testat vom 27.2.02, Seite 5 Punkte Frage 5 „Radioiod“ , 131 53 I zerfällt mit einer Halbwertszeit von 8 Tagen in 131 54 Xe. a) Welche Teilchen werden beim Zerfall abgegeben α- oder β-Teilchen? (1) α-Teilchen β-Teilchen c) Wenn der Gehalt an Einheiten an Antwort: 131 53 I 131 53 I einer Probe zum Zeitpunkt t = 0 x Einheiten beträgt, wie viel sind nach einer Zeit von 32 Tagen noch vorhanden? x/24 = 1/16 x (2) Frage 6 Geben Sie die Valenzelektronenkonfiguration folgender Atome bzw. Ionen an: a) Stickstoff 2s2 2p3 (1) b) Chlor 3s2 3p5 (1) c) Selen 4s2 4p4 (1) d) Magnesium 3s2 (1) e) Cer(III) 4f1 (2) f) Eisen(II) 3d6 oder 4s2 3d4 oder 4s1 3d5 (2) Testat 27.2.02 Grundvorlesung Chemie, Seite 5 Klausuraufgaben Grundvorlesung Testat vom 27.2.02, Seite 6 Punkte Frage 7 Berechnen Sie den pH-Wert des nachfolgend angegebenen Puffergemisches: NaH2PO4 und Na2HPO4 im Konzentrationsverhältnis 1:1 (pKs(NaH2PO4) = 7.2) (Vernachlässigen Sie bei Ihrer Berechnung die Solvolysegleichgewichte, die zu H3PO4 bzw. Na3PO4 führen!) pH = pKs pH = 7.2 (2) Frage 8 Schreiben Sie die Gleichungen für folgende Beziehungen auf: a) Druck P als Funktion von V, T, n, R: P = n R T/ V (2) b) Gleichgewichtskonstante K als Funktion von ∆G , R, T: K = exp(- ∆G /RT) (2) Testat 27.2.02 Grundvorlesung Chemie, Seite 6 Klausuraufgaben Grundvorlesung Testat vom 27.2.02, Seite 7 Punkte c) Wie groß ist die Coulomb-Kraft FM zwischen zwei geladenene Teilchen in einem Medium der Dielektrizitätskonstanten ε, wenn die Coulomb-Kraft zwischen diesen Teilchen im Vakuum FC beträgt: FM = FC / ε (2) d) Schreiben Sie die Nernst’sche Gleichung für folgenden Redoxprozess an MnO4- + 5 e- + 8 H+ → Mn2+ + 4 H2O: Nernst’sche Gleichung: oder E = E0 + RT/5F ln([MnO4-][H+]8 / [Mn2+]) (3) E = E0 + 0.059/5 log([MnO4-][H+]8 / [Mn2+]) Frage 9 a) Schreiben Sie das Massenwirkungsgesetz für folgenden Vorgang an! Um welchen Reaktionstyp handelt es sich? Cl2 + 2 OH- → Cl- + OCl- + H2O Massenwirkungsgesetz: K = [Cl-][OCl-][H2O] / [Cl2][OH-]2 (2) Reaktionstyp: Disproportionierung (1) b) Schreiben Sie die Definitionsgleichung für die Säurekonstante der ersten Solvolysestufe von Schwefelwasserstoff an: KS = [H+][HS-] / [H2S] Testat 27.2.02 Grundvorlesung Chemie, Seite 7 (2) Klausuraufgaben Grundvorlesung Testat vom 27.2.02, Seite 8 Punkte c) Schreiben Sie die Definitionsgleichung für das Löslichkeitsprodukt L von Bleisulfid an: L = [Pb2+][S2-] (2) d) Das Löslichkeitsprodukt von Silberchlorid beträgt etwa 10-10 mol2l-2. Wie viel Mol Silberionen sind in 1 l wässriger Lösung über festem Silberchlorid enthalten? 10-5 mol (2) Frage 10 Skizzieren Sie die Strukturen von elementarem Chlor und von elementarem Phosphor durch Valenzstrichformeln, die zugleich den Bau wiedergeben! Chlor: (2) Cl Cl Phosphor: (3) P P P P Testat 27.2.02 Grundvorlesung Chemie, Seite 8 Klausuraufgaben Grundvorlesung Testat vom 27.2.02, Seite 9 Punkte Frage 11 2.7 g Aluminium (MAl = 27 u) werden mit 2 Mol KOH in Wasser zur Reaktion gebracht und dabei aufgelöst. a) Schreiben Sie die stöchiometrische Gleichung für den Prozess an! Gleichung: 2 Al + 6 H2O + 2 OH- → 2 [Al(OH)4]- + 3 H2 .......................................................................................................................... (3) b) Wie viele Liter H2 entstehen dabei unter Normalbedingungen? Es entstehen 3.4 l. (2) Frage 12 Welche der nachfolgend aufgeführten Verbindungen hat ein von Null verschiedenes Dipolmoment? CCl4 BCl3 Cr(CO)6 CH3COOH (1) Testat 27.2.02 Grundvorlesung Chemie, Seite 9 Klausuraufgaben Grundvorlesung Testat vom 27.2.02, Seite 10 Punkte Frage 13 Mit welchen Lewis-Basen bildet die weiche Lewis-Säure Ag+ jeweils die stabilere Verbindung? a) FI- b) (1) O2S2- c) (1) SO42S2O32- (1) Frage 14 Die Struktur von Korund Al2O3 lässt sich auf der Basis einer hexagonal dichtesten Packung von Oxid-Ionen beschreiben, in denen die Oktaederlücken regelmäßig durch Al(III)-Ionen besetzt sind. Welcher Anteil von Oktaederlücken ist belegt? 2/3 der Oktaederlücken sind belegt. Testat 27.2.02 Grundvorlesung Chemie, Seite 10 (3) Klausuraufgaben Grundvorlesung Testat vom 27.2.02, Seite 11 Punkte Frage 15 Geben Sie die Energien an, die jeweils zur Spaltung der nachfolgend angegebenen Bindungen benötigt wird. Kreuzen Sie das am ehesten Zutreffende an! a) H-H in H2: 10 100 400 1000 kJ mol-1 (1) b) N≡N in N2: 20 300 600 1000 kJ mol-1 (1) c) OH…H in einer Wasserstoffbrückenbindung: 10 40 60 100 kJ mol-1 (1) Frage 16 BCl3 und NO3- sind stabile Teilchen mit jeweils einer Gesamtvalenzelektronenzahl von 24. Welches aus Kohlenstoff C und Sauerstoff O aufgebautes stabile Teilchen ist zu diesen Teilchen isoelektronisch und isostrukturell? Nennen Sie den Namen und zeichnen Sie die Valenzstrichformel mit Formalladungen. Name Carbonat-Ion (1) Valenzstrichformel: (3) O C O O Testat 27.2.02 Grundvorlesung Chemie, Seite 11