cystectomy
Werbung

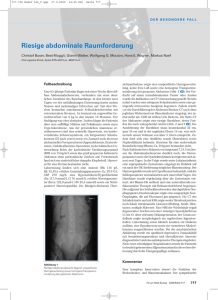
7 Therapie des muskelinvasiven und des lokal fortgeschrittenen Blasenkarzinoms im Jahr 2004 M. Schostak, K. Miller Einleitung Überschreitet oder erreicht das Harnblasenkarzinom die Grenze der Blasenmuskulatur, steigt die Wahrscheinlichkeit einer weiteren lokalen Progression und/oder Metastasierung rapide an. Im Gegensatz zu den oberflächlichen Tumoren der Harnblase gilt die radikale Zystektomie in diesen Fällen heutzutage als Goldstandard. Die lokale Effektivität bei auf das Organ begrenzten Tumoren ist hoch, wie zahlreiche Serien weltweit eindrucksvoll belegen. Wird das Stadium pT3a überschritten, zeigen sich jedoch schlechtere Überlebensraten (Gschwend 2002). Da einerseits für einen Teil der Patienten dieses Verfahren nicht in Frage kommt oder der Eingriff abgelehnt wird und andererseits 50% aller zystektomierten Patienten im weiteren Verlauf an einer hämatogenen Metastasierung versterben (Gschwend 2002; Mameghan et al. 1992; Lerner et al. 1992; Kulkarni 2003), ist die Frage nach Alternativverfahren gerechtfertigt. Im Folgenden werden die heute zur Verfügung stehenden Techniken kritisch bewertet. Radikale Zystektomie Die radikale Zystektomie in Kombination mit einer pelvinen Lymphadenektomie ist ein hocheffektives Verfahren in der Therapie des muskelinvasiven, klinisch organbegrenzten Blasenkarzinoms. Dies wurde in zahlreichen Serien belegt (Bassi 2000; Blandy et al. 1984; Bollack et al. 1989; Bosl et al. 1994; Chang et al. 2001; Frazier et al. 1992; Gschwend 2002; Gschwend et al. 2000; Lebret et al. 2000; Mathur et al. 1981; Montie et al. 1984; Roehrborn et al. 1991; Skinner et al. 1984; Stein et al. 2001). Liegt ein nur oberflächlich infiltrierender Tumor (pT2a) ohne Lymphknotenmetastasierung vor, besteht eine ausgesprochen gute Prognose (mittlere Fünfjahresüberlebensrate ca. 75%). Zeigt der pathologische Befund ein organüberschreitendes Wachstum, so verschlechtert sich die Prognose für den Patienten deutlich. Gleiches gilt für das Vorliegen einer Lymphknotenmetastasierung (Amling et al. 1994; Gschwend 2002; Gschwend et al. 2000; Lebret et al. 2000; Stein et al. 2001; Stein 2000; Takashi et al. 1989, 1992). Die Optimierung der operativen Technik, verbunden auch mit dem Einsatz neuerer Instrumente (Stapler, Elektrische Schere, Ligasure-Gerät u. a.; Dubuc-Lissoir 2003; Landman et al. 2003; Matthews et al. 2001; Heniford et al. 2001) sowie ein verändertes Anästhesie-Management (Ahlering et al. 1983; Parekh et al. 2002; Ryan 1982; Whalley u. Berrigan 2000) haben dazu beigetragen, dass die perioperative Mortalität heutzutage nur noch bei 1–4% liegt und die Morbidität akzeptable Werte erreicht hat (Gschwend 2002; Gschwend et al. 2000; Finlayson u. Birkmeyer 2001; Chang et al. 2002a,b). Finlayson zeigte dabei, dass die Mortalität eine Altersabhängigkeit zeigt (Finlayson u. Birkmeyer 2001; ⊡ Tabelle 7.1). Akute Komplikationen können dabei durch die Komorbidität, durch die Zystektomie bzw. die Ex- 82 Kapitel 7 · Therapie des muskelinvasiven und des lokal fortgeschrittenen Blasenkarzinoms im Jahr 2004 enteration im kleinen Becken oder durch die Verwendung des Darmsegmentes für die Harnableitung bedingt sein. Spätkomplikationen betreffen in den meisten Fällen die Harnableitung (Bassi 2000; Chang et al. 2001; Lerner et al. 1992; Parekh et la. 2002; Cancrini et al. 1996; Game et al. 2001). Erste Berichte über eine radikale Zystektomie in laparoskopischer Technik, z. T. mit Anlage der Harnableitung ebenfalls in laparoskopischer oder roboterassistierter Technik, zeigen vielversprechen- ⊡ Tabelle 7.1. Altersabhängige Mortalität bei der Zystektomie. (Mod. nach Finlayson et al. 2001) 7 Alter [Jahre] Prozent 65–69 2,3 70–74 3,7 75–79 5,5 80–84 7,5 85–99 9,3 Gesamt 4,4 de Ergebnisse. In Anbetracht der kurzen Nachbeobachtungszeit und der geringen Patientenzahl kann dieses Verfahren jedoch noch nicht als ebenbürtig zum Standard der offenen radikalen Zystektomie eingestuft werden (Turk et al. 2001a,b; Beecken et al. 2003; Menon et al. 2003; Simonato et al. 2003; Smith 2003; Peterson et al. 2002; Abdel-Hakim et al. 2002; Matin u. Gill 2002). Durch die heute übliche, sehr frühzeitige Mobilisation ist die Wahrscheinlichkeit der Ausbildung einer tiefen Beinvenenthrombose ebenso wie die der Ausbildung einer Atelektase und/oder Pneumonie deutlich gesunken. Das Risiko einer Lungenarterienembolie liegt bei 2%. Analog zum heutigen Vorgehen bei der radikalen Prostatektomie kann die radikale Zystektomie bei Männern mit erhaltener Potenz inzwischen ebenfalls nach den von Shlegel, Walsh und Marshall veröffentlichten Modifikationen nerverhaltend operiert werden (Schlegel u. Walsh 1987; Walsh 1987; Marshall et al. 1991). Dies führt über die o. g. Faktoren hinaus zu einer verbesserten Akzeptanz des Eingriffs. Analog zu den Daten nach Durchführung einer radikalen Prostatektomie ist dabei der entscheidende Faktor für den erfolgreichen Erhalt der Potenz das Alter des Patienten. Bei Patienten unter 60 Jahren sind die Ergebnisse deutlich besser, bei Patienten über 70 Jahre deutlich schlechter (Schoenberg et al. 1996; ⊡ Tabelle 7.2). ⊡ Tabelle 7.2. Potenz nach nerverhaltender radikaler Zystektomie. (Mod. nach Schoenberg et al. 1986) Pathologisches Stadium 20–29 Jahre 40–49 Jahre 50–59 Jahre 60–68 Jahre 70–79 Jahre Gesamt pT0 – 2/2 5/7 2/4 – 9/13 (69%) pTa – 1/2 – 1/3 – 2/5 (40%) pTis – – 0/2 2/6 – 2/8 ( 25%) pT1 – 2/3 0/2 2/4 – 4/9 (44%) pT2 – 2/2 1/2 1/1 – 4/5 (80%) pT3a – 1/2 1/1 – 0/1 2/4 (50%) pT3b – 0/2 1/4 1/3 1/4 4/14 (29%) pT4 1/1 – 1/1 – – 1/1 (100%) Gesamt 1/1 (100%) 8/13 (62%) 9/19 (47%) 9/21 (43%) 1/5 (20%) 28/59 (48%) 83 Radikale Zystektomie Operative Technik der radikalen Zystektomie beim Mann Um die Dauer des transperitonealen Vorgehens auf das Ausschalten des ilealen Darmsegments zu begrenzen, bevorzugen wir ein primär extraperitoneales Vorgehen analog zur radikalen Prostatektomie. Oft gelingt es, das Peritoneum bis zur endgültigen Entnahme des Präparates inklusive der Lymphadenektomie geschlossen zu halten (Kulkarni et al. 1999; Serel et al. 2003). Zunächst wird eine pelvine Lymphadenektomie im Bereich der externen und internen Iliakalgefäße sowie der Fossa obturatoria durchgeführt. Anschließend werden die Harnleiter beidseits aufgesucht und bis zum Trigonum präpariert. Danach wird die endopelvine Faszie eröffnet und die Prostata analog zur radikalen Prostatektomie präpariert. Nun werden die lateralen Blasenpfeiler zwischen Ligaturen, Clips oder LigaSure-Schweißstellen durchtrennt und das Präparat entnommen. Liegt präoperativ keine Probe der prostatischen Harnröhre vor, so sollte die Tumorfreiheit der Urethra intraoperativ mittels Schnellschnitt untersucht werden. Ist sie befallen, so muss eine Urethrektomie durchgeführt werden (Lebret et al. 1998; Wood et al. 1989; Freeman et al. 1994; Ahlering et al. 1984), vorzugsweise über den präpubischen Zugangsweg (Zhang 1997; Hiebl et al. 1999). Dies erspart eine Umlagerung des Patienten und eine weitere Operationswunde im Perineum. Nach Anlage der Harnableitung kann in vielen Fällen das Peritoneum wieder verschlossen werden. Diese Rekonstruktion der Kompartimente trägt dazu bei, die Morbidität zu senken. Kommt es zu einer Urinleckage, einer Hämatom- oder Abszessbildung im Verlauf, so handelt es sich um ein rein extraperitoneales Problem, das in vielen Fällen ohne operative Intervention z. B. durch eine Pigtail-Einlage erfolgreich behandelt werden kann. 7 trennt. Das Vaginaldach wird nun nach distal bis zum Meatus urethrae, der umschnitten wird, reseziert (⊡ Abb. 7.1). Nach Entfernung des Präparates wird die Vaginalwand mit einer quer verlaufenden Naht fortlaufend wieder verschlossen (⊡ Abb. 7.2). ⊡ Abb. 7.1. Situs nach Entnahme des Operationspräparates mit Resektion der Vaginalvorderwand. (Mit freundl. Genehmigung aus Wammack 1997) Operative Technik der radikalen Zystektomie bei der Frau Im Gegensatz zur Operation beim Mann wird primär transperitoneal vorgegangen. Eine Ovarektomie sowie Hysterektomie werden routinemäßig durchgeführt. Bei jüngeren Frauen können jedoch ohne Erhöhung des onkochirurgischen Risikos die Ovarien erhalten werden (Chang et al. 2002c; Horenblas et al. 2001). Zusätzlich wird das vordere Vaginaldach reseziert. Nach Eröffnung der Vagina im Fundus werden die Blasenpfeiler zwischen Ligaturen, Clips oder LigaSure-Schweißstellen schrittweise durch- ⊡ Abb. 7.2. Vaginalrekonstruktion durch Vernähen des umgeschlagenen kranialen Abschnitts der Vaginalwand mit den Resektionsrändern. (Mit freundl. Genehmigung aus Wammack 1997) 84 Kapitel 7 · Therapie des muskelinvasiven und des lokal fortgeschrittenen Blasenkarzinoms im Jahr 2004 Ist ein orthotoper Blasenersatz geplant, so sollte allerdings nicht nur die Urethra, sondern auch die Vaginalwand erhalten bleiben. Dies erhöht die Wahrscheinlichkeit einer suffizienten Miktion (Stenzl u. Holtl 2003; Chang et al. 2002d). Ein Wachstum des Karzinoms im Bereich des Blasenhalses geht mit der erhöhten Wahrscheinlichkeit eines Befalls der Urethra einher. Eine Metaanalyse zeigte allerdings jüngst, dass der Befall der weiblichen Urethra mit 3,6% wesentlich unwahrscheinlicher ist als bei Männern mit 6,2% (Stenzl et al. 2002). Die Tumorfreiheit des Blasenhalses als proximalem Absetzungsrand und der verbleibenden Urethra sollte intraoperativ mit Hilfe eines Kryoschnittes gesichert werden (Stenzl u. Holtl 2003; Darson et al. 2002). 7 Pelvine Lymphadeneketomie Die pelvine Lymphadenektomie ist ein integraler Bestandteil der radikalen Zystektomie. Sie ermöglicht einerseits ein exaktes Staging (Herr 2003), andererseits führt die Entfernung gering tumorbefallener Lymphknoten zu höheren Überlebensraten (Gschwend 2002; Roehrborn et al. 1991; Skinner u.Lieskovsky 1984; Mills et al. 2001 )1,15,63–65. Die Wahrscheinlichkeit einer Lymphknotenmetastasierung steigt mit dem lokalen Fortschritt der Erkrankung (pT2a 10,5%, pT2b 26,7%, pT3b 58%, pT4 90%) (Leissner et al. 2000). Smith zeigte, dass bei Patienten, die eine radikale Zystektomie erhielten, vor allem die Lymphknoten der Obturatorius-Loge und der Iliaca-externa-Region betroffen sein können. Die Gruppe der Lymphknoten entlang der A. iliaca communis und die präsakrale Gruppe sind nur selten involviert. Aus diesem Grund kann auf die Entfernung der Lymphknoten in diesen Bereichen verzichtet werden (Smith u. Whitmore 1981). Sherif berichtete erstmals von der Möglichkeit, Metastasen in Sentinellokalisationen nachzuweisen. Die geringe Patientenzahl der Studie lässt jedoch noch keine weitergehende Beurteilung zu (Sherif et al. 2001). et al. 1997; Henry et al. 1988; Herr 1987), so muss diese Technik dennoch als verlassen bezeichnet werden. Prinzipiell erlaubt die primäre transurethrale Operation bei pT2-Tumoren in 47% eine Resektion ins Gesunde, weitere 30% sind durch bis zu drei Nachresektionen zu entfernen. Liegt ein organüberschreitendes Wachstum vor, so kann nur noch in 40% Tumorfreiheit erzielt werden. Die erhebliche Gefahr eines Understagings von 50% bedingt eine komplizierte Selektion. Zudem hat sich gezeigt, dass das Auftreten eines schlecht differenzierten Rezidivs die Fünfjahresüberlebenswahrscheinlichkeit um mindestens 20% senkt. Als alleinige Maßnahme kann die TUR daher nur bei kleinen, gut differenzierten, jedoch muskelinvasiven Tumoren in Betracht gezogen werden (Herr 2001). Diese Tumorkonstellation ist jedoch höchst selten. Wird eine Radiochemotherapie (s. unten) geplant, ist in jedem Fall eine transurethrale R0-Resektion anzustreben (Dunst et al. 2001; Rodel et al. 2002). Harnblasenteilresektion Eine Harnblasenteilresektion hat heute nur noch in ausgewählten Einzelfällen ihren Platz: Divertikelkarzinome, kleine Tumore der Vorderwand oder des Blasendaches bei Patienten in grenzwertigem Allgemeinzustand oder hohem Alter sowie Tumore, die ausschließlich das Ostium betreffen, sodass eine Harnleiterneuimplantation notwendig wird. Weiterhin kann sie eine Therapievariante bieten, wenn eine TUR, z. B. wegen Koxarthose o. Ä. nicht möglich ist. Die Indikationsstellung beschränkt sich heute jedoch auf weniger als 5% der Fälle. Größere Serien stammen aus den 70er-Jahren des letzten Jahrhunderts und zeigen schlechtere Fünfjahresüberlebensraten als nach radikaler Zystektomie (25– 60%) (Pontes u. Lopez 1984; Resnick u. O’Conor 1973; Sweeney et al. 1992; Utz et al. 1073). In jedem Fall sollte die Einhaltung eines Sicherheitsabstandes von ca. 1 cm möglich sein. Die Tumorfreiheit der Absetzungsränder sollte intraoperativ mittels Schnellschnitt bewiesen werden. Transurethrale Resektion Neoadjuvante Chemotherapie Wenngleich einige Autoren bis in die späten 90erJahre des letzten Jahrhunderts große Serien präsentieren, in denen Patienten durch eine alleinige »radikale« transurethrale Resektion Fünfjahresüberlebensraten erreichten, die mit der offenen Chirurgie vergleichbar sind (Solsona et al. 1998; Roosen Ob eine neoadjuvante Chemotherapie vor geplanter radikaler Zystektomie Vorteile bringt, wird kontrovers diskutiert. Einerseits könnte sie eine Operation durch die Verkleinerung eines grenzwertig operablen Tumors überhaupt erst ermögli- 85 Radiochemotherapie chen und zudem die Chemosensitivität des Tumors demonstrieren. Andererseits wird das Gesamtüberleben wahrscheinlich nur minimal beeinflusst. Es gibt Hinweise, dass eine Mikrometastasierung mit kleinem Tumorvolumen durch eine neoadjuvante Behandlung kontrolliert werden kann (Raghavan et al. 1984; Fagg et al. 1984; Soloway et al. 1981). Die mit Abstand besten Resultate wurden jüngst von Grossman et al. beschrieben. In der prospektiven, randomisierten Studie an 317 Patienten wurde eine neoadjuvante Therapie mit MVAC mit konsekutiver Zystektomie gegen eine alleinige Zystektomie verglichen. Die Ergebnisse dieser Studie müssen allerdings erheblich in Frage gestellt werden, da nur ein einseitiges Testverfahren angewendet wurde. Die Autoren beschreiben eine signifikante Verlängerung des medianen Überlebens von 46 auf 77 Monate. Die Fünfjahresüberlebensrate lag bei 57% gegenüber 43% in der Kontrollgruppe. Besonders erfolgreich war die Therapie bei den Patienten, bei denen im Zystektomiepräparat ein Stadium pT0 bestand. In dieser Subgruppe wurde sogar ein medianes Fünfjahresüberleben von 85% erreicht. Die Applikation der MVAC-Chemotherapie senkte das Risiko, an der Tumorerkrankung zu versterben, um 33% (Grossmann et al. 2003). Eine aktuelle Metaanalyse zeigte hingegen schlechtere Ergebnisse: Randomisierte Studien mit einer platinhaltigen neoadjuvanten Chemotherapie an insgesamt 2688 Patienten wurden auf ihren Effekt hin untersucht. Es ergab sich ein Fünjahresüberlebensvorteil von nur 5% bei Patienten, die eine medikamentöse Kombination mit Cisplatin erhalten hatten. Wird Cisplatin als Monotherapie eingesetzt, besteht kein signifikanter Überlebensvorteil (Anonymus 2003). Die Toxizität der Therapie und damit die Lebensqualität wird im Rahmen der Analyse jedoch nicht beurteilt. Im Übrigen muss bedacht werden, dass die histopathologische Beurteilung und damit das exakte Staging durch eine neoadjuvante Therapie beeinträchtigt wird. Es bleibt daher weiterhin unklar, welcher Patient einen Vorteil von einer Vorbehandlung haben könnte (Stadler u. Lerner 2003). Junge Patienten ohne Komorbidität profitieren wahrscheinlich von dieser Therapie, allerdings sind die Vorteile einer primären Operation, eines genauen Stagings und gegebenenfalls einer adjuvanten Therapie möglicherweise noch höher. Ältere, schon wegen der Komorbidität nicht operable Patienten erleiden unter Umständen eine Einschränkung der Lebensqualität durch die Therapie selbst als Preis für einen minimalen Überlebensvorteil. Kritisch muss weiterhin bemerkt werden, dass es in o. g. Metaanalyse 7 scheint, der Vorteil der medikamentösen Therapie sei unabhängig von der Art der lokalen Therapie (Radiatio oder Operation). Unbestritten ist jedoch, dass die lokale Tumorkontrolle bei einer Zystektomie höher ist als bei einer Bestrahlung. Das Risiko eines Lokalrezidivs ist entsprechend geringer (Stadler u. Lerner 2003; Lerner u. Skinner 2000). Radiotherapie Das Urothelkarzinom der Harnblase ist prinzipiell strahlensensibel (Dunst et al. 2001; Rodel et al. 2002; Wijnmaalen et al. 1997). Ob eine alleinige Strahlentherapie jedoch vergleichbare Ergebnisse wie eine radikale Zystektomie erwarten lässt, kann nicht abschließend beurteilt werden. Es gibt keinerlei direkte Vergleiche, in denen moderne Methoden der Radiotherapie (primäre 3D-Feld-Bestrahlung) mit der Operation verglichen wurden. Aus älteren Studien sind enttäuschende Ergebnisse bekannt (Blandy et al. 1988; Wallace u. Bloom 1976; Jenkins et al. 1988; Fossa et al. 1988; Hayter et al. 2000). Dies lag jedoch sicherlich zum einen an der ungünstigen Selektion, da nur Patienten der Radiotherapie zugeführt wurden, für die keine operative Maßnahme mehr in Frage kam, zum anderen an der gegenüber dem heutigen Standard veralteten Technologie. Heutzutage ist durch den Einsatz von Hochvoltgeräten und computergestützter 3D-Planung die Wahrscheinlichkeit von Akut- und Spätreaktionen, vor allem am Dünndarm, zwar gesunken (Mohiuddin et al. 1985), jedoch besteht nach wie vor ein ungünstiges Verhältnis der Nebenwirkungen einer Radiomonotherapie gegenüber der onkotherapeutischen Wirksamkeit (Shipley et al. 1999). Die alleinige Radiotherapie sollte Indikationen rein palliativer Zielsetzung bei inkurablen Tumoren vorbehalten sein. Radiochemotherapie Liegen schwerwiegende Faktoren vor, die gegen die Durchführung einer Zystektomie sprechen (erhebliche Komorbidität, hohes Lebensalter oder der ausdrückliche Wunsch nach Blasenerhalt), müssen blasenerhaltende Verfahren diskutiert werden. Im Falle eines muskelinvasiven oder lokal fortgeschrittenen Tumors sind Radiotherapie, TUR oder Chemotherapie als Monotherapie der radikalen Zystektomie in der Frage der lokalen Tumorkontrolle deutlich unterlegen (Shipley et al. 1999). Bestehen zwar wenig oder keine lokalen Symptome, aber eine Mikrome- 86 7 Kapitel 7 · Therapie des muskelinvasiven und des lokal fortgeschrittenen Blasenkarzinoms im Jahr 2004 tastasierung, so kann der Vorsprung der Operation jedoch in den Hintergrund treten. Diese Konstellation würde ohnehin den adjuvanten Einsatz einer Chemotherapie implizieren. Weiterhin können Chemotherapeutika synergistisch die Wirkung der Strahlentherapie erhöhen. Der kombinierte Einsatz der Verfahren (TUR mit Nachresektion, nach Möglichkeit bis zum Status R0, adjuvante Radiochemotherapie) zeigte eine Fünfjahresüberlebensrate zwischen 49 und 93%. Die besten Ergebnisse wurden dabei von Eapen durch eine intraarterielle Gabe von Cisplatin erzielt. Die Toxizität sei dabei gering (Dunst et al. 2001; Rodel et al. 2002; Shipley et al. 1999; Hussain et al. 2001; Eapen et al. 1998; Rotman et al. 1990). In einigen dieser Studien wurde jedoch im Falle eines Nichtansprechens nach TUR und Radiochemotherapie eine SalvageZystektomie durchgeführt. Die Wahrscheinlichkeit eines definitiven Blasenerhaltes lag schließlich nur bei 38–43%. Bei Patienten, die auf die Therapie ansprachen, war die Prognose gut. ⊡ Tabelle 7.3 zeigt die Ergebnisse der wichtigsten Studien. Die Toxizität des kombinierten blasenerhaltenden Vorgehens entspricht den zu erwartenden Risiken und Nebenwirkungen nach Radiatio und systemischer Chemotherapie (Übelkeit, Erbrechen, Durchfall, Fatigue-Syndrom, Neutropenie, radiogene Zystitis, erektile Dysfunktion u. a.). Insbesondere die cisplatinhaltigen Schemata weisen hohe emetische Potenz auf. Neuere Chemotherapeutika, eventuell in Kombination mit den bewährten Substanzen, könnten die Aussicht auf eine effektive Therapie bei gleichzeitiger Reduktion der möglichen Nebenwirkungen verbessern (Hussain et al. 2002; Hussain u. James 2002). Es gibt bis dato keine prospektiv randomisierten direkten Vergleiche zwischen dem Goldstandard der radikalen Zystektomie und dem o. g. blasenerhaltenden, trimodalen Vorgehen. Das ungünstige Verhältnis zwischen unklarer lokaler Tumorkontrolle und erheblicher Toxizität spricht jedoch gegen die blasenerhaltende Kombination. Wegen des schlechten Ansprechens auf die Therapie sollte die trimodale Therapie nicht bei Vorliegen eines Carcinoma in situ angewandt werden. ⊡ Tabelle 7.4 stellt klare Indikationen zur radikalen Zystektomie und Konstellationen, die einen Blasenerhalt prinzipiell erlauben, gegenüber. ⊡ Tabelle 7.3. Erfolg verschiedener Radiochemotherapieregimes Autor (Jahr) Patienten [n] Therapieregime Ergebnisse [%] CR Sauer (1990) 67 Cisplatin + RTX 76 Hussain (2001) 53 Cisplatin + 5Fu + RTX 51 Eapen (1998) 24 Cisplatin i.a. + RTX 93 Rotman (1990) 19 5Fu +/– Mito + RTX 74 ⊡ Tabelle 7.4. Indikationsstellung für bzw. gegen einen Blasenerhalt Zystektomie Blasenerhaltende Strategie Pathologisches Stadium T3/T4 T2 Ausdehnung Multifokaler Tumor oder CIS Monolokulär und kleiner Tumor Status oberer Harntrakt Harnstauung Keine Harnstauung 87 Literatur Palliative Maßnahmen bei lokal fortgeschrittenem Tumor Liegen systemische Metastasen oder ein lokal weit fortgeschrittenes Stadium vor, so ist die Prognose quo ad vitam stark eingeschränkt. Zusätzlich kann eine Reihe von Symptomen auftreten, die eine palliative Therapie notwendig machen. 7 Schmerztherapie Eine medikamentöse Schmerztherapie sollte großzügig nach dem 3-Stufen-Eskalationsschema der WHO verabreicht werden. Die Gabe von Acetylsalicylsäure oder andere Thrombozytenaggregationshemmern ist dabei jedoch zu vermeiden. Palliative Strahlentherapie Blutende Tumorblase Besteht eine Makrohämaturie bei Vorliegen eines metastasierten oder organüberschreitenden Tumors, sollten zunächst alle konservativen Maßnahmen ausgeschöpft werden. Nach instrumenteller Ausräumung einer evtl. vorliegenden Tamponade und Anlage einer Dauerspülung sollten die Gerinnungssituation und der Hämoglobinwert überprüft und ggf. korrigiert werden. In vielen Fällen ist bereits zum Ausräumen der Tamponade ein Eingriff in Narkose notwendig. In gleicher Narkose sollte eine transurethrale Resektion, jedoch nur bis in das oberflächliche Niveau durchgeführt werden. Führen diese Maßnahmen nicht zu einer deutlichen Besserung, sollte als nächstes eine Instillation mit Alaun 1% (Aluminiumkaliumsulfat) oder bei Versagen mit 1–5% (–10%) Formalinlösung erfolgen. Ein vesikorenaler Reflux muss jedoch im Vorfeld ausgeschlossen werden. Bleibt es trotz aller o.g. Maßnahmen bei der schweren Makrohämaturie, so müssen eine transarterielle Embolisation des Tumors und als operative Ultima Ratio eine Salvage-Zystektomie in Betracht gezogen werden. Harnstauung Eine Harnstauung in der palliativen Situation sollte nur behoben werden, wenn dadurch Symptome verschwinden oder der Patient es ausdrücklich wünscht. Insbesondere im Falle einer ansonsten asymptomatischen Urämie kann diese Entscheidung sehr schwierig sein. Liegen Koliken, eine Infektion vor oder ist eine Chemotherapie in weiterer Folge geplant, so sollte zunächst ein perkutaner Nierenfistelkatheter und/oder ein Doppel-J-Katheter eingelegt werden, s.g. »Tumor-Stents« mit einer möglichen Liegezeit bis zu 35 Monaten bieten dabei die meisten Vorteil bezüglich der Lebensqualität (Weissbach 2001; Kulkarni u. Bellamy 2001). Besonders effektiv ist eine Strahlentherapie, die sich gegen durch Knochenmetastasen ausgelöste Schmerzen richtet. Eine fraktionierte Bestrahlung in hoher Gesamtdosis (z. B. 12-mal 3 Gy) führt schnell zum Erfolg. Mittelfristig kann im betroffenen Bereich auch die Frakturgefahr günstig beeinflusst werden. Metastasenchirurgie Können durch begrenzte operative Eingriffe schwere Folgeerscheinungen wie Frakturen usw. vermieden werden, so sollten diese durchgeführt werden. Die Resektion chemotherapierefraktärer Metastasen bietet jedoch insbesondere bei asymptomatischen Patienten keinerlei Überlebensvorteil und beschränkt sich daher auf Einzelfälle (Otto et al. 2001). Chemotherapie mit palliativem Ansatz In sorgfältiger Abwägung möglicher Risiken und Nebenwirkungen mit der zu erwartenden Symptomminderung kann der Einsatz moderner Chemotherapeutika mit geringer Toxizität (Gemcitabine, Taxane usw.) erwogen werden (Kaufman et al. 2000; Garcia del Muro et al. 2002). Literatur Abdel-Hakim AM, Bassiouny F, Abdel Azim MS, Rady I, Mohey T, Habib I, Fathi H (2002) Laparoscopic radical cystectomy with orthotopic neobladder. J Endourol 16: 377–381 Ahlering TE, Lieskovsky G, Skinner DG (1984) Indications for urethrectomy in men undergoing single stage radical cystectomy for bladder cancer. J Urol 131: 657–659 Ahlering TE, Henderson JB, Skinner DG (1983) Controlled hypotensive anesthesia to reduce blood loss in radical cystectomy for bladder cancer. J Urol 129: 953–954 88 7 Kapitel 7 · Therapie des muskelinvasiven und des lokal fortgeschrittenen Blasenkarzinoms im Jahr 2004 Amling CL, Thrasher JB, Frazier HA, Dodge RK, Robertson JE, Paulson DF (2000) Radical cystectomy for stages Ta, Tis and T1 transitional cell carcinoma of the bladder. J Urol. 151: 31–5; discussion 35–6, 1994. Anonymus (2003) Neoadjuvant chemotherapy in invasive bladder cancer: a systematic review and meta-analysis. Lancet 361: 1927–1934 Bassi P: Outcome of radical cystectomy for invasive bladder cancer. Curr Opin Urol 10: 459–463 Beecken WD, Wolfram M, Engl T, Bentas W, Probst M, Blaheta R, Oertl A, Jonas D, Binder J (2003) Robotic-assisted laparoscopic radical cystectomy and intra-abdominal formation of an orthotopic ileal neobladder. Eur Urol 44: 337–339 Blandy JP, Hope-Stone HF, Oliver RT, England HR (1984) Salvage cystectomy in the treatment of invasive bladder cancer. Prog Clin Biol Res 153: 359–363 Blandy JP, Jenkins BJ, Fowler CG et al. (1988) Radical radiotherapy and salvage cystectomy for T2/3 cancer of the bladder. Prog Clin Biol Res 260: 447–451 Bollack C, Jacqmin D, Cuvelier G, Bertrand P (1989) Radical cystectomy in patients over 70 years. Prog Clin Biol Res 303: 613–616 Bosl GJ, Fair WR, Herr HW et al. (1994) Bladder cancer: advances in biology and treatment. Crit Rev Oncol Hematol 16: 33–70 Cancrini A, De Carli P, Pompeo V et al. (1996) Lower urinary tract reconstruction following cystectomy: experience and results in 96 patients using the orthotopic ileal bladder substitution of Studer et al. Eur Urol 29: 204–209 Chang SS, Alberts G, Cookson MS, Smith JA Jr (2001) Radical cystectomy is safe in elderly patients at high risk. J Urol 166: 938–941 Chang SS, Cookson MS, Hassan JM, Wells N, Smith JA Jr (2002a) Routine postoperative intensive care monitoring is not necessary after radical cystectomy. J Urol 167: 1321–1324 Chang SS, Cookson MS, Baumgartner RG, Wells N, Smith JA Jr (2002b) Analysis of early complications after radical cystectomy: results of a collaborative care pathway. J Urol 167: 2012–2016. Chang SS, Cole E, Smith JA Jr, Cookson MS (2002c) Pathological findings of gynecologic organs obtained at female radical cystectomy. J Urol 168: 147–149. Chang SS, Cole E, Cookson MS, Peterson M, Smith JA Jr (2002d) Preservation of the anterior vaginal wall during female radical cystectomy with orthotopic urinary diversion: technique and results. J Urol 168: 1442–1445 Darson M, Blute M, Barrett D (2000) Continent orthotopic urinary diversion in female patients. AUA Update series. 19: 257–264 Dubuc-Lissoir J (2003) Use of a new energy-based vessel ligation device during laparoscopic gynecologic oncologic surgery. Surg Endosc 17: 466–468 Dunst J, Rodel C, Zietman A, Schrott KM, Sauer R, Shipley WU (2001) Bladder preservation in muscle-invasive bladder cancer by conservative surgery and radiochemotherapy. Semin Surg Oncol 20: 24–32 Eapen L, Stewart D, Grimard L, Crook J, Futter N, Aref I, Huan S, Rasuli P, Peterson R (1998) Treatment of cancer of the bladder in elderly patients with an intra-arterial chemotherapy and radiotherapy combination: 10-year experience]. Cancer Radiother 2 [Suppl 1]: 73s–76s Fagg SL, Dawson-Edwards P, Hughes MA, Latief TN, Rolfe EB, Fielding JW (1984) Cis-diamminedichloroplatinum (DDP) as initial treatment of invasive bladder cancer. Br J Urol 56: 296–300 Finlayson EV, Birkmeyer JD (2001) Operative mortality with elective surgery in older adults. Eff Clin Pract 4: 172–177 Fossa SD, Miller A, Ous S, Poppe E, Host H, Kaalhus O (1988) Treatment of muscle-infiltrating bladder cancer: the Norwegian Radium Hospital’s experience 1966–1982. Prog Clin Biol Res 260: 525–541 Frazier HA, Robertson JE, Paulson DF (1992) Complications of radical cystectomy and urinary diversion: a retrospective review of 675 cases in 2 decades. J Urol 148: 1401–1405 Freeman JA, Esrig D, Stein JP, Skinner DG (1994) Management of the patient with bladder cancer. Urethral recurrence. Urol Clin North Am 21: 645–651 Game X, Soulie M, Seguin P, Vazzoler N, Tollon C, Pontonnier F, Plante P (2001) Radical cystectomy in patients older than 75 years: assessment of morbidity and mortality. Eur Urol 39: 525–529 Garcia del Muro X, Marcuello E, Guma J et al. (2002) Phase II multicentre study of docetaxel plus cisplatin in patients with advanced urothelial cancer. Br J Cancer 86: 326–330 Grossmann HB, Natale RB, Tangen CM et al. (2003) Neoadjuvant Chemoterapy plus Cytectomy compared with Cystectomy alone for locally advanced bladder cancer. N Engl J Med 349: 859–866 Gschwend JE (2002) Outcome of patients undergoing radical cystectomy for invasive bladder cancer. Front Radiat Ther Oncol 36: 106–117 Gschwend JE, Fair WR, Vieweg J (2000) Radical cystectomy for invasive bladder cancer: contemporary results and remaining controversies. Eur Urol 38: 121–130 Hayter CR, Paszat LF, Groome PA, Schulze K, Mackillop WJ (2000) The management and outcome of bladder carcinoma in Ontario, 1982–1994. Cancer 89: 142–151 Heniford BT, Matthews BD, Sing RF, Backus C, Pratt B, Greene FL (2001) Initial results with an electrothermal bipolar vessel sealer. Surg Endosc 15: 799–801 Henry K, Miller J, Mori M, Loening S, Fallon B (1988) Comparison of transurethral resection to radical therapies for stage B bladder tumors. J Urol 140: 964–967 Herr HW (1987) Conservative management of muscle-infiltrating bladder cancer: prospective experience. J Urol 138: 1162–1163 Herr HW (2001) Transurethral resection of muscle-invasive bladder cancer: 10-year outcome. J Clin Oncol 19: 89–93 Herr HW (2003) Superiority of ratio based lymph node staging for bladder cancer. J Urol 169: 943–945 Hiebl R, Langen PH, Haben B, Polsky MS, Steffens J (1999) Prepubic urethrectomy with urethral stripping. J Urol 162: 127–128 Horenblas S, Meinhardt W, Ijzerman W, Moonen LF (2001) Sexuality preserving cystectomy and neobladder: initial results. J Urol 166: 837–840 89 Literatur Hussain MH, Glass TR, Forman J et al. (2001) Combination cisplatin, 5-fluorouracil and radiation therapy for locally advanced unresectable or medically unfit bladder cancer cases: a Southwest Oncology Group Study. J Urol 165: 56–60; discussion 60–61 Hussain SA, James ND (2002) Organ preservation strategies in bladder cancer. Expert Rev Anticancer Ther 2: 641–651 Hussain M, Vaishampayan U, Smith DC (2002) Novel gemcitabine-containing triplets in the management of urothelial cancer. Semin Oncol 29: 20–24 Jenkins BJ, Caulfield MJ, Fowler CG et al. (1988) Reappraisal of the role of radical radiotherapy and salvage cystectomy in the treatment of invasive (T2/T3) bladder cancer. Br J Urol 62: 343–356 Kaufman D, Raghavan D, Carducci M et al. (2000) Phase II trial of gemcitabine plus cisplatin in patients with metastatic urothelial cancer. J Clin Oncol 18: 1921–1927 Kulkarni JN, Gulla RI, Tongaonkar HB, Kashyapi BD, Rajyaguru KB (1999) Radical cystoprostatectomy: an extraperitoneal retrograde approach. J Urol 161: 545–548 Kulkarni R, Bellamy E (2001) Nickel-titanium shape memory alloy Memokath 051 ureteral stent for managing longterm ureteral obstruction: 4-year experience. J Urol 166: 1750–1754 Kulkarni JN, Pramesh CS, Rathi S, Pantvaidya GH (2003) Longterm results of orthotopic neobladder reconstruction after radical cystectomy. BJU Int 91: 485–488 Landman J, Kerbl K, Rehman J et al. (2003) Evaluation of a vessel sealing system, bipolar electrosurgery, harmonic scalpel, titanium clips, endoscopic gastrointestinal anastomosis vascular staples and sutures for arterial and venous ligation in a porcine model. J Urol 169: 697–700 Lebret T, Herve JM, Barre P, Gaudez F, Lugagne PM, Barbagelatta M, Botto H (1998) Urethral recurrence of transitional cell carcinoma of the bladder. Predictive value of preoperative latero-montanal biopsies and urethral frozen sections during prostatocystectomy. Eur Urol 33: 170–174 Lebret T, Herve JM, Yonneau L, Barre P, Lugagne PM, Butreau M, Molinie V, Botto H (2000) Study of survival after cystectomy for bladder cancer. Report of 504 cases. Prog Urol 10: 553–560 Leissner J, Hohenfellner R, Thuroff JW, Wolf HK (2000) Lymphadenectomy in patients with transitional cell carcinoma of the urinary bladder; significance for staging and prognosis. BJU Int 85: 817–823 Lerner SP, Skinner DG (2000) Radical cystectomy for bladder cancer. In: Vogelzang NJ, Shipley WU, Scardino P, Coffey D (eds) Comprehensive Textbook of genitourinary oncology. Philadelphia, Lippincott Williams and Wilkins, pp 425–447 Lerner SP, Skinner E, Skinner DG (1992) Radical cystectomy in regionally advanced bladder cancer. Urol Clin North Am 19: 713–723 Lieskovsky G, Skinner DG (1984) Role of lymphadenectomy in the treatment of bladder cancer. Urol Clin North Am 11: 709–716 Mameghan H, Fisher RJ, Watt WH et al. (1992) The management of invasive transitional cell carcinoma of the bladder. Results of definitive and preoperative radiation 7 therapy in 390 patients treated at the Prince of Wales Hospital, Sydney, Australia. Cancer 69: 2771–2778 Marshall FF, Mostwin JL, Radebaugh LC, Walsh PC, Brendler CB (1991) Ileocolic neobladder post-cystectomy: continence and potency. J Urol 145: 502–504 Mathur VK, Krahn HP, Ramsey EW (1981) Total cystectomy for bladder cancer. J Urol 125: 784–786 Matin SF, Gill IS (2002) Laparoscopic radical cystectomy with urinary diversion: completely intracorporeal technique. J Endourol 16: 335–341; discussion 341 Matthews BD, Pratt BL, Backus CL et al. (2001) Effectiveness of the ultrasonic coagulating shears, LigaSure vessel sealer, and surgical clip application in biliary surgery: a comparative analysis. Am Surg 67: 901–906 Menon M, Hemal AK, Tewari A et al. (2003) Nerve-sparing robot-assisted radical cystoprostatectomy and urinary diversion. BJU Int 92: 232–236 Mills RD, Turner WH, Fleischmann A, Markwalder R, Thalmann GN, Studer UE (2001) Pelvic lymph node metastases from bladder cancer: outcome in 83 patients after radical cystectomy and pelvic lymphadenectomy. J Urol 166: 19–23 Mohiuddin M, Kramer S, Newall J, Parsons J, Wiley A, Strong G, Mulholland SG: Combined preoperative and postoperative radiation for bladder cancer. Results of RTOG/Jefferson Study. Cancer 55: 963–966 Montie JE, Straffon RA, Stewart BH (1984) Radical cystectomy without radiation therapy for carcinoma of the bladder. J Urol 131: 477–482 Otto T, Krege S, Suhr J, Rubben H (2001) Impact of surgical resection of bladder cancer metastases refractory to systemic therapy on performance score: a phase II trial. Urology 57: 55–59 Parekh DJ, Clark T, O’Connor J, Jung C, Chang SS, Cookson M, Smith JA Jr (2002) Orthotopic neobladder following radical cystectomy in patients with high perioperative risk and co-morbid medical conditions. J Urol 168: 2454–2456 Peterson AC, Lance RS, Ahuja S (2002) Laparoscopic hand assisted radical cystectomy with ileal conduit urinary diversion. J Urol 168: 2103–2105; discussion 2105 Pontes JE, Lopez R (1984) Tumor recurrence following partial cystectomy. Prog Clin Biol Res 162A: 387–392 Raghavan D, Pearson B, Coorey G, Woods W, Arnold D, Smith J, Donovan J, Langdon P (1984) Intravenous cis-platinum for invasive bladder cancer. Safety and feasibility of a new approach. Med J Aust 140: 276–278 Resnick MI, O’Conor VJ Jr (1973) Segmental resection for carcinoma of the bladder: review of 102 patients. J Urol 109: 1007–1010 Rodel C, Grabenbauer GG, Kuhn R, Zorcher T, Papadopoulos T, Dunst J, Schrott KM, Sauer R (2002) Organ preservation in patients with invasive bladder cancer: initial results of an intensified protocol of transurethral surgery and radiation therapy plus concurrent cisplatin and 5-fluorouracil. Int J Radiat Oncol Biol Phys 52: 1303–1309 Roehrborn CG, Sagalowsky AI, Peters PC (1991) Long-term patient survival after cystectomy for regional metastatic transitional cell carcinoma of the bladder. J Urol 146: 36–39 90 7 Kapitel 7 · Therapie des muskelinvasiven und des lokal fortgeschrittenen Blasenkarzinoms im Jahr 2004 Roosen JU, Geertsen U, Jahn H, Weinreich J, Nissen HM (1997) Invasive, high grade transitional cell carcinoma of the bladder treated with transurethral resection. A survival analysis focusing on TUR as monotherapy. Scand J Urol Nephrol 31: 39–42 Rotman M, Aziz H, Porrazzo M, Choi KN, Silverstein M, Rosenthal J, Laungani G, Macchia R (1990) Treatment of advanced transitional cell carcinoma of the bladder with irradiation and concomitant 5-fluorouracil infusion. Int J Radiat Oncol Biol Phys 18: 1131–1137 Ryan DW (1982) Anaesthesia for cystectomy. A comparison of two anaesthetic techniques. Anaesthesia 37: 554–560 Schlegel PN, Walsh PC (1987) Neuroanatomical approach to radical cystoprostatectomy with preservation of sexual function. J Urol 138: 1402–1406 Schoenberg MP, Walsh PC, Breazeale DR, Marshall FF, Mostwin JL, Brendler CB (1996) Local recurrence and survival following nerve sparing radical cystoprostatectomy for bladder cancer: 10-year followup. J Urol 155: 490–494 Serel TA, Sevin G, Perk H, Kosar A, Soyupek S (2003) Antegrade extraperitoneal approach to radical cystectomy and ileal neobladder. Int J Urol 10: 25–28; discussion 29 Sherif A, De La Torre M, Malmstrom PU, Thorn M (2001) Lymphatic mapping and detection of sentinel nodes in patients with bladder cancer. J Urol 166: 812–815 Shipley WU, Kaufman DS, Heney NM, Althausen AF, Zietman AL (1999) An update of combined modality therapy for patients with muscle invading bladder cancer using selective bladder preservation or cystectomy. J Urol 162: 445–450; discussion 450–451 Simonato A, Gregori A, Lissiani A, Bozzola A, Galli S, Gaboardi F (2003) Laparoscopic radical cystoprostatectomy: a technique illustrated step by step. Eur Urol 44: 132–138 Smith JA Jr, Whitmore WF Jr (1981) Regional lymph node metastasis from bladder cancer. J Urol 126: 591–593 Skinner DG, Lieskovsky G (1984) Contemporary cystectomy with pelvic node dissection compared to preoperative radiation therapy plus cystectomy in management of invasive bladder cancer. J Urol 131: 1069–1072 Skinner EC, Lieskovsky G, Skinner DG (1984) Radical cystectomy in the elderly patient. J Urol 131: 1065–1068 Smith JA Jr (2003) Laparoscopic radical cystectomy with urinary diversion: completely intracorporeal technique. J Urol 169: 1607–1608 Soloway MS, Ikard M, Ford K (1981) Cis-diamminedichloroplatinum (II) in locally advanced and metastatic urothelial cancer. Cancer 47: 476–480 Solsona E, Iborra I, Ricos JV, Monros JL, Casanova J, Calabuig C (1998) Feasibility of transurethral resection for muscle infiltrating carcinoma of the bladder: long-term followup of a prospective study. J Urol 159: 95–98; discussion 98–99 Stadler WM, Lerner SP (2003) Perioperative chemotherapy in locally advanced bladder cancer. Lancet 361: 1922–1923 Stein JP, Lieskovsky G, Cote R et al. (2001) Radical cystectomy in the treatment of invasive bladder cancer: long-term results in 1,054 patients. J Clin Oncol 19: 666–675 Stein JP (2000) Indications for early cystectomy. Semin Urol Oncol 18: 289–295 Stenzl A, Holtl L (2003) Orthotopic bladder reconstruction in women-what we have learned over the last decade. Crit Rev Oncol Hematol 47: 147–154 Stenzl A, Bartsch G, Rogatsch H (2002) The remnant urothelium after reconstructive bladder surgery. Eur Urol 41: 124–131 Sweeney P, Kursh ED, Resnick MI (1992) Partial cystectomy. Urol Clin North Am 19: 701–711 Takashi M, Nagai T, Murase T, Miyake K, Hamajima N, Mizuno S (1989) Multivariate evaluation of determinants affecting regional lymph node metastasis and survival in bladder cancer patients who underwent radical cystectomy. Urol Int 44: 125–131 Takashi M, Sakata T, Nakano Y, Murase T, Miyake K (1992) Superficial bladder cancer treated by total cystectomy: tumour characteristics and patient survival. Int Urol Nephrol 24: 265–271 Turk I, Deger S, Winkelmann B, Schonberger B, Loening SA (2001a) Laparoscopic radical cystectomy with continent urinary diversion (rectal sigmoid pouch) performed completely intracorporeally: the initial 5 cases. J Urol 165: 1863–1866 Turk I, Deger S, Winkelmann B, Baumgart E, Loening SA (2001b) Complete laparoscopic approach for radical cystectomy and continent urinary diversion (sigma rectum pouch). Tech Urol 7: 2–6 Utz DC, Schmitz SE, Fugelso PD, Farrow GM (1973) Proceedings: A clinicopathologic evaluation of partial cystectomy for carcinoma of the urinary bladder. Cancer 32: 1075–1077 Wallace DM, Bloom HJ (1976) The management of deeply infiltrating (T3) bladder carcinoma: controlled trial of radical radiotherapy versus preoperative radiotherapy and radical cystectomy (first report). Br J Urol 48: 587–594 Walsh PC (1987) Radical prostatectomy, preservation of sexual function, cancer control. The controversy. Urol Clin North Am 14: 663–673 Wammack R (1997) Ausgewählte OP-Techniken, 2. Aufl. Thieme, Stuttgart Weissbach L (2001) Palliation of urothelial carcinoma of the bladder. Urologe A 40: 475–479 Whalley DG, Berrigan MJ (2000) Anesthesia for radical prostatectomy, cystectomy, nephrectomy, pheochromocytoma, and laparoscopic procedures. Anesthesiol Clin North America 18: 899–917 Wijnmaalen A, Helle PA, Koper PC, Jansen PP, Hanssens PE, Boeken Kruger CG, van Putten WL (1997) Muscle invasive bladder cancer treated by transurethral resection, followed by external beam radiation and interstitial iridium192. Int J Radiat Oncol Biol Phys 39: 1043–1052 Wood DP, Jr., Montie JE, Pontes JE, Levin HS (1989) Identification of transitional cell carcinoma of the prostate in bladder cancer patients: a prospective study. J Urol 142: 83–85 Zhang G (1997) Simultaneous prepubic urethrectomy with radical cystectomy for transitional cell carcinoma of the bladder. Tech Urol 3: 72–75