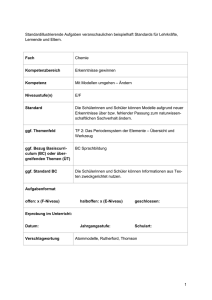
Zum Streuversuch von Rutherford
Werbung

Der Streuversuch Der Streuversuch wurde in Manchester von den Physikern Rutherford, Geiger und Marsden durchgeführt. Sie begannen 1906 mit dem Versuch und benötigten sieben Jahre um das Geheimnis des Aufbaus der Atome vorerst zu lösen. Klick dich in den Streuversuch ein. Los geht‘s! • Vorüberlegungen • Versuchsaufbau • animierte Versuchsaufbau • Durchführung • Beobachtung • Schlussfolgerung © Th. Böse JSG Bad Kissingen Rutherford, Ernest Rutherford wurde am 30.8.1871 in Neuseeland geboren. Sein Studium schloss er in Cambridge (England) ab. Von da ging er an die Universität Montreal in Kanada. 1907 kehrte er nach England zurück und erhielt 1908 für sein Kern-HülleModell den Nobelpreis. Das Radium für seine Forschungsarbeit bekam er von der Wiener Akademie der Wissenschaften. Nach dem 1. Weltkrieg wollte die englische Regierung das Radium als Eigentum des Feindes beschlagnahmen. Rutherford ließ es sich gut bezahlen und unterstützte mit diesem Geld die Wiener Akademie. In sein Familienwappen ließ er die Zerfalls- und Wachstumskurve radioaktiver Substanzen einarbeiten. Rutherford starb am 19.10.1937. Zum Streuversuch von Rutherford Streuversuch - Vorüberlegungen Rutherford ging mit seinen Überlegungen vom Rosinenkuchen-Modell aus. Danach sei das Atom eine Kugel, in der sich positive Ladungen diffus aufhalten, wobei dann die Elektronen wie Rosinen in einem Kuchen eingelagert sind. Dieses Atom wäre außerdem undurchlässig für Teilchen aller Art, egal welche Bewegungsenergie sie auch besitzen würden. Nachdem Philipp Lenard eine Aluminiumfolie mit Elektronen beschoss, kam er zu dem Ergebnis, dass das Atom für Elektronen durchlässig ist. Außerdem erkannte er, dass bei steigender Bewegungsenergie der negativen Ladungsträger mehr Elektronen die Folie durchdringen. Rutherford wiederholte dieses Experiment auf ähnliche Weise; er beschoss eine Goldfolie mit Alpha-Strahlung, und stellte die Vermutung auf, dass diese Heliumkerne durch die gleichmäßig verteilten positiven Ladungen nur wenig in ihrer Flugrichtung beeinflusst und nur in einem Winkel von null bis maximal einem Grad abgelenkt werden. Zum Versuchsaufbau Streuversuch - Aufbau Zinksulfidschirm Goldfolie Mit jeden Klick auf die n-Taste kannst du dir den Aufbau des Streuversuchs von Rutherford animieren lassen! Bleiblock Du kannst dir aber auch den kompletten Versuch hier ansehen! Lochblende radioaktives Radium Zur Versuchsdurchführung © Th. Böse JSG Bad Kissingen Streuversuch - Aufbau Goldfolie Zinksulfidschirm abgelenktes -Teilchen -Teilchen Bleiblock Lochblende radioaktives Radium Zur Versuchsdurchführung Streuversuch - Durchführung Von einem Präparat geht Alpha-Strahlung, so genannte Alpha-Teilchen aus. Der Bleiblock blendet ein schmales Teilchenbündel aus. Die Alpha-Teilchen treffen auf eine extrem dünne Goldfolie (etwa 100 Atomschichten stark). Hinter der Folie befindet sich ein Leuchtschirm als Nachweisgerät, der um die Folie herum bewegt werden kann. Trifft ein Alpha-Teilchen auf diesen Schirm, erzeugt es einen kleinen Lichtblitz, der durch ein Mikroskop beobachtet und gezählt wird. Der Versuch findet im Vakuum ab. Zur Versuchs-Animation Streuversuch - Animation Goldfolie Zinksulfidschirm Bleiblock mit Radium Animation-Start © Th. Böse JSG Bad Kissingen Streuversuch - Animation Goldfolie abgelenktes -Teilchen Bleiblock mit Radium -Teilchen Zinksulfidschirm Animation-Start © Th. Böse Zur Beobachtung JSG Bad Kissingen Streuversuch - Beobachtung Fast alle Alpha-Teilchen durchdringen ungestreut die Folie. Kleine Ablenkwinkel kommen häufiger, große außerordentlich selten vor. Messungen ergaben, dass bei einem Beschuss der Goldfolie mit 132.500 Heliumkernen 132.000 einen Streuwinkel von weniger als 15°, 477 zwischen 15° und 60° und lediglich 33 Alpha-Teilchen zwischen 60° und 150° hatten. Verwendet man Folien unterschiedlichen Materials, so zeigt der Versuch der Messreihen, dass die Wahrscheinlichkeit für die Ablenkung eines Alpha-Teilchens um einen bestimmten Winkel proportional zum Quadrat der Ordnungszahl der Atome des Streumaterials ist. Zur Schlussfolgerung Streuversuch - Folgerung Da Rutherford in seinem Streuversuch auch Ablenkungen um 180° beobachtete, schlussfolgerte er, dass die Alpha-Teilchen mit Teilchen zusammengestoßen sein müssen, deren Massen größer als die des Alpha-Teilchens sind. Bei kleinerer Masse würde das Alpha-Teilchen keine Richtungsumkehr erfahren, bei gleicher würde es zum Stillstand kommen. Deswegen, so erkannte Rutherford, scheiden Elektronen als Streuzentren aus. Für die Ablenkung der Alpha-Teilchen machte Rutherford die Coulombkraft des Kerns verantwortlich; und da diese umgekehrt proportional zum Quadrat der Entfernung r ist, wird ein Großteil der Alpha-Strahlung nur gering abgelenkt und abgebremst. Rutherford schlussfolgerte daher, dass der Raum zwischen dem Kern und der Atomhülle leer sein muss. Des Weiteren überlegte er sich, dass bei einem Auftreffen eines Alpha-Teilchens auf den positiv geladenen Kern (Streuzentrum), die kinetische Energie, in dem Moment, in dem das Alpha-Teilchen die größtmögliche Annäherung an das Streuzentrum erlangt hat, vollständig in potentielle Energie umgewandelt wird. Demnach kann man für diesen Moment die Energien gleichsetzen. Daraus kann man dann die maximale Größe eines Atomkerns bestimmen. Zur Rutherfordschen Atomhypothese Rutherfordsche Atommodell Aus dem Rutherfordschen Streuversuch leitet sich das Rutherfordsche Atommodell ab: 1. Atome haben einen Durchmesser von ca. 10 hoch -10 m. 2. Nahezu 99,9% der gesamten Masse ist jedoch im Atomkern konzentriert. 3. Die gesamte positive Ladung befindet sich in Form von Protonen im Kern. 4. Die negativen Ladungen befinden sich in Form von Elektronen im Raum um den Atomkern. 5. Dieser Raum wird als Atomhülle bezeichnet. 6. Die Elektronen umkreisen den Kern auf beliebigen Bahnen. 7. Diese Bahnen bestimmen die Größe des Atoms. 8. Zwischen den Elektronen ist leerer Raum. 9. Die Kraft zwischen den Elektronen und dem Kern ist die elektrostatische Anziehungskraft. Man bezeichnet das Rutherforsche Atommodell auch als Kern-Hülle-Modell Das Kern-Hülle-Modell Das Kern-Hülle-Modell von Rutherford beinhaltet, dass die Atome aus noch kleineren Teilchen aufgebaut sind. Nach diesem Modell sind Atome aus einem Kern und einer Hülle aufgebaut. Der Atomkern (Nuklid) enthält eine bestimmte Anzahl positiver Ladungen, die man Protonen nennt. Die Gesamtheit aller Protonen im Kern ergibt die Kernladungszahl (Z), die der Ordnungszahl entspricht. Neben Protonen enthält der Kern elektrisch neutrale Neutronen . Protonen und Neutronen werden als Nukleonen bezeichnet. Die Anzahl der Nukleonen ergeben die Massenzahl (A) des Atoms. Die Atomhülle besteht aus negativ geladenen Elektronen . Die Anzahl der Elektronen in der Hülle entspricht der Anzahl der Protonen im Kern. Dadurch ist das Atom nach außen elektrisch neutral. Radioaktive Strahlungsarten Instabile Kerne welche zerfallen tun dies nicht willkürlich sondern sie befolgen bestimmte Gesetzmäßigkeiten: Es sind die drei klassischen Arten der radioaktiven Strahlung: alpha-Strahlung: Aussendung eines 42 He-Kerns (alpha-Teilchen) aus dem instabilen Kern. Es wird ein ganzes Paket 2 Protonen und 2 Neutronen gleichzeitig aus dem Kern gesandt. Bsp: 21084 Po 20682 Pb + 42He beta-Strahlung: Umwandlung eines Neutrons in ein Proton und ein Elektron. Das Elektron entsteht direkt im Kern und wird sogleich emittiert (ausgesandt). Es entsteht zusätzlich ein Neutrino. Bsp: 146 C 147 N + e- gamma-Strahlung: Aussendung hochenergetischer Strahlung (gamma-Quanten Röntgenstrahlung) aus dem instabilen Kern. Die gamma-Strahlung ist meist Begleitstrahlung und verändert weder die Massenzahl noch die Ordnungszahl.