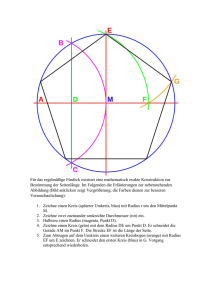
14. Trennungsverfahren
Werbung

Physikalische Grundlagen der Messmethoden der Zell- und molekularen Diagnostik Hydrodynamische Trennungsverfahren Péter Maróti Professor für Biophysik, Universität von Szeged, Ungarn. Lehrbücher: Biophysik für Mediziner (Herausgeber S. Damjanovich, J. Fidy und J. Szöllősi) Medicina, Budapest, 2008. Fercher A.F. Medizinische Physik, Springer, Wien, New York 1992. Haas U.: Physik für Pharmazeuten und Mediziner; Wissenschaftliche Verlagsgesellschaft mbH. Suttgart 2002. Adam G., Läuger P. und Stark G.: Physikalische Chemie und Biophysik; Springer Verlag Berlin 1988 Beier W.: Biophysik; VEB Georg Thieme Leipzig 1975 Maróti P., Laczkó G.: Bevezetés a biofizikába, JATEPress, Szeged 1998 (Ungarisch) P. Maróti, L. Berkes, F. Tölgyesi: Biophysics Problems. A Textbook with Answers. Akadémiai Kiadó, Budapest 1998 (Englisch). P. Maróti: Lasers in Biophysics, Szeged 2012 (Englisch) Sedimentation; Analytische Ultrazentrifugation Sedimentation: Verschiebung von Teilchen (Molekülen) aufgrund von Kräften, die der Teilchen(Molekülen)masse proportional sind. Anwendungen der Sedimentationserscheinungen in Zellbiologie und molekularen Biologie Auftrennung (Separation) gemischter Teilchenpopulationen Charakterisierung von reinen Teilchenpräparationen nach - Größe - Form und - Dichte der Teilchen Große Kräfte zur Auftrennung können mit Hochgeschwindigkeits- bzw. Ultrazentrifugen erreicht werden. Die Ultrazentrifugen rotieren sehr schnell - bis zu 500.000-mal in der Minute und die Beschleunigungen, die die Teilchen erfahren, können bis zu 106 g (Million-mal der Schwerebeschleunigung) erzeugt werden. Verschiedene Rotortypen Die Lage der Partikelbande während Rotation Die Reorientierung der Banden mit den Gradienten nach Stillstand der Rotoren Festwinkelrotor Vertikalrotor Schwenkbecherrotor Auftrennung der verschiedenen Teilchen in Banden Hydrodynamische Parameter der Molekülen Größe, Form, Molmasse und Bewegung Teilchen Dichte des Teilchens kann man bestimmen. Schicht von Lösungsmittel (Wasser) gebunden durch Hydrodynamik Stromlinien des Mediums 1. Das spezifische Volumen: Kehrwert der Dichte des anhydrischen Makromoleküls P, V’P = Volumen/Masse, [VP] = mL/g. Eiweiße: V’P ~ 0,7 – 0,75 mL/g Na+ DNA: V’DNA ~ 0,5 – 0,53 mL/g 2. Das partielle spezifische Volumen: Änderung in Volumen per Masse V V V P M P M P V 'P nP T , p,n mP T , p,m Eiweiße: VP ~ 0,7 – 0,75 mL/g Wir werden V’P ≈ VP annehmen. Na+ DNA: VDNA ~ 0,5 – 0,53 mL/g Für eine binäre Mischung aus makromolekularer Komponente (1 = P) und dem Lösungsmittel Wasser (2 = L) V V P mP V L mL Hier sind mP und mL die in der Lösung des Volumen V enthaltenen Massen der Komponenten P bzw. L, die natürlich additiv die Gesamtmasse mt = mP + mL ergeben. Durch Division des Gesamtvolumens V mit der Gesamtmasse mt, erhalten wir V 1 V V P P V L L mt Gibbs-Duham Formel wobei V das partielle spezifische Volumen der Lösung und χP bzw. χL die Massenbrüche der Komponenten P bzw. L darstellen. 3. Effektive (wirksame) Masse: die redizierte Masse des Teilchens unter Berücksichtigung des Auftriebs (aufgrund der Verdrängung des Volumens an Suspension der Dichte ρ) mP mP V P mP 1 V P P ρ Volumen Masse des verdrängten Wassers 4. Hydration: Das Makromolekül umgibt sich mit einer Hydrathülle und wird als hydrotisiertes (oder aquatisiertes) Partikel bezeichnet. P H2O mH 2O mP mP,h mP mH2O mP 1 V P,h V P V H2O Die Masse des hydratisierten Teilchens Das Volumen des hydratisierten Eiweißes per Gramm Eiweiß = das partielle spezifische Volumen Die Hydrathülle um das Partikel modifiziert (erhöht) die Werte der Masse und des spezifischen Volumens des Teilchens beobachtet durch hydrodynamische Methode. Hydrodynamische Eigenschaften einiger Eiweiße MP VP δH2O (kDa) (mL/Gramm) (Gramm H2O/Gramm Protein) Ribonuclease 13,683 0,728 0,59 1,14 β-Lactogobulin 35 0,751 0,61 1,25 Serumalbumin 65 0,731 0,75 1,31 Hämoglobin 68 0,749 0,69 1,14 Katalase 250 0,73 Tropomyosin 93 0,74 20 3,22 Fibrinogen 330 0,74 10,1 2,34 Kollagen 345 0,695 460 6,8 Myosin 493 0,728 86 3,53 Protein RS: Stokes-sches Radius (gemesst) Rmin: Stokes-sches Radius ohne Hydrathülle (berechnet aus MP und VP) Rs/Rmin 1,25 Die Abweichung kommt aus Hydratation nicht Kugelform Beide 1. Sedimentation im Schwerefeld der Erde Die Reibungskraft kompensiert gerade die wirksame Schwerkraft (Gewicht Minus Auftriebskraft) beim Absinken des Teilchens mit konstanter Geschwindigkeit: VP P g VP g 6 Rs v Reibungskraft: 6 Rs v Auftriebskraft: VP g v Schwerkraft: mP g VP P g gleichmäßige Endgeschwindigkeit Rs unter Verwendung der Stokesschen Reibungsformel für makroskopisches kugelförmiges Teilchen des Radius Rs und Volumen 4 Rs3 VP 3 Die Sedimentationsgeschwindigkeit des Teilchens im Erdschwerefeld beträgt: 2 g P Rs2 v 9 mP: Masse, VP: Volumen und ρP: Dichte des Teilchens ρ: Dichte und η: Viskosität des Suspensionsmediums g: Schwerebeschleunigung der Erde Sedimentationsgeschwindigkeiten von Zellen in Erdschwerefeld 2 g P Rs2 v 9 Unter physiologischen Bedingungen haben Säugetierzellen Die Geschwindigkeit v kann um einen Faktor Radien: 2,5 μm < Rs < 12 μm Dichten: 1,05 g/cm3 < ρP < 1,10 g/cm3 20 variiren. 2 (ρ = 1,0 g/cm3) Unterschiede der Zellsedimentation im Schwerefeld beruhen im wesentlichen auf Größenunterschieden der Zellen. Beispiel: Für 3T3-Mausfibroblasten (Rs = 10 μm und ρP = 1,05 g/cm3) bei Sedimentation im Medium der Dichte ρ = 1,00 g/cm3 und der Viskosität η = 1·10-3 kg·m-1·s-1 ergibt sich Sedimentationsgeschwindigkeit v ≈ 1 mm/min = 6 cm/Std. Das ist eine experimentell durchaus brauchbare Sedimentationsgeschwindigkeit. Anwendung: präparative Auftrennung von Lymphocytenpopulationen. Größere Teilchen sedimentieren sehr viel schneller: Sephadex-Kügelchen (Rs ≈ 100 μm) für Säulenchromatographie in Sekunden bis Minuten. Kleinere Teilchen wie Proteine (Rs ≈ 5 nm) zeigen dagegen im Erdschwerefeld praktisch keine Sedimentation. 2. Sedimentationsgleichgewicht im Zentrifugalfeld Die Grundlage: optische Beobachtung der Verteilung der Teilchen (Makromoleküle) in dem Zentrifugalfeld hochtouriger Ultrazentrifugen, das Beschleunigungen (r·ω2) mehrfachen der Gravitationsbeschleunigung (g) hervorbringt (r·ω2 >> g). 2.1 Das Suspensionsmedium bleibt homogen, d.h. nimmt an der Sedimentation nicht teil. Im Sedimentationsgleichgewicht sedimentiert durch die Zentrifugalwirkung ebensoviel des gelösten Stoffes wie entsprechend der Diffusion zurückwandert. Mit (freier) Energie ausgedrückt: die freie Energie des Stoffes der Konzentration c ist 1 G (r ) G 0 R T ln( c) M P (1 V P ) r 2 2 2 MP Molmasse des Partikels VP Partielles spezifisches Volumen des Partikels (Kehrwert der Dichte) Entropische Energie: Diffusion Potentielle Energie im Zentrifugalfeld sollte die gleiche Größe überall haben, d.h. ist unabhängig von r : dG dr 0 1 dc 2 r M P (1 V P ) c dr RT Hieraus ergibt sich (1) a r Diese Gleichung kann zwischen zwei Positionen a und r in der Zentrifugenzelle integriert werden: c(r ) 2 M P (1 V P ) 2 2 ln c(a) ln c(r) ln c(a) Steigung ~ MP r2 – a2 2 RT (r a ) Durch Messung der Konzentration entlang der Zentrifugenzelle sowie der Dichte des Lösungsmittels ρ, des partiellen spezifischen Volumens des Teilchens und der Kreisfrequenz der Zentrifuge ω ergibt sich also die Molmasse MP des Partikels. Bei diesem Verfahren spielt der Diffusionskoeffizient (Reibungskonstante) keine Rolle weil es sich um Gleichgewicht (und um keine Dynamik (Bewegung)) handelt. Bei sehr hoher Winkelgeschwindigkeit ω des Rotors kann der Gleichgewichtszustand durch den partikelfreien Überstand und das Partikelsediment am distalen Teil (am Boden) der Zentrifugalzelle gegeben sein. Man kann jedoch eine niedrigere Winkelgeschwindigkeit wählen, bei der sich eine räumlich kontinuierliche Konzentrationsverteilung der makromolekularen Komponente einstellt. Sedimentationsgleichgewicht mit analytischer Ultracentrifuge Messung c(r) gegen r mit optischem Method. Man braucht klares Material. Beispiel: Alkyl hydroxyperoxide reductase (AhpF/AhpC complex) aus S. typhimurium Hintergrund: Rekombinant Heterodimer wurde hergestellt zur Untersuchung der Eigenschaften des Elektrontransfers. Das Heterodimer besteht aus zwei Einheiten: AhpF (Molmasse 34 kDa) und AhpC (Molmasse 55 kDa), die man aus E. coli genetisch produzieren kann (co-Expression). Frage: wie groß ist die Molmasse des isolierten Komplex mit enzymatischer Aktivität? Versuchsgerät: Beckman Optima analytische Ultracentrufuge. Die optische Absorption bei 280 nm kann man im Zentrifugenrörchen direkt messen. Bedingungen: verschiedene Protein Konzentrationen zwischen 3 und 34 μM Zellvolumen: 115 μL Partielle spezifisches Volumen: VP = 0.743 mL/g (berechnet) Dichte der Lösungsmittel: ρ = 1,0058 g/mL (gemeßt) Temperatur: 20 oC Drehzahle des Rotors: 8.000, 9.500 und 14.000 rpm Sammeln der Data (Messung): 8, 10 und 12 Std bei jeder Drehzahl Biochemistry (2001) 40, 3912-3919 Sedimentationsgleichgewicht von Alkyl Hydroxyperoxide Reductase (AhpF/AhpC complex) Heterodimer Optische Dichte (Absorption) bei 280 nm 2 1 dc r M P (1 V P ) Nach Gl. (1) c dr RT Die linke Seite kann man umformen 1 dc d ln c d (ln c) 2r 2 c dr dr d (r ) Nach Einsetzung 8.000 rpm 9.500 rpm MP d (ln c) 2 RT d (r ) 2 (1 V P ) 2 Steigung der Kurve 14.000 rpm Klare Abweichung vom Gerade, weil VP nicht Konstante ist. Result: MP = 86,200 ± 200 Schlußfolgerung: das Enzym besteht aus einer-einer Kopie beider Einheiten von AhpF (Molmasse 34 kDa) und AhpC (Molmasse 55 kDa). Sedimentationsgleichgewicht im Zentrifugalfeld 2.2 Zentrifugation im Dichtegradienten Bei diesem Verfahren verwenden wir präformierten Gradienten des Suspensionsmediums, deren Dichten ρ(r) die Partikeldichte (genauer: ihr reziprokes partielles spezifisches Volumen) einschließen. Die zentrifugierten Teilchen werden bei einer bestimmten Position r0 im Gradienten zur Ruhe kommen. Man nennt diese Dichte ρ(r0) die Schwebedichte oder auch (weniger treffend) die Schwimmdichte (engl. buoyant density) der makromolekularen Partikel. Die Form des Dichtegradienten soll in der Nähe der Gleichgewichtsposition (oder sogar im ganzen Bereich) als lineare Funktion in r beschrieben werden: wobei α =(dρ/dr) die (konstante) 1 (r ) r r0 Steigung des Gradienten angibt. VP Setzen wir diese spezielle Ortsabhängigkeit der Dichte des Mediums in Gl. (1) ein: 1 2 r M P 1 V P (r r0 ) 1 dc V P c dr RT Nach Vereinfachung 1 dc 2 r MP VP (r r0 ) c dr RT nach Trennung der unabhängigen (r) und abhängigen (c) Veränderlichen zu beiden Seiten der Gleichung 2 r0 M P V P d ln c d (r r0 ) 2 2 RT und nach Integration c (r ) c (r0 ) e ( r r0 )2 2 2 wobei 2 RT 2 r0 V P M P Es ergibt sich eine Gauß-Verteilung der makromolekularen Konzentration mit bestimmter Bandbreite σ in der Nähe von r0. Die Bande ist um so schärfer, je höher die Molmasse MP der Makromoleküle und die Zentrifugalbeschleunigung ω2r sind. Weiterhin wird die Schärfe der Bande von der Steilheit α des Dichtegradienten bestimmt. Vergleich der Einstellzeiten: Das Sedimentationsgleichgewicht ist viel schneller (in wenigen Stunden) erreicht als das Gradientengleichgewichtes (in Tagen). Daher werden praktisch brauchbare Trennungen auch schon bei nicht vollständig ins Gleichgewicht gekommenen Gradienten erzielt. 3. Sedimentationsgeschwindigkeit im Zentrifugalfeld Die Zentrifugenzelle wird mit einer homogenen Suspension gleich großer Partikel gefüllt. Nach Einschalten der Zentrifuge wird die Teilchensuspension mit konstanter Winkelgeschwindigkeit ω auf einer Kreisbahn bewegt und eine stationäre Sedimentationsgeschwindigkeit v wird sehr schnell erreicht charakterisiert durch das Kraftgleichgewicht: ω ... MP r M P 1V P r 2 f v wirksame Masse des Teilchens Zentrifugalbeschleunigung Zentrifugalkraft Reibungswiderstand Nach Umordnung faßt man die experimentell unmittelbar zugängliche Größe Sedimentationskoeffizient S= Sedimentationsgeschwindigkeit Zentrifugalbeschleunigung M P 1V P S f Die Sedimentationskoeffizient hängt von drei, experimetell und theoretisch zugänglichen Größen ab: Molmasse des Teilchens Kehrwert der Dichte des Teilchens Einheit: s (Sekunde) Da in praktischen Anwendungen meist sehr kleine S-Werte (von den Größenordnung 10-13 s) auftreten, benutzt man die praktische Einheit 1 Svedberg = 10-13 s. M P 1V P S f Man kann messen oder berechnen (z.B. aus der Reihenfolge der Aminosäuren). Bei Proteinen VP ≈ 0,75 mL/g Reibungskoeffizient: Form (Gestalt) des Teilchens Man kann aus unabhängigen Messungen (Gel Filtration, Diffusion usw.) bekommen. Bei kugelförmigem Teilchen f = 6 π η Rs (Stokes’sches Gesetz) Für Proteine findet man Sedimentationskoeffizienten zwischen 1 und 100 S. Für Zellorganellen ergeben sich (ihrer Größe entsprechend) wesentlich höhere Werte: Glycogen ≤ 105 S, Mitochondrien (1...7)·104 S, Kerne (1...10)·106 S, ganze Zellen (1...10)·107 S Messung von S mit analytischer Ultracentrifuge: Wanderung der Grenze Die Suspension soll anfänglich homogen sein. Im Verlaufe des Sedimentationsvorganges bildet sich vom Meniskus der Füllung der Zentrifugenzelle ausgehend ein Bereich teilchenfreier Lösung heraus. Die Grenze zwischen diesem Bereich und der restlichen Teilchensuspension in Abstand r kann (z.B. schlierenoptisch) sichtbar gemacht werden. Die zentrifugale Wanderung dieser Grenze kann während der Zentrifugation kontinuierlich zeitlich verfolgt werden. Nach der Definition von S: S und Integration beider Seiten: dr dt , Separation der Veränderlichen: r2 r ln S 2 t t0 r0 r0 t r t0 t Wanderung der Grenze Rotationsachse dr r wobei r und r0 die Positionen der Grenze zu den Zentrifugationszeiten t bzw. t0 sind. Die graphische Auftragung der experimentellen Daten ln (r) gegen ω2t sollte eine Gerade ergeben, und deren Steigung läßt sich der ln r Sedimentationskoeffizienten S ln r0 unmittelbar t0 entnehmen. S 2 dt Präparation von zellulären Partikelfraktionen: Waschen (Reinigung) der groben Sedimente Nach Homogenisierung eines Gewebes durch Zerreiben oder Zerschlagen und Aufschwemmung in einer physiologischen Pufferlösung unterwirft man das Homogenat sukzessiven Zentrifugationsschritten mit zunehmender Zentrifugalbeschleunigung. Bei jedem Schritt trennt man sorgfältig (durch Absaugen oder Dekantieren) den Überstand vom Sediment. Abschätzung der notwendigen Zeiten zur Sedimentation bestimmter Partikel aus einem dr Zellhomogenat. f dr M P 1V P dt dt S 2 M P 1V P 2 r f r Die maximale Sedimentationszeit tmax benötigen diejenigen Teilchen, die vom oberen Meniskus bei r = ra bis zum Boden bei r = re des Zentrifugenröhrchens wandern müssen tmax f re M P 1V P 2 ra re dr f ln r M P 1 V P 2 ra Mit dieser Gleichung kann man beispielweise die Sedimentationszeit kugelförmiger Teilchen des Radius Rs berechnen; für diese ist VP = 4πRs3/3 und f = 6πηRs: tmax re 9 ln 2 2 2 P Rs ra Beispiel: tmax re 9 ln 2 P Rs2 2 ra Diese Gleichung ist recht brauchbar, weil eine Kugelgestalt in sehr vielen Fällen wenigstens näherungsweise vorausgesetzt werden kann. Ribosomen (Rs ≈ 8 nm, ρP = 1,6 g/cm3) benötigen in einem Sedimentationsmedium der Dichte ρ = 1 g/cm3 und der Viskosität η = 0,001 kg·m-1·s-1 für die Sedimentation von ra = 5 cm bis re = 10 cm bei ω/2π = 30.000 min-1 eine Zeit tmax = 8.230 s ≈ 2,3 Std. Durch Vergleich solcher Rechnungen für Fraktionen von Partikeln verschiedener Größe und Anteile dieser Fraktionen in verschiedenen Bereichen des Sedimentationsraumes kann man auch das Ausmaß möglicher gegenseitiger Kontaminationen der Fraktionen bei verschiedenen gWerten und Zeiten abschätzen. Zirückgelegter Abstand (rel. Einheit) Beispiel: Messung des S-Wertes von GlpF, Glycerol Transport Facilitator protein aus E. coli mit Protein Standard S= Nativ Tetramer MP (1-VP) f Empirische Korrelation der S Werte von verschiedenen wasserlöslichen Protein Standard aufgrund der Sedimentationsgeschwindigkeiten in 5-20% Sucrose Dichtegradient. Zur Beachtung: weder noch f sind Konstante. Die verschiedene Proteine haben verschiedene hydrodynamische Parameter. Sedimentationskoeffizient, S (Svedberg) PNAS (2001) 98, 2888-2893 Standard Method zum Erhalten Molmasse der Makromoleküle Sedimentationsdaten für Proteine und Viren bei 20oC unendliche Verdünnung S020,W Temperatur 20oC (Svedberg, 1/s) in Wasser (cm2·s-1) (cm3·g-1) VP (g·mol-1) MP Sedimentationskoeffizient in S Sedimentationskoeffizient von DNA und BSA (Bovin Serum Albumin) DNA BSA Konzentration (g/100 cc) Die S-Werte von DNA hängen sehr stark von der Konzentration der Lösung ab. Deswegen das Method ist nicht äußerst geeignet zur Untersuchung von DNA. „Zwei dimensionale” Auftrennung Dichtegradient Sedimentationsgleichgewicht Einige Partikel kann man bloß aufgrund der Differenzen der S-Werte nicht separieren. Sediment Differentiale Sedimentation Kombination S M P 1V P D RT von Sedimentation M P 1V P S f Vorteil: die Reibungskoeffizient fällt aus! Zwei Beispiele für Anwendung der Kombination von Sedimentation und Stokes Radius: Experimentelle Bestimmung von MP. und Diffusion RT D f f 6 Rs Theoretically: der Stokes-Radius (Rs) kann man aus TranslationDiffusion Messungen bekommen. In Wirklichkeit aber Gel Filtration oder molekulare Kromatographie sind benutzt. Beispiel 1. Dissoziation von Hämoglobin bei niedrigen pH Experiment: bei Übergang vom hohen zu niedrigen pH Wert nimmt die Molmasse MP ab. Erklärung: die TETRAMER Form von Hämoglobin dissoziert zu MONOMER (oder Mischung von DIMER) Formen. pH nimmt ab D (107 cm2s-1) D Abnehmende pH macht S/D S/D S (Svedberg) - den Sedimentationskoeffizient (S) kleiner und - den Diffusionskoeffizient (D) größer bzw. den Stokes Radius (Rs) kleiner. D ist umgekehrt proportional mit Rs und S ist linear proportional mit MP/Rs. Das Verhältnis S/D ist linear proportional mit MP wenn VP eine Konstante ist. 4x S RT D 6 Rs S M P 1V P 6 Rs S M P 1V P D RT Beispiel 2. Ausdehnung von BSA bei säurigen pH MP bleibt unverändert während Säuern (Acidifikation) und nur der Stokes Radius ändert sich (nimmt zu). Stokes Radius nimmt zu S/D S/D M P 1V P S 6 Rs S (Svedberg) RT D 6 Rs Die Änderungen sind sehr ähnlich: beide Proteinen bewegen sich (sedimentieren) viel langsamer bei niedrigem pH Wert aber die Ursachen sind völlig verschieden: Hämoglobin fällt zu Teilen, BSA dehnt sich aus. D S D (107 cm2s-1) S M P 1V P D RT pH nimmt ab Gel Chromatographie Polymer Partikel des Gels Kleinere Moleküle treten den wässrigen Innenraum des Partikels ein. Andere (trennende) Moleküle Größere Moleküle können können nicht eindringen, sie bleiben außen. Gel Chromatographie Die Moleküle gelöster Stoffe werden aufgrund ihrer Größe (ihres hydrodynamischen Volumens) getrennt. Der Trennungseffekt beruht auf unterschiedlichen Diffusionsvolumina für unterschiedlich große Moleküle. Die porösen Polymere der stationären Phase erlauben kleineren Molekülen einzudringen, wodurch sich das ihnen zur Verfügung stehende Diffusionsvolumen vergrößert und sich somit die Retentionszeit verlängert. Kleine Moleküle werden demnach stärker zurückgehalten als große, denen nur Zwischenräume zwischen dem Polymergranulat zugänglich sind und die daher schneller durch die Säule fließen. Daher sind große Moleküle in den früheren Fraktionen des Eluats, während kleinere Moleküle später eluieren. Gleichgewicht von zwei Effekten (Kräften): - Lösungsmittelfluß und - Partition in die stationären Phase des Gelpartikels oder Partikel in der stationären Phase des Matrix Lösungsmittelfluß Wir müssen die Elutionsvolumen messen; Ve, oder Vo Ve Vi Das erhaltene Elutionsvolumen liegt zwischen zwei Grenzen Vo = Elutionsvolumen der völlig ausgedrängten Moleküle Vi = Elutionsvolumen der völlig aufgenommenen Moleküle Elutionsvolumen = Ve - Vo Vi - Vo Geschwindigkeit des Partikels Geschwindigkeit des Lösungsmittels σ ist das Maß wie der Innenraum des Gelpartikels für das untersuchten Molekül zugänglich ist 0.9 Kleines Molekül 0.1 Großes Molekül Zugängliches Volumen im Matrix hängt von der Größe und Gestalt des Moleküls ab Ve - Vo = Vi - Vo Volumen des Innenraumes des Gelpartikels Das Elutionsvolumen bzw. σ bestimmt den Stokes Radius des Makromoleküls. Bei Eichung der Gel Chromatographie, die Standarde werden lieber nach Molmassen als nach Stokes Radii ausgewählt. Die Gestalt und das spezifische Volumen des geprüften Moleküls soll mit der Form und dem spezifischen Volumen der Standarde übereinstimmen. Beispiel: Elution kugelförmiger Proteine mit Sephadex G-200 In Experimenten, die Retardation des Makromoleküls in Gel Filtration Chromatographie zeigt ausgezeichnete Korrelation mit dem Stokes Radius bestimmt mit Hilfe der Diffusion. Wenn die Standarde und die unbekannte Makromoleküle die selbe Gestalt haben, dann – und nur dann – die Gel Filtration Chromatographie gibt gute Schätzung der Molmasse. Allerleie Abweichungen von der Kugelform resultieren größeren Stokes Radius, d.h. wir bekommen den Maximum Wert des Stokes Radius mit diesem Method. Sucrose Vi 1 3.0 völlig aufgenommen cyt c 2.5 BSA 2 globulare (kugelförmige) Proteine Katalase Dextran blau 0 Vo 1.5 1.0 104 105 log (Molmasse) 106 Ve Vo völlig ausgeschlossen Beispiel: Activer Transport mit Hilfe von außen Membran Proteinen und TonB in E. coli Erforderlich zum Ferric Ion Transport durch Ferrichrome Komplex FhuA Transport Protein Das aktive Transportsystem ist zum TonB gekoppelt. Das TonB Protein ohne das N-Terminal Membrane Anchor wird ausgedrückt und karakterisiert: ein His-tag am N-Terminus begünstigt die Isolation and Reinigung von H6-’TonB in einem einziegen Schritt. Das erhaltene Protein ist wasserlöslich und die berechnete Molmasse beträgt MP ≈ 24.880 Science (1998)282,2202- TonB Gel (Size Exclusion) Chromatographie von H6-TonB mit Superose 12 Säule Totales Volumen: Vi = 21 ml gemesst durch Elution von NaNO3 Experimentelle Resultate Verdrängtes (Void) Volumen: V0 = 7,3 ml gemesst durch Elution von Dextran blau 2000 Kalibration (Eichung) gegen Rs Rs = 4,1 nm Thyroglobulin Rs = 8.6 nm; Ve = 8.8 ml Ferritin Rs = 6.3 nm; Ve = 10.7 ml Katalase Rs = 5.2 nm; Ve = 11.7 ml Aldolase Rs = 4.6 nm; Ve = 12.0 ml Bovine Serum Albumin Rs = 3.5 nm; Ve = 12.5 ml Ovalbumin Rs = 2.8 nm; Ve = 13.4 ml Chymotrypsinogen Rs = 2.1 nm; Ve = 14.9 ml RNase Rs = 1.75 nm; Ve = 15.5 ml Journal of Bacteriology, May 2001, p. 2755-2764, Vol. 183, No. 9 H6-TonB Sedimentationsgeschwindigkeit Sedimentationsgleichgewicht Gel Chromatographie Messung: S20,w = 1.4 S Berechnung von MP = 1.007 g/ml = 1.04 Poise V = 0.7376 ml/g (aus Sequence) Rs = 4.1 nm (aus Gel Filtration) Rs = MP(1 - V)/6NS20,w MP = 28.000 MP = 30.000 0.8 mg/ml Protein 18.000 rpm in der Nacht bei 20oC Steigung = MP(1-V) = 1.007 g/ml V = 0.7376 ml/g Rs = 4,1 nm Berechnung Rmin = (3MPV/4N)1/3 = 1,9 nm (Kugel ohne Hidration mit MP = 24.900 (Sequence) Das Molekül ist äußerst asymmetrisch Schlußfolgerung: H6-TonB bildet Monomer in Lösung Rs/Rmin = 2.1 Gestalt des Proteins TonB mit der Annahme von 0,3 Gramm H2O/Gramm Protein Hydration Rmin = 2.0 nm Rs/Rmin = 2 Das entspricht zu einem Drehellipsoid mit Axialverhältnis von 15:1 240 Å x 16 Å TonB wandert aus der inneren (zytoplasmischen) Membran (CM) zu der äußeren Membran (OM) im periplasmischen Bereich (PP) des Bakteriums. Elektrophorese Elektrophorese Wanderungsrichtungen der Ionen Gleichspannung, U d Elektrophorese bezeichnet die Wanderung großer elektrisch geladener Teilchen (Proteine, ganze Zellen) durch einen als Trägermaterial dienenden Stoff unter dem Einfluß eines elektrischen Feldes. Negativ geladene Moleküle (Anionen) wandern zur positiv geladenen Anode und positiv geladene Moleküle (Kationen) wandern zur negativ geladenen Kathode. Die Wanderungsgeschwindigkeiten verschiedener Ionen hängen von deren Ladung, Form und effektiver Größe sowie von der Lösungsumgebung und von der Stärke des elektrischen Feldes ab. 1) Die einfachste (naivste) Beschreibung: Wenn die auf die Teilchen wirkende Kraft q·E (q = e⋅z, wobei z ist die Anzahl der Ladungen an einem Molekül, E = U/d ist die Feldstärke) gleich der Reibungskraft f·v ist, beobachtet man eine konstante Wanderungs-geschwindigkeit v = q·E/f. Die Wanderungsgeschwindigkeit ist somit proportional der angelegten Spannung. Als charakteristische Grösse für die Mobilität des Moleküls führt man die elektrophoretische Beweglichkeit ein: μ= Wanderungsgeschwindigkeit Elektrische Feldstärke = q f Der Reibungskoeffizient f hängt sowohl von der Masse und der Form des wandernden Moleküls als auch von der Viskosität des umgebenden Mediums ab. Beispiel: Das Protein Albumin hat eine elektrophoretische Beweglichkeit von μ = 4·10-9 m2 V-1 s-1 bei pH = 4. Mit einer Spannung U = 2000 V und einer Laufstrecke von d = 20 cm ergibt sich hieraus eine Wanderungsgeschwindigkeit von v = 4·10-5 m s-1 = 14,4 cm h-1 auf dem Gel. 2) Eine bessere Beschreibung. Die exakte Berechnung von elektrophoretischen Beweglichkeiten ist komplizierter, da - der effektive Wert der elektrischen Ladung eines wandernden Moleküls (q) von seinem hydrodynamischen Verhalten und seinen Solvatationsbedingungen abhängt, - die genaue Form des Moleküls unbekannt ist und - das Teilchen und die (entgegengesetzt geladene) Ionenwolke in entgegengesetzten Richtungen und mit verschiedenen Geschindigkeiten (v und v’) wandern. Die Ionenwolke wird an der Vorderseite des Teilchens ständig wieder neu gebildet. Auf dieser Weise kommt es zu einer zusätzlichen hydrodynamischen Bremsung des Teilchens duch die umgebende Ionenwolke dessen Radius ist durch die Debye-Länge (λD) gegeben. v E D E Beweglichkeit η: Viskosität des Mediums, σE: „elektrophoretisch wirksame” Ladungsdichte auf der Teilchenoberfläche. Elektrophoretische Beweglichkeit Wenn der kleinste Krümmungsradius des Teilchens größer ist als die Dicke λD der Ionenwolke (diffuse Doppelschicht), dann E D Die elektrophoretische Beweglichkeit ist i) proportional zu „elektrophoretisch wirksame” Ladungsdichte auf der Teilchenoberfläche σE, ii) umgekehrt proportional zur Viskosität η des Mediums und iii) wächst linear mit der Debye-Länge λD an. Ad i) Im allgemeinen ist σE verschieden von der eigentlichen Ladungsdichte σ des Teilchens. Dies hängt u.a. damit zusammen, daß wegen Oberflächenrauhigkeiten ein Teil der Gegenionen bei der Wanderung des teilchens mitgeschleppt wird, wodurch der Absolutbetrag der wirksamen Ladungsdichte verkleinert wird. Ad iii) Das erklärt sich daraus, daß bei kleinem λD, d.h. bei eng dem Teilchen anliegender Ionenwolke die hydrodynamische Bremsung (die „extra Kraft”) groß wird. Die Beweglichkeit kann man auch mit dem Zeta-Potential ausdrücken: 0 r Physikochemischer Hintergrund: Ionen in Coulombscher Wechselwirkung Die elektrisch geladene Lösungsmittelmoleküle und Ionen der Elektrolyt stehen in Wechselwirkung miteinander kontrolliert duch das Coulombsche Gesetz der Elektrostatik. Jedes Ion befindet sich im Zentrum einer Wolke aus entgegengesetzt geladenen Ionen (durch Kreise angedeutet). Nachfolgen: 1) Abschirmung der elektrostatische Wirkung der Ionen (Elektrode). Die Ionenwolken (und die Lösungsmittelmoleküle) als Dielektrikum schwächen die Coulombschen Wechselwirkungen ab und schirmen die Ladung des Ions (Elektrode) ab. Die karakteristische Länge der Abschirmung (DebyeℓD Länge λD) wird als Radius der Ionenwolke betrachtet. 2) Räumliche Verteilung der Ionen. Obwohl die Ionen in der Lösung sich gleichmäßig verteilen (siehe die Abbildung), die Verteilung wird nicht mehr gleichmäßig in der direkten Umgebung des ausgewählten Ions (Elektrode) bleiben, worauf die thermische Bewegung zu einer stärkeren Verteilung der Ionen führt. Grundfrage: wie verteilen sich die Ionen um eine Elektrode oder um ein ausgewähltes (Zentral)ion? Ionenverteilung um eine Elektrode in Elektrolytlösung Ionenverteilung um ein zentrales Partikel in Lösung Positiv geladenes Gegenion Negativ geladenes Co-Ion Schubebene Negativ geladenes Zentralion Stern Doppelschicht mit fest gehaltenen Gegenionen Diffuse Schicht mit frei beweglichen Ionen Ions im Gleichgewicht mit der Lösung Debye-Länge Gouy-Chapman-Modell • • • • Grundfrage: Wie verteilen sich die Ionen um eine geladene Platte (Elektrode)? Grundidee: zwei gegenläufig Prozesse Das elektrostatische Feld der Elektrode (oder zentrales Ions) zieht entgegengesetzt geladene Ionen an Die Molekularbewegung zerstört immer wieder jede Ordnung Das elektrische Potential φ(x) hängt von der Ladungsdichte ρ(x) selbst ab: 2 d x dx 2 x r 0 Poisson-sche Gleichung abgeleitet aus dem Gaussschen Gesetz der Elektrostatik Potential, φ [mV] Trotz aller Kompliziertheit: näherungsweise ist die Lösung der Gleichungen rein exponentiell: x x 0 exp D mit der Debye-Länge: I: 2 N A e2 I D r 0 kT Abstand, x [nm] λD NA: Avogadro Konstante e: elementare Ladung ε: Dielektrizitätskonstante kT: Boltzmann Faktor I: Ionenstärke der Lösung: 1 I zi2 ci 2 i zi : Ladungszahlen der Ionensorten ci : Konzentrationen der Ionensorten in der Lösung Gouy-Chapman-Modell Zusammenhang zwischen Flächenladungsdichte σ und Grenzflächenpotential φ0 Analogie zwischen einem Plattenkondensator und einer elektrischen Doppelschicht Die für einen Plattenkondensator gültige Beziehung zwischen Feldstärke E und Ladungsdichte σ 0 r E Kann auf die Doppelschicht übertragen werden, sofern E = -dφ/dx die Feldstärke unmittelbar an der Wand (x = 0) eingesetzt wird: d dx x0 0 r Der exponentielle Verlauf des Potentials ist schon bekannt: x D und die gesuchte Beziehung lautet: x 0 exp D 0 0 r oder E D 0 r Zeta-Potential Trägermaterials Die verschiedene Trägermaterials meist gequollene Gele aus Agarose oder Polyacrylamid führen zu unterschiedlichen Ionen-beweglichkeiten. Die Polymermoleküle des Gels bilden ein mehr oder weniger engmaschiges, dreidimensionales Netzwerk. Gele aus Polyacrylamid werden durch PolyAgarose-Gele sind relativ merisation von Acrylamid hergestellt. Sie weisen groß-porig (150 nm bei 1% wesentlich kleinere Poren auf (3–6 nm). Die und 500 nm bei 0,16 % Porengröße hängt von der AcrylamidGelen). konzentration und dem Vernetzungsgrad ab. Schema der Herstellung des Polyacrylamid Gels aus ungeordneter (random) Struktur. Übergang aus verdünnter Polymer Lösung (A) durch konzentrierte Lösung (B) zu Gel (C). --o– Punkt für Kreuzverbindung Unbekanntes Protein Molmasse Standarde Proteinlösung Schematische Darstellung einer Protein-Aufreinigung analysiert mit Hilfe der SDS-Polyacrylamid-Gelelektrophorese (SDS-PAGE) Richtung der Wanderung --●-- Punkt für Anschluß Anwendungen: 1. Blutbild, Elektrophorese von Blut Serumproteinen, diagnostische Aussagemöglichkeiten Die Untersuchung der Serumproteine ist bei chronisch-entzündlichen Erkrankungen, Verdacht auf monoklonale Gammopathie bzw. Plasmozytom und Verdacht auf Antikörpermangel (humoraler Immundefekt) wichtig. Anwendungen: 2. Ferguson Analyse Empirisch wurde für die (relative) Beweglichkeit folgender Zusammenhang gefunden: log log 0 K R cGel mit μ0, der elektrophoretischen Beweglichkeit ohne den zurückhaltenden Matrixeinfluss des Gels (cGel = 0), KR bezeichnet die Retention durch Reibung und cGel beschreibt die prozentige (%) Konzentration des Trägermaterials. μ0 hängt vom q (Ladung) und Stokes Radius (Gestalt) des Moleküls ab. KR hängt nur vom Stokes Radius, aber nicht vom q ab. In den Ferguson-Plots wird dieser Zusammenhang graphisch ersichtlich. 1 log μ kleine Makromoleküle mit hoher Ladung 2 kleine Makromoleküle mit geringer Ladung 3 cGel (%) grosse Makromoleküle mit hoher Ladung und grosser Steigung Anwendungen der Ferguson Analyse: die Östrogenrezeptoren Östrogenrezeptoren sind Steroidrezeptoren, die durch das Steroidhormon Östrogen aktiviert werden. log μ Steigung cGel (%) KR √KR ? KR Rs Mp Stokes Radius, Rs (nm) Markierung der Rezeptoren auf dem Gel durch Verbindungversuch mit radiomarkierten Östrogen Analogen. Gereinigtes Material ist nicht erforderlich. Die Molmasse MP aus Stokes Radius Rs kann man nur mit Annahme der kugelförmigen Gestalt berechnen. Anwendungen der Ferguson Analyse: SDS-Protein Komplexe Zum Trennmedium auf Plyacrylamidbasis kommt noch SDS (Natriumdodecylsulfat). Dieses anionische Tensid (Detergens) überdeckt die Eigenladungen von Proteinen. Pro Gramm Protein binden ungefähr 1,4 Gramm SDS, sodass die Proteine eine konstante negative Ladungsverteilung aufweisen. Die negativen Ladungen des SDS führen zu einer gegenseitigen Abstoßung, was zusammen mit der Denaturierung durch Aufkochen zu einer Linearisierung der Proteine führt. Dies erlaubt eine Auftrennung nach der Kettenlänge, proportional zur Molekülmasse, denn die längeren Proteine werden im Gel stärker zurückgehalten als kürzere Proteine. Das SDS umgibt das linearisierte Protein mit einer näherungsweise ellipsoiden Hülle. Die Eigenladungen der Proteine sind unter der SDS-Beladung vernachlässigbar. Vorteile: 1) Die verschiedene SDS-Protein Komplexe haben die gleiche Gestalt. Der selbe Zusammenhang ist gültig zwischen dem Stokes Radius Rs und der Molmasse MP bei jedem Protein: KR in Ausdruck von Ferguson hängt von der Molmasse ab. Schematische Darstellung einer Micelle aus Peptidkette und SDS-Molekülen. 2) Größere Proteine bilden längere Komplexe mit mehr Ladungen (q) und größere Retention durch log log 0 K R cGel Reibung (f). Die Ladungen und Größe der SDSProtein Komplexe ändern sich proportioniert. unabhängig abhängig Die Änderungen von q und f werden im Verhältnis von der μ0 = q/f ausgeglichen, deswegen μ0 hängt nicht von der Molmasse ab. Molmasse Der Fixwert von μ0 ermöglicht den Stokes Radius Rs mit Gebrauch von einem Gel und Standarden zu bestimmen. Es reicht nur ein einzieges Gel zu benutzen um Rs (mit Standarden) zu bekommen. Man kann Rs aus einem Gel NICHT erhalten. verschiedene μ0 Werte erhöhter Stokes Radius, Rs elektrophoretische Wanderung schnell der gleiche μ0 Wert langsam 0 1 5 % acrylamid 10 größere Steigung erhöhter Stokes Radius, Rs log μ 0 1 5 % acrylamid 10 Es ist nicht erforderlich die Gelkonzentration zu ändern. NATIVE PROTEINE SDS-PROTEIN KOMPLEXE Weil alle SDS-Protein Komplexe die gleiche Gestalt besitzen, aus dem Stokes Radius Rs kann man die Molmasse MP erhalten. Hausaufgaben 1) In einer Zentrifuge befinde sich eine Suspension einheitlich kleiner Teilchen. Bei einer Rotationsfrequenz von 1 000 Hz beträgt ihre Sedimentationsgeschwindigkeit 2 mm/min. Welchen Wert hat diese, bei Verdoppelung der Rotationsfrequenz? 2) In einer Zentrifuge rotiert eine kleine Masse im Abstand 9,8 cm um die Zentrifugenachse mit einer Winkelgeschwindigkeit 100 1/s. a) Wievielmal größer ist ungefähr die auf die Masse wirkende Radialbeschleunigung (Zentrifugalbeschleunigung) als die Fallbeschleunigung? b) Wie groß ist die Bahngeschwindigkeit der Masse? 3) Wie lange dauert es, bis ein E. -coli Bakterium mit der Dichte 1,10 g/mL und dem Radius 1 μm unter der Einwirkung des Gravitationsfeldes der Erde in Wasser (Dichte 1 g/mL und Viskosität 1·10-3 Ns/m2) 1 cm sedimentiert? Hausaufgaben 4) Bei der Sedimentation von Ribonuklease in einer Ultrazentrifuge wurde bei einer Drehfrequenz von 52.400 min-1 der Abstand r der Phasengrenze der sedimentierenden Moleküle in Abhängigkeit von der Zeit t gemessen: t (min) r (cm) 0 5,908 32 5,980 64 6,045 96 6,112 Berechnen Sie mit Hilfe dieser Meßwerte näherungsweise die Sedimentationskonstante S! 5) Die relative Molekülmasse M und die Dichte ρ von Pepsin und Urease betragen M (Da) ρ (g/mL) Bestimmen Sie daraus den Pepsin 37 000 1,33 Radius r der sphärischen Makromoleküle unter Urease 480 000 1,37 Vernachlässigung der Hydration. Hausaufgaben 6) In 0,25 M Sucroselösung werden Rattenleber-Mitochondrien suspendiert. Bei 0oC hat diese Sucroselösung eine Dichte von 1,035 g/mL und eine Viskosität von 0,0231 g·cm-1·s-1. Die Dichte der Mitochondrien in dieser Lösung bei 0oC ist 1,100 g/mL. Wie lange muß man mindestens bei 0oC und 8.000 min-1 Drehzahl zentrifugieren, damit die Mitochondrien vom oberen Meniskus (ra = 5 cm von der Rotationsachse) auf den Boden des Zentrifugenröhrchens (re = 10 cm von der Rotationsachse) absinken? Die Mitochondrien können näherungsweise als kugelförmige Teilchen mit dem Radius 1 μm angesehen werden, die das Stokessche Reibungsgesetz befolgen. Hausaufgaben 7) In einer KCl-Lösung sei in x-Richtung ein Konzentrationsgradient vorhanden. An der Stelle x betragen die KCl-Konzentration 0,1 M und der Konzentrationsgradient von KCl 1 M/cm. Wie groß mußte man am Ort x die elektrische Feldstärke machen, damit dort der Transport von K+ verschwindet? 8) Wie groß ist die Ionenstärke einer Lösung, die 0,1 M NaCl und 0,1 M CaCl2 enthält? 9a) Das Kulturmedium einer Zellkultur besitze einen pH-Wert von 7,0 und eine Ionenstärke von 0,1 M. Die Zelloberfläche ist negativ geladen mit der Ladungsdichte von einer Elementarladung pro 10 nm2. Man berechne den pH-Wert an der Zelloberfläche! b) Unter diesen Bedingungen wird die elektrophoretische Beweglichkeit der Zellen gemessen. Welchen Weg legt eine Zelle einer Feldstärke von 10 V/cm in 1 min zurück? Man setze hier das elektrophoretische ζ-(Zeta)Potential näherungsweise dem Grenzflächenpotential φ0 gleich. (Debye-Länge 1,0 nm, Dielektrizitätskonstante des Wassers 80, Dielektrizitätskonstante des Vakuums 8,85·10-12 Cb·V-1·m-1, Elementarladung 1,6·10-19 Cb, Viskosität des Mediums 1,0·10-3 kg ·m-1 ·s-1, Temperatur 298 K.)