Vorlesung 2 - Physik (Uni Würzburg)
Werbung

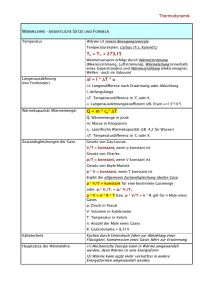
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 Vladimir Dyakonov #2 am 10.01.2007 Raum E143, Tel. 888-5875, eMail: [email protected] 10.2 Temperaturmessung Wärmeausdehnung fester und flüssiger Stoffe*: Ausdehnung von Festkörpern/Flüssigkeiten: Wärmeausdehnung fester und flüssiger Stoffe bei T = 20 oC Feste Stoffe α / 10-6 K-1 Flüssige Stoffe Aluminium 23.8 Wasser 2.07 · 10-4 Eisen 12 Benzin 0.95 · 10-3 Kupfer 16.8 Benzol 1.06 · 10-3 Natrium 71 Quecksilber 1.8 · 10-4 Hartgummi 75-100 Glyzerin 5· γ / K-1 10-4 Benzintank in der Sonne 1 10.2 Temperaturmessung Versuch: Wärmeausdehnung eines Festkörpers: 10.2 Temperaturmessung Versuch: Bimetallstreifen 2 10.2 Temperaturmessung Wärmeausdehnung fester und flüssiger Stoffe: • Bimetallstreifen*: Metalle mit verschiedenen Längenausdehnungskoeffizienten, die fest miteinander verbunden sind. Mit steigender Temperatur krümmt sich dieser Bimetallstreifen in Richtung des Metalls mit dem kleineren Ausdehnungskoeffizienten. Abkühlung αZN > αFe Zn Fe zum Relais Erwärmung • Thermostat: Biegung bei einer bestimmten Temperatur öffnet oder schließt einen elektrischen Stromkreis * „bi“ kommt vom Lateinischen „bis“ für doppelt 10.2 Temperaturmessung Versuch: Thermoelement 3 10.2 Temperaturmessung Thermoelement: Austrittsarbeit WA= (typ.: wenige eV) Energie, die Elektronen zum Verlassen eines Metalls benötigten (Materialspezifisch !) Oberfläche Metallionen + Elektronen - Je größer die kinetische Energie der Elektronen, desto mehr Elektronen können aus dem Metall austreten - Kinetische Energie steigt mit der Temperatur ! (Glühemission!) 10.2 Temperaturmessung Thermoelement: • An einer Kontaktstelle werden zwei Metalle mit unterschiedlicher Austrittsarbeit in Kontakt gebracht: Elektronen aus dem Metall mit der geringeren Austrittsarbeit gehen in das Metall mit der höheren Austrittsarbeit über. Dadurch gibt es im Metall mit der höheren Austrittsarbeit einen Elektronenüberschuss und damit einen Potentialunterschied zwischen den beiden Metallen • Bei der Berührung unterschiedlicher Metalle (mit unterschiedlichen Austrittsarbeiten WA der Elektronen) entsteht eine elektrische Spannungsdifferenz: „Kontaktspannung“ = temperaturabhängig ! UKontakt ~ T + + + Me I Me II + - UKontakt = E ·T E -Thermokraft WA1 < WA2 Typ. Paarungen z.B. Kupfer-Konstantan E = 0.06 mV/K 4 10.2 Temperaturmessung Gasthermometer (Eichthermometer): Beobachtung: (1) Bei konstanten Druck p steigt das Volumen V idealer Gase linear mit der Temperatur T (Gay-Lussac-Gesetz) V (T ) = V0 (1 + γ V T ) (2) Bei konstantem Gasvolumen V0 steigt der Gasdruck p linear mit der Temperatur T (Charles-Gesetz) p (T ) = p0 (1 + γ pT ) (3) Diese Beobachtung gilt für alle (verdünnten) Gase (weit oberhalb des Siedepunktes) (ideale Gase, z.B. He) γV = γ p = γ = 1 o −1 C 273.16 γ = Volumenausdehnungskoeffizient 10.2 Temperaturmessung Gasthermometer mit konstantem Volumen: - Gas in Glaskolben - V wird mittels Hg-U-Rohr konstant gehalten Skala gasgefüllter Kolben - Gasdruck p = ρ g ∆h (+Atmosphärendruck) • Die Temperatur wird beim Gasthermometer durch eine Druckmessung bestimmt: T ( p) = 1 T h p p = 273.16 °C γ p0 p0 ⋅ p0 = Tripelpunkt des Wassers, 610.6Pa Gasthermometer mit konst. V liefert Zugang zur universellen Temperaturskala 5 10.2 Phasendiagramm - Wasser In der Thermodynamik ist der Tripelpunkt (auch Dreiphasenpunkt) der Punkt, beschrieben durch Druck und Temperatur, an dem drei Phasen eines Systems mit genau einer Komponente im Gleichgewicht sind. Der Tripelpunkt des Wassers nach dem international akzeptierten Bestwert von Guildner, Johnson & Jones 1976 liegt bei 611,657 ± 0,010 Pa und 273,16 K (0,01 °C). 10.2 Temperaturskalen • Die Temperatureinheit Kelvin wurde 1954 auf Beschluss der 10. Generalkonferenz für Maß und Gewicht durch: 1 K:= Ttr /273,16 definiert (Ttr die Temperatur des Trippelpunkts von Wasser) • Die Festlegung von Einheit ist Menschenwerk und nicht die Folge der Naturgesetzen • Allerdings: Im täglichen Leben benutzt man eine Temperatur mit willkürlich festgesetztem Nullpunkt, die Celsius-Temperatur: T:= T- T0= T-273,15 K, T0 – Temperatur des Eispunkts 6 10.2 Phasendiagramm - Wasser Temperatur des Eispunkts In der Thermodynamik ist der Tripelpunkt (auch Dreiphasenpunkt) der Punkt, beschrieben durch Druck und Temperatur, an dem drei Phasen eines Systems mit genau einer Komponente im Gleichgewicht sind. Der Tripelpunkt des Wassers nach dem international akzeptierten Bestwert von Guildner, Johnson & Jones 1976 liegt bei 611,657 ± 0,010 Pa und 273,16 K (0,01 °C). 10.2 Kelvin-Skala • Amtliche Übersetzung: „Das Kelvin, die Einheit der thermodynamischen Temperatur, ist der 273,16te Teil der thermodynamischen Temperatur des Tripelpunktes des Wassers.“ • Die Kelvin-Skala ist per Definition seit 1968 nicht mehr in Grad unterteilt. Es heißt deshalb nicht mehr „19 Grad Kelvin“ (oder „19 °K“) sondern einfach nur „19 Kelvin“ (19 K). • Es wurde nach William Thomson, dem späteren Lord Kelvin (1824-1907) benannt, der mit 24 Jahren die thermodynamische Temperaturskala einführte. 7 10.2 Temperatur-Skalen Kelvinskala: TC=TK-273.15º 10.2 Temperaturmessung Gasthermometer/Temperaturskala des idealen Gases: • Bei der Extrapolation des Druckes zu niedrigen Temperaturen ergibt sich für alle (idealen) Gase: p He p = 0 bei T = -273.15 ºC -273 Temperatur/ºCelsius -300 -100 100 300 • Dieser Wert (stoffunabhängig!) wird als „Nullpunkt“ der thermodynamischen Temperaturskala definiert • Kelvinskala: 0 Kelvin (0K): -273.15 ºC Umrechnung: T ( K ) = (T ( o C ) + 273)( K ) T = 0 stellt den prinzipiell nie erreichbaren unteren Grenzwert der Kelvinskala dar; d.h. es gilt immer T > 0 K Die thermodynamische Temperatur eines Körpers (oder Systems) steht im Zusammenhang mit seinem Energiegehalt: keine Energie, dann hat er die Temperatur 0 K • • 8 10.3 Gase Eigenschaft von Gasen: • feste/flüssige Stoffe ändern unter Einwirkung äußerer Kräfte kaum ihr Eigenvolumen • ↔ Gase nutzen jedes Raumangebot (d.h. expandieren beliebig) • ↔ Unter Einwirkung eines äußeren Druckes lassen sie sich bis zu einer gewissen Grenze auch beliebig komprimieren • Gasdichte bei Atmosphärendruck um ca. 103 kleiner als die der festen/flüssigen Phase: ca. 6 ·1023 Atome (Moleküle)/22 Liter - Mittlere Abstand der Teilchen ist ca. 10-mal größer - Mittlere Ekin ist größer als die Epot ihrer Wechselwirkung 10.3 Ideales Gas Modellvorstellung des idealen Gases: (i) Gasteilchen sind „punktförmig“ (kein Eigenvolumen) (ii) Gasteilchen üben keine gegenseitige Wechselwirkungskräfte aufeinander aus (iii) Es gibt nur elastische Stöße untereinander, bzw. mit der Wand Modell hinreichend gut erfüllt für viele Gasarten bei hohen Temperaturen und niedrigem Druck ! 9 10.3 Einschub: Stoffmenge Eine Substanz hat die Stoffmenge 1 mol, wenn die Zahl der darin enthaltenen Teilchen gleich der Zahl der Kohlenstoffatome in 12 g reinem 12C ist. - Die Zahl der Teilchen pro Mol heißt: Avogadrozahl NA = 6.023 ·1023 mol-1 (Loschmidt-Konstante) - Liegen ν mol einer Substanz vor, dann ist die Teilchenzahl N: N = ν · NA -Physikalische Größen, die auf Stoffmengen bezogen werden, heißen molare Größen: Molare Masse M (Masse einer Substanz pro Mol) Beispiele: Masse von 1 mol Wasserstoff (atomar): 1.0078 g Masse von 1 mol H2O: 2 ⋅1,0078g + 16g =18.015 g Masse von 1 mol CO2: 12g +2· 16g = 44 g (natürliche Isotopenverhältnisse beachten) Nebenbemerkung: Molvolumen eines Gases = Volumen, das ein Mol dieses Gases enthält 10.3 Ideales Gas Versuch: Boyle - Mariottsches Gesetz: 10 10.3 Ideales Gas Experimentelle Bestimmung der Zustandsgleichung (ideales Gas): (i) Serie von Experimenten bei konstanter Temperatur T (ii) Gas der molaren Masse M (iii) Variation des Druckes p F = p· A p·V = konstant Durch Einfüllen verschiedener Gasmengen X desselben Gases in die Apparatur findet man: Reibungsfreier Kolben p·V = X·konstant V Durch Variation der Gasart findet man: p·V = ν ·C p ν = Stoffmenge in Mol C = (temperaturabhängige) Konstante T Wärmereservoir 10.3 Ideales Gas Experimentelle Bestimmung der Zustandsgleichung (ideales Gas): (i) Untersuchung der Temperaturabhängigkeit des Produkts p·V (ii) Feste Menge Helium-Gas ist in einem konstanten Volumen eingeschlossen F = p· A (iii) Variation der Temperatur T „Fixer“ Kolben V p Resultat zeigt, dass das Produkt p·V eine lineare Funktion von T ist T Wärmereservoir 11 10.3 Ideales Gas Zustandsgleichung des idealen Gases: Beschreibt den Zusammenhang zwischen den Zustandsgrößen: ( p ⋅V ) Druck p Volumen V Temperatur T T = konstant = C - Gültig für alle Gase genügend kleiner Dichte - C ist proportional zu „Gasmenge“, oder Stoffmenge ν, siehe vorhergehenden Einschub 10.3 Ideales Gas Zustandsgleichung p ⋅V = N ⋅ k ⋅ T p ⋅V = ν · N A ⋅ k B ⋅ T = v · R ⋅ T N = Teilchenzahl ν = Stoffmenge R = NA ·kB = Gaskonstante = 8.314 J mol-1 K-1 Gilt für ideale Gase (ohne Wechselwirkungskräfte, ohne Eigenvolumen) 12 10.3 Ideales Gas Folgerung aus der Zustandsgleichung In vielen Experimenten kann eine der Zustandsgrößen jeweils konstant gehalten werden: 1. Gesetz von Boyle-Mariotte: p ∝ V −1 (T = konstant) T = konstant (Isotherme) ν- konstant p1 · V1 = p2 · V2 = p · V = konst. p T3 > T2 > T1 T2 T1 V 10.3 Ideales Gas Folgerung aus der Zustandsgleichung In vielen Experimenten kann eine der Zustandsgrößen jeweils konstant gehalten werden: 2. (2tes) Gesetz von Gay-Lussac: V, ν = konstant (Isochore) p ∝ T (V = konstant) (führt zur Festlegung der Kelvinskala !!!) p p1 p 2 = T1 T2 T 13 10.3 Ideales Gas Folgerung aus der Zustandsgleichung In vielen Experimenten kann eine der Zustandsgrößen jeweils konstant gehalten werden: 3. Gesetz von Charles: p, ν = konstant (Isobare) V ∝ T ( p = konstant) V V1 V2 = T1 T2 T 10.3 Ideales Gas Folgerung aus der Zustandsgleichung In vielen Experimenten kann eine der Zustandsgrößen jeweils konstant gehalten werden: 4. Gesetz der Gleichförmigkeit (bzw. Homogenität): p, Τ = konstant V ∝v V V1 ν1 = V2 ν2 ν 14 10.3 Ideales Gas 4. Gesetz von Avogadro: p, Τ = konstant • Gleiche Volumina Gas von gleichem Druck und gleicher Temperatur enthalten gleich viele Moleküle unabhängig von ihrer chemischen Beschaffenheit • d.h. ein bestimmtes Normalvolumen V0 enthält daher eine bestimmte Einheitsstoffmenge mit einer bestimmten Anzahl von Teilchen. Häufig verwendete „Normbedingungen“: Normdruck: pn = 1013.25 hPa Normtemperatur: Tn = 273.15K 1 mol eines idealen Gases hat das molare Volumen: Vmol = 22.4 l/mol 15