Lösung 7
Werbung

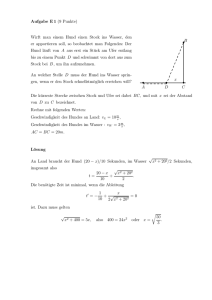
Theorie der Wärme Musterlösung 7. Übung 1. FS 2014 Prof. Renner Joule-Thomson Effekt, Teil II In der vorletzten Übungsserie (siehe Serie 5, Aufgabe 3) wurde gezeigt, dass sich ein Gas beim Joule-Thomson Versuch abkühlt, falls ∂V T −V >0. (1) ∂T p Die thermische Zustandsgleichung eines van der Waals Gases lautet a p + 2 (V − b) = RT . V (2) Bestimme die Inversionstemperatur Ti als Funktion von V und daraus den Inversionsdruck pi als Funktion von T . Zeichne qualitativ im p-T Diagramm das Gebiet, wo bei Joule-Thomson Expansion Abkühlung eintritt, und finde eine mikroskopische Begründung für den Vorzeichenwechsel. Hinweis. Um das Gebiet mit Abkühlung zu bestimmen, betrachte den Fall p → ∞. Wie verhält sich dann V für feste T, und welchem Wert nähert sich damit T ( ∂V ∂T )p − V ? Lösung. Ableitung der Zustandsgleichung nach T bei festem p liefert 2a ∂V a ∂V − 3 (V − b) + p + 2 V ∂T p V ∂T p ∂V 2a RT − 3 (V − b) + ∂T p V V −b =R, =R. (L.1) Auf der Inversionskurve ist (∂V /∂T )p = V /T für T = Ti (V ), also 2a (V − b) = RTi VV−b − 1 = RTi V b−b , V2 2 2a V −b 2 2a Ti = Rb = Rb 1 − Vb . V Umgekehrt: r b RbT =1− , Vi 2a denn das andere Vorzeichen der Wurzel ist wegen V > b auszuschliessen. Einsetzen in die Zustandsgleichung 1 RT a p= − V 1 − (b/V ) V liefert pi = 1 b = a b2 ! r !! r RbT 2RaT a RbT − 1− 2a b b 2a ! r ! r RbT RbT 1−3 −1 . 2a 2a r 1− Um den Bereich, wo Abkühlung stattfindet, zu bestimmen, berechnen wir aus (L.1) 2 2a VV−b − RT b ∂V T −V = . 2 ∂T p − 2a V −b + RT V V Für festes T und p → ∞ gilt V → b nach der Zustandsgleichung, also: ∂V T − V → −b < 0 (für p → ∞). ∂T p 1 8 6 4 2 1 2 3 4 5 7 6 Abbildung 1: Inversionskurve für ein van der Waals Gas. Im schattierten Bereich findet Abkühlung statt. Die 8 a 1 a Einheiten sind T0 = 27 , bzw. p0 = 27 . Auch eingezeichnet sind die Dampfdruckkurve und der kritische bR b2 Punkt (T0 , p0 ). Damit findet bei Joule-Thomson Expansion im schattierten Bereich Abkühlung statt. Man kann die Vorzeichenwechsel in ∂T /∂p|H mikroskopisch mit der Dominanz der kurzreichweitigen abstossenden beziehungsweise der langreichweitigen anziehenden Wechselwirkung zwischen den Gasteilchen begründen. Ist die abstossende Wechselwirkung dominant, so wird bei einer Verringerung des Drucks die potentielle Energie kleiner, also wächst die kinetische Energie und mit ihr die Temperatur (negatives Vorzeichen). Ist hingegen die anziehende Wechselwirkung dominant, so wird bei einer Verringerung des Drucks die potentielle Energie grösser, also werden die Teilchen langsamer und die Temperatur sinkt (positives Vorzeichen). Wird für eine vorgegebene Temperatur der Druck immer weiter erhöht (d.h., man ist irgendwann weit oberhalb der Inversionskurve), so werden die Teilchen auf immer engerem Raum zusammengepfercht, irgendwann wird die abstossende Wechselwirkung über die anziehende dominant sein. Dasselbe passiert, wenn bei konstantem Druck die Temperatur immer weiter abgesenkt wird, das Volumen pro Teilchen sinkt, ab einem gewissen Punkt wird die abstossende Wechselwirkung dominant. Befindet sich das Gas bei nicht zu hohem Druck und nicht zu hoher Temperatur in einem Zustand, bei dem die anziehende Wechselwirkung dominant ist (d.h., man ist unterhalb der Inversionskurve), so wird bei gleichbleibendem Druck und steigender Temperatur die kinetische Energie pro Teilchen wachsen, weswegen es vermehrt zu Kollisionen zwischen den Teilchen kommt, der Einfluss der abstossenden Wechselwirkung wird also wieder wachsen. Übung 2. Hohlraumstrahlung und Stefan-Boltzmann Gesetz Die Energiedichte u(T ) = U (T, V )/V des elektromagnetischen Feldes in einem Hohlraum (Temperatur T , Volumen V ) ist 1 ~2 ~2 + B i, u = hE 2 (3) wobei h·i den zeitlichen Mittelwert bezeichnet. (a) Die Kraft dF~ des Feldes auf ein Oberflächenelement d~σ ist dFi = 1 ~2 ~2 Tij = (E + B )δij − Ei Ej − Bi Bj 2 2 P j Tij doj , wobei (4) der Maxwellsche Spannungstensor ist. Im Hohlraum ist die Strahlung isotrop, also hTij i ∝ δij und damit hdF~ i = pd~o. Zeige dass der Druck durch 1 p(T ) = u(T ) 3 (5) gegeben ist. (b) Berechne die Entropie S(T, V ) des elektromagnetischen Feldes. Verwende eine MaxwellRelation, um das Stefan-Boltzmann Gesetz u(T ) ∝ T 4 (6) herzuleiten. Lösung. (a) Durch Bildung der Spur von hTij i = p(T )δij bekommt man p(T ) = 3 1X 1 3 ~2 ~2 ~2 − B ~ 2 i = 1 u(T ). +B )−E hTii i = h (E 3 i=1 3 2 3 (b) Die partiellen Ableitungen von S(T, V ) sind ∂S = ∂T V ∂S = ∂V T wegen dS = (dU + pdV )/T , u0 (T ) 1 ∂U = V, T ∂T V T ∂U 1 4 u(T ) +p = . T ∂V T 3 T (L.2) (L.3) (L.4) Aus L.4 folgt S(T, V ) = 4 u(T ) V + f (T ), 3 T u0 u − 2 T T V + f 0 (T ) = (L.5) was in L.3 eingesetzt 4 3 u0 (T ) V T (L.6) ergibt. Daraus folgt f 0 (T ) ≡ 0 (also f = 0 in L.4 nach Wahl der Entropiekonstanten), sowie u0 = 4u , T (L.7) was sich auch aus der Maxwell-Relation ∂ 2 S/∂T ∂V = ∂ 2 S/∂V ∂T ergibt. Die Lösung ist u(T ) = σT 4 (L.8) (σ: Integrationskonstante). Alternativ ergibt sich L.5 unmittelbar aus der Homogenitätsrelation 1 (U + pV ); (L.9) T die extensiven Variablen sind hier U , V (im Unterschied zu materiellen Systemen, gibt es beim elektromagnetischen Feld keine Erhaltungsgrösse N ). Die Gleichung L.7 folgt auch as der Maxwell-Relation für dF = −SdT − pdV . S= Übung 3. Adiabatische Entmagnetisierung Eine Methode zur Erzeugung sehr tiefer Temperaturen (∼ 10−3 K) beruht auf der adiabatischen Entmagnetisierung eines paramagnetischen Stoffes (magnetokalorischer Effekt). Die Magnetisierung M (T, H) erfülle das Curie-Gesetz M = KH/T (vergleiche Serie 2, Aufgabe 2) und für die spezifische Wärme cH (T, H) bei festem Magnetfeld H gelte cH (T, H = 0) = b/T 2 , wobei K, b > 0 Konstanten sind. Wie ändert sich die Temperatur als Funktion von H längs einer Adiabaten? 3 Lösung. Wir bestimmen die Entropie S(T, H) anhand ihrer partiellen Ableitungen. Das Differential der Gibbs’schen freien Energie ist dG = −SdT − M dH, so dass ∂S ∂M K = = − 2 H, (L.10) ∂H T ∂T H T und damit K H 2 + f (T ), 2 2T ∂S K cH (T, H) = T = 2 H 2 + T f 0 (T ). ∂T H T S(T, H) = − (L.11) (L.12) Aus der Bedingung für cH (T, 0) folgt T f 0 (T ) = b/T 2 , also f (T ) = −b/(2T 2 ) + const und, nach Wahl der Entropiekonstanten, S(T, H) = − 1 (KH 2 + b). 2T 2 (L.13) Längs einer Adiabaten, S(T1 , H1 ) = S(T2 , H2 ), gilt also T22 KH22 + b = , T12 KH12 + b was < 1 ist wenn H2 < H1 . 4 (L.14)