3. VL (ATP aus Glykolyse, TCC, ATP
Werbung

Vorlesung
Zell- und Molekularbiologie
Stoffwechsel
Metabolismus
(3)
© H.Cypionka
www.icbm.de/pmbio
Überblick
Stoffwechsel
Glykolyse
Citratcyklus
Chemiosmotische
Prinzipien
© H.Cypionka
www.icbm.de/pmbio
1
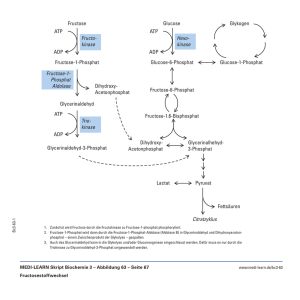
Glykolyse 1
Glucose und in der
Glykolyse daraus
gebildete
phosphorylierte
Metabolite
© H.Cypionka
www.icbm.de/pmbio
Glykolyse 2
Phosphorylierte
C3-Verbindungen
aus der Glykolyse
sowie Pyruvat und
Lactat
© H.Cypionka
www.icbm.de/pmbio
2
Glykolyse,
Umsetzung von
Glucose zu
Pyruvat über
Fructose-1,6Bisphosphat
Glykolyse 3
Anbringen von
zwei P-'Griffen'
Spaltung
Oxidation und
noch ein 'Griff',
daraus dann ATP
2 ATP = 'Griffe'
zurück gewonnen
© H.Cypionka
Energetik und
Regulation der
Glykolyse durch
allosterische
Mechanismen
∆G < 0, irreversibel
www.icbm.de/pmbio
Glykolyse 4
• Irreversible Schritte
mehrfach reguliert
(ATP-Umsetzung)
AMP
ADP
• ATP und G-6-P zum
Teil gleichzeitig
Substrat oder Produkt
und Inhibitor
• ADP und AMP als
korrespondierende
Effektoren
∆G ≈0, reversibel
Vereinfachte,
unvollständige
Darstellung, z.B. je nach
Organismus Reaktionen
u.a. auch von Hormonen
(Insulin) reguliert.
© H.Cypionka
www.icbm.de/pmbio
3
Substratphosphorylierung
Reaktion der
Hexokinase:
Substratphosphorylierung 1
Glucose + ATP → G-6-P + ADP
∆G°' - 15.1 kJ/mol, irreversibel
• Glucose wird unter ATP-Verbrauch aktiviert
• Rückreaktion auf durch Umweg: Glucose-6-Phosphatase
Glucose + ATP → G-6-P + ADP
∆G°' - 16.7 kJ/mol, irreversibel
• 15.1 + 16.7 = 31.8 kJ/mol:
für ATP-Hydrolyse!
• Regulation zwingend zur Vermeidung eines 'futile cycle', der nichts
bewirkt als ATP zu dephosphorylieren!
Energetisch vergleichbar mit
Hexokinase: Reaktion der
Phosphofructokinase:
F-6-P + ATP → F-1,6-BP + ADP
© H.Cypionka
Substratphosphorylierung
www.icbm.de/pmbio
Substratphosphorylierung 2
Reaktion der
1,3-PGA + ADP → 3-PGA + ATP
Phosphoglyceratkinase
∆G °' nahe Null, reversibel
• Woher kommt die zweite, so energiereiche Phosphatgruppe?
GAP + NAD + Pi → 1,3-PGA + NADH2
• Redoxreaktion: Aldehyd wird zur Säure oxidiert, NADH2
gebildet, Energiedifferenz zur Bindung von Phosphat genutzt
= 'Energie konserviert', Energiewandlung
• Reaktion kompliziert aber reversibel
Reaktion der Pyruvatkinase:
PEP + ADP → Pyruvat + ATP
∆G °' < 0, irreversibel
• Liefert das netto ATP, nachdem die obige Reaktion das für die
Aktivierung nötige ATP regeneriert hat ('PEP hat Pep!')
© H.Cypionka
www.icbm.de/pmbio
4
Pyruvat-Dehydrogenase
Reaktion der PyruvatDehydrogenase
Multienzym-Komplex
mit mehreren
Enzymen und
Cofaktoren
Pyr + (HS-)CoA + NAD → Acetyl-CoA + NADH2 + CO2
• Redoxreaktion, erste Bildung von CO2, Aktivierung von Acetat
durch Coenzym A statt ATP
• Aktivierung durch CoA (Thioester) entspricht energetisch der mit
Phosphat, kann sogar ausgetauscht werden:
Phosphotransacetylase: Ac-CoA + Pi <=> Ac-P + CoA
• Acetatkinase wichtige ATP-liefernde Reaktion bei Anaerobiern:
Ac-P + ADP → Ac + ATP
© H.Cypionka
www.icbm.de/pmbio
TCC
Der TricarbonsäureCyclus ist die zentrale
Drehscheibe des
Stoffwechsels zwischen
Anabolismus und
Katabolismus
• Katabolisch leistet er die
vollständige Oxidation zu
CO2 und liefert 8 [H] (3
NADH2,1 FADH2) + 1 ATP
(Substratphosphorylierung)
pro Acetyl-CoA.
© H.Cypionka
www.icbm.de/pmbio
5
TCC-Metabolite
Metabolite des
TricarbonsäureCyclus
© H.Cypionka
www.icbm.de/pmbio
Überblick
Stoffwechsel
Chemiosmotische
Prinzipien
© H.Cypionka
www.icbm.de/pmbio
6
Prinzip der chemiosmotischen Energiekonservierung
-
-
+
+
-
+
+
-
+
+
-
+
+
-
+
+
-
+
+
Energiewandlung :
elektrochemischer
Gradient/chemische
Reaktion
Chemiosmotische
Energiewandlung
• Bakterium oder
Mitochondrium
(= ehemaliges
Bakterium)
• Die Atmungskette
könnte auch ein
Photosystem in einem
Chloroplasten oder
Bakterium sein.
• H+ könnte auch Na+
sein.
• Es gibt keine
ElektronentransportPhosphorylierung,
oxidative Phosphorylierung oder Photophosphorylierung.
© H.Cypionka
www.icbm.de/pmbio
ATPase 1
_
_
_
_
_
_
+
+
+
+
+
+
Reversible Phosphorylierung von ADP gekoppelt an den
Transport von Protonen über eine Membran durch die
ATP-Synthase oder ATPase
© H.Cypionka
www.icbm.de/pmbio
7
ATPase 2
Eines der wichtigsten Enzyme irdischer Lebewesen.
© H.Cypionka
www.icbm.de/pmbio
ATPase 3
© H.Cypionka
www.icbm.de/pmbio
8
Was treibt die Protonen über die Membran?
Chemiosmotische
Energiewandlung
• Die wichtigste chemiosmotische Triebkraft ist nicht der
Protonengradient sondern das Membranpotenzial.
• Obwohl eine Prokaryotenzelle (oder ein Mitochondrium
bzw. Chlorplast) nur ca. sechs freie Protonen enthält,
können viele hunderttausend gepumpt werden. Das Plasma
ist extrem gut gepuffert.
• Elektrische Ladungen werden nicht abgepuffert - jede
Ladung zählt.
• Die Nernstsche Gleichung kann in gleicher Weise für
Redoxreaktionen wie für Membranpotenziale verwendet
werden. Es geht immer nur um die Ungleichverteilung und
die Wahrscheinlichkeit von Vorgängen.
© H.Cypionka
www.icbm.de/pmbio
9