Innate vs. adaptive
Werbung

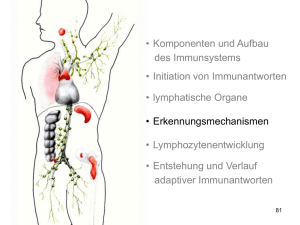
• Komponenten und Aufbau des Immunsystems • Initiation von Immunantworten • lymphatische Organe • Erkennungsmechanismen • Lymphozytenentwicklung • Entstehung und Verlauf adaptiver Immunantworten Die Verteilung der lymphatischen Gewebe im Körper Rachenmandel (Polyopen) Gaumenmandeln rechte subklavikuläre Vene Linke klavikuläre Vene Thymus Lymphknoten Herz Niere Milz Ductus thoracicus Peyersche Platten im Dünndarm Blinddarm Dickdarm Lymphgefäße Innate Knochenmark vs. adaptive 1 lymph node Lymphgefäße • Lymphocyte diameter: ~ 10 µm = 10x10-6 m • Lymphocyte volume: 5x10-13 m3 • Volume of a man (100 Kg): 0.1 m3 • Probability that a lymphocyte stays at a defined place within the body: 1:500 billion • with 6000 identical lymphocytes: 1:314 million 2 lymph node Lymphgefäße • Approx. 1012 αβTCR lymphoctes in humans much ! • However only approx. 6000 of them are specific for a given epitope, such as influenza virus HA not that much • Influenza-infected individual: shedding of several million virus particles nothing ! The multi step model of lymphocyte adhesion from: v. Andrian and Mackay 2000, NEJM 343: 1025-35 3 Lymphocyte adhesion to HEV luminal surfaces is a multi step process. ► Intravital microscopy: Lymphocytes in the LN venular tree. Innate vs. adaptive • Komponenten und Aufbau des Immunsystems • Initiation von Immunantworten • lymphatische Organe • Erkennungsmechanismen • Lymphozytenentwicklung • Entstehung und Verlauf adaptiver Immunantworten 4 Ehrlichs Seitenkettentheorie… Ehrlichs Seitenkettentheorie „….Er nimmt an, daß ein Bakteriengift auf den Organismus nur dann wirken kann, wenn es an bestimmte Zellen des Organismus gebunden wird,….was mittels bestimmter Atomgruppen dieser Zellen geschieht. Diese Atomgruppen nennt er Seitenketten oder in neuerer Zeit Receptoren. Infolge der Schädigung nun, die die Zelle durch diese Bindung erfährt, wird sie angeregt, die betreffenden Atomgruppen neu zu bilden, und zwar thut sie dies…im Übermaß. Dadurch, daß nun durch neu eingeführtes Gift die Receptoren wieder besetzt werden, wird die Zelle immer wieder zur Bildung derselben angehalten und gleichsam daraufhin trainiert. Schließlich … werden die Receptoren von der Zelle abgestoßen und werden zum Schutzstoff, indem sie das Gift in der Blutbahn neutralisieren.“ Ehrlich unterscheidet diese antitoxischen Sera von den bakteriziden Sera. „….Diese bestehen aus zwei Komponenten. Von diesen ist die eine, von Ehrlich als Immunkörper bezeichnete, für jede Krankheit specifisch….die andere, von Ehrlich Komplement genannt, nicht specifisch. Mittels des Immunkörpers wird das Komplement an das Bakterium gebunden und bringt dies zur Auflösung.“ Aus: Brockhaus Konversationslexikon, Stichwort Immunität, 14. Auflage (1902) Immunglobulinmolekühle bestehen aus zwei verschiedenen Arten von Polypeptidketten, den schweren Ketten und den leichten Ketten leichte Ketten Disulfidbrücken schwere Ketten 5 spezifische Antikörper bakterielle Toxine Zelle mit Toxinrezeptoren Neutralisierung Bakterien im extrazellulären Raum Antikörper können auf drei Arten an der Immunabwehr beteiligt sein Bakterien im Plasma Makrophage Opsonisierung Aktivierung des Komlementssystems Komplement 6 Die Anitkörperarme sind durch ein flexibles Gelenk verbunden Winkel zwischen den Armen 0° Winkel zwischen den Armen 60° Winkel zwischen den Armen 90° The Y-shaped immunoglobulin molecule can be dissected by partial digestion with proteases proteolytische Spaltung mit Papain proteolytische Spaltung mit Pepsin 7 In den variablen Domänen gibt es definierte hypervariable Bereiche V-Region der leichten Ketten Variabilität Variabilität V-Region der schweren Ketten Aminosäure Aminosäure Antigene können in Taschen, Gruben oder an ausgedehnten Oberflächen innerhalb der Bindungsstellen von Antikörpern binden 8 Der T-Zell-Rezeptor ähnelt einem membrangebundenem FarbFragment Antigenbindungsstelle Antigenbindungsstelle Antikörper Antigenbindungsstelle T-ZellRezeptor T-Zelle Die Struktur des T-Zell-Rezeptors Kohlenhydrat α-Kette β-Kette variable Region (V) konstante Region (V) Gelenk (H) Transmembranregion Cytoplasmatischer Schwanz Disulfidbrücke Unterschiede in der Antigenerkennung zwischen Immunglobulinen und T Zell Rezeptoren 9 Zwei Hauptgruppen von T-Zellen erkennen Peptid, das an Proteinen von zwei unterschiedlichen Klassen von MHC Molekülen gebunden ist MHC-Moleküle präsentieren die Peptidfragmente von Antigenen auf der Zelloberfläche MHC-Klasse I MHC-Klasse II Peptid Zellmembran MHC-I-Molekül präsentieren Antigene, die aus Proteinen im Zytosol stammen Im Zytosol werden virale Proteine synthetisiert Virus infiziert eine Zelle endoplasmatisches Reticulum MHC-I bindet Peptidfragmente viraler Proteine im ER MHC-I transportiert gebundene Peptide and die Zelloberfläche Zellkern 10 Bakterium infiziert Makrophagen und dringt in Vesikel ein; Peptidfragmente entstehen MHC-II bindet bakterielle Fragmente in den Vesikel MHC-II transportiert gebundene Fragmente an die Zelloberfläche an B-Zell-Rezeptor gebundenes Antigen Antigen wird aufgenommen und zu Peptidfragmente abgebaut Fragmente binden an MHC-II und werden an die Oberfläche transportiert MHC class II molecules present antigen originating in intracellular vesicles Antikörper B-Zelle Cytotoxische T-Zellen erkenn Antigene, die von MHC-I-Molekülen präsentiert werden, und töten die Zelle ab Cytotoxische T-Zelle erkennt Komplex aus viralem Fragment und MHC-I und tötet infizierte Zelle tötet MHCKlasse-I TH1- und TH2-Zellen erkennen Antigene, die von MHC-II-Molekülen präsentiert werden TH1-Zelle erkennt Komplex aus bakteriellem Fragment und MHC-II und aktiviert Makrophagen aktiviert MHCKlasse-II TH2-Helferzelle erkennt Komplex aus antigenem Fragment und MHC-II und aktiviert die B-Zelle T-Helferzelle aktiviert MHCKlasse-II 11 Je nach Art des Antigens können Immunantworten nützlich oder schädlich sein Wirkung der Reaktion auf das Antigen Antigen normale Reaktion ungenügende Reaktion Krankheitserreger Schützende Immunität wiederholte Infektionen harmlose Substanz Allergie keine Reaktion Transplantat Abstoßung Annahme körpereigenes Gewebe Autoimmunität Selbst-Toleranz Tumor Immunität gegen Tumoren Krebs MHC-Moleküle präsentieren die Peptidfragmente von Antigenen auf der Zelloberfläche MHC-Klasse I MHC-Klasse II Peptid Zellmembran Grundzüge der Strukturen der CD4- und CD8-Corezeptormoleküle 12 Die Expression von MHC-Molekülen unterscheidet sich in verschiedenen Geweben Gewebe MHC-Klasse I MHC-Klasse II Lymphatisches Gewebe T-Zellen B-Zellen Makrophagen andere antigenpräsentierende Zellen (z.B. Langerhans-Zellen) epitheliale Zellen des Thymus andere kernhaltige Zellen Neutrophile Zellen Hepatocyten Niere Gehirn kernlose Zellen rote Blutkörperchen Der T-Zell-Rezeptor-Komplex besteht aus Proteinen, die das Antigen erkennen, und unveränderlichen Proteinen, die Signale aussenden Erkennung Signalgebung Die Aggregation des T-Zell-Rezeptors und eines Corezeptors setzt die Verbreitung von Signalen in der Zelle in Gang in ruhenden T-Zellen sind die ITAMs nicht phosphoryliert Bindung des Liganden an den Rezeptor führt zur Phosphorylierung der ITAMs durch rezeptorassoziiete Kinasen ZAP-70 bindet an die phosphorzlierten ITAMs der ζKette; es wird durch Lck phosphoryliert und aktiviert, sobald der Corezeptor an den MHC-Liganden gebunden hat antigenpräsentierende Zelle T- Zelle 13 Gene der variablen Regionen werden aus Gensegmenten aufgebaut leichte Ketten schwere Ketten Keimbahn-DNA Somatische Rekombinatione DJ-verknüpfte umgeordnete DNA Somatische Rekombinatione VJ- oder VDJ-verküpfte umgeordnete DNA Primäres RNA-Transkript Spleißen mRNA Polypeptidkette Die Anzahl funktioneller Gensegmente für die variablen Regionen der schweren und leichten Ketten in menschlicher DNA Zahl der funktionsfähigen Gensegmente in menschlichen Immunglobulinloci Segment leichte Ketten schwere Kette V-Segmente D-Segmente J-Segmente 14 Die genomische Organisation der Loci für die schweren und leichten Immungloblinketten in der Keimbahn des Menschen Locus der leichten λ-Kette Locus der leichten κ-Kette Locus der schwerenKette Gensegmente für variable Regionen werden durch Rekombination verknüpft kappa Gensegmente x J Segmente : 40 x 5 = 200 lambda Gensegmente x J Segmente : 30 x 4 = 120 65 Vh x 27 Dh x 6 Jh Segmente : 65 x 27 x 6 = 11000 Æ Ca 3.5 x 106 verschiedene Spezifitäten 15 Die Einführung von P- und N-Nucleotiden an den Verknüpfungen zwischen Gensegmenten während der Immunglobulingenumlagerung Anfügen von N-Nucleotiden durch TdT RAG-Komplexe binden und spalten Rekombinationssignalsequenzen, sodass eine DNA-Haarnadelstruktur ensteht Paarung der Stränge die RAG-vermittelte Spaltung der Haarnadelstruktur erzeugt palindromartige P-Nucleotide Durch Exonucleasespaltung, DNA-Synthese und DNA-Ligation ensteht die codierende Verknüpfungssequenz Somatische Hypermutation bewirkt Variationen in der umgeordneten variablen Immunglobulinregion, die negativer und positiver Selektion unterliegen, um eine bessere Antigenbindung zu erreichen 6. Tag Verstreute Mutationen in den V-Regionen des Antikörpers 8. – 16. Tag Mutationen häufen sich in den V-Regionen negative Selektion Expansion von B-Zellen mit verbesserter Antigenbildung und mehr Mutation 16 Die Organisation der Loci für α− und β−Κetten des T-Zell-Rezeptors des Menschen in der Keimbahn Locus der α-Kette Locus der β-Kette Umordnung und Expression der Gene für die α- und β-Kette des T-Zell-Rezeptors Keimbahn-DNA Rekombination umgeordnete DNA Transkription Spleißen Translation Protein (T-Zell-Rezeptor) Transkription Spleißen Translation umgeordnete DNA Rekombination Keimbahn-DNA Die Anzahl der menschlichen T-Zell-Rezeptor-Gen-Segmente und die Ursachen der T-Zell-Rezeptor-Vielfalt im Vergleich zu den Immunglobulinen Immunglobulin α:β - Rezeptoren Element V-Segmente D-Segmente D-Segmente, in drei Rastern gelesen selten oft J-Segmente Verknüpfung mit N- und PNucleotiden 50% der Verknüpfungen Anzahl der V-Genpaare junktionale Diversität Gesamtvielfalt 17 Aufbau der γ- und δ-Ketten-Loci desT-Zell Rezeptors beim Menschen Locus der α-Kette Locus der γ-Kette Locus der δ-Kette Der Aufbau der wichtigsten menschlichen Immunglobulinisotypen 18 IgM- und IgA-Moleküle können Multimere bilden IgM-Pentamer J-Kette IgA-Pentamer J-Kette The properties of the human immunoglobulin isotypes Immunglobulin schwere Ketten Molekulargewicht (kDa) Serumspiegel (mittlerer Wert beim Erwachsenen in mg ml-1) Halbwertszeit im Serum (Tage) klassischer Weg der Komplementaktivierung alternativer Weg der Komplementaktivierung Transfer durch Plazenta Bindung an Makrophagen und andere Phagocyten Hochaffine Bindung an Mastzellen und basophile Granulocyten Reaktivität mit Protein A aus Staphylococcus Die Anordnung der Gene für die konstanten Regionen der schweren Ketten der Immunglobuline bei Mensch und Maus Maus Mensch 19 Am Isotypwechsel ist eine Rekombination zwischen spezifischen Umschaltsignalen beteiligt Isotypwechsel Ausstülpen Ausstülpen Rekombination der Schalterregion Rekombination der Schalterregion weitere Umordnung möglich Die Coexpression von IgD und IgM wird durch RNA-Prozessierung gesteuert Expression von IgM Expression von IgD Verschiedene Arten der Variation zwischen Immunglobulinen isotypische Unterschiede allotypische Unterschiede idiotypische Unterschiede 20 Veränderungen in den Immunglobulin- und T-Zell-RezeptorGenen, die während der B-Zell- und T-Zell-Entwicklung und – Differenzierung erfolgen Vorgang erfolgt in Vorgang Art der Änderungen B-Zellen T-Zellen somatische Rekombination von DNA irreversibel ja ja junktionale Diversität unpräzise Verknüpfungen, Insertion von N-Sequenzen in die DNA irreversibel ja ja transkriptionelle Aktivierung Aktivierung des Promotors durch Nähe zum Enhancer irreversibel, aber reguliert ja ja IsotypwechselRekombination somatische Rekombination von DNA irreversibel ja nein Ereignis Zusammensetzung der VRegionen Somatische Hypermutation DNA-Punktmutation irreversibel ja nein IgM-, IgD-Expressionen auf der Oberfläche Differenzielles Spleißen von RNA reversibel, reguliert ja nein Membrangebundene oder sezernierte Form Differenzielles Spleißen von RNA reversibel, reguliert ja nein 21