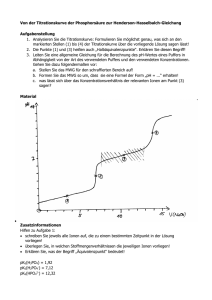
C: Stofftrennung durch Ausschütteln mit Säure/Base
Werbung

Säure/Base-Gleichgewichte 1 leis Säure/Base-Gleichgewichte in Biologie und Medizin Bei den folgenden Anwendungen von Säure/Base-Reaktionen ist eine Tatsache immer wieder entscheidend: Wenn ansonsten hydrophobe Moleküle irgendwo eine ionische funktionelle Gruppe erhalten, werden sie sehr oft hydrophil. Denn zwischen Ionen und den stark polaren Wassermolekülen wirken sehr starke Ion/Dipol-Wechselwirkungen. Aber nicht nur das: Auch ein Cluster aus einem Ion und einer Schicht Wassermolekülen ist als Ganzes noch immer geladen, zieht also weitere Wassermoleküle an, so dass sich um jedes Ion herum viele Schichten aus stark angezogenen Wassermolekülen finden. Ionische Gruppen machen ein Molekül gewissermassen superhydrophil. A: Aufreinigung von Kokain (Chinin) aus Pflanzensaft Kokain wird aus den Blättern des Coca-Strauches gewonnen. Nur etwa 1% des Trockengewichtes dieser Blätter ist Cocain, der Rest besteht aus anderen meist organischen Verbindungen wie Eiweisse, Zucker, Fette, aber darunter sind auch Stoffe, die dem Kokain ähnlich sind. Dennoch gelingt es auch in ganz einfachen Labors im bolivianischen Dschungel, das Kokain aus diesem komplizierten Gemisch relativ sauber aufzureinigen, dank Säure/Base-Reaktionen. 1. Kokain fungiert als einprotonige Base mit einem pKB von 5.6 (der pKS der Säure ist 8.4). An welcher Stelle könnte das Molekül dabei protoniert werden? 2. Zeichne die Skelettformel der konjugierten Säure. (Nur relevanten Ausschnitt zeichnen). 3. Ist das abgebildete Kokain-Molekül hydrophil oder hydrophob? Ist seine konjugierte Säure hydrophil oder hydrophob? Begründe. H CH2 H O H N O H3C N Kokain pKS der konjugierten Säure: 8.4 Chinin pKS des einfach protonierten Chinin (konj. Säure): 8.52 pKS doppelt protoniertes Chinin: 4.1 Da wir leider keine Coca-Blätter zur Verfügung haben, müssen wir die Trennungsschritte mit einem ähnlich gebauten Molekül durchführen: Chinin, das erste Anti-Malaria-Mittel und ein bitterer Zusatzstoff in Indian-Tonic bzw. Tonic-Water-Tafelgetränken wie Schweppes. 4. An welchen zwei Stellen im Molekül kann Chinin gut protoniert werden? Dasjenige N-Atom, welches am π-System beteiligt ist, nimmt etwas weniger gut H+ auf und wird daher erst bei tieferen pH-werten Protoniert. Es könnte gut sein, dass Chinin ein Farbstoff ist. Es sollte daher einfach sein, zu verfolgen, in welcher Phase sich das Chinin befindet. 5. Was spricht dafür, dass Chinin ein Farbstoff ist? Tatsächlich aber ist Chinin farblos, kann aber UV-Strahlung in sichtbares Licht umwandeln. Chinin fluoresziert also unter einer UV-Lampe. Säure/Base-Gleichgewichte 2 leis 6. Wie könnte man vorgehen, um Chinin (Kokain), Traubenzucker und Pflanzenfett voneinander zu trennen? Säure/Base-Gleichgewichte 3 B: Alizarin Alizarin (C14H8O4, 240,20 g/mol) ist ein natürlicher Farbstoff aus der Gruppe der Anthrachinone, der traditionell aus den Wurzeln des Färbekrapp (Färberröte, Rubia tinctorum) gewonnen und zum Färben von Textilien und zur Herstellung von Pigmenten für die Malerei verwendet wurde. Alizarin ist eine zweiprotonige Säure mit den pKS-Werten 6 und 10.5. H H O O H O H H H H O H 3. Zeichne die Pufferkurven für die verschiedenen AlizarinSpezies. 4. Ermittle experimentell, i) welche Alizarinspezies welche Farbe aufweist. ii) Welche Alizarinspezies ungeladen ist. Zur Verfügung stehen Reagenzgläser, eine stark basische Lösung von Alizarin, pH-Pufferlösungen mit verschiedenen pH-Werten und hydrophobes Lösemittel (Diethylether). Dokumentiere Dein Vorgehen. iii) Beschicke einen Schüttelkolben (Scheidetrichter) mit einer wässrigen Phase mit wenig Alizarin und einer Diethyletherphase (nicht zu viel). Lasse das Alizarin in einem Schüttelkolben mindestens einmal aus der wässrigen Phase in die organische wechseln und wieder zurück. Falls du nicht weißt, wie man den Schüttelkolben bedient: bitte mich fragen. Zur Verfügung stehen stark saure und basische Lösungen. Beschreibe dein Vorgehen. leis Säure/Base-Gleichgewichte 4 leis C: Stofftrennung durch Ausschütteln mit Säure/Base-Reaktionen In einem Extrakt der Krappwurzel liegt Alizarin in einem Gemisch mit verschiedenen mehr oder weniger hydrophoben und hydrophilen Stoffen vor. Wie man das Alizarin aus diesem Gemisch aufreinigen kann, zeigt folgender Versuch mit einigen Modell-Verunreinigungen. v) Ein Gemisch aus Alizarin, Neutralrot (siehe folgende Seiten), Glucose, Hexan und Propan-1,2,3-triol (=Glycerin) wird in neutralem Wasser gelöst. Dazu wird das Lösungsmittel Dichlormethan gegeben und der pH der wässrigen Phase durch Säureoder Basenzugabe verändert. Notiere nach jedem Ausschüttlungs-Schritt zu jeder Fraktion (1) bis (6) die darin enthaltenen Stoffe. Basische wässrige Lösung pH 13 Saure wässrige Lösung pH 1 (3) (1) Dichlormethan (4) Dichlormethan (2) Basische wässrige Lösung pH 13 (5) Dichlormethan (6) Rotationsverdampfer („Rotavapor“) Will man eine Substanz rein gewinnen, die in einem Lösungsmittel gelöst ist, so verwendet man oft einen Rotationsverdampfer, um das Lösungsmittel einzudampfen (d.h. zu verdampfen). Die Lösung wird in einen Rundkolben (1) gefüllt, der an einen rotierbaren Schliff angeschlossen wird. Oberhalb des Schliffs befindet sich ein Kühler (2) mit Vakuumansatz (3) und einem Auffangkolben (4). Nun wird ein Vakuum angelegt und das Lösungsmittel beginnt langsam zu verdampfen. Um das Verdampfen zu beschleunigen, wird das Gemisch leicht erwärmt. Zu diesem Zweck lässt man den Rundkolben rotieren (ca. 2 Umdrehungen pro Sekunde, um einen Siedeverzug zu verhindern) und senkt ihn vorsichtig ab, bis er leicht in das Heizbad (5) eintaucht, das auf ca. 30-40°C temperiert ist. Durch die Rotation im Heizbad verdampft das Lösungsmittel und strömt in den Kühler, wo es teils kondensiert und ins Auffanggefäss fliesst. Die Wasserstahl-Vakuumpumpe darf erst abgestellt werden, nachdem der Gaseinlass (6) geöffnet wurde, da sonst Wasser in die Probe strömen würde. Das Vakuum dient dazu, Lösungen bei tiefen Temperaturen einzuengen (abzudampfen). Ohne Vakuum müsste man die Proben weit mehr erhitzen und dabei könnten die Stoffe in der Probe unerwünschte Reaktionen eingehen. Wasserrückstände im Lösungsmittel können im Rotavapor nicht eingeengt werden (dazu wären zu hohe Temperaturen notwendig). Daher muss das Lösungsmittel getrocknet werden, bevor man die Probe in den Rotationsverdampfer gibt. Dies macht man, indem man ein wasserfreies, hygroskopisches Salz wie Natriumsulfat zugibt. Dieses Salz entzieht dem Lösungsmittel das Wasser und baut es als Kristallwasser in seine eigene Struktur ein. Säure/Base-Gleichgewichte 5 leis D: Ion trapping (Ionenfalle) mit Neutralrot Vakuolen Zitronensaft ist so sauer, dass er viele gewöhnliche Proteine sofort zerstört (daher flockt Milch beim Zutropfen von Zitronensaft aus). Ist es überhaupt möglich, dass Zitronen leben und wachsen können? Ganz einfach: Die saure Lösung ist sicher in der Vakuole verpackt, während der Rest der Zelle einen neutralen pH aufweist. Isst man eine Zitrone, platzen die Vakuolen auf und man bekommt die saure Lösung ab. Die Hydroxonium-Ionen (H3O+) sind wegen ihrer Ladung so hydrophil, dass sie nicht durch die Vakuolen-Membran (Tonoplast) hindurch entweichen können. Dieses Beispiel zeigt zwei wichtige Dinge über Pflanzenzellen: Vakuolen sind sauer (typischerweise pH 5-5.5), wenn auch nicht immer so sauer wie in Zitronen (pH 2.5). Und Stoffe, die für die Pflanze selber toxisch sind, werden meist in einer sehr hydrophilen Form in der Vakuole sicher aufbewahrt. Aber dazu später mehr. Neutralrot 1. Ergänze in folgender Skelettformel von Neutralrot die nEPs (nichtbindende Elektronenpaare). H3C N N N H CH3 H N CH3 2. Neutralrot in der oben abgebildeten Form ist nicht sehr gut wasserlöslich. Im Handel ist aber eine ausgezeichnet wasserlösliche „Neutralrot-Variante“ käuflich. Auf welche Weise wird dabei Neutralrot löslich gemacht? 3. Neutralrot kann nur an den zwei zentralen N-Atomen gut protoniert werden, nicht aber an den Amion- und Dimethyl-Amin-Gruppen links und rechts unten im Molekül. Versuche diesen Sachverhalt zu erklären anhand von a. Grenzformeln b. Einer Darstellung des Moleküls im Ladungswolkenmodell (nur π-Bindungen und nEPs als Ladungswolken darstellen). c. Neutralrot ist bei tiefem pH kirschrot, bei hohem orange. Warum ist es einleuchtend, dass die Neutralrot-spezies unterschiedliche Farben haben? 4. Um Heroin (Skelettformel rechts) gut wasserlöslich zu machen, wird es mit Zitronensaft angerührt. Warum wohl? O N O O O O Säure/Base-Gleichgewichte 6 leis Ion trapping mit Neutralrot Für Neutralrot findet man verschiedene pKS–Werte, der pKs scheint sehr stark von den Bedingungen abzuhängen (z.B. Ionengehalt). Wir gehen für diese Aufgabe von einem pKS von 7 aus. 1. Ergänze im rechten Diagramm eine Skala für den pOH und zeichne die Pufferkurve für Neutralrot (HNeuR+/NeuR). Orange Kirschrot 2. Behandelt man Pflanzenmaterial mit neutralen oder leicht basischen Neutralrot-Lösungen, so stellt man fest, dass sich das Neutralrot recht spezifisch in den Vakuolen ansammelt. Vakuolen weisen typische pH-Werte zwischen pH 5.5 (Rose) und 2.5 (Zitrone) auf. i) Welche Neutralrotspezies schafft es wohl, die Zellmembran zu durchdringen? ii) Betrachten wir nun nur diese Spezies. Die Geschwindigkeit, mit der diese Spezies die Membran durchdringt, hängt davon ab, wie gross ihre Konzentration ist, wie oft die entsprechenden Teilchen also auf die Membran prasseln. Angenommen, die Konzentration dieser Spezies sei in der Vakuole c0. Wie gross muss dann im Gleichgewicht die Konzentration dieser Spezies ausserhalb der Zelle sein? iii) Wie viel mal mehr Neutralrot enthält eine Vakuole (pH 5) als die neutrale Umgebung (pH 7) im Gleichgewicht? Stoffe, die wie Neutralrot in einer elektrisch ungeladenen Form Membranen durchdringen können, sammeln sich in denjenigen Kompartimenten an, in denen sie zu hohen Anteilen ionisch vorliegen. Sie werden also ionische Spezies gefangen. Daher spricht man in diesem Zusammenhang von Iontrapping oder Ionenfallen. iv) Würde sich das Neutralrot ebenfalls im Inneren der Vakuolen ansammeln, wenn es den pKs 2 aufweisen würde? Vakuolen von Zwiebelzellen, in denen sich Neutralrot angesammelt hat. Durch die Färbung mit Neutralrot kann man die Vakuole gut vom Cytoplasma unterscheiden. Säure/Base-Gleichgewichte 7 leis Vitalfärbungen mit Neutralrot Neutralrot ist ein beliebter Farbstoff für Vitalfärbungen, da es sich passiv (durch Diffusion) in den Vakuolen anreichert, ohne die Zellen zu zerstören (siehe unten). Die Energie für diese Anreicherung stammt aus dem pH-Unterschied zwischen Cytosol und Vakuoleninnerem. Dieser pH-Gradient wird von den Pflanzen aktiv aufrecht erhalten, stirbt eine Zelle ab, so gleicht sich der pH-Wert schnell aus und das Neutralrot wird nicht mehr angereichert. Experimente mit Neutralrot 1. Neutralrot-Stammlösung: 0.10 g Neutralrot in 100 mL dH2O lösen. Vor Gebrauch mit Leitungswasser (leicht basisch) 1:10 verdünnen (=„Neutralrot-Farblösung“) 2. Gib in zwei RG je 1-2 mL Neutralrot-Farblösung und überschichte die Lösung mit 1-2 mL Hexan. Versuche nun, mit Hilfe von einzelnen Tropfen Salzsäure oder Natronlauge (1M), das Neutralrot möglichst weitgehend in die wässrige bzw. hydrophobe Phase zu bringen. 3. Die innere Zwiebelschuppenepidermis einer Küchenzwiebel wird abgezogen. Die Epidermisstückchen werden in einem Tropfen Neutralrot-Farblösung auf einen Objektträger gebracht. Nach 10 bis 20 Minuten zeigt sich unter dem Mikroskop eine deutliche Anreicherung des Farbstofes in den Vakuolen der immer noch lebenden Zellen, besonders am Rand der Probe. 4. Mit Durchsaugen einer Kaliumthiocyanat-Lösung (1 mol/L, 9.7g / 100mL) können die Zellen leicht plasmolysiert werden. Offenbar sind die Zellmembranen noch intakt. 5. Wenn die Neutralrot-Lösung leicht sauer ist, unterbleibt die Anreicherung (Neutralrot in deionisiertem Wasser statt Leitungswasser verdünnen). Statt der Vakuolen färben sich nun die Mittellamellen der Zellwände, denn diese bestehen aus dem Makro-Polyanion Polygalakturonsäure, die den geladenen Farbstoff als Gegenion (adsorptiv) bindet (vermutlich nur bei tiefer Ionenkonzentration im Medium!) 6. Saugt man stark verdünnte Ammoniaklösung (0.1%) unter dem Deckglas durch, so entfärben sich die Vakuolen: Ammoniak-Moleküle gelangen genau wie das Neutralrot in die Ionenfalle der sauren Vakuolen, aber die Konzentration des Ammoniak steigt so lange, bis der pH der Vakuolen weit über den pKS-Wert des Neutralrots steigt und die Ionenfalls für Neutralrot nicht mehr funktioniert (Ammoniak hat einen deutlich höheren pK S von über 9.). 7. Auch tierische Zellen können Neutralrot akkumulieren, und zwar in den Lysosomen. Lysosomen sind von einer einfachen Membran umschlossene Vesikel mit vielen Enzymen für den Abbau von Makromolekülen. Diese Enzyme funktionieren nur in saurem Milieu, und so weisen Lysosomen typsischerweise einen pH von 4.5 – 5 auf. Dies schützt die Zelle beim Platzen eines Lysosoms: die Enzyme werden durch den neutralen pH im Cytosol sofort inaktiviert. Nur lebende Zellen können Neutralrot in ihren Vakuolen oder Lysosomen akkumulieren. Somit kann Neutralrot als Zytotoxizitätstest eingesetzt werden: Die Aufnahmefähigkeit von Neutralrot kann als Mass dafür verwendet werden, wie viele zellen noch lebend sind. Teste damit die Frische von Gemüse oder einem Stück Fleisch. Säure/Base-Gleichgewichte 8 leis Welche der folgenden Stoffe lassen sich gut in einer Vakuole aufbewahren, welche entwischen schnell durch die Membran? NaCl Glucose Fett Kokain: Ethansäure (Essigsäure) Alizarin: H H O O H O H H H H O H Ruberythrinsäure: Hinweis: Viele Teilchen, die so lipophil sind, dass sie früher oder später Membranen durchdringen, liegen in Pflanzen an Zucker gebunden vor. So tritt Alizarin im Krapp in Form von Ruberythrinsäure auf. Säure/Base-Gleichgewichte 9 leis Alkaloide Alkaloide sind organische Stickstoffverbindungen, die spezifisch von bestimmten Pflanzen hergestellt werden, wie z.B. die Amine Cocain oder Chinin. Die meisten Alkaloide sind giftig und haben interessante Wirkungen auf Menschen und Tiere. Viele der stärksten Pflanzengifte sind Alkaloide. Pflanzen stellen Alkaloide her, um sich vor Pflanzenfressern zu schützen. Dabei haben unglaublich viele Pflanzen eine unglaubliche Vielzahl von verschiedenen Alkaloiden entwickelt. Dies dürfte damit zusammenhängen, dass Alkaloide oft in kleinster Konzentration sehr heftig wirken (z.B. analog wie die unten beschriebenen Lokalanästhetika). Aber Alkaloide sind aus einem weiteren Grund für Pflanzen sehr bequeme Gifte. Denn da Alkaloide oft auch für die Pflanzen selbst giftig sind, müssen sie in den Vakuolen aufbewahrt werden und dürfen von dort nicht entweichen1. 3. Dabei kommt den Pflanzen eine Eigenschaft der Aminogruppen sehr zugute. Welche und warum? Zitronensäure Zitronen verwenden zum Ansäuern ihrer Vakuolen v.a. Zitronensäure, andere Pflanzen Äpfelsäure. Warum sind diese Säuren sehr viel besser geeignet als z.B. Essigsäure (Ethansäure)? Anders gesagt: warum würde es sehr viel mehr Energie kosten, Vakuolen mit Essigsäure sauer zu halten? Zitronensäure, Dihydrogencitrat-, Hydrogencitrat- und Citrat-Ionen OH OH O O O - O O O O - H+ O - H+ O - H+ O HO + HO + HO + O +H HO HO +H HO O - O +H HO O - - HO O O - - O O Äpfelsäure, Hydrogenmalat- und Malat-Ionen OH O O 1 O O + -H O HO - OH + H+ O O HO - OH - H+ O + H+ O - OH Tatsächlich lassen Pflanzen ihre Alkaloide in der Regel nicht nur passiv in die Vakuolen diffundieren, sondern verfügen über schnelle ATP-verbrauchende Pumpen, um die Zellgifte möglichst schnell und vollständig in die Vakuolen zu lokalisieren. Hartmann, T.: Alkaloids. In: Rosental, G.A. und Berenbaum, M.R: Herbivores, their interaction with secondary plant metabolites, Volume 1, 2nd Ed. Academic Press, 1991, p. 87 Säure/Base-Gleichgewichte 10 leis D: Ion trapping (Ionenfalle) in der Pharmakologie Naproxen Naproxen ist ein schmerzstillender, fiebersenkender, entzündungshemmender Stoff mit einem pK SWert von 5.0. In seiner Ungeladenen Form kann es Zellmembranen durchdringen, und da es von der ungeladenen in die geladene Form und wieder zurück wechseln kann, durchdringt es ganze Zellschichten. 1. Naproxen wird aus dem Magen sehr gut in den Körper aufgenommen, nicht aber aus dem Darm. Wieso? 2. Viele Amine und Carbonsäuren verschwinden mit der Zeit aus dem Blut, die einen sammeln sich im sauren Magen an, die anderen im oft leicht basischen Urin. Welche Stoffklasse endet wo? Säure/Base-Gleichgewichte 11 leis Lokalanästhetika Hemmer von spannungsaktivierten Natriumkanälen macht man sich auch in der Medizin zunutze, und zwar als Lokalanästhetika (d.h. Mittel zur örtlichen Betäubung, oder präziser Schmerzmittel, die reversibel und unspezifisch die periphere Erregungsweiterleitung blockieren, ohne das Bewusstsein zu beeinflussen). 2 Typische derartige Lokalanästhetika sind Lidocain oder Bupivacain: Lidocain, pKS der konjugierten Säure: 7.7 2 Bupivacain, pKS der konjugierten Säure: 8.1 Quelle: Narkotika/Lokalanästhetika: Skript von Dr. U. Quitterer, Molekulare Pharmakologie, ETH Zürich Säure/Base-Gleichgewichte 12 leis 3. Wie viele andere Amine (organische Stickstoffverbindungen) blockieren diese Teilchen Kationenkanäle. Warum ist es nicht sehr erstaunlich, dass viele Amine ausgerechnet Kationenkanäle blockieren (und nicht etwa Anionenkanäle)? Dass diese Stoffe hingegen ausgerechnet spannungsabhängige Natriumkanäle verstopfen, hängt mit Details ihrer speziellen Struktur zusammen. Lokalanästhetika verstopfen Natriumkanäle stets von der Zellinnenseite her, nur von dort können sie in den Kanal eindringen und diesen binden. Bevor sie wirken können, müssen Lokalanästhetika also in die Zelle eindringen – und da kommt den Aminen natürlich wieder die Tatsäche zugute, dass sie bei neutralem pH immer auch zu gewissen Anteilen als ungeladene Teilchen vorliegen 3. 4. Skizziere die Pufferkurven von Lidocain und Bupivacain. 5. Für die klinische Wirksamkeit ist es günstig, dass diese Lokalanästhetika im Gleichgewicht höhere Konzentrationen im Zellinneren haben als im Blut. Woran liegt dies? 6. Lidocain und Bupivacain wirken unterschiedlich. Die Wirkung von Lidocain setzt viel schneller ein, dafür wirkt es nur kurz (1-2h), während die Wirkung von Bupivacain erst nach 4-5 h wieder abflaut.Letzteres hängt damit zusammen, dass es deutlich länger dauert, bis Körper das Bupivacain wieder los ist. Erkläre diese zwei Unterschiede anhand der Pufferkurven. 7. Gelangt Flusssäure (HF (aq) auf die Haut, kommt es zu Verätzungen der tiefen Gewebeschichten und gar der Knochen, die tödlich sein können. Im Gegensatz dazu gibt Salzsäure (HCl (aq) nur oberflächliche Verätzungen, die weniger gefährlich sind. Wieso? 3 Quelle: Narkotika/Lokalanästhetika: Skript von Dr. U. Quitterer, Molekulare Pharmakologie, ETH Zürich Säure/Base-Gleichgewichte 13 leis F: Elektrophorese Eine Zelle enthält tausende verschiedener Proteine, die sehr verschiedene Funktionen erfüllen: sie halten die Struktur der Zelle aufrecht, katalysieren unzählige Reaktionen, übermitteln Signale zwischen den Zellen und innerhalb von Zellen, usw. usf. In enorm vielen Forschungsgruppen in der ganzen Welt werden die Eigenschaften und Funktionen einzelner Proteine untersucht. Doch wie fischt man sich diese Proteine einzeln heraus aus dem Chaos einer lebenden Zelle? Diese enorm vielen Proteine haben sehr ähnliche chemische Eigenschaften. Es wäre ein hoffnungsloses Unterfangen, diese Proteine durch Ausschütteln voneinander trennen zu wollen. Hingegen hilft eine andere Trennmethode weiter, die ebenfalls auf den Säure/Base-Eigenschaften der Proteine beruht und kleine Unterschiede in diesen Eigenschaften ausnützen kann: die Elektrophorese. Prinzip: Taucht man in eine wässrige Lösung einen Plus- und einen Minuspol, so wandern aufgrund der Coulomb-Kräfte die Kationen zum Minuspol, die Anionen zum Pluspol. Auf diese Weise kann man Ionen voneinander Trennen. Beschrifte oben ungeladene, sowie negativ und positiv geladene Teilchen. Bei der Elektrophorese gibt man die Proben auf ein Trägermaterial, zum Beispiel ein getränktes Papier (Papierelektrophorese) oder ein wässriger Gel (Gelelektrophorese). Das Trägermaterial verhindert Strömungen in der wässrigen Lösung, bremst die Diffusion der Teilchen und ermöglicht dadurch eine schärfere Auftrennung der Proben. Über den pH-Wert kann man die Ladung der interessierenden Teilchen steuern. Beispielsweise wäre Chinin bei hohem pH ungeladen und würde im elektrischen Feld nicht wandern, während es bei tiefem pH-Wert positiv geladen ist und zum negativen Pol hinwandert. Die Wanderungsgeschwindigkeit der Teilchen hängt nicht nur von der Ladung ab, sondern auch von anderen Parametern, wie der räumlichen Ausdehnung, der molaren Masse (Diffusionsgeschwindigkeit), oder davon, auf welche Weise das Molekül mit dem Trägermaterial wechselwirkt. Also kann es gelingen, durch geschickte Wahl von pH und Trägermaterial, auch sehr ähnliche Moleküle gut voneinander zu trennen. 1. Überlegung: Zu welchem Pol (Pluspol oder Minuspol) hin sollten sich folgende Stoffe bei pH 5.5 bewegen (siehe nächste Seite) Säure/Base-Gleichgewichte 14 leis Proben Die bei dem Versuch verwendeten Proben sind alles Säure/Base-Indikatoren, also Säuren und Basen, die bei Säure/Base-Reaktionen ihre Farbe ändern. Für die Auftrennung mittels Gel-Elektrophorese muss der ungefähre pKS-Wert aller Proben bekannt sein. Im Prinzip könnte man zu diesem Zweck eine Titration mit diesen Stoffen durchführen. Da der pKS-Wert aber nicht sehr genau sein muss, und man gut von Auge feststellen kann, ob die Basenoder Säureform vorliegt, kann man den pKS-Wert gut mit Hilfe von Pufferlösungen abschätzen. 2. Warum sind folgende Stoffe farbig und warum kommt es bei ihnen bei Säure/BaseReaktionen zu einem Farbwechsel? 3. Die Säure Bromphenolblau gibt ein bestimmtes H ab. Warum kann dieses H abgespalten werden? 4. Schätze den pKS-Wert folgender Stoffe mit Hilfe von Pufferlösungen ab. Halte dabei fest, welche Spezies welche Farbe aufweist. Bromphenolblau: Cyanidin (in Rotkohlsaft): rot tiefblau farblos purpur gelb Neutralrot: rot Metanilgelb (Acid yellow 36) Konjugierte Säure: rot orangegelb konjugierte Base: gelb Säure/Base-Gleichgewichte 15 Phenolrot leis 4-Nitrophenol O + N H O O H2In Rot HIn− Gelb In2− rotviolett farblos O + N O - O Herstellung der Pufferlösungen und Gele Kaliumhydrogenphthalat (M= 204.22 g/mol) und ortho-Phthalsäure (M=166.13 g/mol): pKS1 = 2.95 pKS2 = 5.41 Rechts: Pufferkurven der Säure/Base-Paare H2Phth, HPhth- und Phth2-. Der Puffer pH 5.5 wird hergestellt, indem zu 100 mL Kaliumhydrogenphthalat 0.1M die entsprechende Menge NaOH 0.1 M zugegeben wird. Ermittle die notwendige Menge an NaOH mit Pufferkuren und der Hendersson/HasselbalchGleichung, gib diese Menge zu, überprüfe den pH mit dem pHMeter und justiere gegebenenfalls mit NaOH oder HCl 0.1M. fülle dann in einem Messkolben mit Wasser auf 100mL auf. Pro Gelkammer 250 mL Laufpuffer bereitstellen: den obigen Puffer pH 5.5 mit deionisiertem Wasser auf halbe Konzentration verdünnen (für ein Gel und eine Gelkammer als 125 mL Puffer pH 5.5 mit 125 mL deionisiertem Wasser mischen. TBE-Puffer („Tris-Borat-EDTA-Puffer“) TBE-Puffer weist etwa pH 8.3 auf. gelb Säure/Base-Gleichgewichte 16 leis Proben Die bei dem Versuch verwendeten Proben sind alles Säure/Base-Indikatoren, also Säuren und Basen, die bei Säure/Base-Reaktionen ihre Farbe ändern. 1. Warum sind folgende Stoffe farbig und warum kommt es bei ihnen bei Säure/Base-Reaktionen zu einem Farbwechsel? 2. Die Säure Bromphenolblau gibt ein bestimmtes H ab. Warum kann dieses H abgespalten werden? Bromphenolblau: pKS ca. 3.5 Xylencyanol: Alizaringelb R: pKS ca. 11.5 gelb rot Neutralrot: pKS ca. 7.5 rot orangegelb Metanilgelb (Acid yellow 36): pKS ca. 2 Konjugierte Säure: rot konjugierte Base: gelb Cyanidin (in Rotkohlsaft): pKS 2 rot pKS 5.5 farblos pKS 13 tiefblau gelb pKS 7 purpur Säure/Base-Gleichgewichte 17 leis Agarose-Gele giessen Giessvorrichtung: Gelträger aus Plexiglas in trockene Gelkammer legen, vorne und hinten mit Metallkeil verschliessen. In einem Becherglas 0.3 g Agarose mit 30 mL Laufpuffer in kleinem Erlenmeyer mehrfach kurz (ca. 20 Sekunden) im Mikrowellenofen erhitzen und schwenken (Vorsicht: Siedeverzug), bis die Agarose gelöst ist. Danach auf 45°C abkühlen lassen (handwarm). Gel in die Giessvorrichtung giessen, Kamm in der Mitte der Vorrichtung einsetzen und erhärten lassen. Experiment: a Gegebenenfalls Laufpuffer herstellen (separates Blatt) Ladepuffer herstellen: Glycerin (Propan-1,2,3-triol) zu ca. 50%Volumenprozen in Laufpuffer lösen. b Löse die Farbstoffe im Ladepuffer. Durch das Glycerin werden die Proben so dicht, dass sie beim Auftragen in die Aussparungen im Gel (Slots) sinken. c Gel auf dem Gelträger (aber ohne Metallkeile) in die Pufferlösung legen (Pufferlösung soll Gel knapp zudecken). Die längere Laufstrecke ausgehend von den Slots im Gel sollte Richtung Pluspol weisen (einige Anionen sind besonders stark geladen und laufen besonders schnell). d Von jeder Probe 20 μL auftragen. Von schwach gefärbten Proben kann auch mehr aufgetragen werden (Slot ganz füllen). e Deckel aufsetzen und während 2-10 Minuten bei etwa 300V (pro Gel ca. 50 mA) laufen lassen. Generell können solche Gele bei maximal 80-100 mA (6-7mA/cm) laufen. Bei zu hohen Strömen erhitzt sich das Gel zu stark, in diesem Fall den Strom bzw. die Spannung senken. Falls es noch freie Slots gibt f Einzelne Kriställchen Kaliumpermanganat (höchstens ein winziges Kriställchen) oder Kupfer(II)nitrat (möglichst viele Kriställchen) können direkt in ein Slot gegeben werden. Kaliumpermanganat kann Plexiglas schädigen, darf also nicht aus Gel entweichen. g Falls die Probe von Kupfer(II)-nitrat sehr langsam läuft: 20 μL konzentrierten Ammoniak ins Slot geben. Wie verändert sich dadurch die Laufgeschwindigkeit der Kupferionen?) 3. Skizziere das Gel, interpretiere die Resultate 4. Überprüfe den pH des Puffers beim Minus- und Pluspol auf beiden Seiten des Gels. Erkläre. 5. Welche Auswirkungen hat die gemessene pH-Veränderung im Prinzip auf Proben wie Neutralrot, 4-Nitrophenol oder Kupfer(II)-Ionen (Verfärbung? Veränderung der Laufgeschwindigkeit?). 6. Wie könnte man vorgehen, um ein Gemisch aus Methylrot (pKS 5), Methylorange (pKS 3.5) und Neutralrot (pKS 7.4) gut aufzutrennen? E: Aminosäuren, Peptide, Eiweisse O H HN 7. Zeichne die Pufferkurve für die drei Spezies der Aminosäure Glycin (Formelsammlung). 8. Wandert Glycin bei einer Elektrophorese bei pH 7 zum Pluspol oder Minuspol? 9. Wandert Lysin bei pH 6 zum Pluspol oder Minuspol? 10. Mit einem Gemisch aus Lysin, Alanin und Asparaginsäure wird eine Papier-Elektrophorese bei pH 6 durchgeführt. Skizziere den Papierstreifen und gib für jede Aminosäure den Ort an, wo du sie erwartest. Die Wanderungsgeschwindigkeit hänge nur von der durchschnittlichen Gesamtladung der Teilchen ab. 11. Peptide und Proteine entstehen durch - Zusammenhängen von Aminosäuren. Aus welchen O zwei Aminosäuren besteht das folgende Peptid und wohin wandert dieses bei pH 6 wohl: zum MinusH oder Pluspol? Nimm in grober Näherung an, dass die pKS-Werte der Amiosäuren sich beim Zusammenkoppeln nicht verändern. O + H NH3 + H3N Säure/Base-Gleichgewichte 18 leis Auftrennung von Proteinen mittels Gelelektrophorese Lebende Zellen enthalten tausender verschiedener Proteine (Eiweisse). Proteine bestehen aus miteinander verknüpften Aminosäuren. Weil Aminosäuren chemisch sehr verschiedenartige Seitenketten haben, können Proteine sehr verschiedenartig sein (hydrophil, hydrophob, amphiphil wie Tenside, mit negativer oder positiver Oberflächenladung, sehr unterschiedlich reaktiv) – obwohl das Grundgerüst bei jedem Protein gleich ist. Damit können Proteine sehr verschiedene Funktionen in der Zelle erfüllen – Zellgerüst, Motoren, Enzyme, Signalmoleküle und Rezeptoren, … Die Aminosäureabfolge jedes Proteins ist durch ein Gen auf der DNA gespeichert. Um die Funktionen der Proteine in der Zelle einzeln zu untersuchen, muss man sie voneinander trennen können. Dies ist aber sehr schwierig, weil jede Zelle sehr viele verschiedene Proteine enthält, die chemisch oft sehr ähnlich sind. Mittels Gel-Elektrophorese lassen sich auch sehr ähnliche Proteine oft scharf voneinander trennen. Auftrennung nach Grösse mit SDS Page Bei der SDS-Page-Methode (Sodium dodecylsulfonat polyacrylamid gel electrophoresis) werden Proteine mit SDS (Sodium dodecyl sulfonat, also Natriumdodecylsulfonat) behandelt. Protein Der hydrophobe Teil dieses Tensids schiebt sich in die hydrophoben Bereiche der Proteine. Dadurch werden die verknäulten Proteine auseinandergefaltet, bis sie als lange Ketten vorliegen, deren Oberfläche mit SDS gespickt und damit stark negativ geladen ist. Diese Proben werden auf ein Polyacrylamid-Gel aufgetragen. Ein solches Gel besteht aus riesigen Ketten von Acrylamid, die an manchen Stellen miteinander verknüpft (cross-links) sind, und die mit Wasser gut Wasserstoffbrücken ausbilden, so dass sich in den Raum zwischen den Polyacrylamid-Ketten Wassermoleküle einlagern. H H O N C H H O N C H H O N C H H O N C H H O N N H O N H C H H O N C H H O N C H O N C H C O H2C H O N C C H H H O N C H Dodecylsulfonat H H O N C H O N C SDS Page-Gel Bei der Elektrophorese werden die negativen SDS-Protein-Ketten in Richtung Pluspol gezogen. Je länger eine Kette ist, desto mehr verheddert sie sich dabei mit der Gel-Matrix (die langkettigen Moleküle, die den Gel aufspannen), so dass ein Protein umso langsamer vorankommt, je grösser es ist. Proteine werden also nach ihrer Grösse aufgetrennt. Lässt man die Eiweisse verschiedener Zellen nebeneinander laufen, so kann man Unterschiede in ihrer Protein-Zusammensetzung erkennen. Man kann die Proteine aus dem Gel extrahieren und weiter untersuchen. Die allermeisten Proteine, die mit dieser Methode aufgetrennt wurden, funktionieren nicht mehr richtig – ihre dreidimensionale Struktur wurde ja durch das SDS zerstört. Man kann aber beispielsweise ihre Aminosäurenabfolge chemisch bestimmen. Säure/Base-Gleichgewichte 19 leis 2-dimensionale Elektrophorese Mit einer gewöhnlichen SDS-Page lassen sich die tausenden verschiedener Proteine einer Zelle natürlich nicht scharf voneinander trennen. Um eine bessere Auftrennung zu erreichen, verwendet man die sogenannte 2D-Elektrophorese, bei der die Eiweisse nacheinander unter verschiedenen Bedingungen in verschiedenen Richtungen (Dimensionen) wandern. O OH C O OH C NH2 Erste Dimension: Isoelectric focussing Zuerst werden die Proteine auf ein Gel aufgetragen, das am einen Ende sauer, am anderen basisch ist, das also einen pH-Gradienten aufweist. Dies erreicht man, Gel in Wasser quellen lassen indem man in die Polyacrylamid-Ketten am einen Ende saure, am anderen Ende basische funktionelle Gruppen + + einbaut (Abbildung rechts): H3O H3O HO In diesem Gel laufen negativ geladene Proteine richtung Pluspol und kommen dabei in Regionen mit O O O O + einem immer höheren pH. Dadurch werden ihre NH3 C C negativen Seitenketten sukzessive protoniert, bis das Protein insgesamt ungeladen ist und stehen bleibt. Positiv geladene Eiweisse laufen hingegen Richtung Minuspol, in Bereiche mit immer höherem pH. Ihre positiven funktionellen Gruppen werden also mehr und mehr deprotoniert, bis das Protein als Ganzes ungeladen ist und stehen bleibt. Die Proteine werden also nach dem pH aufgetrennt, an dem sie insgesamt ungeladen sind. Diese Technik heisst isoelectric focussing (weil Proteine aufgrund ihrer elektrischen Ladung an bestimmten Stellen im Gel aufkonzentriert, also fokussiert, werden). Zweite Dimension (z.B. SDS-Page): Nun lädt man alle Eiweisse negativ, beispielsweise indem man sie mit SDS behandelt, dreht den Gel um 90° und lässt die Elektrophorese in dieser Richtung laufen. Proteine, die bei demselben pH ungeladen waren, werden nun jetzt noch – wie bei SDS Page - nach ihrer Grösse aufgetrennt. Beim Isoelectric focussing bleiben viele Proteine intakt – Enzyme funktionieren beispielsweise immer noch. Lässt man den zweiten Trennungsschritt weg oder führt ihn unter besonders schonenden Bedingungen durch, kann man unter Umständen voll funktionsfähige Proteine gewinnen für Experimente. Auftrennung nach isoelektrischem Punkt (pH, bei dem das Protein dem ungeladen ist) Auftrennung nach Grösse Abbildung: 2D-Elektrophoresegele von Proteinen, die auf verschiedene Weise sichtbar gemacht wurden: Links: In die Eiweisse wurde radioaktives Material eingebaut. Danach wurde ein Fotopapier auf den Gel gelegt. Je mehr radioaktive Zerfallsprodukte auf dem Fotopapier auftrafen, desto dunkler wurde das Papier. Rechts: Nach der Elektrophorese wurden die Gele mit dem Farbstoff Coomassie Brilliantblau eingefärbt. Bilderquelle: Wikipedia H2N HO - + H3N Säure/Base-Gleichgewichte 20 leis Material Stofftrennung mit Hilfe von Säure/Base-Reaktionen Stoffauftrennung durch Ausschütteln Demo-Experiment Chinin Schweppes oder anderes Chinin-haltiges Getränk UV-Lampe Scheidetrichter in Ständer Deionisiertes Wasser Diethylether Pufferlösung pH 12 Konz. Natronlauge mit Tropfpipette Konz. Salzsäure mit Tropfpipette 3 kleine Bechergläser Rotationsverdampfer Alizarin: Farben der verschiedenen Spezies; Trennmethode ausprobieren Pro Klasse Alizarin mit Mikropolylöffel (nicht!!! Alizaringelb) pH-Pufferlösung pH 4, pH 8, pH 12 und einige dazwischen 3 Tropfpipetten in kleinen Erlenmeyerkolben Konz. Natronlauge mit Tropfpipette in Erlenmeyer 2 mal (in verschiedenen Abzügen) Konz. Salzsäure mit Tropfpipette in Erlenmeyer 2 mal (in verschiedenen Abzügen) Diethylether Pro Gruppe 3 Reagenzgläser im Gestell Scheidetrichter in Ständer Gel-Elektrophorese Pro Klasse Elektrophoresekammer mit Spannungsquelle Puffer pH 5.5 nach CRC-Handbook o 50 ml 0.1 M Kaliumhydrogenphthalat + 36.6 ml 0.1 M NaOH, mit Wasser auf o pH überprüfen und bei Bedarf mit NaOH oder HCl einstellen o mit Wasser auf 100 mL ergänzen Pro Gelkammer 250 mL Laufpuffer bereitstellen: den obigen Puffer pH 5.5 mit deionisiertem Wasser auf halbe Konzentration verdünnen (für ein Gel und eine Gelkammer als 125 mL Puffer pH 5.5 mit 125 mL deionisiertem Wasser mischen. 2 Agarose-Gele giessen o Giessvorrichtung: Gelträger aus Plexiglas in trockene Gelkammer legen, vorne und hinten mit Metallkeil verschliessen. o In einem Becherglas 0.3 g Agarose (geeignet für Gele) mit 30 mL Laufpuffer mehrfach kurz (ca. 20 Sekunden) im Mikrowellenofen erhitzen und schwenken (Vorsicht: Siedeverzug), bis die Agarose gelöst ist. Danach auf 45°C abkühlen lassen (handwarm). Gel in die Giessvorrichtung giessen, Kamm in der Mitte der Vorrichtung einsetzen und erhärten lassen. Alternative: Herstellung des Puffers pH 5.5 nach CRC-Handbook durch Schüler: Dieser Puffer enthält K: 50 mM; HPh: 14.4 mM, Ph2: 36.6 mM; Na: 36.6 mM, also 50 mM Phthalsäurespezies, 86.6 mM Kationenäquivalente, (bzw. Anionenäquivalente). Pro Klasse o o o 500 mL Kaliumhydrogenphthalat 0.1 M mit Messzylinder 50 mL NaOH 0.1 M mit Messpipette 20 mL und Tropfpipette HCl 0.1 M mit Tropfpipette o o o o geeichtes pH-Meter Messkolben 100 mL Messzylinder 200 mL Erlenmeyer 100 mL Pro Gruppe Säure/Base-Gleichgewichte o o 21 2 Bechergläser 200 mL Mikrowellenofen oder pro Gruppe: Gasbrenner mit Feuerzeug Proben Pro Klasse Glycerin mit Pipette Lösungen von o Bromphenolblau (evtl. mit Xylencyanol, Laufpuffer Biologie), 0.1 g in 16 mL 0.01 M NaOH + 234 mL water o o o o o o o o o Rotkohlsaft Neutralrot (0.01% in Ethanol) Metanilgelb (0.01% in Wasser) Methylrot 0.02 g in 100 mL 60% v/v ethanol-water Methylorange 0.1% in water p-Nitrophenol 0.1% in water Alizaringelb R (0.01% in Wasser) Phenolrot 0.1 g in 28.2 mL 0.01 M NaOH + 221.8 mL water Universalindikator o Ammoniak konz Feststoffe mit Polylöffel o Kupfer(II)-chlorid o Kaliumpermanganat Universalindikator-Papier zur Überprüfung des pH des Laufpuffers Spitzen für 20 μL-Pipette Eine Serie Pufferlösungen mit Erlenmeyer und Pipette Möglichst in Schritten von nicht mehr als 1 pH-Einheit Möglichst ab pH 1 bis 13. Pro Gruppe Socorex 20 μL eine Tüpfelplatte zum Vorbereiten der Proben leis Säure/Base-Gleichgewichte 22 leis TBE-Puffer („Tris-Borat-EDTA-Puffer“) TBE-Puffer weist etwa pH 8.3 auf und wird hergestellt aus 10.8 g (89 mM) TRIS-Base 5.5 g (89 mM) Borsäure und 0.7g (2mM) Na2H2EDTA „Tris“ = Tris(hydroxymethyl)aminomethan Borsäure (und konjugierte Base !!!!) H O - B O H O O H H pKB = 5.8 (pKS der konjugierten Säure: 8.06 bei 25°C) pKS nimmt pro °C Erwärmung um 0.03 ab) M = 121.14 g/mol pKS1: 9.25 M =61.83 g/mol. Der pH-Wert stimmt nicht mit dem rechnerischen (pH 8.65) überein. Dies liegt vermutlich daran, dass der Säuregrad von Borsäure durch die Reaktion mit mehrwertigen Alkoholen (Tris) wesentlich gesteigert wird, bei anderen Tris-Puffern („TAE-Puffer“) stimmen der rechnerische und der experimentelle Wert überein. TAE-Puffer weist etwa pH 8.3 auf und wird hergestellt aus TAE-Laufpuffer für Agarose-Gele enthält 40 mM Trisacetat. 242 g TRIS-Base (M=121.14 g/mol) 57.1 mL Eisessig (M=60.05 g/mol, Dichte = 1.05 g/mL) 100mL EDTA 0.5M pH 8 Auf 1 L mit Wasser auffüllen (50x Stock), bei Gebrauch 50x verdünnen auf 40 mM TRIS und 20 mM Acetat. Dieser Puffer puffert weniger gut, Kapazität ist eher erschöpft, aber dafür werden Enzyme nicht inhibiert durch Borate wie bei TBE Puffer. „Tris“ = Tris(hydroxymethyl)aminomethan pKB = 5.8 (pKS der konjugierten Säure: 8.06 bei 25°C) pKS nimmt pro °C Erwärmung um 0.03 ab) M = 121.14 g/mol Acetat pKS14.76 M =60.05 g/mol. Säure/Base-Gleichgewichte 23 leis Beispiel-Resultate Elektrophorese-Gele Gel A Minuspol Ne Np Ro Mg Alg BX KV Pluspol Phthalat-Puffer pH 5.5 300 V, ca. 5 Min. Ne Np Ro Mg Alg BX KV Proben Ungefährer pKS Neutralrot Nitrophenol Rotkohlsaft Methanilgelb Alizaringelb R Bromphenolblau Xylencyanol Kristallviolett Hinweis: Durch Elektrolyse an den Platindrähten ändert sich der pH-Wert in der Pufferlösung mit der Zeit und dadurch auch die relative Wanderungsgeschwindigkeit einiger Banden. pKS 7.5 pKS 7 Konj. Säure Farbe (Ladung) Blaurot (+) Farblos (0) Konj Base Farbe (Ladung) Orangegelb (0) Gelb (-) pKS 2 Rot (0) Gelb (-) pKS 3.5 - Gelb (-) Türkis (-) Violettblau (2-) Puffer beim Minuspol Ursprünglicher Puffer Puffer beim Pluspol Pufferlösung mit Universalindikator nach Ablauf des Experiments Säure/Base-Gleichgewichte 24 leis Lösungen A: Aufreinigung von Kokain (Chinin) aus Pflanzensaft 1. Kokain fungiert als einprotonige Base mit einem pKB von 5.6 (der pKS der Säure ist 8.4). An welcher Stelle wird das Molekül dabei protoniert? Begründe. Grundsätzlich können H+ bei den nEPs (nichtbindenden Elektronenpaaren) am N- oder an den O-Atomen aufgenommen werden. Tatsächlich werden die H+ beim N-Atom aufgenommen: - Gemäss Säure/Base-Reihe sind Teilchen mit N-Atomen stärkere Basen als vergleichbare, gleich geladene Teilchen mit O-Atomen: NH3 ist die stärkere Base als H2O, NH2- ist stärkere Base als OH-. Also sind vergleichbare Teilchen mit N-Atomen stärkere Basen. - Wird an einem O-Atom protoiniert, so weist das entstehende Kation eine polarere Bindung auf als bei Protonierung am N-Atom (alle anderen Faktoren sind etwa gleich). Aus dem O-Atom wird das H+ somit wieder besser abgespalten, die O-Atome nehmen daher weniger gut H+ auf, es wird also vorwiegend an den H-Atomen protoniert. - Nach Protonierung tragen N- wie O-Atome eine positive Partialladung. Positive Partialladungen sind tendenziell umso besser möglich, je weniger elektronegativ ein Atom ist, also besser auf N-Atomen, somit stellen N-Atome bessere H+-Akzeptoren dar. 2. Zeichne die Skelettformel der konjugierten Säure. H H3C + R1 N 3. Ist das abgebildete Kokain-Molekül hydrophil oder hydrophob? Ist seine konjugierte Säure hydrophil oder R2 hydrophob? Begründe. Das Molekül weist grosse hydrophobe Bereiche auf: der Cycloheptanring, der Benzolring (=C6-Ring mit konjugiertem System) und die Methylgruppen. Die möglichen Wasserstoffbrücken sind zudem schwach, da an jedem O- bzw. N-Atom immer nur negative Halbbrücken vorhanden sind (negative und positive Halbbrücken können sich gegenseitig verstärken über induktiven Effekt). Also sollte das ungeladene Molekül als ganzes hydrophob sein [und der Stoff ist tatsächlich hydrophob. Überraschungen sind aber nie ganz ausgeschlossen, es könnte ja z.B. sein, dass sich die Teilchen ausserordentlich gut zu einer Art Micelle zusammenlagern mit den hydrophoben Stellen nach aussen...]. Die Konjugierte Säure weist aber eine kationische Gruppe auf. Zumindest diese ionische, geladene Gruppe ist sicher sehr hydrophil. Das reicht hier höchstwahrscheinlich [und das Experiment zeigt: tatsächlich] aus, um die ganzen Teilchen in die wässrige Phase zu holen, als ganzes hydrophil zu machen. Kokain pKS der konjugierten Säure: 8.4 Chinin pKS einfach protoniertes Chinin (konj. Säure): 8.52 pKS doppelt protoniertes Chinin: 4.1 4. An welcher Stelle nimmt Chinin das erste Proton auf, an welcher Stelle das zweite? Einer der pKs-Werte von Chinin ist sehr ähnlich wie bei Kokain, also muss die entsprechende Gruppe auch ähnlich beschaffen sein: ein N-Atom, das nur über Einfachbindungen gebunden ist. Das N-Atom im konjugierten System ist hingegen recht anders gebunden und weist eine ganz andere Basenstärke auf. Da die Konjugierte Säure beim einfach gebundenen N schwächer ist (der pKB dort also tiefer), wird an dieser stelle zuerst protonmiert. 5. Was spricht dafür, dass Chinin ein Farbstoff ist? Konjugiertes bzw. mesomeres System 6. Wie könnte man vorgehen, um Chinin (Kokain), Traubenzucker und Pflanzenfett voneinander zu trennen? Hexan oder anderes hydrophobes Lösemittel Frisches Hexan Alkaloid (Chinin oder Kokain) Pflanzenfett Saure wässrige Lösung pH 1 Traubenzucker Alkaloid (Chinin Kokain) und oder Wässrige Phase mit NaOH auf hohen pH bringen, z.B. pH 13 Basische wässrige Lösung pH 13 Traubenzucker Hexan möglichst schonend eindampfen, damit das Alkaloid nicht zerstört wird (bei möglichst tiefen Temperaturen unter Sauerstoffausschluss: Rotavap). Alkaloid als Reinstoff Säure/Base-Gleichgewichte 25 leis B: Alizarin H H O H O H H O O H O O H - O O H - O H H H H O ca. pKS 6 H H H H O H O ca. pKS 10.5 H H H H O H O H Möglichst polar gebundene H+, konjugierte Basen sollen mesomerie-stabilisiert sein (Teilchenladung, Bindungslängen, Induktiver Effekt sind überall etwa gleich), O H H H O - chinoide Grenzformel 7. Siehe oben 8. Zeichne die Pufferkurven für verschiedenen Alizarin-Spezies. H die 9. gibt man sehr wenig Alizarin in Pufferlösungen, so wird die Farbe über pH 12 (Ali2-) blau, unter pH 4 gelb (H2Ali), und um pH7 bis pH8 rot (HAli-). Nimmt man zu viel Alizarin, sieht man bei pH 8 und 4 eine rote Trübung. Sie besteht aus schlecht wasserlöslichem H2Ali, das verklumpt und ausfällt. Diese Trübung verdeckt die gesuchte Farbe. In diesem Fall kann man die Probe mit etwas Diethylether überschichten. Das ungelöste Alizarin wechselt dann in die Diethylether-Phase. Diese H2Ali-Trübung tritt auch auf, wenn vom pH her viel mehr HAli- als H2Ali vorliegen müsste. Denn wenn sich ein Gleichgewicht zwischen den Spezies eingestellt mit viel HAli- und wenig H2Ali und nun das hydrophobe H2Ali beginnt, aus der wässrigen Phase zu verschwinden, fehlt es nachher dem Gleichgewicht, und dieses verschiebt sich auf die Seite von mehr H2Ali, das auch wieder aus dem Wasser verschwindet, etc. Siehe auch Aufgabe 12. Ali2Blau bis violett HAlirot H2Ali gelb 10. Bei tiefem pH wandert gelbes Alizarin in die hydrophobe Phase, bei hohem pH hingegen blau in die wässrige Lösung. 11. Etwas gelbes Alizarin wandert in die organische Phase, also stehen die verschiedenen Alizarinspezies miteinander im Gleichgewicht. Auch wenn der pH so gewählt wird, dass praktisch kein H2Ali mehr in der Lösung vorliegen sollte, beispielsweise pH 8, ist die Diethyletherphase doch erstaunlich gelb. Bei pH 8 wäre in der wässrigen Phase im Gleichgewicht nur noch etwa 1% des Alizarins in der gelben Form. Diese gelbe Form geht aber bevorzugt in die hydrophobe Phase, die wässrige Phase enthält praktisch gar keins mehr. Dadurch wird aber das Gleichgewicht im Wasser verschoben: das entwichene H2Ali wird ersetzt und wandert erneut in die hydrophobe Phase. Dadurch wird die Alizarinkonzentration in der wässrigen Phase so tief, dass man die Farbe der mittleren Form gut erkennen kann. H - Säure/Base-Gleichgewichte 26 leis C: Stofftrennung durch Ausschütteln mit Säure/Base-Reaktionen 12. Ein Gemisch aus Alizarin, Neutralrot, Glucose, Hexan und Propan-1,2,3-triol (=Glycerin) wird in neutralem Wasser gelöst. Dazu wird das Lösungsmittel Dichlormethan (Hydrophob!!) gegeben und der pH der wässrigen Phasen von Schritt zu Schritt verändert. (Neutralrot: siehe unten) Basische wässrige Lösung pH 13 Saure wässrige Lösung pH 1 Neutralrot Glucose Glycerin Dichlormethan Neutralrot Dichlormethan Alizarin Hexan Glucose Glycerin Basische wässrige Lösung pH 13 Alizarin Dichlormethan Hexan Säure/Base-Gleichgewichte 27 leis D: Ion trapping (Ionenfalle) mit Neutralrot Vakuolen Zitronensaft ist so sauer, dass er viele gewöhnliche Proteine sofort zerstört (daher flockt Milch beim Zutropfen von Zitronensaft aus). Ist es überhaupt möglich, dass Zitronen leben und wachsen können? Ganz einfach: Die saure Lösung ist sicher in der Vakuole verpackt, während der Rest der Zelle einen neutralen pH aufweist. Isst man eine Zitrone, platzen die Vakuolen auf und man bekommt die saure Lösung ab. Die Hydroxonium-Ionen (H3O+) sind wegen ihrer Ladung so hydrophil, dass sie nicht durch die Vakuolen-Membran (Tonoplast) hindurch entweichen können. Dieses Beispiel zeigt zwei wichtige Dinge über Pflanzenzellen: Vakuolen sind sauer (typischerweise pH 5-5.5), wenn auch nicht immer so sauer wie in Zitronen (pH 2.5). Und Stoffe, die für die Pflanze selber toxisch sind, werden meist in einer sehr hydrophilen Form in der Vakuole sicher aufbewahrt. Aber dazu später mehr. Neutralrot 5. Ergänze in folgender Skelettformel von Neutralrot die nEPs (nichtbindende Elektronenpaare). N H3C H N N N H CH3 CH3 6. Neutralrot ist nicht sehr gut wasserlöslich. Warum? Grosse hydrophobe Bereiche. Flache hydrophobe Ringe, die sich gut aneinander lagern können. 7. Im Handel ist aber eine ausgezeichnet wasserlösliche „Neutralrot-Variante“ käuflich. Auf welche Weise wird dabei Neutralrot löslich gemacht? Durch Reaktion mit HCl wird das Neutralrot-Molekül an einer Stelle protoniert, damit zu einem Ion und somit gut wasserlöslich. 8. Neutralrot kann nur an den zwei zentralen N-Atomen gut protoniert werden, nicht aber an den Amion- und Dimethyl-Amin-Gruppen links und rechts unten im Molekül. Versuche diesen Sachverhalt zu erklären anhand von a. Grenzformeln Die positive Ladung kann mesomerie-stabilisiert werden. b. Einer Darstellung des Moleküls im Ladungswolkenmodell (nur π-Bindungen und nEPs als Ladungswolken darstellen). (seitliche Überlappung ist der besseren Übersichtlichkeit halber nicht durch Striche symbolisiert) H + CH3 N N N H H CH3 N H H + CH3 N N N H H CH3 N H3C H N H3C N H3C N N CH3 CH3 Die nEP der N-Atome links und rechst können sich am π-System beteiligen und stehen dann nicht mehr für Protonierungen zur Verfügung, die mittleren N-Atome sind anderweitig am π-System beteiligt und weisen noch nEPs auf für die Aufnahme von H+. Säure/Base-Gleichgewichte 28 leis 9. Um Heroin (Skelettformel rechts) gut wasserlöslich zu machen, wird es mit Zitronensaft angerührt. Warum wohl? Heroin weist ein „basisches“ N-Atom auf, das bei saurem pH H+ aufnimmt, so dass das ganze Teilchen hydrophil wird. Ion trapping mit Neutralrot 4. Ergänze im rechten Diagramm eine Skala für den pOH und zeichne die Pufferkurve für Neutralrot. 5. Behandelt man Pflanzenmaterial mit NeutralrotLösungen, so stellt man fest, dass sich das Neutralrot recht spezifisch in den Vakuolen ansammelt. Vakuolen weisen typische pH-Werte zwischen pH 5.5 (Rose) und 2.5 (Zitrone) auf. v) Welche Neutralrotspezies schafft es wohl, die Zellmembran zu durchdringen? Neutralrot HNeutralrot+ Nur hydrophobe Spezies kommen effizient durch die Membran (abgesehen von sehr kleinen Molekülen wie NH3). Also durchdringt nur die ungeladene Spezies die Membran. v) Betrachten wir nun nur diese Spezies. Die Geschwindigkeit, mit der diese Spezies die Membran durchdringt, hängt davon ab, wie gross ihre Konzentration ist, wie oft die entsprechenden Teilchen also auf die Membran prasseln. Angenommen, die Konzentration dieser Spezies sei in der Vakuole c 0. Wie gross muss dann im Gleichgewicht die Konzentration dieser Spezies ausserhalb der Zelle sein? Ebenfalls c0. Nur wenn beide Konzentrationen gleich sind, treffen auch gleich viele Teilchen pro Zeit von innen wie von aussen auf die Membran, durchdringen gleich viele Teilchen die Membran und die Konzentrationen bleiben gleich (Gleichgewicht) vi) Wie viel mal mehr Neutralrot enthält eine Vakuole (pH 5) als die neutrale Umgebung (pH 7) im Gleichgewicht (Konzentration)? Bei pH 5 beträgt das Verhaltnis Neu:HNeu+ gemäss Pufferkurve bzw. Hendersson/HasselbalchGleichung 1:100 (saurer als pKS, also mehr saure Form), bei pH 7 gerade 1:1. Das gibt folgende Konzentrationsverhältnisse (eben: die Konzentration der ungeladenen Spezies muss innen und aussen gleich sein, siehe oben: Vakuole, pH 5 Cytosol, pH 7 Neu Neu HNeu+ 100 : 1 : 1 : HNeu+ 1 Von insgesamt 103 Teilen (100+1+1+1) befinden sich 101 im Inneren der Vakuole, das Konzentrationsverhältnis ist also 101/2 ≈ 50/1. Im Inneren der Vakuole befindet sich etwa 50 mal mehr Neutralrot. vii) Würde sich das Neutralrot ebenfalls im Inneren der Vakuolen ansammeln, wenn es einen pKs 2 aufweisen würde? Unter diesen Bedingungen ergäben sich folgende Konzentrationsverhältnisse: (ausgehend von der am wenigsten konzentriert vorliegenden Spezies, HNeu+ im Cytosol). Die Konzentrationen in Cytosol und Vakuole sind also etwa gleich (rechnerisch 100‘100/100‘001) Säure/Base-Gleichgewichte 29 leis Vakuole, pH 5 Cytosol, pH 7 Neu Neu HNeu+ : 100‘000 100‘000 : : HNeu+ 100 1 Alkaloide 6. Dabei kommt den Pflanzen eine Eigenschaft der Aminogruppen sehr zugute. Welche und warum? Alkaloide werden bei tiefem pH (in den Vakuolen) besonders stark ionisch, werden hier also durch Ion trapping festgehalten (siehe oben). Zitronensäure Zitronen verwenden zum Ansäuren ihrer Vakuolen v.a. Zitronensäure, Äpfel z.b. Äpfelsäure. Warum sind diese Säuren sehr viel besser geeignet als z.B. Essigsäure (Ethansäure)? Anders gesagt: warum würde es sehr viel mehr Energie kosten, Vakuolen mit Essigsäure sauer zu halten? Zitronensäure, Dihydrogencitrat-, Hydrogencitrat- und Citrat-Ionen OH OH O O O - O O O O - H+ O - H+ O - H+ O HO + H+ HO + HO + O HO HO +H HO O - O +H HO O - - HO O O - - O O Äpfelsäure, Hydrogenmalat- und Malat-Ionen OH O O O O + -H O HO - OH + H+ O + O HO - OH -H O + H+ O - OH Essigsäure hingegen könnte aus den Vakuolen entweichen, so dass dort der pH dauernd steigen und im Cytosol der pH sinken würde. Die Zellen müssten die Essigsäure unter Energieaufwand dauernd zurückpumpen. Zitronensäure und Äpfelsäure bleiben auch bei tiefem pH so hydrophil, dass sie die Membran nicht durchdringen: sie weisen ja mehrere Carboxylgruppen auf (mit höherer Wahrscheinlichkeit ist das Teilchen somit ein Ion) und viele mögliche H-Brücken.. Säure/Base-Gleichgewichte 30 leis D: Ion trapping (Ionenfalle) in der Pharmakologie Naproxen 8. Naproxen wird aus dem Magen (pH etwa 2) sehr gut in den Körper aufgenommen. Wieso? Hier liegt Naproxen protoniert und damit neutral vor und kann Zellmembranen gut durchdringen. 9. Viele Amine und Carbonsäuren verschwinden mit der Zeit aus dem Blut, die einen sammeln sich im sauren Magen an, die anderen im oft leicht basischen Urin. Welche Stoffklasse endet wo? Sie sammeln sich jeweils dort an, wo sie zu möglichst hohen Anteilen ionisch (elektrisch geladen) vorliegen: Ion Trapping. Also die Amine bei tiefem pH, im Magen, und die Carbonsäuren bei hohem pH, im Urin. Nervengifte und Lokalanästhetika 10. Tetrodoxin hemmt spannungsaktivierte Natriumkanäle, wie sie in motorischen und sensorischen Nervenzellen auftreten. Neuronen im Gehirn sind hingegen kaum betroffen. Welche Symptome zeigt eine Tetrodoxin-Vergiftung daher und wie kann man Vergifteten helfen? Typische Symptome: Lähmungserscheinungen und Unempfindlichkeit (Anästhesie), Lähmung der Atemmuskulatur kann es zum Erstickungstod führen, künstliche Beatmung bis zum Abklingen der Vergiftungserscheinungen das Leben retten. Lokalanästhetika Lidocain, pKS der konjugierten Säure: 7.7 Bupivacain, pKS der konjugierten Säure: 8.1 11. Wie viele andere Amine (organische Stickstoffverbindungen) verstopfen diese Stoffe Kationenkanäle. Warum ist es nicht sehr erstaunlich, dass viele Amine ausgerechnet Kationenkanäle verstopfen? Amine können H+ aufnehmen, werden damit zu Kationen und haften an den (partiell) negativ geladenen „Innenauskleidungen“ von Kationenkanälen. 12. Skizziere die Pufferkurven von Lidocain und Bupivacain. 13. Für die klinische Wirksamkeit ist es günstig, dass diese Lokalanästhetika im Gleichgewicht höhere Konzentrationen im Zellinneren haben als im Blut. Woran liegt dies? Cytosol: pH7, Blut pH 7.4, also ist der pH im Zellinneren etwas tiefer (vgl. Formelsammlung) , hier werden also Amine per Ion-Trapping aufkonzentriert. Da die Unterschiede relativ klein sind, ist auch die konzentration im zellinneren nur wenig grösser. Cytosol, pH 7.0 Blut, pH 7.4 Lid Lid HLid+ 5 : 1 : 1 : HLid+ 2 14. Lidocain und Bupivacain wirken unterschiedlich. Die Wirkung von Lidocain setzt viel schneller ein, dafür wirkt es nur kurz (1-2h), während die Wirkung von Bupivacain erst nach 4-5 h Säure/Base-Gleichgewichte 31 leis wieder abflaut.Letzteres hängt damit zusammen, dass es deutlich länger dauert, bis Körper das Bupivacain wieder los ist. Erkläre diese zwei Unterschiede anhand der Pufferkurven. Der pKS von Lidocain ist etwas tiefer, also liegt bei gleichem pH etwas mehr der basischen, hydrophoben Form vor, Lidocain kann also die Membran schneller durchdringen, gelangt schneller in die Zelle, von innen an die Kationenkanäle und kann diese schneller blockieren. Umgekehrt verlässt es die Zelle auch wieder schneller, wenn ausserhalb die Konzentration abnimmt, daher wird es auch schneller wieder ausgewaschen und wirkt weniger lange. Cytosol, pH 7.0 Blut, pH 7.4 Bup 1 : HBup+ 5 Cytosol, pH 7.0 Blut, pH 7.4 Lid 1 : HLid+ 2 F: Elektrophorese Kationen Elektr. neutral Anionen Beschrifte oben ungeladene, sowie negativ und positiv geladene Teilchen. 1. Überlegung: Zu welchem Pol (Pluspol oder Minuspol) hin sollten sich folgende Stoffe bei pH 5.5 bewegen (siehe nächste Seite) Proben Ungefährer pKS BX Bromphenolblau pKS 3.5 Konj. Säure Farbe und Ladung Gelb (-) Konj Base Farbe und Ladung pH 5.5 wanderung richtung Violettblau (2-) Pluspol (Anode) (schnell) Pluspol (Anode) Minuspol (Kathode) Bleibt im Slot (ganz langsam richtung Pluspol Pluspol (Anode) Ne Ni Xylencyanol Neutralrot Nitrophenol pKS 7.5 pKS 7 Türkis (-) Blaurot (+) Farblos (0) Orangegelb (0) Gelb (-) Mg Methanilgelb pKS 2 Rot (0) Gelb (-) Säure/Base-Gleichgewichte 32 leis Mo Mr Methylorange Methylrot pKS 3.5 pKS 5 Rot (0) Rot (0) Gelb (-) Gelb (-) Pr Phenolrot pKs 8 Gelb (0) Rot (-) U1 U2 K CA Universalindikator 1 Universalindikator 2 CuCl2 CuCl2 + Ammoniak Pluspol (Anode) Pluspol (Anode), etwas langsamer als Methylorange, da jedes Teilchen zeitweise ungeladen. Bleibt im Slot (ganz langsam richtung Pluspol Minuspol (Kathode) Minuspol (Kathode) Türkis Dunkelblau 2. Warum wird Neutralrot bei den mittleren N-Atomen protoniert, nicht aber bei den anderen NAtomen? Erkläre im Orbitalmodell bzw. mit Grenzformeln. Die nEP der äusseren N-Atome beteiligen sich am konjugierten System, was nur möglich ist, solange sie nicht protoniert sind. Die mittleren N-Atome hingegen sind bereits mit anderen Elektronenpaaren am konjugierten System beteiligt, die nEPs können also daran nicht auch noch teilhaben. Diese Beteiligung am konjugierten System ist in folgenden Grenzformeln und dem darunter dargestellten Ladungswolkenbild erkennbar (seitliche Überlappung der p-Orbitale ist der besseren Übersichtlichkeit halber nicht durch Striche symbolisiert). H + CH3 N N N H H CH3 N H H + CH3 N N N H H CH3 N H3C H N H3C N H3C N N CH3 CH3 3. Warum sind folgende Stoffe farbig und warum kommt es bei ihnen bei Säure/BaseReaktionen zu einem Farbwechsel? Diese Stoffe sind farbig, weil die Teilchen ausgedehnte konjugierte Systeme aufweisen. Bei Säure/Base-Reaktionen werden Atome aus diesem konjugierten System protoniert (bzw. deprotoniert), so dass die Elektronenbahnen leichte Änderungen erfahren. Dadurch werden andere Wellenlängen absorbiert und andere wahrgenommen, die Farben verändern sich. 4. Die Säure Bromphenolblau gibt ein bestimmtes H ab. Warum kann dieses H abgespalten werden? 5. Schätze den pKS-Wert folgender Stoffe mit Hilfe von Pufferlösungen ab. Halte dabei fest, welche Spezies welche Farbe aufweist. Siehe Tabelle oben Säure/Base-Gleichgewichte 33 leis E: Aminosäuren, Peptide, Eiweisse 6. Zeichne die Pufferkurve für die drei Spezies der Aminosäure Glycin 7. Wandert Glycin bei einer Elektrophorese bei pH 7 zum Pluspol oder Minuspol? In erster Näherung wandert Glycin bei pH 7 nicht: Das Teilchen liegt ja vorwiegend ungeladen vor. Gemäss Hendersson Hasselbalch liegt zu jedem Zeitpunkt nur jedes 600ste Teilchen in der negativ geladenen Form vor, also liegt jedes einzelne Teilchen nur zu 1/600 der Zeit als anionische Spezies vor. Gleichzeitig ist jedes Teilchen nur zu 1/45‘000 der Zeit ein Kation. Nun überwiegt aber der Anteil der Anionen gegenüber den Kationen ganz leicht, also wird das Teilchen sehr langsam richtung Pluspol wandern. Bemerkung: Der Durchschnitt der pKSWerte beträgt 6.0, also wird Glycin bei pH 6 überhaupt nicht wandern (die Probe diffundiert bei pH 6 nur auseinander). H2N-R-COO H3N-R-COO H3N-R-COO H3N-R-COOH Säure/Base-Gleichgewichte 34 leis 10. 11. Wandert Lysin bei pH 6 zum Pluspol oder Minuspol? Wie den Pufferkurven entnommen werden kann, ist Lysin bei pH 6 vorwiegend einfach positiv geladen (zwei positiv und eine negativ geladene Gruppe) Lysin wird somit zum Minuspol wandern. O H2N O - NH2 O + H3N O - NH2 O 12. Mit einem Gemisch aus Lysin, Alanin und Asparaginsäure wird eine Papier-Elektrophorese bei pH 6 durchgeführt. Skizziere den Papierstreifen und gib für jede Aminosäure den Ort an, wo du sie erwartest. Die Wanderungsgeschwindigkeit hänge nur von der durchschnittlichen Gesamtladung der Teilchen ab. + H3N O - + NH3 O + Bei pH 6 heben sich die Ladungen der Hauptkette H3N (Amino- und Carboxyl-Gruppe) weitgehend auf, denn der pH liegt ziemlich genau zwischen den beiden pK S+ NH3 Werten. Bei Alanin kommt keine weiter Ladung dazu. Weil der Durchschnitt der beiden pKS-werte von Alanin praktisch genau bei 6 ist (6.11), bleibt diese Aminosäure stehen – höchstens ganz langsam läuft sie Richtung Pluspol, weil der pH ganz leicht näher beim oberen pKs liegt. Lysin weist eine positiv geladene Seitenkette auf (siehe oben), ist meist insgesamt einfach positiv geladen und wandert zum Minuspol. Asparaginsäure weist hingegen bei pH 6 eine negativ geladene Carboxylat-Gruppe auf und wandert zum Pluspol. 13. Peptide und Proteine entstehen durch Zusammenhängen von Aminosäuren. Aus welchen zwei Aminosäuren besteht das folgende Peptid und wohin wandert dieses bei pH 6 wohl: zum - Minus- oder Pluspol? O Nimm in grober Näherung an, dass die pKS-Werte der Amiosäuren sich beim Zusammenkoppeln nicht verändern. O H H HN O Das Peptid besteht aus kondensierten Gylcin und Lysin. Seine Gruppen zeigen gerade die vorwiegende Ladung bei neutralem pH: Carboxyl-Gruppen deprotoniert und AminoGruppen protoniert. Das Teilchen trägt insgesamt eine positive Ladung und wandert zum Minuspol. + H NH3 + H3N OH