Hepatitis-Update Univ.-Prof. Dr. Peter Ferenci 17.09.2015
Werbung
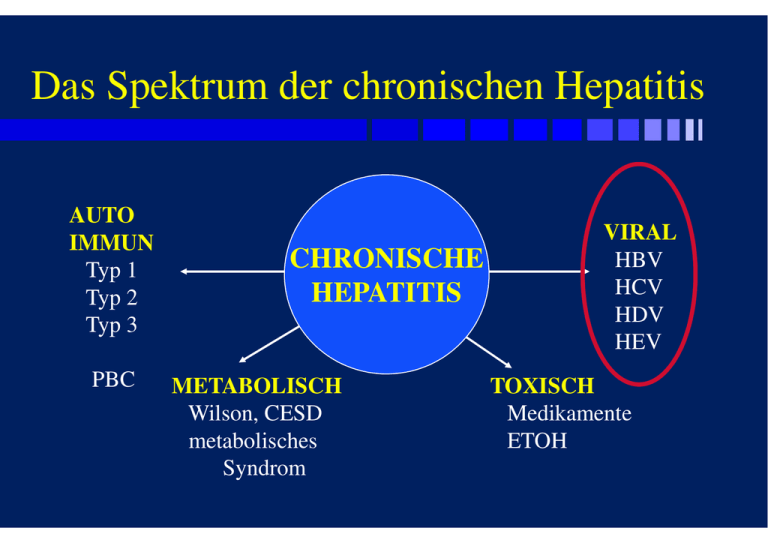
Das Spektrum der chronischen Hepatitis AUTO IMMUN Typ 1 Typ 2 Typ 3 PBC CHRONISCHE HEPATITIS METABOLISCH Wilson, CESD metabolisches Syndrom VIRAL HBV HCV HDV HEV TOXISCH Medikamente ETOH Die HCV Revolution Nov. 2011 HEPATITIS C Diagnose – anti-HCV (2. oder 3.Generation) – HCV-RNA (falls anti-HCV neg.) Therapieentscheidung – HCV-RNA – Genotypen – Quantifizierung der HCV-RNA Therapieüberwachung – Transaminasen, HCV-RNA Naturgeschichte der Hepatitis C Virus infektion Faktoren die Progression beeinflussen: Alkohol Übergewicht chronische Männliches Geschlecht Hepatitis Alter Dekompensation 50-80% 1%/a Zirrhose HCV 3-5%/a 1-2%/a 20-50% HCC Spontanheilung 0 10 20 30 Jahre 40 50 HCV Infection: Extrahepatische Manifestationen Hematologic • • • • Mixed cryoglobulinemia Aplastic anemia Thrombocytopenia Non-Hodgkin’s β-cell lymphoma Dermatologic • Porphyria cutanea tarda • Lichen planus • Cutaneous necrotizing vasculitis Renal • Glomerulonephritis • Nephrotic syndrome Endocrine • Anti-thyroid antibodies • Diabetes mellitus Ocular • Corneal ulcer • Uveitis Vascular • Necrotizing vasculitis • Polyarteritis nodosa Neuromuscular • Weakness/myalgia • Peripheral neuropathy • Arthritis/arthralgia Autoimmune Phenomena • CREST syndrome Salivary • Sialadenitis Hadziyannis SJ. J Eur Acad Dermatol Venereol. 1998;10:12-21. Formen der chronischen Hepatitis C alle anti HCV+ GPT HCVRNA HBsAg anti-HIV Abgeheilte HC normal neg - - Carrier??? normal pos - - normal bis erhöht pos - - erhöht pos pos/neg pos/neg Chronische HC Koinfektion Was braucht man zur Indikationsstellung zur Therapie bei Hepatitis C (laut Hauptverband) • HCV Viruslast, HCV Genotyp • Fibrosegrad (Genehmigung nur für F≥2) • Sonographie der Leber HISTOLOGISCHE STADIEN (METAVIR) F0 NO FIBROSIS F1 PORTAL FIBROSIS F2 FEW SEPTA F3 NUMEROUS SEPTA F4 CIRRHOSIS HISTORISCH !! Menghini, Gastroenterology 1958 Nicht-invasive Fibrosemarker • • • • • • • FIB-4 APRI FibroTest HepaScore FibroMeter ELF Fibroskan } kommerziell, teuer, nicht notwendig Fibroskan APRI und FIB4 zum Fibrose Staging FIB4 Alter (a) x GOT (IU/L) Thrombo (109/L) x √GPT (IU/L) Cut off F4 > 3.25 AST to Platelet Ratio Index (APRI) GOT aktuell /GOT oberer Normalwert Thrombo (109/L) Cut off F4 > 1 HCV Life Cycle and DAA Targets Receptor binding and endocytosis Transport and release Fusion and uncoating ER lumen (+) RNA LD LD Translation and NS3/4 protease polyprotein inhibitors processing Membranous web LD ER lumen NS5A* inhibitors *Role in HCV life cycle not well defined Adapted from Manns MP, et al. Nat Rev Drug Discov. 2007;6:991-1000. Virion assembly NS5BRNA polymerase inhibitors replication Nucleoside/nucleotide Nonnucleoside In Österreich zugelassene DAA zur Therapie der chronischen Hepatitis C • 12/2013 Sofosbuvir (SOVALDI®)*, dzt. gelbe Box • 5/2014 Simeprevir (OLYSIO®) • 8/2014 Daclatasvir (DAKLINZA®) • 12/2014 Sofosbuvir/Ledipasvir (HARVONI®) • 1/2015 Abbvie Combo ( Paritaprevir/r+Ombitasvir [VIEKIRAX®]+ Dasabuvir [EXVIERA®]) * Nur in Kombination mit Ribavirin oder anderen DAA Die HCV Revolution Zulassung IFN/(RBV) freier Therapien in Österreich • 12/2013 Sofosbuvir (SOVALDI®)*, dzt. gelbe Box • 5/2014 Simeprevir (OLYSIO®) • 8/2014 Daclatasvir (DAKLINZA®) • 12/2014 Sofosbuvir/Ledipasvir (HARVONI®) • 1/2015 Abbvie Combo (VIEKIRAX®+EXVIERA®) * Nur in Kombination mit Ribavirin oder anderen DAA September 2015 Von der Krankenkasse refundierte DAA zur Therapie der chronischen Hepatitis C Nonnuc NS5B Hemmer GT 1 PI + NS5A Hemmer GT 1, 4 NS5B Hemmer + NS5A Hemmer Alle GT Ausnahme: Sovaldi+Daklinza für GT3, Sovaldi+Ribavirin für GT2 Heilungsraten bei GT1 mit in Österreich zugelassenen Therapien ohne RBV Nach Afdahl,Kowdley, Zeuzem,Feld,Ferenci,Poordad alle NEJM 2014, Andreone Gastroenterology 2014 mit RBV Sofosbuvir/Ledipasvir/Ribavirin in decompensated cirrhosis and post LTX Charlton et al, Gastroenterology 2015 Vergleich der zugelassenen Therapien Beide Therapien sehr effektiv mit Anspechraten von 85-100% SOF/LDV Abbvie 3D Genotyp Pangenotypisch* Genotyp 1 und 4 F0-F3 Ja (8-12 Wochen) Ja (12 Wochen) Ribavirin notwendig? Bei Nonrespondern Bei GT1a F4 Child A Ja (12-24 Wochen) Ja (24 Wochen) F4 Child B/C Ja (12-24 Wochen) Nein!! Nierenversagen Vorsicht! Ja?? St.p. LTX ja Ja (F0-F2) PREIS ?? ?? * Schwäche bei Gt 3a UNGEKLÄRTE FRAGEN • Notwendige Therapiedauer (8-24 Wochen) • Welcher Patient braucht Ribavirin (ist für Nebenwirkungen verantwortlich • Was bringt die Therapie Transplant freies Überleben F0 - F2 Warten? PEG/RBV/PI? F3 / F4 Priorität!!! Viele vertragen kein IFN 719 patients treated between 1987 and 2012 162 with cirrhosis at baseline Mean follow up 7.6 years (1-21.1 years) 553 SVR, 166 NR Rutter et al, APT 2015 Sofosbuvir/Ledipasvir bei dekompensierter Zirrhose Verbesserung des MELD Score Flamm et al, AASLD 2014 Wichtige nichtmedikamentöse Interventionen bei Nonrespondern • Lebensstilmodifikation • Alkoholabusus - stop • Marihuana - stop • Übergewicht/Diabetes– Diät, Bewegung • Kaffee – mehr trinken! • HCC Screening HEPATITIS B akute Hepatitis B » anti-HBc IgM, » Serokonversion HBsAg / anti-HBs chronische Hepatitis B » HBsAg, HBeAg, anti-HBe, Transaminasen – Diagnose: » 6-monatige Beobachtung – Therapieentscheidung und -überwachung: » HBV-DNA quantitativ, Transaminasen Impfung ? » anti-HBs Naturgeschichte der Hepatitis B Virus Infektion HBsAg Elimination <1%/a HBsAg Carrier akute 45% ikterisch Hepatitis 50% anikterisch <1% fulminant 10-15% /a <5% HBV chronische Hepatitis ? Zirrhose Jahre ? ? HCC Formen der chronischenHepatitis B alle HBsAg +! GPT HBeAg antiHBe anti-δ HBsAg Carrier normal neg pos neg HBeAg+ CHB erhöht pos neg neg antiHBe+ CHB erhöht neg pos neg Hep. D erhöht +/- +/- pos Therapieziele bei chronischer Hepatitis B HBeAg neg→ Anti-HBe HBeAg Positiv HBV DNA < 105 Normale Transaminasen HBeAg Negativ Besserung der Histologie HBsAg neg→ Anti-HBs Rolle der HBeAg Serokonversion bei chronischer Hepatitis B IFN unbehandelt kumulative 5 Jahresserokonversionsrate HBeAg HBsAg antiHBe antiHBs 56.0% 11.6% 28% 0% kumulative 5 Jahresüberlebensrate HBeAg neg HBeAg pos 98% 78% Niederau et al, NEJM 1996; 103 IFN-behandelte, 53 unbehandelte Pats. 100% 38% Incidence/100,000 pyfu HCC incidence rate by cohort entry (Taiwan cohort) 1400 1149,5 1200 953,1 1000 800 600 400 200 314,9 145,2 112,3 <300 300-<10,000 0 10,000<100,000 HBV DNA (copies/ml) 100,000<1,000,000 >1,000,000 Therapieindikation bei chronischer Hepatitis B GPT normal oder max. 2fach erhöht GPT > 2 fache der Norm keine Therapie, beobachten HBV DNA HBV DNA < 2000 IU > 2000 IU < 2000 IU F0-F1 LBX F2-F4 > 2000 IU Therapie klinische Hinweise auf Zirrhose HBV-DNA pos. Wann Interferon? Junge Patienten HBeAg positiv Keine (dekomp.) Zirrhose HBV-DNA (<2x105IU/ml) Hohe ALT (> 2-5 x ULN) HAI>4 Keine Kontraindikationen HBV-Genotyp A,B PEG-IFN +/- Lamivudin: Loss of HBe-Antigen 50 Patients (%) • • • • • • • • 47% 44% 40 28% 30 25% 20 10 0 A B n=90 n=23 C D n=39 n=103 Janssenet al, Lancet 2005 Buster et al. Gastroenterology 2009 Therapie der Hepatitis B Verfügbare Substanzen Adefovir (ADV, Hepsera®, 10mg/d) HISTORISCH! 1998 Lamivudin (LAM, Zeffix®, 100mg/d) HISTORISCH! 1982 Interferon-alpha (IntronA®, Roferon®) HISTORISCH! Peginterferon-alpha (Pegasys® 180µg) Entecavir (ETV, Baraclude®, 0.5mg/d) Telbivudin (LdT, Sebivo®) Tenovofir (TDV, Viread®) 2004 2006 2008 2010 Nucleosidanaloga Nucleotidanalogon Interferon NUC´s: HBV DNA < Limit of detection 48-52 Wochen: kein “head to head” HBeAg positive HBeAg negative 100 91 88 74 72 % PATIENTEN 90 67 60 51 50 39 21 0 LAM ADV ETV LdT TDF EASL Treatment Guidelines., J Hep 2009 HBeAg und HBsAg Verlust 48-52 Wochen: kein “head to head” % PATIENTEN 100 HBeAg loss HBsAg loss 50 30 22 3 <1 0 PegIFN 26 24 LAM 21 22 <1 ADV 1.7 ETV 3 <1 LdT Hoofnagle et al., Hepatology 2007, EASL Treatment Guidelines., J Hep 2009 TDF Pros & Cons: PEG-IFN vs. NUC´s Pegyliertes Interferon alfa Nucleoside/Nukleotide Vorteile Begrenzte (fixe) Dauer Fehlen von Resistenzen Höhere Raten (≥30%) von HBeAg und HBsAg Serokonversion Potente antivirale Substanzen Gute Verträglichkeit Orale Anwendung Auch bei Leberzirrhose Moderater antiviraler Effekt Schlechte Verträglichkeit Subcutane Anwendung Bei dekompensierter Leberzirrhose kontraindiziert Unklare Therapiedauer Risiko der Resistenz Niedrigere Raten der HBeAg und HBsAg Serokonversion Nachteile Therapie der Hepatitis D IFN und Nukleosidanaloga: nur bescheidene Wirkung NEUE HOFFNUNG: Farnesyltransferasehemmer (Koh et al, AASLD 2014) Myrcludex (Entry Inhibitor, Urban et al, AASLD 2014) Risikogruppen für GT3 Infektion: Verzehr von rohen Schweinefleisch Jäger, Tierpfleger, Fleischhauer GT3 GT1 Hepatitis E bei Blutspendern • 225 000 Blutkonserven (SO England) wurden retrospektiv auf HEV RNA untersucht • 79 Spender waren virämisch (Genotype 3 HEV; Prävalenz: 1/2848 • Die meisten virämischen Spender waren anti-HEV negativ zum Zeitpunkt der Spende • 62 Konserven wurden verwendet, 18/43 (42%) der nachuntersuchten Empfänger wurden infiziert. • Bei Immunosupprimierten verzögerte Klärung oder Chronizierung (bei 10). Hewitt et al, Lancet 2014 Chronische HEV bei Transplantierten GT 1 3.Welt Übertragung: Feco-oral GT3 Europa N.America Übertragung: Schweinefleisch Plischke et al- American Journal of Transplantation 2012; 12: 3128–3133 Zusammenfassung Therapie der chronischen Virushepatitis kann Morbidität und Mortalität verhindern Risikogruppen gzielt testen Impfen! Erhöhte Transaminasen (oder der GGTP) sind nicht notwendigerweise Indikatoren einer schwerwiegenden Erkrankung Der chronisch Leberkranke bedarf einer kompetenten Dauerbetreuung











