Liebe/r Frau Mustermann
Werbung

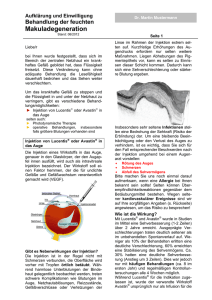
Aufklärung und Einwilligung xxx Behandlung der CNV bei Angioid streaks Stand: 04/2015 Liebe/r Frau Mustermann, bei Ihnen wurde festgestellt, dass sich im Bereich der zentralen Netzhaut ein krankhaftes Gefäß auf Grund einer sehr seltenen Gewebsschwäche gebildet hat, das Flüssigkeit freisetzt. Diese Veränderung kann ohne adäquate Behandlung die Lesefähigkeit dauerhaft bedrohen und das Sehen weiter verschlechtern. Um das krankhafte Gefäß zu stoppen und die Flüssigkeit in und unter der Netzhaut zu verringern, gibt es verschiedene Behandlungsmöglichkeiten: ► Injektion von Avastin in das Auge selten auch: ► Photodynamische Therapie Injektion von Avastin in das Auge Die Injektion eines Wirkstoffs in das Auge, genauer in den Glaskörper, der den Augapfel innen ausfüllt, wird auch als intravitreale Injektion bezeichnet. Der Wirkstoff soll einen Faktor hemmen, der für undichte Gefäße und Gefäßwachstum verantwortlich gemacht wird (VEGF). Seite 1 Beeinträchtigung oder den Verlust des Auges zu verhindern, ist es wichtig, dass Sie sich für den Fall entsprechender Beschwerden nach der Injektion umgehend bei einem Augenarzt vorstellen: Rötung des Auges Schmerzen Abfall des Sehvermögens Bitte machen Sie uns noch einmal darauf aufmerksam, wenn eine Allergie bei Ihnen bekannt sein sollte! Selten können Überempfindlichkeitsreaktionen gegenüber dem Betäubungsmittel bestehen. Wegen seltener kardiovaskulärer Ereignisse sind wir auf Ihre sorgfältigen Angaben (s. Rückseite) angewiesen, um das Risiko zu besprechen! Eine evtl. Schwangerschaft sollte ausgeschlossen oder durch sichere Verhütungsmethoden für mind. 6 Wochen vermieden werden, weil schädigende Auswirkungen auf ein ungeborenes Kind durch die lokale Gabe von Avastin nicht ausgeschlossen werden können. Bitte halten Sie auch mit uns Rücksprache, falls Sie aktuell stillen. Wie ist die Wirkung? Gibt es Nebenwirkungen der Injektion? Die Injektion ist in der Regel nicht mit Schmerzen verbunden, die Oberfläche wird vorher mit Tropfen örtlich betäubt. Während harmlose Unterblutungen der Bindehaut gelegentlich beobachtet werden, treten schwere Komplikationen wie Blutungen im Auge, Netzhautablösungen, Reizzustände, Gefäßverschlüsse oder Verletzungen der Linse im Rahmen der Injektion extrem selten auf. Kurzfristige Erhöhungen des Augendrucks erfordern nur selten weitere Maßnahmen. Liegen Abhebungen des Pigmentepithels vor, kann es selten zu Einrissen dieser Schicht kommen. Dadurch kann sich eine Sehverschlechterung oder stärkere Blutung ergeben. Insbesondere sehr seltene Infektionen stellen eine Bedrohung der Sehkraft (Risiko der Erblindung) dar. Um eine bleibende Mit Avastin® wurde in Fallserien im Mittel eine Sehverbesserung (1 Zeile) über 1-2 Jahre erreicht. Ausgeprägte Verschlechterungen traten deutlich seltener als im unbehandelten Spontanverlauf auf. In der Regel muss auf Grund der Aggressivität der Behandlung mit vielen Behandlungen (7-8 Behandlungen pro Jahr) gerechnet werden. Regelmäßige Kontrolluntersuchungen (im Abstand von ca. 4 Wochen) sind in den ersten Monaten notwendig. Für diese Indikation sind andere Wirkstoffe (Lucentis®, Eylea®) noch nicht zugelassen. Das verwandte Avastin® wurde ursprünglich nur als Infusion für die Behandlung von Darmkrebs eingesetzt, eine Zulassung für die Anwendung am Auge liegt nicht vor. So muss man berücksichtigen, dass für Avastin® wenige kontrollierte Studien zur Wirksamkeit und Sicherheit vorliegen. Die Behandlung mit Avastin® erfolgt außerhalb der zugelassenen Indikation (Off-labelBehandlung). Insoweit besteht keine Produkthaftung des pharmazeutischen Unternehmens. Das bedeutet aber nicht, dass die Behandlung ohne Haftung stattfindet. Wie üblich haften der Arzt für die CNV infolge PXE xxx rechtes Auge linkes Auge Qualität seiner Behandlung und der Apotheker für die Qualität der von ihm durchgeführten Herstellung des anwendungsfertigen Arzneimittels. Die Aufteilung eines Medikaments (sog. Auseinzelung) kann evtl. ein zusätzliches Risiko für Verunreinigungen bedeuten. Um dieses Risiko zu verringern, hat die AOK die kooperierenden Apotheker vertraglich verpflichtet, strengste Qualitätsanforderungen einzuhalten. In bestimmten Situationen (Nachlassen der Wirkung, Nichtansprechen auf ein Medikament) kann ein Wechsel der Wirkstoffe sinnvoll sein. Allerdings sind mögliche Alternativen für diese Erkrankung noch nicht zugelassen; für Lucentis® wurden bisher Ergebnisse einer kontrollierten Studie berichtet. Verhaltensregeln nach der Injektion: Sie dürfen in den ersten 24 Stunden nach der Operation kein Kraftfahrzeug oder Zweirad steuern, keine gefährlichen Tätigkeiten ausführen (z.B. Arbeiten an gefährlichen Maschinen oder ohne festen Halt). Sie sollten zunächst auf das Tragen von Kontaktlinsen und auf das Schminken der Augen verzichten und nicht am Auge reiben. Eine augenärztliche Untersuchung innerhalb von 5 Tagen bzw. eine weitere innerhalb von 3 Wochen wird empfohlen. Photodynamische Therapie (PDT) Im Rahmen der PDT soll das Gefäß mit einem lichtsensitiven Farbstoff (Visudyne) verschlossen werden, der über Laserlicht aktiviert wird. Die Therapie kann je nach Ansprechen einer Injektionstherapie eher die Stabilisierung als eine Verbesserung der Sehkraft unterstützen. Bei oder nach der Infusion kann es an der Infusionsstelle zu Schmerzen kommen, selten sind Überempfindlichkeitsreaktionen, Kopfschmerzen, Übelkeit, Schwindelgefühl und Blutdruckabfall. Mögliche Nebenwirkungen können vorübergehend reduziertes Sehvermögen, Blutungen im Auge. Verhaltensregeln nach der Behandlung: Nach der PDT werden Ihre Haut und Ihre Augen stark lichtempfindlich. Um ernste Reaktionen, ähnlich einem schweren Sonnenbrand, zu vermeiden, ist es erforderlich, dass Sie Ihre Augen und Haut in den ersten 48 Stunden vor Sonnenbestrahlung und Innenbeleuchtung Seite 2 schützen. Wenn Sie sich im Freien aufhalten, sollten Sie entsprechende Kleidung und eine dunkle Sonnenbrille tragen. Außerdem sollten Sie sich keinem starken künstlichen Licht aussetzen (Solarium, Op-Lampe). Patientenname: Birgit Mustermann geb. am 24.12.2008 Inhalte des Gesprächs ___________________________________ ___________________________________ ___________________________________ ___________________________________ ___________________________________ ___________________________________ Für die Injektion von Avastin® müssen wir eventuelle Kontraindikationen oder Begleiterkrankungen kennen. Bitte lesen Sie daher die Liste aufmerksam durch, ob folgende Punkte bekannt sind: Schwangerschaft / Minderjährigkeit (Therapiemöglichkeiten evtl. eingeschränkt) akute (intraokulare) Entzündung (akuter) Herzinfarkt, Schlaganfall vor kurzem (< 6 Monate) früher:__ (instabile) Angina pectoris (schlecht eingestellter) Bluthochdruck arterielle Verschlusskrankheit Niereninsuffizienz Glomerulonephritis neurodegenerative Erkrankung (ALS, Demenz) Infektionserkankungen, zB Hep HIV Blutungsneigung, z.B. ASS Marcumar Allergien oder Überempfindlichkeit gegen: Jod Pflaster Medikamente: ____________ Latex Penicillin Weitere Besonderheiten/Erkrankungen: ___________________________________ ___________________________________ Bitte sagen Sie uns, wenn Sie noch Fragen haben oder ergänzende Literatur wünschen. Die Art meiner Erkrankung und ihre möglichen Folgen und Komplikationen sowie die Behandlungsalternativen und deren Zweck sind mir von Herrn/Frau _______________ verständlich und ausführlich in einem persönlichen Gesprächs geschildert worden. Ich habe keine weiteren Fragen, fühle mich ausreichend aufgeklärt und willige hiermit nach ausreichender Bedenkzeit in folgende Behandlung ein: __________________________________ CNV infolge PXE rechtes Auge linkes Auge Mit unvorhersehbaren, notwendigen Erweiterungen des Eingriffes bin ich ebenfalls einverstanden. Ich versichere, dass ich alle mir bekannten Leiden und Beschwerden genannt habe. ________________ Unterschrift Patient ________________ Unterschrift Ärztin/Arzt Ort, den xxx Seite 3