Buch 5.indb - fructose.at
Werbung

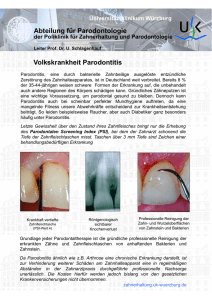
25 Kapitel 25 ERNÄHRUNG BEI KARIES UND PARODONTALEN ERKRANKUNGEN I. Kapferer 1. Einleitung 2. Der dentale Biofilm Karies, Gingivitis und Parodontitis sind die häufigsten Infektionserkrankungen weltweit. In Deutschland ist nur ca. 1 % der Erwachsenen kariesfrei. Über die Prävalenz parodontaler Erkrankungen gibt es unterschiedliche Angaben, was daran liegt, dass der Übergang von einer Gingivitis zu einer Parodontitis nicht genau definiert ist. In einer groß angelegten epidemiologischen Studie in den USA (NHANES III) wurde für die über 60-jährige Bevölkerung eine Prävalenz der Parodontitis von 17 bis 39 Prozent angegeben (Borrell et al., 2005). Andere Studien sprechen von Parodontitisprävalenzen bis zu 95 Prozent, weil in diesen Studien auch leichtere Formen der Parodontitis inkludiert wurden (Bourgeois et al., 2007). Rasch fortschreitende Formen der Parodontitis im Kinder-, Jugend- und jungen Erwachsenenalter (= aggressive Parodontitis) sind relativ selten. Sie stellen aber für den Betroffenen und seinen Zahnarzt ein schwerwiegendes Problem dar, da es hierbei häufig zu sehr frühem Zahnverlust kommt. Essgewohnheiten und Nahrungszusammensetzung haben einen großen Einfluss auf Erkrankungen der Mundhöhle. Zum einen spielt die lokale Wirkung der Nahrung während des Kauaktes eine Rolle, zum Beispiel die Härte der Nahrung und die Verweildauer in der Mundhöhle. Zum anderen werden Nahrungsbausteine systemisch über den Blutweg für Auf- und Umbauprozesse an Zähnen und Zahnhalteapparat zur Verfügung gestellt. Hauptursache von Karies und den parodontalen Erkrankungen ist der Zahnbelag, „Plaque“ oder auch „dentaler Biofilm“ genannt. Der dentale Biofilm besteht zu 60 –70 % aus bakteriellen und nicht-bakteriellen (Pilze, Protozoen, Viren) Mikroorganismen, sowie aus Wirtszellen, die in eine interzelluläre Matrix eingebettet sind. Diese Matrix besteht aus Polysacchariden und Wasser und wird von den Mikroorganismen selbst gebildet. Schon wenige Minuten nach dem Zähneputzen lagert sich auf der gesäuberten Zahnoberfläche aus dem Speichel eine 1 μm dicke zellfreie Glykogenschicht ab. Dieses Pellikel schützt die Zähne vor dem Austrocknen. Es dient aber auch speziellen Bakterien (Pionierkeimen) als Substrat zum Andocken an die Zahnoberfläche. Diese Pionierkeime, vor allem Streptokokken und Aktinomyzeten, können sich über Oberflächenmoleküle (Adhäsine) an Pellikelrezeptoren anheften. Weitere Mikroorganismen docken sich nun über Fimbrien, Pili und die Glykokalyx an die Pionierkeime an, und durch Vermehrung entstehen Mikrokolonien. Nach sieben Tagen ist der Biofilm 100 bis 300 Bakterienzellschichten dick. Ein Milligramm ausgereifte Plaque enthält mehr als 108 Mikroorganismen (Lang et al., 2003). Insgesamt gibt es etwa 500 verschiedene Bakterienspezies in der Mundhöhle. Die bakterielle Zusammensetzung des dentalen Biofilms ist von Mensch zu Mensch verschieden, und sogar innerhalb ein und derselben Mundhöhle variiert Buch 5.indb 925 15.10.2009 11:37:00 Kap. 25 I. Kapferer Abb. 1. Der dentale Biofilm Abb. 2. Kariesschema nach König (König, 1987) die bakterielle Zusammensetzung des Biofilms je nach Nische. Auch die Verweildauer des Biofilms auf dem Zahn, die Qualität und Quantität des Speichels, die Zahnstellung und die Qualität der dentalen Restaurationen spielen eine Rolle. Die Zusammensetzung des Biofilms ist also kein Zufallsprodukt. Vielmehr zeigt der Biofilm einen räumlich geordneten Aufbau. Die Bakterien bilden Kommunitäten, mit Stadtvierteln vergleichbar, und in der interzellulären Matrix besitzt der Biofilm Wasserkanäle, die als Verbindungs- und Transportwege für Nahrung und Stoffwechselprodukte dienen. Die verschiedenen Bakterien bilden untereinander eine Symbiose, das heißt, sie versorgen sich gegenseitig mit Stoffwechselprodukten. 3. Infektionserkrankung Karies Nicht jeder Zahnbelag und nicht alle Bakterien sind odontopathogen. Mehrere Jahrzehnte galt die Auffassung, dass Laktobazillen die Hauptrolle in der Kariesgenese spielen. Heute gilt Streptokokkus mutans als das Hauptkariesbakterium (Al Shukairy et al., 2006). Die Besiedelung der Mundhöhle mit Streptokokkus mutans erfolgt mit dem Durchbruch der ersten Zähne, und die Ansteckung erfolgt meistens durch die Eltern, wenn diese Löffel oder Schnuller des Babys selbst in den Mund nehmen. In einer Studie wurde gezeigt, dass bei den sechs bis neun Monate alten Kindern nur 4,5 % Streptokokkus mu- tans positiv waren, während der Anteil bei den 18 bis 24 Monate alten schon bei 56 % lag (Mohan et al., 1998). Die Kariesbakterien nehmen aus der Nahrung niedermolekulare Kohlenhydrate auf, verstoffwechseln diese, und als Endprodukt scheiden sie unter anderem Milchsäure aus. Diese Milchsäure senkt den pH-Wert im Mund und in der Plaque, und löst Mineralien aus der Zahnhartsubstanz heraus. Zahnschmelz wird bei einem pH-Wert von 5,7 demineralisiert. Normalerweise liegt der pH-Wert des menschlichen Mundes etwa bei pH 7. Bei jedem Abfall des pH-Wertes unter pH 5,7 findet eine Demineralisation des Zahnschmelzes statt. Diese ist aber meist so gering, dass bei einem Wiederanstieg des pH-Wertes der Schmelz remineralisiert wird, die Mineralien werden in den Schmelz wieder eingebaut. So findet eine ständige Deund Remineralisation an der Zahnoberfläche statt. Erst bei langer Verweildauer der Plaque und häufiger Kohlenhydratzufuhr werden die Demineralisationsphasen immer länger und die Phasen der Remineralisation immer kürzer, eine vollständige Remineralisation der entstandenen Läsion ist nicht mehr möglich – es entsteht Karies. Zusammenfassend gibt es vier Grundvoraussetzungen für die Entstehung von Karies, die alle erfüllt sein müssen. Fehlt nur eine, entsteht keine Karies (siehe Abb. 2). 926 Buch 5.indb 926 15.10.2009 11:37:01 Ernährung bei Karies und parodontalen Erkrankungen Karies ist daher keine klassische Infektionskrankheit, denn Kariesbakterien alleine machen noch keine Karies. Erst die Veränderung der oralen „Umweltbedingungen“ führt zu einer Erhöhung ihrer Virulenz und einer pathogenen Wirkung. Diese Veränderungen der Umweltbedingungen werden im Wesentlichen durch eine Ernährung verursacht, die zu reich an niedermolekularen Kohlenhydraten ist. Da Karies also das Resultat einer Aktivität endogener Bakterien ist, die erst aufgrund einer Veränderung der Ökologie der Mundhöhle Pathogenität erlangt haben, ist sie als opportunistische Infektion aufzufassen. Diese Erkenntnis ist für die Vorbeugung der Karies von großer Bedeutung (Zimmer, 2000). 3.1. Die Rolle des Speichels in der Kariesgenese Der Speichel hat einen hohen Stellenwert für die Erhaltung der Integrität der Zähne, des Zahnhalteapparates und der Weichgewebe in der Mundhöhle. Seine Glykoproteine überziehen alle Schleimhäute und Festkörper im Mund, und schützen sie so vor dem Austrocknen. Seine reinigende Wirkung hängt entscheidend von der Fließrate und Viskosität ab. Die puffernde und remineralisierende Wirkung wird durch den Gehalt von Bikarbonat, Phosphat, Kalzium und Fluorid gewährleistet. Eine antimikrobielle Aktivität des Speichels kommt durch sekretorische Immunglobuline (sIgA), Lysozym, Katalase, Laktoperoxidase und weitere Enzyme zustande. Der Speichel macht Speisen beim Essen weich, Geschmacksstoffe werden so aus der Nahrung gelöst, und schon in der Mundhöhle beginnt die Verdauung, indem Kohlenhydrate durch die Speichel-Amylase gespalten werden. Der Speichel besteht zu 99 % aus Wasser. Außerdem enthält er anorganische Ionen (Natrium, Kalzium, Kalium, Ammonium, Magnesium, Kupfer, Chlorid, Fluorid, Phosphat, Iodid u. a.), organische Stoffe (Enzyme, Glykoproteine, Histamin, Harnstoff u. a.), Fette, Säuren, Hormone, Vitamine, spezifische und unspezifische Abwehrfaktoren, Medikamente, sowie toxische Substanzen aus der Umwelt (Klimm, 1997). Produziert wird der Speichel von den großen Speicheldrüsen der Mundhöhle (Gl. sublingualis, Gl. submandibularis, Gl. parotis) und den kleinen Speicheldrüsen der Mundschleimhaut. Einige produzieren wässrigen (serösen), andere eher schleimigen (mukösen) Speichel. Je nachdem welche Speicheldrüse den Hauptanteil zum Gesamtspeichel beisteuert, ist dieser eher wässrig oder zäh. Die Sekretionsrate und die Qualität des Speichels werden von gustatorischen Reizen, von der Art und Dauer der Stimulation, von Medikamenten, Stress und von der Tageszeit bestimmt. Während des Schlafes wird die Speichelfließrate auf 0,25 – 0,35 ml/min reduziert, während sie nach Stimulation 1– 2 ml/min beträgt. 3.1.1. Xerostomie Die Bedeutung des Speichels für die orale Gesundheit und Wohlbefinden wird erst begreiflich, wenn er nicht mehr in ausreichendem Maße zur Verfügung steht. Ein trockener Mund kann zu eingeschränkter Geschmackswahrnehmung, Schwierigkeiten beim Essen und Trinken, schmerzhaften Entzündungen des Zahnfleisches sowie rapide fortschreitenden kariösen Zerstörungen der Zahnhartsubstanz führen (Zimmer, 2000). Die Reduktion der Speichelfließrate ist eine häufige Nebenwirkung verschiedener Arzneimittel, wie Psychopharmaka, Diuretika und Anticholinergika wie z. B. Atropin. Strahlentherapien oder die chirurgische Entfernung von Speicheldrüsen führen oft zu starker Xerostomie. Eher seltenere Ursachen können auch Erkrankungen wie Sialadenitis, Sjögren-Syndrom oder Heerfordt-Syndrom sein. Bei Patienten mit Depressionen führen mehrere Faktoren zu einem erhöhten Kariesrisiko. Zum einen neigen depressive Patienten zu einer kariogenen Diät und zu einer mangelnden Mundhygiene. Als zusätzlicher kariogener Faktor kommen Anti927 Buch 5.indb 927 15.10.2009 11:37:02 Kap. 25 I. Kapferer depressiva mit der häufigen Nebenwirkung der Mundtrockenheit hinzu. Deshalb leiden depressive Patienten häufig an rapid fortschreitender Karies und generalisierter Parodontitis. Zur Therapie der Xerostomie stehen verschiedenste Speichelersatzmittel zur Verfügung, die jedoch bei einigen Patienten auf geringe Akzeptanz stoßen und nur kurzfristig Erleichterung bringen. Wichtig ist bei den Speichelersatzmitteln auf die Zuckerfreiheit zu achten. Im Mittelpunkt der Therapie steht aber die Kariesprophylaxe mit engmaschiger professioneller Zahnreinigung, wiederholter Mundhygiene-Instruktion und der Verwendung von antiseptischen Mundspülungen und Fluoridpräparaten. 4. Einfluss der Ernährung auf die Kariesentstehung 4.1. Einfluss des Zuckerkonsums Karies ist eine Zivilisationskrankheit. Seit dem Mittelalter ist die Kariesverbreitung stark angestiegen. Dafür verantwortlich sind verschiedene Ernährungsfaktoren (Theilade et al., 1986): r r r r Hoher Anteil rasch vergärbarer Kohlenhydrate Geringerer Anteil kauzwingender Kost Häufigere Nahrungsaufnahme Weniger karieshemmende Bestandteile in der Nahrung. 1946 bis 1951 wurde eine groß angelegte Studie in einem schwedischen Heim für geistig Behinderte durchgeführt (Gustafsson et al., 1954). Den Probanden wurde zuckerarme Kost verabreicht, oder stark zuckerhaltige Nahrung in unterschiedlicher Zusammensetzung und Konsistenz zu den Hauptmahlzeiten allein, oder zu den Haupt- und Zwischenmahlzeiten. Die Studie zeigte, dass sich bei zuckerarmer Kost am wenigsten neue Karies bildete. Bei zuckerhaltiger Nahrung hing der Karieszuwachs von der Konsistenz und der Häufigkeit des Zuckerkonsums Abb. 3. Stephan-Kurve ab. Je häufiger der Zuckerkonsum, desto stärker der Karieszuwachs. Und: wurde der Zucker in gelöster Form zu sich genommen, war der Karieszuwachs geringer als bei der Gruppe, wo klebrige Kaubonbons gegessen wurden. Es kommt also nicht auf die absolute Menge des konsumierten Zuckers an, sondern auf die Häufigkeit und die Verweildauer im Mund. Dieser Sachverhalt wird durch die Stephan-Kurve verständlich (siehe Abb. 3). Bei jeder Aufnahme von Glukose sinkt innerhalb von fünf Minuten der pH-Wert des Speichels. Zur Erinnerung: Beim Abfall des pH-Wertes unter pH 5,7 findet eine Demineralisation des Zahnsubstanz statt. Die Puffersysteme des Speichels heben den pH-Wert wieder auf etwa pH 7 an, dies dauert 35 bis 40 Minuten. Wird zum Beispiel alle 60 Minuten ein Stück Schokolade konsumiert, sind die Phasen der Remineralisation kürzer als die Phasen der Demineralisation, es entsteht Karies. Für die Zahngesundheit ist es also besser, die ganze Tafel Schokolade auf einmal zu essen! Für die Kariesprophylaxe entscheidend sind ausreichende Pausen zwischen den 928 Buch 5.indb 928 15.10.2009 11:37:02 Ernährung bei Karies und parodontalen Erkrankungen Mahlzeiten, damit die angegriffene Zahnsubstanz remineralisiert werden kann. Es kommt nicht auf die absolute Menge des konsumierten Zuckers an, sondern auf die Häufigkeit und Dauer des Zuckerkonsums, und auf den Grad der Gelöstheit. 4.2. Das Baby Bottle Syndrom Beim „Baby-Bottle-Syndrom“ handelt es sich um eine ausgeprägte Glattflächenkaries bei Kleinkindern, vor allem an den Oberkieferfrontzähnen. Ursache dafür ist das Dauernuckeln von zucker- oder säurehaltiger Flaschennahrung (zuckerhaltige Tees und Säfte, gesüßte Milch, Honig auf dem Schnuller). Besonders während dem Schlafen ist das Nuckeln von zuckerhaltigen Getränken fatal, da der schützende Speichelfluss in der Nacht stark vermindert ist. Die von der Karies zerstörten Zähne müssen komplett entfernt werden, was zu Problemen bei der Nahrungsaufnahme, aber auch zu Störungen der Sprachentwicklung führen kann. Der frühzeitige Verlust der Milchzähne führt auch oft zu Zahnfehlstellungen bei den bleibenden Zähnen. Zur Vermeidung des Baby-Bottle-Syndroms werden folgende Ratschläge gegeben: r r r r r r r die Verwendung von Glasflaschen wird empfohlen, da diese schwerer sind und von den Kindern nicht so lange gehalten werden können, wie Plastikflaschen das Kind nicht mit der Flasche im Mund einschlafen lassen zuckerfreie und wenig saure Getränke Absetzen der Saugflaschen nach dem 12. Lebensmonat tägliche Zahnreinigung ab dem ersten Zahn Fluoridzufuhr ab dem ersten Zahn (siehe Kapitel Fluoride) Rechtzeitige Behandlung durch den/die Zahnärzt/in beim Auftreten von Läsionen Abb. 4. Baby-Bottle-Syndrom 4.3. Zuckeraustauschstoffe und Zuckerersatzstoffe Zuckeraustauschstoffe haben einen zuckerähnlichen chemischen Aufbau. Sie werden von Bakterien nur langsam oder gar nicht verstoffwechselt und sind daher gering oder nicht kariogen. Der Zuckeraustauschstoff Xylit spielt eine besondere Rolle in der Kariesprophylaxe. Die Reduktion der Kariesinzidenz durch regelmäßiges Kauen (3 bis 5-mal täglich) von xylithaltigem Kaugummi („Zahnpflegekaugummis“) basiert auf verschiedenen Wirkmechanismen (Burt, 2006): r r r r Nach Xylitkonsum kommt es nicht zu einem pH-Wertabfall in der Plaque, und dadurch auch nicht zur Demineralisation der Zahnhartsubstanz Die Proliferation von Streptokokkus mutans wird gehemmt Die Plaqueakkumulation auf der Zahnoberfläche wird reduziert Die Speichelfließrate wird stimuliert und damit die Bufferwirkung des Speichels erhöht. Zuckerersatzstoffe sind synthetische oder natürliche in Pflanzen vorkommende chemische Verbindungen, die von Bakterien bei der extrazellulären Polysaccharidsynthese nicht in Plaque umgewandelt werden. Sie sind daher nicht kariogen. 929 Buch 5.indb 929 15.10.2009 11:37:03 Kap. 25 I. Kapferer Tabelle 1. Übersicht der gängigsten Zuckeraustauschund Zuckerersatzstoffe Zuckeraustauschstoffe Zuckerersatzstoffe (Süßstoffe) Isomalt (E 953) Lactit (E 966) Maltit (E 965) Mannit (E 421) Sorbit (E 420) Xylit (E 967) Acesulfam (E 950) Aspartam (E 951) Cyclamat (E 952) Neohesperidin DC (E 959) Saccharin (E 954) Thaumatin (E 957) Zahnfreundliche Süßwaren mit Zuckeraustausch- oder Zuckerersatzstoffen erkennt man an dem international geschützten Markenzeichen „Zahnmännchen mit Schirm“. Dieses Signet darf nur auf Süßwaren angebracht werden, wenn während und bis 30 Minuten nach deren Genuss der Säuregehalt im Zahnbelag eine bestimmte Sicherheitsschwelle nicht überschreitet. Die gängigsten Zuckeraustausch- und Zuckerersatzstoffe sind in Tabelle 1 zusammengefasst. 4.4. Versteckte Zucker Viele Eltern wissen gar nicht, in welchen Nahrungsmitteln überall Zucker verarbeitet ist. Man findet Zucker im Ketchup und im Senf, in Kartoffelchips, in Wurstwaren, Fertigsaucen und Beutelsuppen, aber auch in vermeintlich „gesunden“ Produkten wie Müsliriegel und Fruchtjoghurt. Vorsicht ist bei Säften, Tees und Süßigkeiten geboten, die Aufschriften wie „ohne Zuckerzusatz“, „nur mit natürlichem Zucker“ oder sogar „zuckerfrei“ tragen. Diese enthalten meistens Fruchtzucker, der nach wissenschaftlichen Untersuchungen ebenfalls kariesfördernd ist (Tanzer et al., 2006). Weil nach dem einschlägigen „Gesetz über den Verkehr mit Zucker“ nur Rohrzucker (Saccharose) als Zucker bezeichnet wird, sind derartige Deklarationen zulässig, für den Verbraucher sind sie jedoch irreführend (Zimmer, 2000). 4.5. Fluoride Die Fluoridapplikation ist eine wichtige Säule in der Kariesprophylaxe. Fluoride sind die Salze der Fluorsäure. Fluorid ist ein wichtiges Spurenelement und hat eine hohe Bedeutung für die Bildung von Knochen und Zähnen. Der Körper eines Erwachsenen enthält insgesamt etwa 2,6 g Fluorid (Zimmer, 2000). In zahnmedizinischen Präparaten kommen vor allem Aminfluorid, Natriummonofluorphosphat und Zinnfluorid zur Anwendung. Egal ob Fluorid in lokalen Präparaten (Lacke, Gele, Zahnpasta, Spülungen) oder systemisch angewandt wird (Tabletten, Speisesalz, Trinkwasser), entscheidend für die kariespräventive Wirkung ist immer die lokale Verfügbarkeit, weniger der systemisch zugefügte Anteil (Gülzow et al., 2005). Systemisch zugeführte Fluoride werden im Magen-Darm-Trakt resorbiert und anschließend in nur geringen Mengen über den Speichel wieder ausgeschieden. Bei im Wachstum befindlichen Zähnen kommt es auch zu einem Einbau von Fluorid in die Zahnhartsubstanzen, der kariespräventive Effekt ist allerdings umstritten. Bei der Anwendung von lokalen Fluoridpräparaten lagern sich Kalziumfluorid-Partikel auf der Zahnoberfläche ab. Diese KalziumfluoridDeckschicht kann Fluorid an der Zahnoberfläche besonders bei kariogenen Bedingungen in hoher Konzentration zur Verfügung stellen. Die kariesprophylaktische Wirksamkeit von Fluorid beruht auf folgenden Mechanismen: r r r Verbesserung der Remineralisation Verminderung der Demineralisation Antibakterielle Wirkung. 4.5.1. Verminderung der Demineralisation Fluorid dringt in den Schmelz ein und führt dort zu einer Kristallisation. Dabei entsteht stabil in der Zahnhartsubstanz gebundenes Fluorid (Zimmer, 2000). Hydroxylapatit, die chemische Basis des Zahnschmelzes, wird in Fluorapatit 930 Buch 5.indb 930 15.10.2009 11:37:04 Ernährung bei Karies und parodontalen Erkrankungen umgewandelt. Während Hydroxylapatit bei einem pH-Wert von 5,7 demineralisiert wird, wird Fluorapatit erst bei einem pH-Wert von 4,6 demineralisiert. Man nennt diesen Prozess auch „posteruptive Schmelzreifung“. 4.5.2. Verbesserung der Remineralisation Die Verbesserung der Remineralisation ist der bedeutendste Wirkmechanismus der Fluoride. Er basiert auf der umgekehrten Reaktion als die Hemmung der Demineralisation, wie sie oben beschrieben wurde. Das heißt, dass bei Anwesenheit von ausreichend Fluorid im Speichel die Zahnsubstanz bereits bei einem pH-Wert von 4,6 remineralisiert wird, während das ohne Fluorid erst ab einem pH von 5,7 der Fall ist. 4.5.3. Antibakterielle Wirkung Fluorid wirkt antibakteriell, indem es Stoffwechselfunktionen der Kariesbakterien behindert (Zimmer, 2000). Dadurch wird die Energiegewinnung der Bakterienzelle als auch die Produktion von Milchsäure reduziert. Ebenso wird die Bildung intra- und extrazellulärer Polysaccharide, und somit die Produktion der interzellulären Matrix vermindert. Wenn die interzelluläre Matrix aber nicht in ausreichendem Maße gebildet wird, werden Plaquewachstum und -reifung behindert. Da eine sehr hohe Fluoridkonzentration für diese antibakterielle Wirkung notwendig wäre, spielt sie in der Praxis eine eher untergeordnete Rolle. 4.5.4. Lokale Fluoridierungsmaßnahmen Fluoridhaltige Zahnpasten Die Verwendung fluoridhaltiger Zahnpasten ist die am weitesten verbreitete und auch eine effektive kariespräventive Maßnahme, deren Wirksamkeit durch hohe wissenschaftliche Evidenz untermauert ist (Gülzow et al., 2005). Die übliche Fluoridkonzentration in Zahnpasten beträgt 1000 bis 1500 ppm. Da Kinder unter sechs Jahren einen Großteil der Zahnpasta schlucken, sollte eine fluoridreduzierte Zahnpasta (500 ppm) zur Anwendung kommen. Fluoridlacke Fluoridlacke werden im Rahmen einer professionellen Zahnreinigung oder anderen zahnärztlichen Tätigkeiten in der Praxis appliziert. Die Anwendung erfolgt zwei- oder mehrmals jährlich und kann unabhängig von anderen Fluoridierungsmaßnahmen durchgeführt werden. Fluoridgele Der kariespräventive Effekt von Fluoridgel ist wissenschaftlich nachgewiesen (Gülzow et al., 2005), und ihre Anwendung wird besonders bei kariesaktiven Patienten empfohlen. Es gibt verschiedenste Präparate, die entweder in der Zahnarztpraxis oder von den Patienten selbst appliziert werden. Es gibt Gele zur täglichen oder wöchentlichen Verwendung, beide Methoden sind gleich wirksam (Gülzow et al., 2005). Das Gel wird nach der Zahnreinigung auf die Zähne verteilt und soll einige Minuten einwirken. Da die Fluoridkonzentration in den Gelen sehr hoch ist und Kleinkinder erhebliche Mengen schlucken könnten, werden Fluoridgele in diesem Alter nicht empfohlen. Fluoridhaltige Mundspüllösungen Wird von den Patienten bereits eine fluoridhaltige Zahnpasta verwendet, scheint eine zusätzliche Fluorid-Mundspülung wenig Effekt auf die Kariesinzidenz zu haben (Gülzow et al., 2005). Empfohlen werden fluoridhaltige Mundspüllösungen oft bei Patienten, die homöopathische Zahnpasten verwenden, da diese häufig kein Fluorid enthalten. 4.5.5. Systemische Fluoridierungsmaßnahmen Fluoridtabletten Der kariespräventive Effekt von Fluoridtabletten basiert vor allem auf der lokalen Wirksamkeit, 931 Buch 5.indb 931 15.10.2009 11:37:04 Kap. 25 I. Kapferer daher sollten Fluoridtabletten gelutscht werden. Sie gelten als Alternative zur Speisesalzfluoridierung. Ein Vorteil ist die genaue Dosierungsmöglichkeit, ein Nachteil ist die oft mangelnde Compliance der Eltern. Setzt die Fluoridierungsmaßnahme allerdings erst im Kindergarten oder in der Volkschule ein, sind gerade bei kariesaktiven Kindern die Milchzähne schon oft kariös zerstört. Während der Schwangerschaft macht die Gabe von Fluoridtabletten wenig Sinn, da dies keinen Einfluss auf die Kariesprävalenz des ungeborenen Kindes hat. Fluoridiertes Speisesalz Die Verwendung von fluoridiertem Speisesalz wird generell empfohlen (Gülzow et al., 2005), da sie sehr breitenwirksam, kostengünstig und effektiv ist, und auch von Patienten mit geringer Compliance angewandt wird. Dabei ist wieder die lokale Verfügbarkeit des Fluorids beim Kauakt für die Kariesprävention entscheidend, und nicht der systemisch resorbierte Anteil. Um zu hohe Fluoridkonzentrationen und damit eine chronische Fluoridüberdosierung zu vermeiden, soll in Gegenden mit hohem Fluoridgehalt im Trinkwasser und zusätzlicher Einnahme von Fluoridtabletten kein fluoridiertes Speisesalz verwendet werden. Natürliches Trink- und Mineralwasser Achtzugeben ist bei Mineralwässern, denn diese haben oft einen sehr hohen Fluoridgehalt. Bei Kindern, die viel Mineralwasser trinken, ist daher mit zusätzlichen systemischen Fluoridgaben Vorsicht geboten, da es sonst leicht zu einer chronischen Toxizität kommen kann. Babynahrung sollte grundsätzlich mit abgekochtem Trinkwasser zubereitet werden. Es gibt aber Gegenden, wo auch das natürliche Trinkwasser sehr hohe Fluoridkonzentrationen aufweist. Über den Fluoridgehalt des Trinkwassers kann das jeweilige Gemeindeamt Auskunft geben. Aus dem Fluoridgehalt des Trinkwasser ergeben sich bei Kindern folgende praktische Konsequenzen: r r r r 0 – 0,29 mg Fluorid/l = zusätzliche systemische Fluoridzufuhr empfohlen 0,3 – 0,69 mg Fluorid/l = systemische Fluoridzufuhr je nach Kariesaktivität empfohlen 0,7–1,50 mg Fluorid/l = keine zusätzliche systemische Fluoridzufuhr empfohlen Über 1,50 mg Fluorid/l = Gefahr der Fluoridüberdosierung. 4.5.6. Toxikologische Aspekte Akute Fluoridvergiftungen sind äußerst selten und bedürfen derart hoher Mengen, die es nahezu ausschließen, überhaupt verzehrt werden zu können. Bei Fluorid wird eine letale Dosis erst erreicht, wenn etwa das 100-fache der Menge aufgenommen wird, die aus kariesprophylaktischer Sicht angezeigt ist (Zimmer, 2000). Die minimale Dosis, die toxische Zeichen und Symptome verursachen kann und ein sofortiges therapeutisches Eingreifen erfordert, wird mit 5 mg Fluorid pro Kilogramm Körpergewicht angegeben (Whitford, 1996). Ein 10 kg schweres Kind müsste also 100 g Kinderzahnpasta (Fluoridkonzentration 500 ppm) schlucken, um lebensgefährlich zu erkranken. Viel häufiger kommt es bei ein- bis sechsjährigen Kindern zu einer chronischen Fluoridüberdosierung und als Folge zu einer Dentalfluorose, und der Bildung weißlicher Schmelzflecken. Bei schweren Formen einer Fluorose können auch lochartige Vertiefungen entstehen, die mit einer Karies verwechselt werden können. Für die Entstehung einer Fluorose wird eine Grenzdosis von etwa 0,1 mg Fluorid/kg Körpergewicht pro Tag angegeben. Um das Fluoroserisiko zu senken wird für Kinder unter sechs Jahren eine Zahnpasta mit reduziertem Fluoridgehalt (< 500 ppm) empfohlen, da Kinder ja immer wieder Zahnpasta schlucken. 932 Buch 5.indb 932 15.10.2009 11:37:04 Ernährung bei Karies und parodontalen Erkrankungen 5. Infektionserkrankungen Gingivitis und Parodontitis 5.1. Gingivitis Die Gingivitis ist eine bakteriell verursachte Entzündung des Zahnfleisches. Klinische Zeichen der Gingivitis sind Blutung, Rötung, Schwellung und Ulzerationen des Zahnfleisches. Hauptursache der Gingivitis ist eine mangelnde Zahnreinigung. Ihre Ausprägung kann aber durch Schwankungen im Hormonhaushalt (z. B. orale Kontrazeptiva, Pubertät, Schwangerschaft), durch systemische Erkrankungen (z. B. Diabetes mellitus Typ I und II, Depressionen, HIV) oder durch Medikamente (z. B. Phenytoin, Dihydropyridin, Ciclosporin) moduliert werden. Mangelernährung als Ursache oder Kofaktor einer Gingivitis wird in der nördlichen Hemisphäre praktisch nicht beobachtet. Unter extremen Bedingungen können aber Ascorbinsäuremangel und Eiweißmangel Auswirkungen auf die Mundschleimhaut zeigen. Sobald die Zahnreinigung durch den Patienten optimiert wird, heilt die Gingivitis innerhalb weniger Tage vollständig aus. Die Gingivitis kann, aber muss sich nicht zu einer Parodontitis entwickeln. Sie kann auch jahrelang ohne Behandlung stabil bleiben. 5.2. Parodontitis Bei der Parodontitis gehen die entzündlichen Prozesse vom Zahnfleisch auf die tiefer liegenden Strukturen des Zahnhalteapparates über, also auf den zahntragenden Knochen und das Desmodont. Als Folge kommt es zum Knochenverlust und zur Zahntaschenbildung. Mit zunehmendem Knochenverlust beginnen die Zähne zu wackeln und fallen schlussendlich aus. Es gibt eine chronische Parodontitis, die durch einen langsamen Verlauf gekennzeichnet ist, und eher Menschen ab 45 Jahren betrifft. Die aggressive Parodontitis zeigt einen raschen Verlauf mit frühzeitigem Zahnverlust bei typischerweise jungen Menschen. Die Parodontitis ist eine multifaktorielle Erkrankung. Der primäre ätiologische Faktor sind parodontopathogene Bakterien des subgingivalen Biofilms (Wolf, 2004). Nach dem derzeitigen Wissensstand gibt es fünf parodontopathogene Leitkeime: Aggregatibacter actinomycetemcomitans, Porphyromonas gingivalis, Prevotella intermedia, Fusobacterium nucleatum, Tanerella forsythensis. Es gilt der Grundsatz: „ohne Bakterien keine Parodontitis“, aber andererseits auch die Tatsache, dass parodontopathogene Bakterien nicht unbedingt eine Parodontitis verursachen müssen (Wolf, 2004). Voraussetzung für die Entstehung, und maßgebend für den Verlauf einer Parodontitis ist der empfängliche Wirt. So kann die gleiche Bakterienmenge bei verschiedenen Patienten ganz unterschiedliche Schweregrade einer Parodontitis hervorrufen. Die genetisch determinierte Immunreaktion (überschießend oder defekt) ist ein entscheidender Faktor. Außerdem erhöhen bestimmte Lebensstile das Risiko des Patienten. Tabakrauchen zum Beispiel erhöht das Parodontitisrisiko um ein Vielfaches, und erschwert deutlich die Therapie derselben. Alkohol, Drogenabusus, psychische Belastung und Stress, sowie schlechte Mundhygiene sind weitere häufige Risikofaktoren. Neben diesen Faktoren gibt es noch systemische Erkrankungen, die mit einem erhöhten Parodontitisrisiko mit teilweise dramatischem Verlauf einhergehen. Dazu zählen Diabetes mellitus Typ I und II, HIV, Trisomie 21, Papillon-Lefèvre-Syndrom, Chediak-Higashi-Syndrom, erworbene sowie hereditäre und zyklische Neutropenien, Glykogenspeicherkrankheiten, Agranulozytose, Cohen-Syndrom, Ehlers-Danlos-Syndrom, Histiozytosen u. a. m. Eine Parodontitis kann nicht geheilt sondern nur gestoppt werden, und der einmal entstandene Knochenverlust ist nur in Ausnahmefällen regenerierbar. Die Therapie der Parodontitis besteht aus einer konservativen Basistherapie, während dieser alle Zähne supra- und subgingival von Zahnstein und Belägen befreit werden, und der Patient durch wiederholte Instruktionen eine op933 Buch 5.indb 933 15.10.2009 11:37:04 Kap. 25 I. Kapferer timale Mundhygiene erlernen muss. Die perfekte häusliche Zahnreinigung ist die Voraussetzung für jeden Behandlungserfolg. In einem zweiten Schritt können Zahntaschen chirurgisch abgetragen werden, oder an einzelnen Zähnen der Zahnhalteapparat regeneriert werden. Bei aggressiven Parodontitiden kommen auch systemische Antibiotika zum Einsatz, allerdings immer nur in Kombination mit einer perfekten Zahnreinigung. 5.3. Akut nekrotisierende Gingivitis und Parodontitis Die Gingivitis und Parodontitis ulcerosa sind akute, sehr schmerzhafte, ulzerierende Entzündungen des Zahnhalteapparates. Im Anfangsstadium dominieren die zerfallenden, weißen Papillenspitzen das klinische Bild. Später geht die Entzündung auf den Knochen über. Häufig treten auch Abklatschgeschwüre an den benachbarten Weichgeweben auf. Als Ursache für Parodontitis und Gingivitis ulcerosa gelten chronische Erschöpfungszustände, psychischer Stress (typisch sind Schubhäftlinge und Examensstudenten), Rauchen, ein stark geschwächtes Immunsystem (z. B. HIV-Patienten), und schlechte Mundhygiene. Bakteriell dominieren Spirochäten, fusiforme Bakterien und Prevotella intermedia. Die Basis der Therapie bildet wieder die mechanische Zahnreinigung durch den Zahnarzt. Da die häusliche Zahnreinigung aufgrund der starken Schmerzen fast nicht möglich ist, werden antiseptische Spülungen empfohlen. Unterstützend kann in schweren Fällen systemisch Metronidazol verabreicht werden. In Entwicklungsländern bilden Gingivitis und Parodontitis ulcerosa häufig die Vorstufe zur Noma (destruierende gangränöse Stomatitis). Voraussetzung für eine Erkrankung mit Noma ist ein durch starke Mangelernährung oder Vorerkrankungen geschwächtes Immunsystem. Besonders häufig sind Eiweiß-, Vitaminund Elektrolytmangel. Meistens sind Kinder davon betroffen, seltener Erwachsene. 6. Einfluss der Ernährung auf die Parodontalerkrankungen Über den Einfluss der Ernährung auf den Verlauf der Parodontalerkrankungen gibt es nur wenige Studien. In den Jahren 1988 bis 1994 wurde in einer groß angelegten amerikanischen Studie bei 12 110 Probanden der Zusammenhang zwischen gesundem Lebensstil und Parodontitis untersucht (Al-Zahrani et al., 2005). Als gesunder Lebensstil wurden drei Parameter definiert: Normalgewicht, gesunde Ernährung, sportliche Betätigung. „Gesunde Ernährung“ wurde mittels dem „healthy eating index“ (HEI) (National Center for Health Statistics, 1999) erhoben, der die Menge der konsumierten Nahrung innerhalb von 24 Stunden und die Nahrungszusammensetzung evaluiert. Für diese Studie wurden Individuen mit HEI > 80 mit „gesunder Ernährung“ betitelt, wie es von dem „United States Department of Agriculture“ empfohlen wird. Die Untersuchung ergab, dass wenn nur einer der drei Parameter erfüllt wird, dass Parodontitisrisiko um 16 % reduziert wurde. Wurden zwei Parameter erfüllt, senkte sich das Parodontitisrisiko um 29 %, und bei Erfüllung aller drei Parameter um 40 %. Der positive Einfluss der gesunden Ernährung auf die Parodontitis wird von den Autoren folgendermaßen erklärt (Al-Zahrani et al., 2005): bei reichlichem Zuckerangebot nimmt zunächst einmal die Plaquemasse schnell zu und bietet auch den parodontopathogenen Mikroorganismen Lebensraum. Des Weiteren haben Nahrungsmittel mit einem natürlichen Faseranteil (z. B. Gemüse) aufgrund ihrer Konsistenz selbst schon eine gewisse Reinigungskraft. Es gibt auch Studien, die Zusammenhänge zwischen der Körperzusammensetzung und der Parodontitis zeigen (Wood et al., 1993). Diese Studien zeigen, dass Adipositas nicht nur ein Risikofaktor für Diabetes, Dyslipidämie und Bluthochdruck ist, der Fettmetabolismus scheint auch in der Pathogenese der Parodontitis eine entscheidende Rolle zu spielen (Wood et al., 1993). Als Grundlage für diese Annahme 934 Buch 5.indb 934 15.10.2009 11:37:05 Ernährung bei Karies und parodontalen Erkrankungen dient die Tatsache, dass durch Fettleibigkeit die Sekretion von proinflammatorischen Zytokinen (IL-6, TNF-D u. a.) erhöht wird (Al-Zahrani et al., 2005), die wiederum in der Parodontitispathogenese eine Rolle spielen. Auch in der Komplementärmedizin wird die Parodontitis als ein multikausales Geschehen betrachtet. Das Zahnfleisch wird hier als „Fenster zum Darm“ gesehen, da sein Zustand dem der Darmschleimhaut entspricht. 7. Andere Auswirkungen der Ernährung auf die Zähne In der heutigen Zeit sind Karies, Gingivitis und Parodontitis die zivilisatorischen Zahnerkrankungen. In ur- und frühgeschichtlicher Zeit war es die Zahnabrasion (Abkauung). Die Kariesfrequenz war zwar sehr gering, stattdessen führte die grobe und mit Mineralstäuben verunreinigte Nahrung aber zu starker Abkauung der Zähne. Auch heute sieht man manchmal bei Ernährung mit stark kauzwingender Kost eine vermehrte Abnutzung der Zähne, die jedoch selten einen pathologischen Stellenwert hat. Drastische Auswirkungen auf die Zahnsubstanz haben Ernährungsstörungen wie Bulimie und Anorexie. Durch das häufige Erbrechen sind die Zähne der Magensäure ausgeliefert, und mit der Zeit wird die Zahnsubstanz in einer ganz typischen Art und Weise weggeätzt (= Erosionen). Davon betroffen sind vor allem die Innenseiten der Zähne (palatinal) im Oberkiefer. Aber nicht nur die Säuren aus dem Magen können die Zähne anätzen. Auch der extrem überhöhte Konsum saurer Getränke oder von kohlensäurehaltigen Getränken, kann die Zahnsubstanz auflösen. Liegen die Zahnhälse aufgrund von Parodontitis oder Rezessionen frei, sind sie oft überempfindlich auf heiße oder kalte Nahrung, aber auch auf saure Getränke oder Obst, das Fruchtsäure enthält. Abb. 5. Zahnerosionen bei Bulimie 8. Auswirkungen von Parodontitis und Karies auf die Ernährung Karies verursacht im Gegensatz zur Parodontitis und Gingivitis schon im Anfangsstadium Schmerzen, daher wird die Nahrungsaufnahme für die Patienten zur Qual. Vor allem kalte oder süße Speisen reizen das offen liegende Dentin. Sind die Zähne durch die Karies vollständig zerstört oder fehlen einige Zähne, beginnt der Kauapparat zu kollabieren, die Zähne beginnen zu wandern oder zu elongieren, und behindern so aus der Reihe stehend den Kauakt. Bei fehlender Abstützung im Seitenzahngebiet sinkt die Bisshöhe ab, und als Folge sinkt die Kaukraft. Stark reduziertes Parodontalgewebe hat ähnliche Auswirkungen, die Zähne beginnen aufgrund der reduzierten Verankerung im Knochen zu wandern, und das Kausystem kollabiert. Wegen der stark gelockerten Zähne ist auch die Kaukraft stark reduziert – „es fehlt der Biss“, und die Speisen werden nicht mehr gut durchgekaut. 935 Buch 5.indb 935 15.10.2009 11:37:06 Kap. 25 I. Kapferer Literatur Al Shukairy H, Alamoudi N, Farsi N, Al Mushayt A, Masoud I (2006) A comparative study of Streptococcus mutans and lactobacilli in mothers and children with severe early childhood caries (SECC) versus a caries free group of children and their corresponding mothers. J Clin Pediatr Dent 31(2): 80 – 5 Al-Zahrani MS, Borawski EA, Bissada NF (2005) Periodontitis and three health-enhancing behaviors: Maintaining normal weight, engaging in recommended level of exercise, and consuming a high-quality diet. J Periodontol 76: 1362 –1366 Borrell LN, Burt BA, Taylor GW (2005) Prevalence and trends in periodontitis in the USA: the [corrected] NHANES, 1988 to 2000. J Dent Res 84(10): 924 – 30 Bourgeois D, Bouchard P, Mattout C (2007) Epidemiology of periodontal status in dentate adults in France, 2002 – 2003. J Periodontal Res 42(3): 219 – 27 Burt BA (2006) The use of sorbitol- and xylitol-sweetened chewing gum in caries control. J Am Dent Assoc 137(2): 190 – 6 Gülzow HJ, Hellwig E, Hetzer G (2005) Leitlinie Fluoridierungsmaßnahmen. In: Heideman D (Hrsg.) Check-up und Prävention, 4. Aufl., Urban und Fischer, München, S 201– 205 Gustafsson BE, Quensel CE, Swendander Lanke L, Lundqvist C, Grahnen H, Bonow BE, Krasse B (1954) The Vipeholm dental caries study. The effects of different levels of carbohydrate intake of caries activity in 436 individuals observed for five years (Sweden). Acta Odont Scand 11: 232 Klimm W (1997) Kariologie. Hanser Verlag, München König KG (1987) Karies und Kariesprophylaxe. Thieme, Stuttgart Lang NP, Mombelli A, Attsröm R (2003) Dentalm Plaque and Calculus. In: Lindhe J, Karring T, Lang NP (Eds.) Clinical periodontology and implant dentistry, 4th edn., Blackwell Munksgaard, UK Mohan A, Morse DE, O‘Sullivan DM, Tinanoff N (1998) The relationship between bottle usage/content, age, and number of teeth with mutans streptococci colonization in 6 – 24-month-old children. Community Dent Oral Epidemiol 26: 12 – 20 National Center for Health Statistics (1999) Third National Health and Nutrition Examination Survey, 1988 –1994. NHANES III Healthy Eating Index Data File (Series 11, No. 6A). Hyattsville Tanzer JM, Thompson A, Wen ZT, Burne RA (2006) Streptococcus mutans: fructose transport, xylitol resistance, and virulence. J Dent Res 85(4): 369 –73 Theilade E, Birkhed D (1986) Diet and dental caries. In: Thylstrup A, Fejerskov O (Eds.) Textbook of cariology. Munksgaard, Copenhagen Whitford GM (1996) The metabolism and toxicity of fluoride, 2nd edn. Karger, Basel Wolf FW (2004) Epidemiologie, Epidemiologie der Gingivitis. In: Rateitschak KH, Wolf FW (Hrsg.) Farbatlanten der Zahnmedizin 1: Parodontologie, 3. Aufl., Thieme, Stuttgart/New York, S 79 Wood N, Johnson RB, Streckfus CF (1993) Comparison of body composition and periodontal disease using nutritional assessment techniques: Third National Health and Nutrition Examination Survey (NHANES III). J Clin Periodontol 30: 321– 327 Zimmer S (2000) Kariesprophylaxe als multifaktorielle Präventionsstrategie. Habilitationsschrift, HumboldtUniversität zu Berlin, Berlin 936 Buch 5.indb 936 15.10.2009 11:37:06