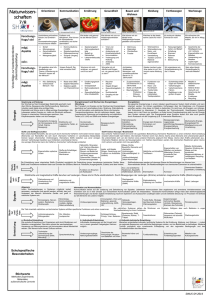
Schwermetalle in Seen und Flüssen
Werbung

Metalle in Seen und Flüssen • • • • Bindung von Metallen an Fulvin- und Huminsäuren Quellen von Metallen in natürlichen Gewässern Metalle in Seen: Spezierung und Sedimentation Metalle in Flüssen: Abfluss und Partikel Vminteq zur Berechnung der Gleichgewichte Komplexe mit Hauptionen und Spurenmetallen Ca2+ + NTA3- CaNTA- KCa = 4 x107 Cu2+ + NTA3- CuNTA- KCu = 2 x1014 NTAT = 2x10-7 M CaT = 1.3x10-3 M CuT = 5x10-8 M [NTA]T = [NTA3-]+[HNTA2-]+[H2NTA-]+[H3NTA]+[CaNTA-]+[CuNTA-] Komplexbildungsgleichgewichte mit vielen Komponenten und Spezies Bsp. : NTA, Ca2+, Cu2+,CO32-, H+ Spezies: Ca2+, Cu 2+, H+ CaNTA-, CuNTA-, NTA3-, HNTA2-, H2NTA-, H3NTA CO32-, HCO3-, H2CO3 CuCO30, Cu(CO3)22-, CuOH+, Cu(OH)20 … Vorgehen bei vielen Komponenten und Spezies -Berechnung mit Hilfe von Computerprogramm: VMINTEQ : - Definieren der Komponenten: Ca2+ , Cu2+ , NTA3- , CO32- , H+ - Angabe der totalen oder der freien Konzentrationen - Definieren der Spezies und der Konstanten aus Datenbank VMINTEQ: www.lwr.kth.se/english/OurSoftware/vminteq/ Resultate aus Berechnung mit Vminteq Konz. Ca(NTA)2-4 Ca+2 CaCO3 (aq) CaHCO3+ CaNTACaOH+ CO3-2 Cu(CO3)2-2 Cu(NTA)2-4 Cu(OH)2 (aq) Cu(OH)3Cu(OH)4-2 Cu+2 Cu2(OH)2+2 Cu2OH+3 Cu3(OH)4+2 1.9178E-16 1.2589E-03 1.4525E-05 2.6425E-05 1.5390E-07 1.8546E-08 1.5936E-05 1.8183E-10 3.6057E-15 4.0136E-11 1.7356E-13 1.9238E-18 1.0331E-10 2.2630E-15 2.3080E-19 7.8563E-20 Aktivität 3.6668E-17 8.3244E-04 1.4558E-05 2.3829E-05 1.3878E-07 1.6725E-08 1.0538E-05 1.2024E-10 6.8939E-16 4.0228E-11 1.5651E-13 1.2721E-18 6.8317E-11 1.4964E-15 9.1004E-20 5.1951E-20 Log Akt. -16.436 -3.080 -4.837 -4.623 -6.858 -7.777 -4.977 -9.920 -15.162 -10.395 -12.805 -17.895 -10.165 -14.825 -19.041 -19.284 Schwermetalle in Seen und Flüssen Bindung von Metallen an Fulvin- und Huminsäuren Quellen von Metallen in natürlichen Gewässern Metalle in Seen: Spezierung und Sedimentation Metalle in Flüssen: Abfluss und Partikel Bindung von Metallen durch Fulvin- und Huminsäuren -Funktionelle Gruppen für Bindung von Metallen -R-COOH OH - kleine Anzahl von S- und N-Gruppen Strukturen von Fulvinsäuren Molgewicht Fulvinsäuren 500 - 2000 Huminsäuren 2000 - > 5000 Beispiel Bindung von Cd an Fulvinsäuren Cd (mol/gFA) (Tipping 1998) Modellierung der Bindung an Humin- und Fulvinsäuren - Heterogeneität der funktionellen Gruppen: Vielzahl von Gruppen mit unterschiedlicher Affinität zu Metallen - elektrostatische Effekte - Bindung von Protonen und von Metallionen Modellierung der Bindung an Humin- und Fulvinsäuren Model VI (Tipping 1994/1998) - Protonen: (HumH)Z (Hum)Z-1 + H+ 8 verschiedene Säuregruppen mit : pKa = pKi + f ∆pKi - Metalle : HumZ + My+ (HumM)Z+y Für jede der 8 Säuregruppen: log Ki = log KMA + f ∆log KMA Zusätzlich bidentate und tridentate Komplexe Total 80 verschiedene Metallkomplexe (pro Metall) Berechnete Spezierung mit Fulvinsäuren Fulvinsäuren (als C) 5 mg/L; Ca 1.3x10-3 M; Mg 5x10-4 M; Alkalinität 3x10-3 M; Cu 5x10-8 M; Zn 5x10-8 M, pH 8.0. Wege von Metallen in die aquatische Umwelt Quellen von Metallen in Gewässern Atmosphärische Niederschläge (Verbrennungsprozesse usw.) Pb, Hg Meteorwasser (Dächer, Verkehr) Cu, Zn häusliche Abwässer (Cu-Installationen) Abwässer aus Gewerbe und Industrie Zn, Cd, Cr, Hg ... Erosion aus landwirtschaftlichen Böden Cu, Zn Minenabwässer (vgl. Unfall Aznalcollar: Zn, Pb, As, Cu, Sb, Co, Tl, Bi, Cd, Ag, Hg, Se) Beispiel: Herkunft von Kupfer im Abwasser Kanalisiertes Abwasser Meteorwasser Strassen Häusliche Abwässer Dachwässer (Abschätzung für Region Töss) (nach Meier, Boller et al. 1998) Metalle in Seen Atmosphäre Me gelöst, part. Regen, Aerosole Abwässer, Zuflüsse Me gelöst, part, MeNP. Wasser MeNP Me gelöst Men+MeL Gesteine, Boden Adsorption Me part., gelöst Mineralische Part. ≡Fe-O-Me ≡Al-O-Me Flüchtige Spezies ? Aufnahme Abbau Biota Me-Algen Trophischer Transfer Fe-, Mn-Oxid. Sedimente Fe(III) → Fe(II) Mn(IV) → Mn(II) Me part. Me2+ + HS- → MeS(s) Sedimentation Ausfluss Me gelöst, part Typische Konzentrationen von Metallen in Wassersäule von Seen Cu Konzentration nM (10-9 M) 10 - 30 Zn 10 - 40 Cd 0.05 - 0.1 Pb 0.02 - 1 Tiefenprofile Cu, Zn im Greifensee Januar September Tiefenprofile Zn, P, Si Zn: essentiell Zn:P ? Bindung von Metallen an Liganden im See - Fulvinsäuren, Huminsäuren - Starke Liganden, wahrscheinlich von Algen ausgeschieden Me2+ + L1 MeL1 K1 Me2+ + L2 MeL2 K2 L1, L2, K1, K2 experimentell bestimmt Cu, Zn, Cd in See Gelöst (M) Log [Me2 ] Cu 1- 3x10-8 -14 – -16 Zn 1 – 4x10-8 -9 – -10 Cd 0.05 – 0.2x10-9 -10 – -12 Bindung von Metallen an Partikeln - Bindung an Algen durch Adsorption und Aufnahme - Bindung an mineralischen Partikeln: FeOOH, MnO2 - abhängig von pH, Bindungsstellen an Partikeln Bestimmung von Sedimentationsraten Sedimentation Sedimentationsrate g m-2 d-1 Sedimentationsraten von Cu und Zn in Greifensee Cu Zn Sedimentationsraten von C, Mn im Greifensee C Mn Pb in Sedimenten aus Zugersee (Moor und Schaller 1996) Metalle in Flüssen - Konzentrationen und Abfluss - Wechselwirkungen mit Periphyton Transport im Fluss und Resuspension Me part Me part Sedimentation Me gelöst Me part Resuspension Me partikulär und gelöst - Verteilung Me partikulär/ Me gelöst: abhängig von Partikelzusammensetzung, Partikelgrösse, Komplexbildung in Lösung - Me partikulär nimmt mit Abfluss zu [Me(total)] =[Me(part.)] + [Me(gelöst)] Kupfer und Zink während Regen in einem kleinen Bach Me-Akkumulation in Periphyton - Wie hängt Metallakkumulation in Periphyton von Metallspeziierung im Wasser ab ? - Metallspeziierung: [Me2+], Me schwach komplexiert Akkumulation von Metallen im Periphyton Periphyton wächst auf künstlichen Substraten Metallakkumulation im natürlichen Biofilm Messungen bei natürlichen Konzentrationsänderungen oder Experimente mit zugegebenen Metallen und Liganden (Mikrokosmen) Messungen an Periphyton im Bach Periphyton auf Glasplatten exponiert Metallkonzentrationen nehmen bei Regen zu Messungen im Wasser und im Periphyton Konzentration und Spezierung von Cd in Bach 0.25 Cd (nM) 0.2 Cd2+ Cd-inorg Cd-FA 0.15 0.1 0.05 0 0.9 1.7 2.9 4.7 time (d) Aufnahme von Cd in Algen: Cd anstelle von Zn 5.7 Cd (nM or nmol/g) Cd in Periphyton während Regen Zeit (Bradac et al. 2010) Hg in Gewässern - Hg: toxisches Element - in natürlichen Gewässern: Hg(II), Hg(0), CH3Hg+ - flüchtige Spezies : Hg(0), CH3HgCl usw. - Umwandlungen zu CH3Hg+ - Akkumulation in Nahrungskette Zusammenfassung - Speziierung der Metalle in Lösung wichtig für ihr Verhalten in Gewässern und ihre Wechselwirkungen mit Organismen - Sedimentation in Seen reguliert Metallkonzentrationen in Wassersäule - Erhöhte Metallkonzentrationen in Bächen führen zu erhöhter Konzentration in Periphyton