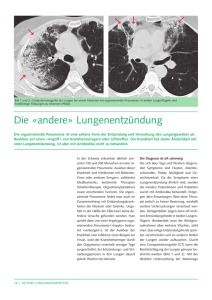
Nosokomiale Pneumonie Neues aus der Leitlinie
Werbung

Pneumologie | Commentary 2571 Nosokomiale Pneumonie Neues aus der Leitlinie Hospital-acquired pneumonia: news from the guidelines 3Aktuelle S3-Leitlinie: Die interdisziplinäre Leitlinie der deutschen Fachgesellschaften legt den Fokus auf gezielte mikrobiologische Diagnostik und risikoadaptierte Therapie. 3Welche Erreger? Staphylokokken, Enterobakterien und Nonfermenter stehen im Vordergrund. Die Situation wird zunehmend durch multiresistente Erreger wie MRSA, Enterobakterien mit Extended-spectrum-Betalaktamasen (ESBL), multiresistente Pseudomonas aeruginosa und Acinetobacter baumannii kompliziert. 3Invasive oder nichtinvasive Diagnostik? Inzwischen ist klar, dass beide Optionen bei korrekter Technik zu vergleichbaren Resultaten führen. Entscheidend ist, dass respiratorisches Material vor Beginn der antimikrobiellen Therapie abgenommen wird. 3Rechtzeitiger Therapiebeginn, rechtzeitige Deeskalation: Vor allem bei schweren Infektionen ist eine frühe, adäquate Initialtherapie innerhalb der ersten Stunden prognostisch wichtig. Die Therapie sollte also bereits bei klinischer Verdachtsdiagnose eingeleitet werden. Um eine Übertherapie und dadurch ausgelösten Selektionsdruck zu vermeiden, werden stringente Konzepte zur Deeskalation und Begrenzung der Therapiedauer empfohlen 3Monotherapie oder Kombinationstherapie? Dieses Thema wird weiter kontrovers diskutiert. Randomisierte Studien zeigten keine Überlegenheit der Kombinationstherapie. Allerdings erhöht diese die Treffsicherheit der Therapie bei Vorliegen multiresistenter Erreger (MRE). Die Leitlinie empfiehlt eine initiale Kombinationstherapie bei hohem Risiko für MRE. Falls mikrobiologisch keine MRE nachgewiesen werden und der Patient sich stabilisiert, kann 48–72 Stunden nach Therapiebeginn auf eine Monotherapie deeskaliert werden. Einleitung ▼ Die nosokomiale Pneumonie („hospital-acquired pneumonia“, international abgekürzt: HAP) ist unverändert eine ernste und häufige Komplikation im Laufe eines Krankenhausaufenthalts. Wesentliche Elemente des erfolgreichen Umgangs mit dieser Erkrankung sind präventive Maßnahmen für den vermeidbaren Anteil dieser Infektion, eine hohe Aufmerksamkeit für die rechtzeitige klinische Verdachtsdiagnose, eine adäquate mikrobiologische Diagnostik vor Therapiebe- ginn, die sichere Indikationsstellung für eine rechtzeitige, kalkulierte antimikrobielle Therapie und die Begrenzung des Antibiotikagebrauchs durch Deeskalation und weitestgehende Begrenzung der Therapiedauer. Neue S3-Leitlinie zur Epidemiologie, Diagnostik und Therapie der nosokomialen Pneumonie ▼ Die S3-Leitlinie [5] wurde in den Jahren 2010– 2012 von einer interdisziplinären Arbeitsgruppe auf der Basis einer systematischen Literaturrecherche erarbeitet. Sie unterscheidet sich von anderen Leitlinien darin, dass das international umstrittene Konzept der „health care associated pneumonia“ (HCAP) [7] nicht in die Definition der nosokomialen Pneumonie übernommen wird und dass Patienten mit definierter Immundefizienz wegen des unterschiedlichen Erregerspektrums ebenfalls nicht einbezogen sind. Patienten mit Charakteristika der HCAP unterscheiden sich in Mitteleuropa nicht wesentlich von Patienten mit ambulant erworbener Pneumonie. Die Leitlinie vermittelt in einem allgemeinen Teil zunächst einen Überblick zu Epidemiologie und Erregerspektrum der nosokomialen Pneumonie sowie den Eigenschaften häufig eingesetzter antimikrobieller Substanzen. Handlungsorientierte, evidenzbasierte Empfehlungen werden dann zu zentralen Fragen der Diagnostik und Therapie abgegeben, die Hintergründe hierfür im Fließtext erklärt. Neben der kalkulierten Therapie werden auch Empfehlungen zur gezielten Therapie bei positivem Erregernachweis sowie zum Vorgehen bei Therapieversagen gegeben. Die Empfehlungen wurden nach dem GRADE-System abgefasst, das neben der Evidenzqualität der berücksichtigten Literatur gleichrangig eine Abwägung von Nutzen und Risiko sowie Nutzen und Aufwand im klinischen Kontext vornimmt. Graduierung und Empfehlungsstärke entsprechen der Methodik der Nationalen Versorgungsleitlinien. Auf Empfehlungen zur Prävention der nosokomialen Pneumonie wurde bewusst verzichtet. Die Leitliniengruppe verweist hierzu auf die Empfehlungen des Robert Koch-Instituts. Welche Erreger? ▼ Die wesentliche Änderung im Erregerspektrum der nosokomialen Pneumonie besteht in einem Anstieg der Rate multiresistenter Erreger (MRE) K. Dalhoff1 J. Lorenz2 Pneumologie, Infektiologie Pneumologie | Commentary Schlüsselwörter nosokomiale Pneumonie HAP S3-Leitlinie q q q Keywords hospital-acquired pneumonia HAP German guideline q q q Institut 1Medizinische Klinik III – Pneumologie / Infektiologie, Universitätsklinikum Schleswig-Holstein 2Klinik für Pneumologie und Internistische Intensivmedizin (Infektiologie, Schlafmedizin), Klinikum Lüdenscheid Bibliografie DOI 10.1055/s-0032-1327324 Online Publikation: 19.11.2012 Dtsch Med Wochenschr 0 2012; 1370 0:2571–2573 · © Georg Thieme Verlag KG · Stuttgart · New York · ISSN 0012-04721439-4 13 Korrespondenz Prof. Dr. med. Klaus Dalhoff Medizinische Klinik III – Pneumologie / Infektiologie, Universitätsklinikum Schleswig-Holstein Ratzeburger Allee 160 23538 Lübeck Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. Was ist neu ? Pneumologie | Commentary Tab. 1 Risikofaktoren für multiresistente Infektionserreger (MRE) bei nosokomialer Pneumonie. Antimikrobielle Therapie Hospitalisierung > 4 Tage (late-onset) Invasive Beatmung > 4–6 Tage Aufenthalt auf Intensivstation Malnutrition Strukturelle Lungenerkrankung Bekannte Kolonisation durch MRE Aufnahme aus Langzeitpflegebereichen, chronische Dialyse, Tracheostomalträger, offene Hautwunden wie MRSA, ESBL-bildende Klebsiellen und E.-coli-Stämme sowie gram-negative Nonfermenter [12]. Zu diesen gehören Pseudomonas aeruginosa und Acinetobacter baumannii, die meist bereits intrinsisch Resistenzen gegenüber mehreren Breitspektrumantibiotika aufweisen. Stämme, die nur noch gegenüber Reserveantibiotika wie Colistin empfindlich sind, stellen auch auf deutschen Intensivstationen keine Seltenheit mehr dar. Für den klinischen Umgang mit dem Problem der Multiresistenz ist neben der Beachtung der Hygienevorschriften eine gute Einschätzung des individuellen Risikos für die Akquisition von Infektionen mit MRE entscheidend. q Tab. 1 zeigt klinische Risikofaktoren, die an derartige Infektionen denken lassen sollten. Darüber hinaus ist die Kenntnis des lokalen Erreger- und Resistenzspektrums wichtig, da sich Krankenhäuser unterschiedlicher Versorgungsstufen, Fachabteilungen und Regionen in dieser Hinsicht deutlich unterscheiden. Unter den nichtbakteriellen Erregern spielen Candida spp. bei der HAP keine Rolle; mit Aspergillusinfektionen ist dagegen insbesondere bei Langzeitbeatmung und schweren Komorbiditäten wie struktureller Lungenkrankheit im Einzelfall zu rechnen. Klinische Relevanz Für eine erfolgreiche antimikrobielle Therapie der nosokomialen Pneumonie ist die Abschätzung des Risikos multiresistenter Erreger entscheidend. Grundlage hierfür sind die Beurteilung klinischer Risikofaktoren und die Kenntnis des lokalen Erregerspektrums. Invasive oder nichtinvasive Diagnostik? ▼ Rechtzeitiger Therapiebeginn, rechtzeitige Deeskalation ▼ Die Frage, ob eine invasive, d. h. bronchoskopische Diagnostik der einfacheren Materialentnahme durch tracheobronchiale Absaugung überlegen ist, wurde lange kontrovers diskutiert. Inzwischen besteht hinreichende Evidenz dafür, dass nichtinvasive und invasive Materialentnahme sich im mikrobiologischen Ergebnis nicht deutlich unterscheiden, wenn die Asservierung sorgfältig und standardisiert erfolgt [3]. Ein verlässlicher Schwellenwert zwischen signifikanten und nichtsignifikanten Keimzahlen existiert nicht, eine semiquantitative Aufarbeitung ist dennoch zur Abschätzung der Bedeutung der Isolate empfehlenswert. Prognostisch gibt es nach überwiegender Evidenz ebenfalls keine Differenzen zwischen nichtinvasivem und invasivem Vorgehen. Entscheidend ist, dass die Materialentnahme überhaupt erfolgt und dass sie vor Einleitung der antimikrobiellen Therapie durchgeführt wird. Schwerpunkt der mikrobiologischen Aufarbeitung bleiben Ausstrich und Kultur mit Antibiogramm sowie im Einzelfall Antigentests [11], da molekulare Methoden noch nicht ausreichend für den klinischen Einsatz validiert sind. Im Gegensatz zu früheren Aussagen verschlechtert ein Probentransport über maximal 24 Stunden bei gekühlter Lagerung die Ergebnisqualität nicht wesentlich [6]. Neben der Diagnostik aus respiratorischem Material wird die Abnahme von Blutkulturen empfohlen, die allerdings nur selten positiv ausfallen. Ihr Wert besteht neben dem Nachweis einer Bakteriämie insbesondere in der Aufdeckung extrapulmonaler Infektionsquellen. Zur erfolgreichen Steuerung der Therapie gehört ein zügiger Therapiebeginn, da in großen Kohortenstudien gezeigt werden konnte, dass bei schweren Infektionen eine rasche, adäquate Initialtherapie die Prognose verbessert [10]. Dies erklärt die Bedeutung einer rechtzeitigen klinischen Verdachtsdiagnose, die bislang durch Biomarker und Scores nicht zu ersetzen ist. Bei Verdacht auf pneumogene Sepsis sind zusätzlich Sepsismarker wie Procalcitonin und Sepsis-Scores hilfreich. Um einen unnötigen Antibiotikaeinsatz zu vermeiden, wird eine Reevaluation nach 48–72 Stunden empfohlen. Auf der Basis der klinischen Entwicklung, einer radiologischen Kontrolle, der Beatmungssituation und der mikrobiologischen Ergebnisse sollte die antimikrobielle Therapie abgesetzt werden, falls sich die Verdachtsdiagnose Pneumonie nicht bestätigt hat. Ansonsten erfolgt eine Deeskalation bei Stabilisierung des Patienten. Die Therapiedauer soll im Regelfall auf 8 Tage begrenzt werden [4]. Klinische Relevanz Eine mikrobiologische Diagnostik aus respiratorischem Material sollte bei der nosokomialen Pneumonie immer vor Einleitung der antimikrobiellen Therapie erfolgen. Eine sorgfältige Entnahmetechnik und Verarbeitung ist notwendig. Die Entscheidung über die Anwendung invasiver oder nichtinvasiver Verfahren kann individuell erfolgen, da sich die Ergebnisse hinsichtlich der Prognose nicht unterscheiden. Klinische Relevanz In der Therapie der nosokomialen Pneumonie hat sich das Deeskalationsprinzip durchgesetzt. Um den Antibiotikaeinsatz und damit die Selektion von multiresistenten Erregern zu begrenzen, werden wirksame Konzepte zur Deeskalation einer initial breiten Therapie und zur Begrenzung der Therapiedauer empfohlen. Die Entscheidung hierüber sollte im Anschluss an eine Reevaluation 2–3 Tage nach Therapiebeginn getroffen werden. Monotherapie oder Kombinationstherapie? ▼ Um die Treffsicherheit der antimikrobiellen Therapie zu gewährleisten, empfiehlt die Leitlinie bei hohem Risiko für Infektionen mit MRE eine initiale Kombinationstherapie. Dieses Thema wird kontrovers diskutiert, da in zwei randomisierten Studien [2, 9] kein Unterschied zwischen einer Monotherapie mit sehr breitem Spektrum und einer Kombinationstherapie gefunden wurde und eine Metaanalyse unter Einschluss älterer Studien zu dem gleichen Ergebnis kam [1]. Allerdings waren in einer der randomisierten Studien Infektionen mit multire- Dtsch Med Wochenschr 2012; 137: 2571–2573 · K. Dalhoff u. J. Lorenz, Nosokomiale Pneumonie Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. 2572 Tab. 2 Differenzialdiagnose der nosokomialen Pneumonie (HAP). Bei korrekter Diagnose 3 Infektion mit primär resistenten bakteriellen oder nicht bakteriellen Erregern 3 Resistenzentwicklung unter Therapie 3 Unterdosierung der antimikrobiellen Therapie 3 Superinfektion mit „neuem“ Erreger 3 Einschmelzende/organübergreifende Infektion (z. B. Lungenabszess, Pleuraempyem) Diese Diagnosen können durch adäquate mikrobiologische Diagnostik bzw. thorakale Bildgebung bestätigt oder ausgeschlossen werden. Bei Fehldiagnose HAP 3 Interstitielle Lungenerkrankung (z. B. kryptogen organisierende Pneumonie [COP], medikamenös induzierte Pneumonitis) 3 Kongestive Herzinsuffizienz 3 Lungenembolie/Lungeninfarkt 3 Alveoläre Hämorraghie 3 Aspirationssyndrom 3 Atelektase Die Überprüfung dieser Diagnosen erfordert Echokardiographie, Bronchoskopie mit Differenzialzytologie bzw. Angio-CT sistenten Erregern unterrepräsentiert [9], in der anderen nur ein Kombinationspartner gegen gram-negative MRE wirksam [2]. Das Hauptargument für die Empfehlung einer initialen Kombinationstherapie bestand für die Leitliniengruppe in der höheren Wahrscheinlichkeit, auf diese Weise MRE mit zumindest einer Substanz zu erreichen. Hierzu gibt es u. a. Evidenz in einer retrospektiven Kohortenstudie, in der ausschließlich beatmungsassoziierte Pneumonien mit Nachweis von P. aeruginosa untersucht wurden [8]. Um andererseits einen unnötigen Antibiotikaeinsatz und den damit verbundenen Selektionsdruck auf die körpereigene Darmflora zu begrenzen, empfiehlt die Leitlinie 48– 72 Stunden nach Therapiebeginn auf eine Monotherapie zu deeskalieren, falls mikrobiologisch keine MRE nachgewiesen wurden und der Patient sich stabilisiert hat. Dies kann bei Nachweis eines ursächlichen Erregers gezielt erfolgen; wenn kein Erreger nachgewiesen wurde, sollte in der Regel auf die Betalaktamkomponente deeskaliert werden. Falls sich zu diesem Zeitpunkt keine Stabilisierung gezeigt hat, sollten Diagnose und Therapie überprüft werden. Hierzu empfiehlt sich ein strukturiertes Vorgehen (q Tab. 2). Eine weitere Option der Therapie von MRE besteht in der zusätzlichen inhalativen Applikation von Aminoglykosiden oder Colistin. Für diese Therapieform wird wegen spärlicher Evidenz in der Leitlinie keine generelle Empfehlung gegeben. Im Einzelfall sollte aber die kombinierte sys- temisch/inhalative Antibiotikatherapie geprüft werden, wenn Infektionen vermutet werden, die auf systemischem Weg allein nicht erfolgversprechend behandelt werden können. Klinische Relevanz Generell besteht kein Vorteil einer antimikrobiellen Kombinationstherapie der nosokomialen Pneumonie. Bei dringendem Verdacht auf Infektionen mit multiresistenten Erregern wird eine initiale Kombinationstherapie dennoch empfohlen, um die Wahrscheinlichkeit einer bereits zu Beginn der Behandlung adäquaten Therapie zu erhöhen. 4 Chastre J, Wolff M, Fagon JY et al. Comparison of 8 vs 15 days of antibiotic therapy for ventilator-associated pneumonia in adults. JAMA 2003; 290: 2588–2598 5 Dalhoff K, Abele-Horn M, Andreas S et al. Epidemiologie, Diagnostik und Therapie erwachsener Patienten mit nosokomialer Pneumonie. Pneumologie 2012; 66: im Druck 6 de Lassence A, Joly-Guillou ML, Salah A et al. Accuracy of delayed (24 hours) processing of bronchoalveolar lavage for diagnosing bacterial pneumonia. Crit Care Med 2004; 32: 680–685 7 Ewig S, Welte T, Chastre J et al. Rethinking the concepts of community-acquired and health-care-associated pneumonia. Lancet Infect Dis 2010; 10: 279–287 8 Garnacho-Montero J, Sa-Borges M, Sole-Violan J et al. Optimal management therapy for Pseudomonas aeruginosa ventilator-associated pneumonia: an observational, multicenter study comparing monotherapy with combination antibiotic therapy. Crit Care Med 2007; 35: 1888–1895 9 Heyland DK, Dodek P, Muscedere J et al. Randomized trial of combination versus monotherapy for the empiric treatment of suspected ventilator-associated pneumonia. Crit Care Med 2008; 36: 737–744 10 Kumar A, Roberts D, Wood KE et al. Duration of hypotension before initiation of effective antimicrobial therapy is the critical determinant of survival in human septic shock. Crit Care Med 2006; 34: 1589–1596 11 Meersseman W, Lagrou K, Maertens J et al. Galactomannan in bronchoalveolar lavage fluid: a tool for diagnosing aspergillosis in intensive care unit patients. Am J Respir Crit Care Med 2008; 177: 27–34 12 Nationales Referenzzentrum für Surveillance von nosokomialen Infektionen. KISS (Krankenhaus-Infektions-SurveillanceSystem). www.nrz-hygiene.de/surveillance/kiss Autorenerklärung: K.D. hat Honorare für nicht produktgebundene Vorträge von Astra-Zeneca, Bayer Vital, GSK, MSD Novartis und Pfizer erhalten sowie klinische Auftragsstudien für Johnson + Johnson, Cerexa und Optimer durchgeführt. J.L. hat Vortragshonorare von Pfizer erhalten. Literatur 1 Aarts MA, Hancock JN, Heyland D et al. Empiric antibiotic therapy for suspected ventilator-associated pneumonia. Crit Care Med 2008; 36: 108–117 2 Brunkhorst FM, Oppert M, Marx G et al. Effect of empirical treatment with moxifloxacin and meropenem vs meropenem on sepsis-related organ dysfunction in patients with severe sepsis. JAMA 2012; 307: 2390–2399 3 Canadian Critical Care Trials Group. A randomized trial of diagnostic techniques for ventilator-associated pneumonia. N Engl J Med 2006; 355: 2619–2630 Prof. Dr. med. K. Dalhoff Medizinische Klinik III – Pneumologie/Infektiologie, Universitätsklinikum Schleswig-Holstein Prof. Dr. med. J. Lorenz Klinik für Pneumologie und Internistische Intensivmedizin (Infektiologie, Schlafmedizin), Klinikum Lüdenscheid Dtsch Med Wochenschr 2012; 137: 2571–2573 · K. Dalhoff u. J. Lorenz, Nosokomiale Pneumonie 2573 Heruntergeladen von: Thieme E-Books & E-Journals. Urheberrechtlich geschützt. Pneumologie | Commentary