Lithium-Iminofluorsilan und Natriumfluorsilylamid
Werbung
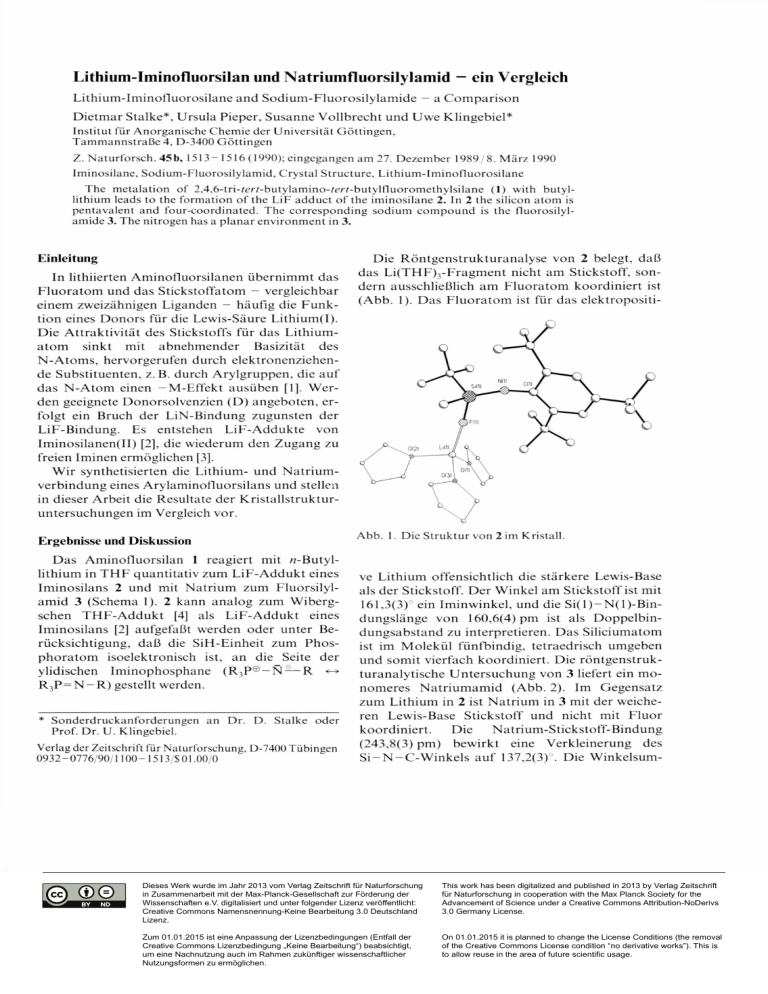
Lithium-Iminofluorsilan und Natriumfluorsilylamid - ein Vergleich Lithium-Iminofluorosilane and Sodium-Fluorosilylamide - a Com parison Dietm ar Stalke*, Ursula Pieper, Susanne Vollbrecht und Uwe Klingebiel* Institut für Anorganische Chemie der Universität Göttingen, Tammannstraße 4, D-3400 Göttingen Z. Naturforsch. 45b, 1513 - 1516 (1990); eingegangen am 27. Dezember 1989/8. März 1990 Iminosilane, Sodium-Fluorosilylamid, Crystal Structure, Lithium-Iminofluorosilane The metalation o f 2,4,6-trw m -butylam ino-te/'/-butylfluorom ethylsilane (1) with butyllithium leads to the formation o f the LiF adduct o f the iminosilane 2. In 2 the silicon atom is pentavalent and four-coordinated. The corresponding sodium com pound is the fluorosilylamide 3. The nitrogen has a planar environment in 3. Einleitung In lithiierten Aminofluorsilanen übernimmt das Fluoratom und das Stickstoffatom - vergleichbar einem zweizähnigen Liganden — häufig die F unk­ tion eines Donors für die Lewis-Säure Lithium(I). Die A ttraktivität des Stickstoffs für das Lithium ­ atom sinkt mit abnehmender Basizität des N-Atom s, hervorgerufen durch elektronenziehen­ de Substituenten, z. B. durch Arylgruppen, die au f das N-Atom einen -M -E ffekt ausüben [1], W er­ den geeignete Donorsolvenzien (D) angeboten, er­ folgt ein Bruch der LiN-Bindung zugunsten der LiF-Bindung. Es entstehen LiF-Addukte von Iminosilanen(II) [2], die wiederum den Zugang zu freien Iminen ermöglichen [3]. W ir synthetisierten die Lithium- und N atrium ­ verbindung eines Arylaminofluorsilans und stellen in dieser Arbeit die Resultate der K ristallstrukturuntersuchungen im Vergleich vor. Ergebnisse und Diskussion Das Aminofluorsilan 1 reagiert mit «-Butyllithium in T H F quantitativ zum LiF-Addukt eines Iminosilans 2 und mit Natrium zum Fluorsilylamid 3 (Schema 1). 2 kann analog zum Wibergschen TH F-A ddukt [4] als LiF-Addukt eines Iminosilans [2] aufgefaßt werden oder unter Be­ rücksichtigung, daß die SiH-Einheit zum Phos­ phoratom isoelektronisch ist, an die Seite der ylidischen Iminophosphane (R 3P® —N ——R R 3P = N - R ) gestellt werden. * Sonderdruckanforderungen an Dr. D . Stalke oder Prof. Dr. U. Klingebiel. Verlag der Zeitschrift für Naturforschung, D-7400 Tübingen 0932-0776/90/1100- 1513/$ 01.00/0 Die R öntgenstrukturanalyse von 2 belegt, daß das Li(TH F)3-Fragm ent nicht am Stickstoff, son­ dern ausschließlich am Fluoratom koordiniert ist (Abb. 1). Das Fluoratom ist für das elektropositi- Abb. 1. Die Struktur von 2 im Kristall. ve Lithium offensichtlich die stärkere Lewis-Base als der Stickstoff. Der Winkel am Stickstoff ist mit 161,3(3)° ein Iminwinkel, und die S i(l)-N (l)-B in dungslänge von 160,6(4) pm ist als Doppelbin­ dungsabstand zu interpretieren. Das Siliciumatom ist im Molekül fünfbindig, tetraedrisch umgeben und somit vierfach koordiniert. Die röntgenstruk­ turanalytische U ntersuchung von 3 liefert ein m o­ nomeres Natrium am id (Abb. 2). Im Gegensatz zum Lithium in 2 ist Natrium in 3 mit der weiche­ ren Lewis-Base Stickstoff und nicht mit Fluor koordiniert. Die Natrium-Stickstoff-Bindung (243,8(3) pm) bewirkt eine Verkleinerung des S i-N -C -W in k e ls auf 137,2(3)°. Die Winkelsum- Dieses Werk wurde im Jahr 2013 vom Verlag Zeitschrift für Naturforschung in Zusammenarbeit mit der Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. digitalisiert und unter folgender Lizenz veröffentlicht: Creative Commons Namensnennung-Keine Bearbeitung 3.0 Deutschland Lizenz. This work has been digitalized and published in 2013 by Verlag Zeitschrift für Naturforschung in cooperation with the Max Planck Society for the Advancement of Science under a Creative Commons Attribution-NoDerivs 3.0 Germany License. Zum 01.01.2015 ist eine Anpassung der Lizenzbedingungen (Entfall der Creative Commons Lizenzbedingung „Keine Bearbeitung“) beabsichtigt, um eine Nachnutzung auch im Rahmen zukünftiger wissenschaftlicher Nutzungsformen zu ermöglichen. On 01.01.2015 it is planned to change the License Conditions (the removal of the Creative Commons License condition “no derivative works”). This is to allow reuse in the area of future scientific usage. D . Stalke et al. - L ith iu m -Im in o flu o rsilan und N atrium fluorsilylam id 1514 Tab. I. Ausgewählte Bindungslängen (pm) und -winkel (°) im Vergleich. Abb. 2. Die Struktur von 3 im Kristall. me am Stickstoff beträgt 357,2°, dam it ist der Stickstoff innerhalb der Fehlergrenzen trigonal­ planar umgeben. Die Planarität des Stickstoffs er­ klärt sich aus der Wechselwirkung des N atrium s mit beiden freien Elektronenpaaren des Stick­ stoffs. In die gleiche Richtung weist der Befund, daß sowohl die S i(l)-N (l)-B in d u n g mit 164,5(3) pm als auch die C (l)-N (l)-B in d u n g mit 140,8(5) pm länger ist als in der vergleichbaren Li­ thiumverbindung 2 (Tab. I). W ährend sich bei 2 Verbindung 2 Verbindung Imin 2 Amid 3 Alkalimetall Li Na Winkel [°] S i(l)-N (l)-C (l) 161,3 137,2 Bindungslänge [pm] N (l) -C ( l) N ( 1) Si( 1) Si( 1) F(1) 136,2 160,6 167,6 140,8 164,5 163,7 die freien Elektronenpaare des Stickstoffs an der SiN- und der CN-Bindung beteiligen, hat der Stickstoff in 3 anionischen Charakter. Tab. I hebt die wesentlichen Unterschiede der beiden Verbin­ dungen noch einmal hervor. In Tab. II finden sich ausgewählte Bindungslängen und -winkel, in den Tab. III und IV sind die Koordinaten und Auslenkungsparam eter der Verbindungen 2 und 3 wie­ dergegeben. Die kristallstrukturanalytischen Befunde erklä­ ren die gegenüber dem Aminofluorsilan 1 nach hö­ herem Feld verschobenen 29Si-NMR- und zu tiefe­ rem Feld verschobenen 19F-NM R-Resonanzen der Alkaliverbindungen 2 und 3. Tab. II. Ausgewählte Bin­ dungsabstände (pm) und -win­ kel Q . Verbindung 3 Si( 1 ) —F( 1 ) S i( l)- N ( l) F( 1) Li( 1) L i ( l ) - 0 ( 1) L i( l ) - 0 ( 2 ) L i( l ) - 0 ( 3 ) N (l) -C ( l) 167,6(3) 160,6(4) 185,5(8) 192,1(7) 196,5(9) 195,1(8) 136,2(6) Si( 1) F( 1 ) Si( 1) N ( 1 ) N a (l) -N ( l) N a (l) -0 (1 ) N a (l)-0 (2 ) N a (l) -0 (3 ) N (l) -C ( l) 163,7(2) 164,5(3) 243,8(3) 231,8(3) 236,1(3) 244,2(3) 140,8(5) F( 1) —Si( 1) —N (l) F( 1)—Si( 1) —C( 19) N( 1) —Si( 1)-- C( 19) F( 1) Si( 1) —C(23) N ( 1) —Si( 1)- -C(23) C( 19) Si( 1) -C (2 3 ) Si( 1) F( 1) —L i(l) F( 1) Li( 1) —0 ( 1 ) F( l ) - L i ( l ) - 0 ( 2 ) 0 ( 1) —Li( 1) -- 0 ( 2 ) F( 1)—Li( 1) —0 (3 ) 0 ( 1) Li( 1)--0 (3 ) 0 ( 2 ) - L i( l ) - -0 (3 ) Si( l ) - N ( l ) - -C (l) 114,6(2) 99,0(2) 115,1(2) 98,3(2) 117,3(2) 109,9(2) 156,6(3) 110,1(4) 111,2(4) 99,8(4) 117,6(4) 114.4(4) 101,9(4) 161,3(3) F (l) -S i( l)- N ( l) F ( l) - S i( l) - C ( 1 9 ) N ( 1) Si( 1) C( 19) F ( l) - S i( l) - C ( 2 0 ) N ( l) - S i( l) - C ( 2 0 ) C (1 9 )-S i(l)-C (2 0 ) S i(l)-N (l)-N a (l) N (l)-N a (l)-0 (3 ) N (l)-N a (l)-0 (1 ) 0 (3 )-N a (l)-0 (l) N (l)-N a (l)-0 (2 ) 0 (3 ) -N a ( l)- 0 (2 ) 0 (l)-N a (l)-0 (2 ) S i( l)- N ( l)- C (l) N a (l) -N ( l)- C ( l) 113,3(1) 103,7(2) 116,2(2) 97,8(2) 114,5(2) 109,2(2) 117,6(2) 127,4(1) 116,3(1) 94,3(1) 127,1(1) 8 8 , 1( 1 ) 94,8(1) 137,2(3) 102,4(2) D. Stalke et al. ■ L ithium -Im inofluorsilan und N atrium fluorsilylam id 1515 Tab. III. Atomkoordinaten (* 104) und äquivalente iso­ trope Auslenkungsparameter (pm 2 x l 0 -1) von Verbin­ dung 2 . Tab. IV. A tom koordinaten (x 104) und äquivalente iso­ trope Auslenkungsparameter (pm 2 x l 0 “') von Verbin­ dung 3. Atom u eq* A tom X y 35(1) 44(1) 37(2) 35(1) 27(1) 29(1) 32(1) 31(1) 35(2) 31(1) 38(2) 50(2) 50(2) 57(2) 40(2) 64(2) 71(3) 71(2) 42(2) 51(2) 51(2) 57(2) 51(2) 67(2) 80(3) 78(3) 62(2) 43(1) 52(2) 126(4) 107(3) 52(2) 56(1) 88(3) 142(5) 139(6) 61(2) 59(1) 86(3) 73(2) 73(3) 66(2) S i(l) N a (l) F (l) N (l) C (l) C(2) C(3) C(4) C(5) C(6) C(7) C(8) C(9) C(10) c ( i 1) C (12) C( 13) C(14) C (15) C(16) C(17) C(18) C(19) C(20) C(21) C(22) C(23) 0 (3 ) C(32) C(33) C(34) C(35) 0 (1 ) C(24) C(25) C(26) C(27) 0 (2 ) C(28) C(29) C(30) C(31) 3219(1) 4454(1) 2643(1) 3597(2) 3424(2) 2831(2) 2694(2) 3131(2) 3726(2) 3910(2) 2280(2) 2707(2) 1666(2) 1838(3) 2944(2) 3129(4) 2108(3) 3421(3) 4612(2) 5088(3) 4357(3) 5174(2) 2629(3) 3927(3) 3498(3) 4345(3) 4515(3) 5824(2) 6292(2) 7096(3) 7080(3) 6316(3) 4585(2) 4543(3) 4313(5) 4165(3) 4537(3) 4340(2) 4998(3) 4777(3) 3996(4) 3682(3) 3071 5170(1) 4138(2) 3404(3) 3194(3) 3809(3) 3519(3) 2676(3) 2145(3) 2372(3) 4773(4) 5760(4) 4137(4) 5509(4) 2418(4) 3563(5) 2120(5) 1351(5) 1697(3) 1021(4) 718(4) 2597(4) 1638(4) 3076(4) 2918(5) 4288(5) 2043(5) 5212(3) 5770(5) 5708(5) 4894(9) 4646(5) 6090(3) 5469(4) 6392(5) 7527(5) 7381(4) 7041(3) 7611(5) 8576(5) 8257(6) 7583(5) S i(l) F (l) L i(l) N (l) Q i) C(2) C(3) C(4) C(5) C(6) C(7) C(8) C(9) C(10) C d 1) C(12) C( 13) C(14) C( 15) C (16) C(17) C (18) C (19) C(20) C(21) C(22) C(23) 0 (1 ) C(24) C(25) C(26) C(27) 0 (2 ) C(28) C(29) C(30) C (3 1) 0 (3 ) C(32) C(33) C(34) C(35) y 1224 1171(2) 1327(6) 106(3) - 810(3) -1 6 9 3 (3 ) -2 5 6 3 (3 ) -2 6 5 5 (3 ) -1 8 4 3 (4 ) - 966(3) -1 7 2 9 (4 ) -1 4 1 9 (4 ) -1 0 1 6 (4 ) -2 8 2 6 (4 ) -3 5 9 1 (4 ) -4 1 3 8 (5 ) -4 4 3 9 (5 ) -3 2 3 7 (5 ) - 209(4) - 155(5) 897(4) - 593(4) 1904(4) 1123(5) 2810(5) 2364(5) 2187(5) 475(3) 534(4) - 114(8) - 691(8) - 224(5) 2727(3) 2853(6) 3909(7) 4441(6) 3748(4) 1249(3) 2143(6) 1827(5) 897(5) 429(5) 8273(1) 8831(2) 9734(4) 8103(2) 8212(2) 8613(2) 8791(2) 8578(3) 8113(2) 7893(2) 8886(3) 8218(3) 9607(3) 9140(4) 8812(3) 8079(3) 9262(4) 9331(4) 7285(3) 6573(3) 7620(3) 6962(3) 7379(3) 6890(3) 7612(4) 6864(4) 8872(4) 9668(2) 8951(3) 9084(5) 9752(5) 10200(3) 9783(2) 10291(5) 10583(7) 10163(5) 9591(4) 10741(2) 11044(4) 11754(4) 12028(3) 11309(3) z 8955 8159(2) 7600(4) 9174(2) 9422(2) 8958(3) 9287(3) 10029(3) 10439(3) 10159(3) 8109(3) 7616(3) 8132(3) 7681(3) 10389(3) 10626(4) 9809(4) 11101(4) 10617(3) 10087(3) 10935(3) 11334(3) 8640(3) 8059(4) 8253(5) 9351(5) 9658(4) 6565(2) 6141(3) 5376(5) 5370(5) 6068(3) 7345(2) 6727(4) 6915(7) 7558(8) 7792(4) 8117(2) 8670(5) 9000(4) 8413(5) 8043(4) z 6096(1) 7238(1) 5651(1) 6942(1) 7582(2) 7780(2) 8420(2) 8913(2) 8740(2) 8108(2) 7313(2) 7016(2) 6716(2) 7734(2) 9611(2) 10079(2) 9475(2) 10023(2) 8010(2) 8692(2) 7430(2) 7831(2) 5893(2) 5556(2) 4766(2) 5634(2) 5761(2) 7369(1) 8010(2) 7984(3) 7422(3) 7017(3) 8328(1) 8954(2) 9397(3) 9005(3) 8436(2) 6608(1) 6513(3) 5972(2) 5599(3) 6121(2) u eq* 35(1) 37(1) 51(1) 30(1) 24(1) 27(1) 30(1) 29(1) 26(1) 25(1) 36(2) 41(2) 50(2) 53(2) 35(2) 76(3) 66(2) 63(2) 31(1) 45(2) 43(2) 39(2) 55(2) 37(2) 62(2) 65(2) 63(2) 40(1) 50(2) 67(2) 150(5) 61(2) 42(1) 46(2) 101(4) 69(2) 54(2) 44(1) 72(2) 64(2) 102(3) 60(2) * Äquivalente isotrope U berechnet als ein Drittel der Spur des orthogonalen Ü -T en sors. * Äquivalente isotrope U berechnet als ein Drittel der Spur des orthogonalen U^-Tensors. Experimenteller Teil tropft. Nach 2 h wird 1 destillativ gereinigt und an­ schließend aus «-Hexan umkristallisiert. 1: C , 3H 4?FNSi, Mol.-Gew.: 379,68; Ausbeute 3,2 g (42%); Sdp.: 91 °C/0,01 mbar; Fp. - 60 °C; MS (70 eV): m /z = 379 (M +); IR (Film): v = 3375 cm “ 1 (NH); 'H -N M R : Ö = -0 ,1 9 SiMe (3/ hf = 6,5 Hz), 1,07 SiCM e 3 (V HF = 1,1 Hz), 1,29 4-CM e 3C 6H „ 1,46 2 ,6 -C M e,C Ji„ 3,06 NH, 7,15 C 6H-,; 13C-NM R: ö = -7 ,1 7 SiCH 3 (2JCF = 21,93 Hz), 18,45 SiCC 3 (VCF = 18,94 Hz), 26,95 Die Versuche wurden unter Feuchtigkeitsaus­ schluß ausgeführt. NM R-Spektren: 30-proz. Lö­ sungen in CDCI 3 (1) bzw. C 6H 6/C 6D 6 (2, 3), TMS int., Bruker-AM 250-Kernresonanzgerät. Aminofluorsilan (1) 0,02 mol (CM e 3)MeSiF 2 werden rasch zu 0,02 mol LiNHC 6H 2(CMe 3)3 in 50 ml Toluol ge- 1516 D. Stalke et al. ■ L ithium -Im inofluorsilan und N atrium fluorsilylam id SiCC3, 30,33 4-CC 3C6, 31,46 2,6-CC 3C6, 34,46 4-CC 3C6, 37,09 2,6-CC 3C6, 122,83 3,5-C 6 (V CF = 1,98 Hz), 145,41 4-C6, 148,16 2,6-C 6 (VCF = 1,80 Hz); l9F-NM R: ö = 29,03; 29Si-NM R: S = -0 ,1 ( / SiF = 299,55 Hz). Iminqfluorsilan (2) 0,01 mol 1 werden mit n-Butyllithium in 50 ml «-Hexan/THF lithiiert. Die Reaktionslösung wird kurz bis zum Sieden erhitzt. Durch Abkühlung auf Raum tem peratur kristallisiert 2 nach kurzer Zeit aus. C 35H 65F L iN 0 3Si, Mol.-Gew.: 601,93; Ausbeute 5,9 g (98%); 'H -N M R : ö = 0,21 SiMe, 1,01 SiCMe 3 (V hf = 1,2 Hz), 1,27 K X C H ,C H ,),k 1,37 4-CM e 3C 6H 2, 1,54 2,6-CMe 3C 6H „ 3,31 K X CH.CH Qk 13C-NM R: ö = - l , 3 l " S i C H 3 (2/ cf = 27,04 Hz), 22,06 SiCC 3 (2/ CF = 23,04 Hz), 25,58 [OC0CJ3, 29,97 SiCC3, 31,85 4-CC 3C6, 32,29 2.6-CC 3C6, 33,14 4-CC 3H 6, 34,08 2,6-CC 3C6, 68,10 [OC 2C2]3, 122,56 3,5-C6, 135,84 4-C6, 142,57 1-C6 (3/ cf = 4,73 Hz), 148,83 2,6-C 6 (V CF = 1,77 Hz); 19F-NM R: ö = 41,93; 29Si-NMR: ö = -24,45 (282,69 Hz). Fluorsilylam id (3) 0,01 mol 1 und 0,005 mol Styrol werden in 10 ml T H F gelöst und zu 0,01 mol N atrium in 30 ml T H F getropft. Anschließend erhitzt man unter Sieden des Lösungsmittels bis zum Ende der R eak­ tion. Die Reaktionslösung wird mit 5 ml Toluol versetzt. Beim Abkühlen auf - 8 °C kristallisiert 3 zu farblosen Kristallen aus. C 35H 65F N N a 0 3Si, Mol.-Gew.: 617,98; Ausbeu­ te 6,0 g (97%); 'H -N M R : ö = 0,44 SiMe (3/ HF = 5,08 Hz), 1,31 SiCMe3, 1,34 4-CM e 3C 6H 2, 1,38 rO (C H ,C H ,),k 1,82 2,6-CMe 3C 6H „ “ 3,27 [0(CHoCH,)2]3, 7,45 N C 6H 2; , 3C -N M R :'^ = 1,36 SiCH3, 21,21 SiCC3, 25,51 fb C 2C2]3, 29,39 SiCC3, 3 1 ,4 4 4-CC 3C6, 32,12 2,6-CC 3C6, 33,49 4-CC 3H 6, 37,15 2,6-CC 3C6, 67,95 [OC 2C2]3, 126,00 3,5-C6, 133,94 4-C6, 136,67 1-C6 (3/ CF = 1,97 Hz), 148,68 2.6-Q (VCF = 1,71 Hz); 19F-NM R: <5 = 39,39; 29SiNM R: ö = -2 9 ,2 (JsiF = 279,75 Hz). [1] D. Stalke, N. Keweloh, U. Klingebiel, M. N oltemeyer und G. M. Sheldrick, Z. Naturforsch. 42b, 1237(1987). [2] R. Boese und U. Klingebiel, J. Organomet. Chem. 315, C 17 (1986). [3] M. Hesse und U. Klingebiel, Angew. Chem. 98, 638 (1986). Kristallstruktur von 2 Kristalldaten: monoklin, Cc, a = 1301,0(3), b = 1703,4(3), c = 1748,8(3) pm, ß = 101,92(3)°, V = 3,791 nm 3, £ber = 1,060 M g m '3, Z = 4, //M oK ffStrahlung; G raphitm onochrom ator, /u = 0,09 m m -1, 4938 gesammelte Reflexe, davon 2527 unabh., 2452 beob., mit F > 3erF verfeinerte Para­ meter: 377, 2 9 max. = 45°, R = 0,048, Rw = 0,051, w 1 = cr2(F) + 0,0005 F 2, maximale Restelektro­ nendichte: + 2 ,2 x l0 2, -2 ,4 x 102 enm 3, ^-Verfei­ nerung von + 1 auf - 1,5(4) darauffolgende Inver­ sion der Koordinaten, GOOF: 2,28. Kristallstruktur von 3 Kristalldaten: m onoklin, P 2 ,/a, a = 1829,9(3), b = 1087,9(2), c = 1971,2(3) pm, ß = 107,33(1)°, V = 3,746 nm 3, ^ber = 1,096 M gm -3, Z = 4, //(M o K J = 0,11 m m "1, 8366 gesammelte Reflexe, davon 4856 unabh., 3831 beob., mit F > 4erF, ver­ feinerte Parameter: 378, 26 max. = 45°, R = 0,074, Rw = 0,076, w “' = cr2(F) + 0,0002 F 2, maximale Restelektronendichte: +6,52x 102, - 4 ,0 X102 enm “3, GOOF: 2,75. Alle Messungen wurden auf einem Stoe-AED bei T = -8 5 °C durchgeführt, Strukturlösung und -Verfeinerung mit SHELX 86 [5], Beide Strukturen wurden durch Direkte Methoden gelöst. Alle Nichtwasserstoffatome wurden anisotrop verfei­ nert. Die W asserstoffatome wurden geometrisch ideal positioniert und nach dem Reitermodell in die Verfeinerung einbezogen. Weitere Einzelheiten zu den Kristallstrukturuntersuchungen können beim Fachinformationszentrum Karlsruhe, Gesellschaft für wissenschaft­ lich-technische Inform ation mbH, D-7514 Eggenstein-Leopoldshafen 2, unter Angabe der Hinterle­ gungsnummer CSD 54766, der Autoren und des Zeitschriftenzitats angefordert werden. F ür die Unterstützung dieser Arbeit danken wir dem Fonds der Chemischen Industrie und der Deutschen Forschungsgemeinschaft. [4] N . Wiberg, K. Schurz und G. Fischer, Angew. Chem. 97, 1058 (1985); N. Wiberg, K. Schurz. G. Reber und G. Müller, J. Chem. Soc. Chem. Commun. 1986, 591. [5] SH E L X - 8 6 , G. M. Sheldrick, Göttingen (1986).











