Molecular Structural Biology Molekulare Struktur
Werbung

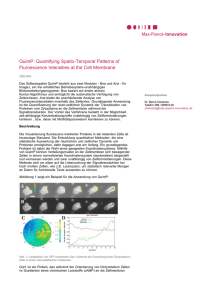
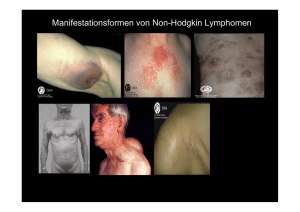
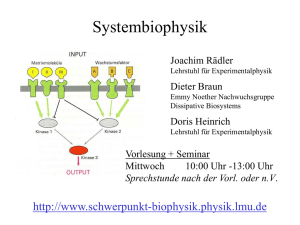
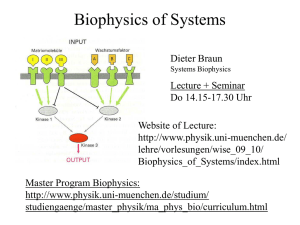
Forschungsabteilung Research Department Molekulare Strukturbiologie Entdeckungsreise zu den Landschaften des Lebens Molecular Structural Biology Expedition to the Landscapes of Life P r o f . D r. W o l f g a n g B a u m e i s t e r A Prof. Dr. Wolfgang Baumeister [email protected] www.biochem.mpg.de/baumeister uf den physischen Karten der Erde finden sich keine weißen Flecken mehr, im zellulären Nanokosmos dagegen gibt es noch unbekannte Landstriche: Große Proteinkomplexe bilden hier fragile molekulare Strukturen. Die Architektur dieser Moleküle aufzuklären, ist eine Herausforderung, der sich Wolfgang Baumeister und sein Team stellen. Als Pioniere der Strukturforschung entwickelten sie Methoden, die faszinierende Einblicke in die zelluläre Landschaft erlauben. In jeder Zelle arbeiten unzählige molekulare Maschinen unablässig daran, lebenswichtige Prozesse in Gang zu halten. Dazu gehören beispielsweise die zellulären Proteinfabriken (Ribosomen) und „Häckselmaschinen“ (Proteasomen), die defekte oder nicht mehr benötigte Proteine entsorgen. Aufgebaut sind die molekularen Maschinen aus Proteinen, die sich zu großen Komplexen zusammengeschlossen haben. Wie funktionieren diese Komplexe und wie arbeiten sie mit anderen Zellbestandteilen zusammen? Für die Beantwortung dieser Fragen sind Informationen über ihre Struktur unverzichtbar. Allerdings entzogen sich viele große Molekülkomplexe lange dem Blick der Strukturforscher, weil sie für die etablierten Untersuchungsmethoden zu groß oder zu instabil waren. Die Informationsverarbeitung und -speicherung im Gehirn basiert auf der Reizübermittlung durch Nervenzellen. Als Kontaktstellen zwischen zwei Nervenzellen, an denen die Signalweitergabe erfolgt, dienen sogenannte Synapsen. Mit Hilfe der Kryo-Elektronentomographie gelang es den Wissenschaftlern, die wichtigsten Strukturelemente der Synapse in noch nie erreichter Genauigkeit darzustellen. Die Abbildung zeigt die präsynaptische Endigung einer Nervenzelle. Hier befinden sich zahlreiche Vesikel (gelb), die Neurotransmitter enthalten. Durch die Freisetzung der Neurotransmitter in den synaptischen Spalt (rechts, hellgrün), werden Signale zum postsynaptischen Komplex (orange) der nächsten Nervenzelle übertragen. Neuronal communication underlies all forms of information processing and storage in the brain, and takes place at specialized neuronal compartments called synapses. Cryo-electron tomography revealed key structural components of this process at unprecedented resolution. The illustration shows the presynaptic terminal, where neurotransmitters contained in numerous vesicles (yellow) are released into the extracellular space. The postsynaptic complexes (orange) and the components of the synaptic cleft (right, light green) can also be seen. O n the physical maps of the world there are no longer any white spots denoting “terra incognita”, but in the nanocosmos of the cell, by contrast, there are still unexplored areas and uncharted territory: here large protein complexes form fragile molecular structures. Wolfgang Baumeister and his team have taken up the challenge to elucidate the architecture of these molecules. As pioneers of structural research they have developed methods which allow fascinating insights into the cellular landscape. In each cell countless molecular machines work ceaselessly to keep vital processes going. These include for example the protein factories (ribosomes) and the “shredders” (proteasomes), which dispose of defective or no longer needed proteins. This molecular machinery is made up of proteins which have joined forces in large complexes. How do these complexes function and how do they work together with other cell components? To answer these questions, information about their structure is indispensable. However, many of these large molecule complexes have long eluded the scrutiny of structural researchers, because they were too large or unstable for established research methods. Live und in 3D – Schnappschuss in die Zelle Ganz neue Möglichkeiten eröffnete Baumeister der Strukturforschung mit einer bahnbrechenden Entwicklung: Der Kryo-Elektronentomographie (CET), mit der dreidimensionale Strukturen der Zelle direkt untersucht werden können. Der Trick: Die gesamte Zelle oder einzelne Zellbestandteile werden blitzartig „schockgefroren“ und in glasartiges Eis eingeschlossen, sodass die fragile Zellarchitektur erhalten bleibt. Anschließend werden aus verschiedenen Blickwinkeln zweidimensionale Bilder des Objekts aufgenommen, aus denen dann ein dreidimensionales Bild rekonstruiert wird. Mittels dieser Liveschaltung in die Zelle können sogar flüchtige Interaktionen zwischen Molekülen sichtbar gemacht und so nie dagewesene Einblicke in die Zellfunktionen gewonnen werden. Baumeisters Expertise trug entscheidend dazu bei, dass die Baupläne molekularer Maschinen, die an Proteinfaltung und - abbau beteiligt sind, aufgeklärt werden konnten. Aber auch zahlreiche andere Zellstrukturen interessieren die Wissenschaftler, zum Beispiel Ribosomen, Poren in der Zellkernhülle, die Kontaktstellen zwischen Nervenzellen (Synapsen) oder auch Membranen und Zellwände. Langfristig wird so von immer mehr Zellen ein dreidimensionaler Atlas erstellt werden können, in dem es keine weißen Flecken mehr gibt. Live and in 3D – Snapshot into the Cell Baumeister opened up totally new possibilities for structural research with a groundbreaking development: cryo-electron tomography (CET), with which three-dimensional structures of the cell can be investigated directly. The trick: The entire cell or individual cell components are shock-frozen and enclosed in glass-like ice, thus preserving the delicate cell-like structure. Next, two-dimensional images are taken of the object from different perspectives, out of which then a three-dimensional image is reconstructed. By means of this live link into the cell, even fleeting interactions between molecules can be made visible, and insights into the cell function can be gained which were never possible before. With his expertise, Baumeister has made a significant contribution to the successful elucidation of molecular machines that are involved in protein folding and degradation. But numerous other cell structures also interest the scientists, for example ribosomes, pores in the cell nucleus membrane, the contact sites between nerve cells (synapses) or membranes and cell walls. Hence, from a long-term perspective, for more and more cells it will be possible to create a 3D atlas, in which there are no longer any white spots. Prof. Dr. Wolfgang Baumeister 1973 PhD in Biology, University of Düsseldorf 1973 – 1980 Research Associate, Dept. of Biophysics, University of Düsseldorf 1978 Habilitation in Biophysics, University of Düsseldorf 1981 – 1982 Heisenberg Fellowship, University of Cambridge, UK 1983 – 1988 Head of the Research Group Molecular Structural Biology at the MPI of Biochemistry, Martinsried, Germany Since 1988 Director of the Department Molecular Structural Biology at the MPI of Biochemistry, Martinsried, Germany Since 2000 Honorary Professor of Chemistry and Physics, TU Munich Wolfgang Baumeister has been honored with numerous awards for his research including the Otto Warburg Medal of the German Society for Biochemistry and Molecular Biology (1998), the prize of the Geneva-based Louis-Jeantet Foundation for Medicine (2003), the Ernst Schering Prize (2006), the Schleiden Medal of the German Academy of Sciences Leopoldina (2005) and the Harvey Prize in Science and Technology of the Technion, Haifa (2005). Endstation für Proteine: Das 26S-Proteasom ist eine molekulare Maschine, die defekte oder nicht mehr benötigte Proteine in kleinere Stücke zerlegt. Den Abbau bewerkstelligt der zentrale Komplex, das 20S-Proteasom. Dieses ist vom Bakterium bis zum Menschen einheitlich aufgebaut. In den Zellen von Eukaryonten assoziiert das 20S-Proteasom mit ein oder zwei regulatorischen Komplexen, die den Abbau von Substraten – unter anderem durch deren Entfaltung – vorbereiten (links). Die Tripeptidyl­ peptidase II (TPPII) baut die vom Proteasom generierten Fragmente weiter ab (rechts). End of the line for proteins: The 26S proteasome is a large molecular machine that degrades defective or redundant proteins into smaller fragments. The degradation is carried out by the core module, the 20S proteasome, which has a conserved structure in all living organisms from prokaryotes to humans. In eukaryotic cells the core complex associates with one or two regulating complexes preparing substrates for degradation, which includes their unfolding (left). The tripeptidyl peptidase II (TPPII), an even larger complex, further degrades the protein fragments released by the proteasome (right). Selected Publications Brandt, F., S.A. Etchells, J.O. Ortiz, A.H. Elcock, F.-U. Hartl and W. Baumeister (2009) “The native 3D organization of bacterial polysomes”, Cell 136, 261-271. Beck, M., V. Lucic, F. Förster, W. Baumeister and O. Medalia (2007) “Snapshots of nuclear pore complexes in action captured by cryoelectron tomography”, Nature 449, 611-615. Robinson, C.V., A. Sali and W. Baumeister (2007) “The molecular sociology of the cell”, Nature 450, 973-982. Research Group Leaders Dr. Radostin Danev, Dr. Harald Engelhardt, Dr. Vladan Lucic, Dr. István Nagy, Dr. Jürgen Plitzko, Dr. Beate Rockel 12 | 13