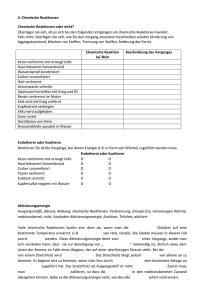
Chemische Gleichungen
Werbung

_________________________ Chemische Gleichungen __________________________________ Chemische Reaktionen werden durch chemische Gleichungen beschrieben. Chemische Gleichungen sollten die kleinstmöglichen Koeffizienten für die Edukte (Ausgangsstoffe) und Produkte enthalten ⇒ Stöchiometrie einer chemischen Gleichung Beispiel einer Rohgleichung: CH4 + O2 ⇒ CO2 + H2O Die korrekte Gleichung lautet: 91 _________________________ Die Verbrennung von Methan __________________________________ 92 _________________________ Ein Beispiel __________________________________ rot: Sauerstoff, blau: Stickstoff Schreibe die chemischen Formeln für die Edukte und Produkte und schreibe die balancierte Gleichung für diese chemische Reaktion. 93 _________________________ Noch ein Beispiel __________________________________ weiß: Wasserstoff, blau: Stickstoff Wieviel NH3 Moleküle müssen in der rechten Box stehen? 94 _________________________ Chemische Reaktionen: Kombinationsreaktion __________________________________ Bei einer Kombinationsreaktion reagieren zwei oder mehr Substanzen um ein Produkt zu bilden: 2Mg(s) + O2(g) ⇒2 MgO(s) 95 _________________________ Chemische Reaktionen: Zersetzungsreaktion __________________________________ In einer Zersetzungsreaktion reagiert ein Edukt zu zwei oder mehr Verbindungen: CaCO3 (s) ⇒ CaO (s) + CO2(g) Kalkstein (Seemuscheln) werden durch Erhitzen zu Kalk und CO2 zersetzt. Eine andere Zersetzungsreaktion ist die Reaktion, die den Airbag auslöst: 2 NaN3 (s) ⇒ 2 Na(s) + 3 N2 (g) Bei Aufprall wird ein Detonationsmechanismus ausgelöst, der zur explosionsförmigen Zersetzung von NaN3 (Natriumazid) führt (nur 100 g NaN3 erzeugen dabei ∼ 50 L N2 (Stickstoff)). 96 _________________________ Endotherme und exotherme chemische Reaktionen __________________________________ Im Rahmen chemischer Reaktionen werden chemische Bindungen gebrochen und neu gebildet. Um eine chemische Bindung zu brechen wird immer Energie benötigt. Diese Energie wird als Bindungsenthalpie bezeichnet und mit dem Symbol ∆H (kJ/mol) charakterisiert. Umgekehrt wird bei der Bildung einer neuen chemischen Bindung Energie frei. Je stärker die chemische(n) Bindung(en) in einem Molekül ist (sind), desto geringer ist generell seine Tendenz in einer chemischen Reaktion Veränderungen einzugehen. Für die Abschätzung von Reaktionsenthalpien ∆Hr (also die bei chemischen Reaktionen umgesetzten Energien) können die Bindungsenthalpien der Edukte (Ausgangsstoffe) und Produkte herangezogen werden. Dabei wird die Energie zum Brechen einer Bindung positiv gerechnet (+∆H) und die bei der Bildung neuer Bindungen freiwerdende Energie negativ (-∆H) (Systembezug !). Wird in der Gesamtbilanz einer Reaktion Energie frei, so nennt man die Reaktion exotherm und die entsprechende Reaktionsenthalpie ∆Hr ist negativ. Eine Reaktion für die insgesamt Energie aufgewendet werden muss (∆Hr ist positiv), nennt man endotherm. 97 _________________________ Endotherme und exotherme chemische Reaktionen __________________________________ Das “System“ ist die chemische Reaktion. 98 _________________________ Abschätzung von ∆Hr aus Bindungsenthalpien: ein Beispiel __________________________________ CH4 + Cl2 ⇒ CH3Cl + HCl ∆H ? 99 _________________________ Bindungsenthalpien für ausgewählte chemische Bindungen __________________________________ 100