Kursbuch Ultraschall - ReadingSample - Beck-Shop
Werbung

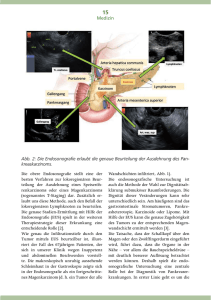
Kursbuch Ultraschall Nach den Richtlinien der DEGUM und der KBV Bearbeitet von Günter Schmidt, Prof. Dr. med. Christian Görg 5., überarbeitete und erweiterte Auflage 2008. Buch. 408 S. Gebunden ISBN 978 3 13 119105 2 Format (B x L): 19 x 27 cm Weitere Fachgebiete > Medizin > Klinische und Innere Medizin Zu Inhaltsverzeichnis schnell und portofrei erhältlich bei Die Online-Fachbuchhandlung beck-shop.de ist spezialisiert auf Fachbücher, insbesondere Recht, Steuern und Wirtschaft. Im Sortiment finden Sie alle Medien (Bücher, Zeitschriften, CDs, eBooks, etc.) aller Verlage. Ergänzt wird das Programm durch Services wie Neuerscheinungsdienst oder Zusammenstellungen von Büchern zu Sonderpreisen. Der Shop führt mehr als 8 Millionen Produkte. 30 Endo­sono­graphie U. Will Überblick 30.1 Einführung Nach der klinischen Untersuchung und der Laborchemie gilt die symptomorientierte perkutane Sonographie unbestritten als die Methode der Wahl zur ­Klärung einer unklaren abdominellen Beschwerdesymptomatik. Häufig werden hierbei nur indirekte Zeichen für einen organpathologischen Befund am Gastrointestinaltrakt – wie eine segmentale Aufweitung von Magen, Dünn- oder Dickdarm – als Hinweis auf eine existente Stenose erkannt, ohne dass eine eigentliche Ursache, wie z. B. eine pathologische Tumorkokarde, erkennbar wird. Selbst wenn diese zu verifizieren ist, lassen sich oft Entität und Dignität des pathologischen Prozesses nicht ausreichend einschätzen. Für die Diagnostik der intra- und extrahepatischen Cholestase gilt die Sonographie als überragend mit einer Sensitivität von nahezu 100 %. Aber auch hier lässt M1 M2 M3 sich die eigentliche Ursache der Cholestase sonographisch wie computertomographisch nur in 50–70 % erkennen. Der endoskopische Ultraschall (EUS) macht durch die Kombination von Endoskopie und interner Sonographie die bekannten Nachteile der abdominellen Sonographie in der Diagnostik folgender Bereiche z. T. wett: Ü intestinale Wandschichten (Abb. 30.1), Ü biliopankreatischer Bereich, Ü Mediastinum, Ü Retroperitoneum und Ü kleines Becken, insbesondere Perirektum für das Staging des Rektumkarzinoms. Abschlusskurs Nach einer Einführung und Methodenbeschreibung wird eine detaillierte Übersicht über Indikationen, vergleichende Wertigkeit des EUS gegenüber anderen bildgebenden Verfahren und praktische Anwendung im Bereich des Ösophagus, Magens und Duodenums sowie der angrenzenden Organe des pankreobiliären Systems vorgestellt. Andere Anwendungs­ bereiche des mediastinalen und retroperitonealen Lymphknotenstagings werden vorgestellt. Zum Staging von Rektumtumoren und in der inter­ ventionellen EUS zur endoskopischen diagnostischen Punktion und ­therapeutischen Drainage gilt der EUS als unverzichtbar. III Die direkte Ankopplung mit hohen Schallfrequenzen (5–20 MHz) an den endoskopisch auffälligen Befund oder an das pankreatobiliäre System ermöglicht eine SM1 1. Schicht - echodicht - Mukosaeintrittsreflex 2. Schicht - echoarm - Mukosa uT1 3. Schicht - echoreich - Submukosa 4. Schicht - echoarm - Lamina muscularis propria Abb. 30.1 Wandschichten des Darms. Endosonographie der Wand des Gastrointestinums zur Beurteilung der Tumoreindringtiefe. Frühkarzinome (T1) M = Mukosatyp SM= Submukosatyp UT1= Ultraschallstaging 5. Schicht - echoreich - Serosa, Adventitia, Perirektum 361 Schmidt u.a., Kursbuch Ultraschall (ISBN 9783131191052) © 2008 Georg Thieme Verlag KG Abschlusskurs Endo­sono­graphie III detailgetreue, hohe Auflösung im Diskriminanzbereich von 2–3 mm, welche mit keinem anderen bildgebenden Verfahren erreichbar ist. Die Endosonographie erlaubt zudem als einzige bildgebende Methode die exakte Darstellung der lamellären Grundstruktur der Gastrointestinalwand, sodass ein präinterventionelles Tumor­ staging möglich wird (Abb. 30.2 a, b). Störende Luftartefakte gibt es nicht, da die Ankopplung von intestinal über eine Wasserballon- oder luminale Wasservorlaufstrecke realisiert wird. Neben elektronischen Longitudinalscannern mit einem axialen 120°–170°-Sektorbildaufbau (HitachiPentax, Aloka-Olympus) sind sowohl elektronische und mechanische Radialscanner (270°, 360°) als auch elektronische Minisonden im Einsatz, die v. a. für den endoluminalen diagnostischen Schall anwendbar sind. Sie sind wesentlich preisgünstiger, verfügen aber nicht über einen Longitudinalschall und somit nicht über die Möglichkeit einer EUS-gesteuerten Feinnadelpunktion (EUS-FNP). Die elektronischen Scanner ermöglichen zusätzlich eine interne Farb- und Duplexsonographie von Gefäßen und Tumoren. Neuere Techniken wie Elastographie oder kontrastunterstützte Endosonographie zur nichtinterventionellen Entitäts- und Dignitätsanalyse erhöhen die Trefferrate. Die Hauptindikation der Endosonographie liegt im lokoregionären Tumorstaging, der Resektabilitätsbeurteilung gastrointestinaler Tumoren und der Detektion kleiner pankreatobiliärer Tumoren, die anderen Verfahren entgehen. Zudem gibt eine zusätzliche EUSFNP mit Histologie eine Antwort auf die Frage nach der therapeutischen Konsequenz eines zuvor in der Dignität unklaren Befundes. Tumorsuspekte Herdbefunde am pankreatobiliären System wie auch viszerale und mediastinale Lymphknoten können während der EUSUntersuchung mit Feinnadeln (19G, 22G) punktiert werden. Es gilt aber zu bedenken, dass die Rate falsch negativer und falsch positiver Feinnadelpunktionsergebnisse je nach Organ zwischen 5–15 % schwankt. Bei endoskopisch und histologisch gesichertem Primärtumor am Ösophagus, Magen, Duodenum oder Rektum oder einem Tumorverdacht (Sonographie/CT) am pankreatobiliären System sollte der EUS nur nach vorherigem Ausschluss von Fernmetastasen durchgeführt werden. Andernfalls wäre ein palliatives Therapie­ konzept zu verfolgen, für das die Kenntnis der lokalen Tumorausdehnung mit Überlegungen zu alternativen Therapiestrategien keine Rolle mehr spielt. Die Komplikationsraten der diagnostischen Endosonographie sind äußerst gering (<0,01 %). Neben leichtem Fieber und Dysphagie wird in Einzelfällen über eine Pankreatitis berichtet. Die Komplikationsraten der interventionellen EUS sind häufiger (1–3 %) – hier wird über Infektionen des Mediastinums, über infizierte Zysten sowie über Blutungen und Pankreatitiden berichtet. Eine antibiotische Kurzzeitprophylaxe ist bei geplanten Interventionen an Zysten oder vor Punktionen sinnvoll, insbesondere bei immunsupprimierten Patienten. Eine Dignitätsdiagnose allein anhand endosonographischer Kriterien ist bei fehlenden Infiltrationszeichen unmöglich. 30.2 EUS bei Ösophagustumoren Mit der perkutanen Sonographie können regelhaft die ersten 4 cm des Ösophagus hinter dem oberen Ösophagusmund von links lateral am Hals eingesehen werden, während die letzten 2 cm des distalen Ösophagus vor der Kardia der sonographischen Einsicht entgehen. Am Magen gibt es ebenfalls schlecht anschallbare Regionen (Fundus, proximaler Korpus). Mit der Endosonographie lassen sich der gesamte Ösophagus und Magen systematisch untersuchen; bei Vorliegen einer Stenose bedarf es allerdings der vorherigen Bougierung. a Abb. 30.2 a, b Frühkarzinom des Magens: uT1 m, echo­ arme Auftreibung der Mukosa. a EUS-Bild, Pfeile: Tumorausdehnung. b Endoskopisches Bild. b 362 Schmidt u.a., Kursbuch Ultraschall (ISBN 9783131191052) © 2008 Georg Thieme Verlag KG Bei Symptomen der Dysphagie, Anämie, Dyspepsie und Schmerzen ist eine Endoskopie erforderlich. Hierbei lässt sich die Ursache optisch erkennen und bioptisch verifizieren. Darüber hinaus fordert der Nachweis von Tumoren die Kenntnis der lokoregionalen Tumor­ ausdehnung als Grundlage für den Einsatz multimodaler Therapiekonzepte. Hierzu dient die EUS. Die Treffsicherheit der EUS im lokoregionärem Tumorstaging liegt zwischen 80–90 % für das T-Stadium und 70–80 % für das N-Stadium. Die Entscheidung für ein primär palliatives Vorgehen oder eine Operation in kurativer Absicht mit oder ohne neoadjuvante Radio-Chemotherapie wird durch die Kenntnis der Tumorausdehnung erleichtert. In fortgeschrittenen Stadien können aufwendige Untersuchungen und Explorativoperationen durch eine frühzeitige EUS vermieden werden, da der EUS mit einer Trefferrate um 85–90 % die Resektabilität richtig vorhersagen kann (Abb. 30.3, Abb. 30.4). Der EUS ermöglicht v. a. die Detektion früher Tumorstadien (uT1 m, N0; Abb. 30.2, Abb. 30.5 a, b, Abb. 30.6 a–c), die minimal invasiven Therapieverfahren wie die kurative endoskopische Mukosektomie bei Ösophagus- und Magenkarzinomen zugeführt werden können. Die Wahrscheinlichkeit von Lymphknotenmetastasen beim Mukosatyp liegt unter 1–3 %. Finden sich verdächtige Lymphknoten, kann vor einer geplanten Mukosektomie und zur Komplettierung des Staging die EUS mit einer FNP kombiniert werden. Patienten mit Ösophaguskarzinomen im Stadium uT3, N1 können keiner lokalen Tumortherapie zugeführt werden, vielmehr profitieren diese von einer neoadjuvanten Radio-Chemotherapie. 30.3 EUS bei Magentumoren Abb. 30.3 Fortgeschrittenes Ösophaguskarzinom mit In­ filtration der rechten Lunge. Abb. 30.4 Stenosierendes Ösophaguskarzinom mit Infil­ tration des rechten Stammbronchus und lokoregionären Lymphknotenmetastasen. Fortgeschrittene Tumoren des Magens können mit hoher Treffsicherheit in der Endosonographie gesehen werden. Der Nachweis von Aszites perigastral weist auf eine Peritonealkarzinose hin. In diesen Fällen sollte eine laparoskopische Exploration einer Operation vorgeschaltet werden. Bei infiltrativen Magenkarzinomen uT4, Nx hat die neoadjuvante Chemotherapie eine Berechtigung, da sich die R0-Resektionsraten deutlich erhöhen lassen (Abb. 30.7, Abb. 30.8). Der Wert der Endosonographie nach neoadjuvanter Chemotherapie von primär inoperablen oder lokal fortgeschrittenen Tumoren ist unsicher, die Trefferrate der Tumorausdehnung im Restaging beträgt maximal 50 %. Einzig die Größenregredienz lässt sich gut beurteilen und gilt als Kriterium für ein Ansprechen auf die Therapie. Im Allgemeinen führt eine peritumoröse Entzündung und ­Fibrose in der Umgebung gastrointestinaler Tumoren aufgrund des identischen Echomusters zu einem EUS-Overstaging von 10–20 %, während Mikroinvasionen des Tumors in angrenzende Gewebe in 5– 10 % nicht erkannt werden können (Understaging). Der EUS im Follow-up nach kurativer Resektion von Ösophagus- und Magentumoren ist die sicherste Methode, um intramurale oder perianastomosale Lokalrezidive frühzeitig zu erfassen. Bei gastralen Lymphomen (Maltome) kommt dem EUS eine richtungweisende Rolle in der Entscheidung über das therapeutische Vorgehen zu (Abb. 30.9). Im Stadium I1 n. Lugano (nur Mukosabeteiligung im EUS) und dem histologischen Nachweis eines niedrig malignen Lymphoms ist eine HP-Eradikationstherapie als Therapie der ersten Wahl gerechtfertigt. Abschlusskurs EUS bei Magentumoren III 363 Schmidt u.a., Kursbuch Ultraschall (ISBN 9783131191052) © 2008 Georg Thieme Verlag KG Endo­sono­graphie a a b Abschlusskurs c III b Abb. 30.5 a, b Frühkarzinome eines Plattenepithelkarzinoms im Ösophagus im EUS mit isolierter echoarmer Verdi­ ckung der Mukosa (Pfeil). Abb. 30.6 a–c Barrett-Karzinom, uT1 m, endoskopische ku­ rative Mukosektomie. Abb. 30.7 Echoarmes transmurales exzentrisches Magenkar­ zinom mit lokoregionärem Lymphknoten – uT3, N1. Abb. 30.8 Diffus wachsendes Magenkarzinom mit Pseu­ dolamellierung. 364 Schmidt u.a., Kursbuch Ultraschall (ISBN 9783131191052) © 2008 Georg Thieme Verlag KG Remissionsraten von 70–80 % werden beschrieben. Endoskopisch-bioptische und endosonographische Verlaufskontrollen sind halbjährlich angezeigt. Patienten mit lokal fortgeschrittenen hochmalignen Maltomen (I2, II2, III,) können sofort chemotherapeutisch behandelt werden, eine Explorativlaparotomie wird den Patienten somit erspart. Niedrig maligne Maltome im Stadium I2, II2 sollten einer Strahlentherapie unterzogen werden; ein operatives Vorgehen bleibt im Einzellfall auf die niedrig malignen Tumoren II1, 2 als alternative Methode beschränkt (Abb. 30.9, 30.10). Die Endosonographie vermag bei negativen gastralen Biopsien von makroskopisch vergröberten Falten oder unklaren Vorwölbungen gut zwischen malignen, infiltrativen Wandprozessen und anderen mukosal oder intramural gelegenen Prozessen zu unterscheiden. Die auffallend verdickte Lamina muscularis propria bei einer scheinbar erhaltenen Schichtung wird neben dem Szirrhuskarzinom nur bei Lymphomen gesehen (Abb. 30.8). Dieser EUS-Befund ist Grundlage für forcierte endoskopisch bioptische Techniken (Rugektomie), um die Diagnose eines szirrhösen Magenkarzinoms histologisch zu sichern oder auszuschließen. Wenn bei Impressionen durch angrenzende Organe, die endoskopisch als unklare Vorwölbungen imponieren, eine regelrechte lamelläre Schichtung der Wand im EUS erkennbar ist, kann auf weiterführende Untersuchungen oder endoskopische Kontrollen verzichtet werden (Abb. 30.11). Intramurale Tumoren als Ursache solcher endoskopisch auffälligen Vorwölbungen lassen sich im EUS den entsprechenden Wandschichten gut zuordnen, sodass bereits hierdurch eine Einordnung der Entität erfolgen kann. Lipome zeigen sich als echodichte, glatt konturierte Tumoren, die spindelförmig in der 3. Schicht der Submukosa gelegen sind; eine weiterführende Diagnostik ist nicht erforderlich (Abb. 30.12). GIST-Tumoren („gastro-intestinale Stroma-Tumore“) weisen eine potenziell maligne Potenz auf. Sie sind von Leiomyomen im B-Bild nicht zu unterscheiden. Beide werden von der 2. Schicht (Lamina muscularis mucosae) oder der 4. Schicht (Lamina muscularis propria) generiert. Die weiterführende Diagnostik dieser 70 % der mesenchymalen Tumoren des Magens ausmachenden GIST-Typen kann durch endoskopische Resektion (2. Schicht) oder EUS-FNP mit Immunhistologie (CD 117) erfolgen (Abb. 30.13, Abb. 30.14). Bei positivem Nachweis ist eine Exstirpation anzustreben. Hinter echoarmen, gemischt echogenen und irregulär die Schichtung nicht akzeptierenden Tumoren mit oder ohne lokoregionär suspekten Lymphknoten können sich folgende pathologische Prozesse verbergen: Ü neuroendokrine Tumoren (NET), Ü Metastasen, Ü Plasmozytome Ü und Sarkome. Abschlusskurs EUS bei Magentumoren III Abb. 30.10 Maltom im Stadium II1 – Infiltration bis Submu­ kosa mit lokoregionären Lymphknoten. Abb. 30.9 Maltom Stadium EI2 – transmurale Infiltration. Abb. 30.11 Impression des Antrums durch die Gallenblase, Nebenbefund: Cholesterolpolypen. 365 Schmidt u.a., Kursbuch Ultraschall (ISBN 9783131191052) © 2008 Georg Thieme Verlag KG Endo­sono­graphie Sie sind daher stets einer histologischen Klärung zuzuführen (Abb. 30.15, Abb. 30.16). Endosonographische Verlaufskontrollen (halbjährlich oder jährlich) sind bei kleineren intramuralen Tumoren (1–2 cm) angezeigt, wenn diese als Zufallsbefunde bei asymptomatischen Patienten entdeckt wurden und keine Hinweise auf Überschreitung der generierenden Schicht erkennbar sind. Abschlusskurs 30.4 EUS bei Kolon- und Rektumtumoren Bei der perkutanen Sonographie des Gastrointestinaltrakts kann man häufig pathologische echoarme Wandverdickungen sehen, deren Dignität sich durch die Endoskopie mit Biopsie klären lässt. Bei malignen Tumoren des Kolons folgt die unmittelbare Operation; die Beurteilung der lokalen Tumorausdehnung hat keine Konsequenz auf die Therapieentscheidung, sodass bei Kolontumoren auf eine EUS verzichtet werden kann. Eine Ausnahme bilden größere, endoskopisch nur mit höherem Risiko abzutragende Adenome. Bei diesen kann in Einzelfällen durch Einsatz der Minisonde nach einer Tiefeninfiltration oder suspekten lokoregionären Lymphknoten gefahndet werden, die dann einer endo­ skopischen Intervention entgegenstehen. Der EUS ist hingegen bei Rektumtumoren stets obligat. Die Trefferquote des EUS im lokoregionalen Tumorstaging liegt zwischen 85–95 % für das T-Stadium und 60–70 % für das N-Stadium beim Rektumkarzinom (Abb. 30.17, Abb. 30.18). Aus der Infiltrationstiefe lassen sich differenzierte therapeutische Vorgehensweisen ableiten (endoskopische Abtragung bei uT1 m, TEM bei uT1 s, anteriore Resektion uT1–3 N0, neoadjuvante Radio-Chemotherapie bei uT3, N1). In der Nachsorge von Patienten nach minimal-invasiven Eingriffen bei Rektumtumoren kommt dem EUS eine hervorragende Bedeutung in der Detektion von lokoregionären Rezidiven zu. Endoskopisch nicht zu sichernde extraluminale Rezidive können früher erfasst und mit einer EUS-FNP gesichert werden. Nach minimal-invasiven Eingriffen (TEM, transrektale endoskopische Mucosaresektion) sollte deshalb der EUS in halbjährlichen Abständen über zwei Jahre als Screeningverfahren in Kombination mit der Rektoskopie durchgeführt werden. III Abb. 30.12 Lipom im Duodenum. Abb. 30.13 Kleiner mesenchymaler Tumor der Lamina muscularis propria (Distanzmarken). Abb. 30.14 GIST im Magen, gut vaskularisiert. Abb. 30.15 Neuroendokriner Tumor im Duodenum. 366 Schmidt u.a., Kursbuch Ultraschall (ISBN 9783131191052) © 2008 Georg Thieme Verlag KG