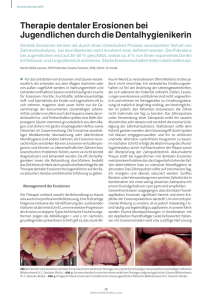
Der Einfluss von Maaloxan auf die Remineralisation des Schmelzes
Werbung

Aus der Universitätsklinik für Zahn-, Mund- und Kieferheilkunde der Albert-Ludwigs-Universität Freiburg i. Br. Abteilung für Zahnerhaltungskunde und Parodontologie Der Einfluss von Maaloxan auf die Remineralisation des Schmelzes und den oralen pH-Wert nach erosiven Attacken The Influence of Maaloxan on Enamel Remineralisation and oral pHValue after acidic Attacks INAUGURAL-DISSERTATION zur Erlangung des Zahnmedizinischen Doktorgrades der Medizinischen Fakultät der Albert-Ludwigs-Universität Freiburg i. Br. Vorgelegt 2012 von Nele Bärsch geboren am 31. Oktober 1983 in Berlin Dekan: Prof. Dr. Dr. h.c. mult. Hubert Erich Blum 1. Gutachter: Prof. Dr. Elmar Hellwig 2. Gutachter: Prof. Dr. Dr. Rainer Schmelzeisen Jahr der Promotion: 2012 Widmung Dem der ist, der war und der immer sein wird. Dafür, dass Er mich durch mein Leben trägt und ich durch Ihn alles vermag. „Erschrick nicht und hab keine Angst, denn ich der HERR, dein Gott, bin bei dir, wohin du auch gehst.“ (Josua 1,9) Und all denen, die mich auf diesem Weg begleiten und begleitet haben. Inhaltsverzeichnis Inhaltsverzeichnis 1. Einleitung ................................................................................................................5 2. Literaturübersicht ....................................................................................................7 2.1 Kariöse Zahnhartsubstanzdefekte .................................................................... 7 2.1.1 Definition .................................................................................................... 7 2.1.2 Ätiologie ..................................................................................................... 7 2.2 Nicht-kariöse Zahnhartsubstanzdefekte ........................................................... 8 2.3 Erosionen ......................................................................................................... 9 2.3.1 Definition .................................................................................................... 9 2.3.2 Klinisches Bild .......................................................................................... 10 2.3.3 Klassifizierung .......................................................................................... 10 2.3.4 Prävalenz ................................................................................................. 12 2.3.5 Ätiologie ................................................................................................... 15 2.3.5.1 Extrinsische Genese .......................................................................... 15 2.3.5.1.1 Ernährung .................................................................................... 15 2.3.5.1.1.1 chemische Einflüsse…....………………………………….............16 2.3.5.1.1.2 biologische Einflüsse………………………………………………..18 2.3.5.1.1.3 verhaltensbezogene Einflüsse……………………………………..19 2.3.5.1.2 Sport und Beruf ........................................................................... 20 2.3.5.1.3 Mundhygieneprodukte und Medikamente .................................... 21 2.3.5.2 Intrinsische Genese ............................................................................ 22 2.3.6 Prävention ................................................................................................ 23 2.3.7 Therapie ................................................................................................... 23 2.3.7.1 Kausal ................................................................................................ 24 2.3.7.2 Symptomatisch .................................................................................. 24 2.4 Assoziierte Erkrankungen ............................................................................... 25 2.4.1 Bulimia Nervosa ....................................................................................... 25 2.4.2 Reflux ....................................................................................................... 26 2.4.3 Weitere Ursachen intrinsisch bedingter Erosionen.................................... 27 2.5 Antacida ......................................................................................................... 28 2.5.1 Definition .................................................................................................. 28 2.5.2 Indikation .................................................................................................. 29 Inhaltsverzeichnis 2.5.3 Chemie und Wirkungsweise ..................................................................... 29 2.5.4 Unerwünschte Wirkungen ........................................................................ 30 3. Material und Methode ...........................................................................................31 3.1 Vorversuch ..................................................................................................... 31 3.2 Aufbau der Studie und Versuchsplan ............................................................. 31 3.3 Probenherstellung .......................................................................................... 32 3.4 Schienenherstellung ....................................................................................... 34 3.5 Probandenauswal ........................................................................................... 34 3.6 Bravo® pH-Überwachungssystem ................................................................. 34 3.7 Maalox 70mVal Suspension ........................................................................... 35 3.8 Messverfahren zur Auswertung der Proben ................................................... 35 3.8.1 pH-Wert .................................................................................................... 36 3.8.2 Mikrohärte ................................................................................................ 36 3.8.3 Transversale Mikroradiographie ............................................................... 37 3.9 Statistische Auswertung ................................................................................. 38 4. Ergebnisse ............................................................................................................39 4.1 pH-Werte ........................................................................................................ 39 4.2 Mikrohärte ...................................................................................................... 43 4.3 Transversale Mikroradiographie ..................................................................... 43 5. Diskussion ............................................................................................................46 5.1 Material und Methode ..................................................................................... 46 5.1.1 Versuchsaufbau ....................................................................................... 46 5.1.2 Messverfahren ....................................................................................... 488 5.2 Ergebnisse ..................................................................................................... 49 5.2.1 pH-Wert-Messung .................................................................................. 499 5.2.2 Mikrohärte .............................................................................................. 499 5.2.3 Transversale Mikroradiographie ............................................................... 50 5.3 Fazit ............................................................................................................... 50 6. Zusammenfassung ...............................................................................................51 7. Literaturverzeichnis ..............................................................................................52 8. Danksagung .........................................................................................................68 Einleitung 1. Einleitung Seit etwa 60 Jahren findet sich in unserer westlichen Kultur ein verändertes Ernährungsverhalten: Der Konsum saurer Lebensmittel und Getränke ist deutlich angestiegen. Gerade in Zusammenhang mit neuen Diäten und Wellnessprogrammen wird der Verzehr von Rohkost, Fruchtsäften und isotonischen Fitnessgetränken propagiert. Eine ganze Reihe von Lebensmitteln und Getränken enthält Säure in Form von Geschmackstoffen oder Konservierungsmitteln. Zudem finden Säurungsmittel als Bestandteile von Medikamenten eine weite Verbreitung. Unter anderem sind sogenannte nicht-kariöse Zahnhartsubstanzdefekte Folge des übermäßigen Säurekonsums. Wobei Erosionen die häufigste Erscheinungsform darstellen. Sie entstehen nach häufigem Erbrechen oder dem Konsum saurer Nahrungsmittel, Getränke oder Medikamente. Dadurch sinkt der orale pH-Wert. Sobald der kritische pH-Wert von 5,5 in der Mundhöhle unterschritten wird, setzt an der Zahnoberfläche ein Demineralisationsprozess ein. Andererseits wird durch die Säure auch die Speichelsekretion gefördert, wodurch sich der Speichel nach und nach von selbst wieder neutralisiert. Werden Werte von über halb pH 5,5 erreicht, beginnt ein Remineralisationsprozes. Während extrinsische, vor allem durch Nahrungsmittel bedingte Säureangriffe durch eine Umstellung der Ernährung therapiert werden können, stellen intrinsische Säureangriffe durch Magensäure ein erheblich schwierigeres therapeutisches Problem dar. Hauptursache ist hier das Erbrechen oder der Reflux von Magensäure, welches oft als Symptom einer Grunderkrankung einzuordnen ist. In diesem Zusammenhang sind vor allem psychisch bedingte Essstörungen wie Bulimie aber auch gastrooesophagealer Reflux (GERD), chronischer Alkoholabusus und Schwangerschaft zu nennen. Hier ist eine Therapie oft schwierig. Die Schäden an den Zähnen jedoch zeigen sich bereits nach relativ kurzer Zeit. Oft ist der Zahnarzt der erste Arzt, der eine entsprechende Verdachtsdiagnose stellt und somit ein möglichst frühes therapeutisches Eingreifen ermöglicht. 5 Einleitung Bislang versucht man symptomatisch diese Säure bedingten Schäden durch das Spülen mit remineralisationsfördernden Mundhygieneprodukten in ihrem Ausmaß einzuschränken. Dabei werden fluorid-, kalzium- und phosphat- sowie zinnhaltige Verbindungen eingesetzt. Der Therapieerfolg ist jedoch sehr eingeschränkt. Ein neuartiger Therapieansatz besteht darin auf den pH-Wert des Speichels Einfluss zu nehmen. Durch das Spülen mit Pufferlösungen sollen die H+-Ionen im Mund gebunden und der intraorale pH-Wert schneller neutralisiert werden. Die Zeitspanne des erosiven Angriffes auf die Zahnhartsubsanz verkürzt sich und die Remineralisierung findet schneller statt. Ziel der vorliegenden Studie soll es sein den oralen pH-Wert nach Säureexposition mit einem Softgetränk zu messen. Im Anschluss wird in einer Gruppe nach der Säureexposition mit einer magnesium-/aluminiumhaltigen Lösung gespült, während in der Kontrollgruppe lediglich mit Wasser nachgespült wird. Es wird erwartet, dass nach dem Spülen mit der Lösung der orale pH-Wert schneller wieder ansteigt als in der Kontrollgruppe. 6 Literaturübersicht 2. Literaturübersicht 2.1 Kariöse Zahnhartsubstanzdefekte 2.1.1 Definition Karies ist eine lokalisiert auftretende, unspezifische, opportunistische Infektionserkrankung der Zahnhartsubstanz, die zu einem irreversiblen Verlust des mineralisierten Gewebes führt (Arends, 1969; König, 1971) und durch organische Säuren verursacht wird (Coogan und Motlekar, 1996). 2.1.2 Ätiologie Bereits Ende des 19. Jahrhunderts wurde die in ihrer Grundform heute immer noch gültige Theorie der chemoparasitären Kariesentstehung beschrieben. Sie besagt, dass Karies durch im Mund lebende, säureproduzierende Bakterien verursacht wird (Miller, 1899; Williams, 1897). Heute weiß man, dass an der Entstehung einer kariösen Läsion zahlreiche Faktoren beteiligt sind, die sich gegenseitig bedingen und beeinflussen. Die zentrale Rolle spielen dabei die Faktoren Wirt, Substrat und Mikroorganismus (Keyes, 1962). Später wurde dem Modell noch der Faktor Zeit hinzugefügt (König, 1971). An der Oberfläche eines gründlich gereinigten Zahnes bildet sich innerhalb kurzer Zeit eine dünne Schicht aus Speichelbestandteilen, die acquired Pellikel. Recht schnell lagern sich Verstoffwechselung Bakterien, vor allem niedermolekularer Streptokokken, Kohlenhydrate setzen an. die Durch die Bakterien organische Säuren wie Laktat und Pyruvat frei. Diese wiederum lassen den intraoralen pH-Wert abfallen, was zu einer erhöhten Löslichkeit der Zahnhartsubstanzen führt. Dabei gehen Kalzium und Phosphat aus Schmelz und Dentin in Lösung und werden vom Speichel abtransportiert. Ein Prozess, der als Demineralisation der Zahnhartsubstanz bezeichnet wird. Das orale Puffersystem ist bis zu einem gewissen Grad in der Lage diesen alltäglich ablaufenden Prozess zu kompensieren. In der Säure enthaltene Protonen werden durch Speichelbestandteile neutralisiert und Kalzium und Phosphat können im demineralisierten Schmelz präzipitieren, es kommt zur Remineralisation der Zahnhartsubstanz. Erst, wenn dieses Gleichgewicht aus Demineralisation und Remineralisation durch die oben genannten Faktoren in Richtung Demineralisation verlagert wird entsteht ein kariöser Defekt (Hellwig et al., 2009). 7 Literaturübersicht Betrachtet man diese chemischen Prozesse detailliert, so lässt sich zusammenfassend sagen, dass eine Karies das Ergebnis eines vor allem in tieferen Zahnschichten stattfindenden Prozesses ist, der sich nur bedingt an der Oberfläche zeigt. Die bakteriell produzierte Säure diffundiert in tiefer gelegene Zahnschichten und führt dort zur Konzentrationsgradient Auflösung folgend der mineralisierten diffundieren Kalzium Substanzen. und Phosphat Ihrem an die Zahnoberfläche. Hier nehmen ihre Konzentrationsgradienten und damit ihre Diffusionsgeschwindigkeit ab. Beide Mineralien können präzipieren und neue Kristalle ausbilden. Dadurch entsteht eine so genannte pseudointakte Oberfläche. Im Gegensatz dazu stehen die nicht-kariösen Zahnhartsubstanzdefekte. Sie stellen in erster Linie ein Oberflächenphänomen dar (Attin, 2009). Die Demineralisationsprozesse finden direkt an den oberflächlichsten Schichten des Zahnes statt (Wiegand und Attin, 2010). 2.2 Nicht-kariöse Zahnhartsubstanzdefekte Im Laufe des Lebens werden Zähne verschiedenen mechanischen und chemischen Einflüssen ausgesetzt, durch die es zu unterschiedlichen Formen der Abnutzung kommt, den nicht-kariösen Zahnhartsubstanzdefekten. Je nach Art und Weise ihrer Entstehung werde sie in Erosionen, Abrasionen, Attritionen und Abfraktionen/Abflexionen bzw. keilförmigen Defekten unterteilt (Gallien et al., 1994). Oft überlagern sich die verschiedenen Prozesse, da die vorgeschädigten Zähne den verursachenden Faktoren gegenüber weniger resistent sind (Lussi et al., 1991). Erosionen Nicht-bakteriell, chemisch verursachter oberflächlicher Zahnhartsubstanzverlust wird als dentale Erosion beschrieben (Zipkin und McClure, 1949). Siehe dazu 2.3. Abrasionen Durch die mechanische Einwirkung exogener Hartsubstanzen auf die Zähne kommt es im Laufe der Zeit zu Abnutzungserscheinungen. Sie stellen sich im Allgemeinen als konkave, glattflächige Vertiefungen dar (Kaidonis et al., 1992). Erosiv erweichte Zahnhartsubstanz ist für Abrasionen besonders anfällig. In Folge kann es vor allem beim Zähneputzen zu einem hohen Substanzabtrag kommen (Addy und Hunter, 2003; Noack, 1989). Aber auch Angewohnheiten wie das Kauen 8 Literaturübersicht auf Fingernägeln, Stiften oder Tabakpfeifen können abrasive Defekte verursachen, sogenannte Usuren (Schumacher, 1997). Iatrogen können Abrasionen durch im Rahmen konservierender und prothetischer Versorgung verwendeter Materialien (z.B. Füllungsmaterialien, Metallklammern, Prothesenzähne) hervorgerufen werden (Mericske-Stern, 2007). Ebenso tragen orale Weichgewebe durch eine kontinuierliche Einwirkung auf erodierte Zahnflächen ihren Teil zur Entstehung abrasiver Defekte bei (Gregg et a., 2004). Durch Nahrung verursachte Abrasionen werden auch als Demastikationen bezeichnet (Imfeld T, 1996). Attritionen Der direkte Kontakt zwischen Antagonisten oder Nachbarzähnen kann zum Abrieb von Zahnhartsubstanzen führen (Yip et al., 2002). Zu diesen Zahnkontakten kommt es während der Kau- und Sprechvorgänge, aber auch während des Schluckaktes. Klinisch sind glatte, plane Schlifffacetten, die sowohl im Schmelz als auch im Dentin liegen können, für diese Art der Zahnhartsubstanzdefekte charakteristisch (Imfeld, 1996). Als pathologische Folgeerscheinung treten Attritionen typischerweise als ein Symptom von Parafunktionen wie Bruxismus auf (Attin, 1999). Abfraktion/Abflexion Im Rahmen von Funktion und Parafunktionen des stomatognathen Systems treten exzentrische Kräfte auf. Sie erzeugen durch Schubspannungen und Fehlbelastungen Mikrofrakturen im Bereich der Schmelz-Dentin-Grenze. So entstehen kleinste Frakturteile, die aus dem strukturellen Verbund des Zahnhartgewebes herausgelöst werden können (Imfeld, 1996). Im Laufe der Zeit entsteht das klinische Bild des keilförmigen Defektes. Sie liegen in der Regel am vestibulären Zahnhals und weisen eine scharfkantige Begrenzung auf (Attin, 1999). 2.3 Erosionen 2.3.1 Definition Oberflächliche Zahnhartsubstanzverluste, die durch Säuren und ohne Beteiligung von Mikroorganismen entstehen werden als dentale Erosionen bezeichnet (Zipkin und McClure, 1949). Sie treten lokalisiert auf und sind irreversibel (Ten Cate und Imfeld, 1996; Schroeder et al, 1995). Schreitet der Prozess voran, kann es auf Grund 9 Literaturübersicht physikalischer und chemischer Reize zu schmerzhaften Empfindungen kommen, sobald Dentin frei liegt. Im Allgemein jedoch gelten Erosionen als schmerzlos. Klinisch ist eine Erweichung des Schmelzes durch erosive Vorgänge nur schwer feststellbar (Schweizer-Hirt et al., 1978). Experimentell lässt sich ein Verlust der Mikrohärte nachweisen (Ganss und Schlüter, 2010). 2.3.2 Klinisches Bild Erosionen führen zu einer farblichen und morphologischen Veränderung der betroffenen Zähne. Durch Verlust der Perikymatien erscheint der Zahnschmelz matt und farblos (Lussi und Jaeggi, 2008). Mit Fortschreiten des Prozesses werden die Zähne gelber, da unter der dünner werdenden Schmelzschicht das gelbliche Dentin immer deutlicher hervortritt (Schweizer-Hirt et al., 1978). Morphologisch sind dellenförmige Defekte zu beobachten. Auf den okklusalen Flächen erscheinen die Höckerspitzen eingedrückt. Die Veränderungen sind progredient und prägen sich im Laufe der Zeit immer stärker aus. Je weiter der Zahn erodiert, desto flacher wird das okklusale Relief. In schweren Fällen kann es sogar ganz verschwinden. Sind die betroffenen Zähne konservierend mit einer Füllung versorgt, ragt diese typischerweise über die Zahnfläche hinaus (Lussi und Jaeggi, 2008). Zervikal bleibt, bei rein erosiv verursachten Defekten, auch im fortgeschrittenen Stadium eine Schmelzleiste erhalten. Dies ist auf zwei Einflüsse zurückzuführen: Zum einen stellt sich zervikal ablagernde Plaque eine Diffusionsbarriere für die Säure dar (SchweizerHirt et al., 1978), zum anderen wird dieser Bereich durch das Sulcus-Fluid mit seinem pH-Wert von 7,5 bis 8,0 geschützt (Stephen et al., 1980). Das klinische Erscheinungsbild lässt eine Einschätzung bezüglich des Schweregrades nur bedingt zu, da der Schmelz an den unterschiedlichen Zahnflächen verschieden dick ist. Ein gleich großer Verlust von Schmelz kann so an der einen Stelle bereits zu einer Dentinexposition führen und dadurch ausgeprägter erscheinen, als an einer anderen Stelle (Lussi und Jaeggi, 2009). 2.3.3 Klassifizierung Die Bestimmung des Schweregrades einer Erosion dient der Wahl der richtigen Therapie. Im Laufe der Zeit wurden verschieden Klassifikationen dentaler Erosionen vorgestellt (Lussi et al., 1991; Eccles, 1979; Fares et al., 2009). Eine einfache und leicht durchzuführende Methode stellt die Basic Erosive Wear Examination (BEWE) 10 Literaturübersicht dar. Dabei werden, außer den dritten Molaren, alle Zähne oral, okklusal und vestibulär auf erosive Defekte hin untersucht. Es gilt die in Tabelle 1 aufgeführte Einteilung der Schweregerade. Der jeweils höchste Wert pro Sextant wird notiert. Aus der Summe aller Sextanten folgt dann die in Tabelle 2 aufgeführte Therapieempfehlung. Auf die Unterscheidung zwischen „mit Dentinexposition“ und „ohne Dentineposition“ wird verzichtet, da dies kein zuverlässiges Kriterium zur Beurteilung des Schweregrades einer Erosion ist (Barlette et al., 2008). Siehe dazu auch Abschnitt 2.3.2. Tabelle 1: Klassifizierung dentaler Erosionen nach der BEWE Grad Klinisches Bild 0 Kein erosiver Zahnhartsubstanzverlust 1 Beginnender Verlust der Oberflächenstruktur 2 Klar ersichtlicher Verlust von Zahnhartsubstanz; < 50% der Oberfläche 3 Ausgeprägter Verlust von Zahnhartsubstanz, > 50 % der Oberfläche Quelle: Adrian Lussi und Thomas Jaeggi: Dentale Erosionen – von der Diagnose zur Therapie, 2009, Berlin, QuintessenzVerlag, Seite 12 Tabelle 2: Therapieempfehlung in Abhängigkeit der ermittelten Schweregrades (BEWE) Schweregrad der Erosion Summe aller Sextanten Management Nihil ≤2 • • Gering 3–8 • • Mittel • • 9- 13 • • Hoch ≥ 14 • • • Aufklärung und Überwachung Wiederholung der BEWE aller drei Jahre Mundhygieneinstruktion; Ernährungsabklärung und Beratung, bei Reflux: Aufklärung und Überwachung; momentane Situation mit Modellen und Fotos festhalten Wiederholung der BEWE aller zwei Jahre wie oben zusätzlich Empfehlung von Fluoridierungsmaßnahmen; Erhöhung der Widerstandsfähigkeit der Zahnhartsubstanz Restaurative Maßnahmen in Betracht ziehen Wiederholung der BEWE aller sechs bis zwölf Monate wie oben zusätzlich spezielle Betreuung bei schnellem Fortschreiten der Erosion; restaurative Maßnahmen Wiederholung der BEWE aller sechs bis zwölf Monate Quelle: Adrian Lussi und Thomas Jaeggi: Dentale Erosionen – von der Diagnose zur Therapie, 2009, Berlin, QuintessenzVerlag, Seite 12 11 Literaturübersicht 2.3.4 Prävalenz Dentale Erosionen sind kein Phänomen der Neuzeit, wie Untersuchungen an prähistorischen Skeletten zeigen (Turner und Machado, 1983). Wissenschaftliche Untersuchungen zu ihrem Auftreten innerhalb verschiedener Bevölkerungsschichten und -gruppen finden allerdings erst seit etwa 50 Jahren statt. So waren Sognnaes et al. im Jahre 1972 mit die Ersten, die sich diesem Thema widmeten. Sie untersuchten extrahierte Zähne und kamen für dentale Erosionen auf eine Prävalenz von 18% (Sognnaes et al., 1972). Mittlerweile gibt es zahlreiche Arbeiten, deren Ergebnisse zum Teil stark variieren. Verschiedene Studiendesigne erschweren einen Vergleich der erhobenen Daten (Nunn, 1996; Lussi et al., 2006). Feststeht jedoch, dass Erosionen oft und in allen Altersstufen vorkommen (Amaechi und Higham, 2005). Ein Untersuchung von knapp 2000 chinesischen Kindergartenkindern im Alter von drei bis fünf Jahren ergab bei 5,7% erosive Defekte. In 0,9% der Fälle mit Dentinbeteiligung. Dabei wurden lediglich die oberen Inzisivi begutachtet (Luo et al., 2005 ). In Saudi-Arabien untersuchten Al-Malik und seine Mitarbeiter ebenfalls die oberen Inzisivi von Kindergartenkindern. Sie konnten an 31% der untersuchten Zähne Erosionen feststellen (Al-Malik et al., 2002). Millward et al. schauten sich alle Milchzähne an und kamen zu dem Schluß, dass fast die Hälfte aller untersuchten Zähne durch Erosionen geschädigt waren (Millward et al., 1994). Jaeggi und Lussi fanden im Wechselgebiss schweizer Kinder im Alter von fünf bis neun Jahren sogar 100% betroffene Milchzähne (Jaeggi und Lussi, 2004). Eine in Deutschland durchgeführte Auswertung im Rahmen kieferorthopädischer Behandlungen angefertigter Situationsmodelle der Jahre 1977 bis 1999 ergab, dass 70,6% der Milchzähne von Erosionen betroffen waren. 11,6% der Modelle zeigten an mindestens einem bleibenden Zahn Erosionen. Dabei weisen Kinder mit erosiv geschädigten Milchzähnen ein höheres Risiko auf auch an bleibenden Zähnen entsprechende Defekte zu entwickeln (Ganss et. al, 2001). 1994 wurden in England 1035 Schülerinnen und Schüler auf Erosionen hin untersucht. Dabei fanden sich bei 30 % der Probanden Erosionen, die bis ins Dentin reichten. Bei männlichen Probanden war dies deutlich häufiger der Fall als bei weiblichen (Milosevic et al., 1994). Eine akutellere Studie aus Dänemark wies bei 14% der Untersuchten im Alter von 15 bis 17 Jahren nach, dass mindestens drei Zahnflächen befallen waren. Am 12 Literaturübersicht häufigsten fanden sich Erosionen an den palatinalen Flächen der Oberkieferzähne (Larsen et al., 2005). Tabelle 3 fasst diese und weitere Studien zur Prävalenz dentaler Erosionen bei Kindern und Jugendlichen zusammen. Tabelle 3: Prävalenz dentaler Erosionen bei Kindern und Jugendlichen Autor(en) und Jahr Altersgruppe Ergebnisse Millward et al., 1994 4 Jahre • fast 50% der Milchzähne betroffen Milosevic et al., 1994 14 Jahre • 30% Erosionen bis ins Dentin • häufiger männliche als weibliche Probanden betroffen • Beobachtungszeitraum 1977 bis 1999 • 73,6% der untersuchten Modelle wiesen erosive Defekte auf • in den 1990 Jahren zeigte sich eine Verdoppelung der Prävalenz im Vergleich zum Jahrzehnt davor • Milchzähne waren deutlich stärker betroffen als bleibenden Zähne • 31% der oberen Milchinzisivi weisen Erosionen auf • davon 40% mit Dentinbeteiligung bis hin zur Pulpaexposition • in 47% der Fälle konnten Erosionen gefunden werden • in 21% der Fälle mit Dentin- und/oder Pulpabeteiligung • 100% der Milchzähne betroffen • 14% der bleibenden Zähne betroffen 3 bis 5 Jahre • 5,7% der oberen Milchinzisivi betroffen, 0.9% mit Dentinbeteiligung 15 bis 17 Jahre • bei 14% mindestens drei Zahnflächen betroffen, vor allem palatinal Wiegand et al., 2006 2 bis 7 Jahre • 32% der Kinder weisen mindestens einen erosiv geschädigten Zahn auf Kazoullis et al., 2007 5 bis 15 Jahre • 25% der bleibenden Zähne betroffen • 68% der Untersuchten weisen mindestens eine Erosion auf • es waren in 45% der Fälle leichte und in 22% der Fälle mittelschwere Erosionen zu finden Ganss et al., 2001 Al-Malik et al., 2002 Harding et al., 2003 Jaeggi und Lussi, 2004 Lou et al., 2005 Larsen et al., 2005 El Karim et al., 2007 11,4 Jahre 2 bis 5 Jahre 5 Jahre 5 bis 9 Jahre 12 bis 14 Jahre Quellen: Siehe Literaturverzeichnis 13 Literaturübersicht Im Vergleich zu Milchzähnen finden sich an bleibenden Zähnen deutlich weniger erosive Defekte. Erklärt wird dies damit, dass Milchzähne eine dünnere Schmelzschicht aufweisen und somit chemischen und mechanischen Einflüssen gegenüber weniger resistent sind (De Menezes Oliveira et al., 2010). Dennoch wird eine Zunahme erosiv geschädigter Zähne im Laufe des Lebens beobachtet. Eine Untersuchung der Altersgruppe 26 bis 30 Jahre im Vergleich zur Altersgruppe 46 bis 50 Jahre wies neben einem zunehmenden Erosionsbefall aller Zahnflächen auch eine Zunahme des Schweregrades nach. Zeigten sich bei den Jüngeren Schmelzerosionen in 11,9% (facial), 35,6% (okklusal) und 3,6% (palatinal), so waren es bei den Älteren bereits 9,6% (facial), 40,1% (okklusal) und 6,1% (palatinal). Erosionen die bis ins Dentin reichten fanden sich bei Ersteren zu 7,7% (facial), 29,9% (okklusal) und 0% (palatinal) und bei Letzteren 13,2% (facial), 42,6% (okklusal) und 2,0% (palatinal) (Lussi et al., 1991). Auch in einer neueren Studien findet sich dieser Verlauf: Schiffner und Mitarbeiter fanden in der Altersgruppe 35 bis 44 Jahre an 8,7% der untersuchten Zähne Erosionen. In der Altersgruppe 65 bis 74 Jahre zeigten fast doppelt so viele Zähne (16,4%) entsprechende Schäden (Schiffner et al., 2002). Tabelle 4 fast diese und weitere Studien zur Prävalenz dentaler Erosionen bei Erwachsenen zusammen. Tabelle 4: Prävalenz dentaler Erosionen bei Erwachsenen und Senioren Autor(en) und Jahr Altersgruppe Ergebnisse Sognnaes et al., 1972 -------------------- • 18% der extrahierten Zähne wiesen erosive Defekte auf • häufiger Zähne des Unterkiefers als des Oberkiefers betroffen Xhonga und Valdmanis, 1983 14 bis 88 Jahre • 25% der Probanden betroffen Lussi et al., 1991 26 bis 30 Jahre • betroffen sind vor allem die Okklusalflächen (35,6% bzw. 40,1%) • Zunahme der Erosion (mit und ohne Dentinbeteiligung) mit steigendem Alter und 46 bis 50 Jahre Johansson et al., 1996 19 bis 25 Jahre • 28% der OK-Frontzähne waren erosiv geschädigt Jaeggi et al., 1999 19 bis 25 Jahre • an den bukkal Flächen fanden sich in 15% der Fälle Erosionen • in 20% der Fälle konnten keilförmige Defekte nachgewiesen werden 14 Literaturübersicht Schiffner et al., 2002 Schiffner et al., 2002 35 bis 44 Jahre 65 bis 74 Jahre • 6,4% Personen zeigten Schmelzerosionen und 4,3% Erosionen mit Dentinbeteiligung • insgesamt waren 8,7% aller Zähne betroffen • etwa ein Drittel der Untersuchten zeigte keilförmige Defekte • 4,1% Personen zeigten Schmelzerosionen und 3,8% Erosionen mit Dentinbeteiligung • insgesamt waren 16,4% aller Zähne betroffen • etwa ein Drittel der Untersuchten zeigte keilförmige Defekte Quellen: Siehe Literaturverzeichnis 2.3.5 Ätiologie Die Entstehung dentaler Erosionen beruht auf einem Wechselspiel zahlreicher schützender und schädigender Faktoren, welche intrinsischer oder extrinsischer Genese sein können. Letztlich führen chemische Prozesse an der Zahnoberfläche zu einer Herauslösung von Mineralien, in deren Folge es schließlich zum irreversiblen Verlust von Schmelz und Dentin kommen kann (Zero und Lussi, 2005). 2.3.5.1 Extrinsische Faktoren 2.3.5.1.1 Ernährung Bereits im ausgehenden 19. und beginnenden 20. Jahrhundert wurde beobachtet, dass verschiedene Lebensmittel erosive Schäden an Zähnen verursachen können (Darby, 1892; Miller, 1907). Im Gegensatz zu damals wurde in den letzten Jahren ein deutlich zunehmender Konsum saurer Lebensmittel und/ oder säurehaltiger Getränke verzeichnet (Packer, 2009; West et al., 2000). Die Bandbreite erosiv wirkender Nahrungsmittel und Getränke erstreckt sich von Zitrusfrüchten über Salatsaucen und Ketchup bis hin zu sauren Fruchtbonbons, von Wein über Fruchtsäfte und Sportgetränke bis hin zu Essigprodukten (Grobler et al., 1989; Lussi und Jaeggi, 2009; Gandara und Truelove, 1999; Davies et al., 2008, ). Selbst der Genuss verschiedener Kräutertees birgt ein Erosionsrisiko, das laut einer britischen Studie sogar höher liegt als das von Orangensaft (Phelan und Rees, 2003). 15 Literaturübersicht Dabei sind vor allem Zitronen-, Apfel-, Milch- und Phosphorsäure zu nennen (Hughes et al., 2000). Aber auch Weinsäure (Grenby, 1996), Ascorbin- und Maleinsäure (Young und Tenuta, 2011) können eine erosive Wirkung entfalten. Andererseits gibt es Lebendmittel, die Erosionen vorbeugen können. Dazu zählt zum Beispiel Käse auf Grund seines hohen Gehalts an Kalzium und Phosphat (Gedalia et al., 1991). Milch und Eier enthalten Proteine, die eine anti-erosive Wirkung entfalten (Hemingway et al., 2010). Eine brasilianische Studie zeigt, dass grüner Tee in der Lage ist vor Erosionen genauso effektiv zu schützen wie eine handelsübliche 250ppm fluoridhaltige Spüllösung (Magalhães et al., 2009). Auch gegen Abrasionen welche mit Erosionen einhergehen soll grüner Tee helfen (Kato et al., 2009). Das Spülen mit Milch oder Wasser kann ferner zu einem schnelleren Erhärten der erosiv erweichten Zahnhartsubstanz führen und so den Zahnhartsubstanzverlust einschränken (Wiegand et al., 2008). Zur Abklärung, ob den diagnostizierten Erosionen ein übermäßiger Säurekonsum zu Grunde liegt, empfiehlt es sich, eine Ernährungsanamnese zu erheben. Bestandteil dieser Anamnese sollte ein Ernährungsprotokoll sein, welches über einen Zeitraum von mindestens vier Tagen geführt wird und sowohl Arbeits- als auch freie Tage einschließt, da die Ernährungsweise an Arbeitstagen oft von der an freien Tagen abweicht (Lussi und Jaeggi, 2009). Ob ein Lebensmittel oder Getränk Erosionen verursacht, hängt von verschiedenen chemischen, biologischen und nicht zuletzt von verhaltensbezogenen Aspekten ab. 2.3.5.1.1.1 Chemische Einflüsse Unter normalen Bedingungen gilt Speichel als eine an Mineralien gesättigte Lösung (Attin, 1999). Sobald er es nicht mehr ist, beginnen Zahnhartsubstanzen zu demineralisieren. Durch das Herauslösen der Mineralien aus dem Zahn steigt die Sättigung des Speichels wieder an und die erosiven Prozesse kommen zum Stillstand. Da hier zahlreiche Einflüsse eine Rolle spielen, lässt sich kein kritischer pH-Wert für Erosionen festlegen (Lussi et al., 2011). Neben dem pH-Wert an sich ist die Sättigung des einwirkenden Agens mit Mineralien der Zahnhartsubstanz entscheidend. Getränke, die auf Grund eines geringen pHWerts eine erosive Wirkung entfalten können, waren wesentlich weniger erosiv, wenn sie mit Kalzium, Phosphat und/oder Fluorid angereichert wurden (Attin et al., 2005). Auch saure Bonbons, wie sie Patienten nach Bestrahlung im Kopf-Hals-Bereich zur 16 Literaturübersicht Stimulation des Speichelflusses empfohlen werden, führen zu weniger erosiven Folgeschäden, wenn sie zusätzlich mit Kalzium angereichert werden (Jensdottir et al., 2010). Der hohe Kalziumgehalt erklärt auch, warum Jogurt trotz eines pH-Wertes von etwa 4 kein erosives Lebensmittel ist (Ganss und Schlüter, 2010). Verschiedene Säuretypen sind unterschiedlich stark in der Lage dentale Erosionen zu verursachen. Carbonsäure erhöht zwar das erosive Potential eines Getränks, jedoch nur in unerheblichem Maß, weshalb reines Mineralwasser keine entsprechenden Schäden verursacht (Parry et al., 2001). Softdrinks und Fruchtsäfte können ebenfalls Carbonsäure enthalten. Für die Erosionen sind hier aber vor allem Säuren wie Phosphor-, Ascorbin-, Zitronen- und Maleinsäure verantwortlich (Young und Tenuta, 2011) sowie, neben dem pH-Wert der Säure, weitere chemische Eigenschaften. Einige Säuren besitzen die Fähigkeit der Chelatbildung. Zitronensäure zum Beispiel kann dadurch bis zu 32% des im Speichel gelösten Kalziums abfangen. Die reduzierte Sättigung des Speichels in Bezug auf die Zahnhartsubstanz kann erosive Prozesse unterstützen (Meurman und ten Cate, 1996). Durch Chelatbildung kann das Kalzium aber auch direkt aus der Zahnoberfläche herausgelöst werden. Ethylendiamintetraacetat (EDTA) ist auf Grund dieser Eigenschaft selbst bei neutralem pH-Wert in der Lage mineralhaltige Oberflächen zu erodieren (Featherstone und Lussi, 2006). Ebenso entscheidet die Pufferkapazität eines Getränks oder Lebensmittels darüber, wie schnell die Säure durch den Speichel neutralisiert werden kann. Je höher die Pufferkapazität der einwirkenden Säure, desto länger dauert die Demineralisationsphase (Lussi et al., 2011). Die Zugabe von Kalzium kann die Pufferkapazität verringern, und damit eine schnellere Neutralisation bewirken. Das erosive Potential des Getränks oder Lebensmittels wird herabgesetzt (Lussi und Jaeggie, 2006). Einfluss auf die Erosionsentwicklung hat auch die Temperatur des konsumierten Getränks. Mit zunehmender Termperatur erosiver Flüssigkeiten konnte ein Anstieg der Läsionstiefe und des Mineralverlust festgestellt werden (Amaechi et al., 1999; West et al., 2000). 17 Literaturübersicht 2.3.5.1.1.2 Biologische Einflüsse Speichel gilt als der wichtigste biologische Faktor bei der Entstehung dentaler Erosionen. In Ruhe beträgt die Speichelmenge im Mund etwa 1 ml (Young und Tenuta, 2011). In Form eines dünnen Schutzfilms bedeckt er den Zahn. Während der Nahrungsaufnahme wird der Speichelfluss durch Geruch, Geschmack und Anblick der Nahrung sowie durch Kaubewegungen gefördert. Dabei stimuliert vor allem saure Nahrung den Speichelfluss (Yeh et al., 2000; Engelen et al., 2003; Christensen und Navazesh, 1984). Kommt es zu einem Säureangriff, wird die Zahnoberfläche einem Säure-Speichel-Gemisch ausgesetzt. Indem er verdünnt, puffert und Säuren neutralisiert, die Mundhöhle reinigt und als Kalzium- und Phosphatreservoir für Remineralisationsprozesse dient, entfaltet Speichel seine Schutzfunktion. Außerdem ist er an der Entstehung der schützenden Pellikel beteiligt. Allein jedoch ist er nicht in der Lage erosive Prozesse vollständig zu vermeiden (Hara et al., 2006; Young und Tenuta, 2011). Bei intrinsisch einwirkender Säure fehlt die vorausgehende Stimulation der Speicheldrüsen in manchen Fällen. Während es beim Erbrechen zu einer Stimulation der Speicheldrüsen kommt (Edgar, 1992), fehlt diese bei Refluxerscheinungen. Erklärt wird dies damit, dass es sich bei letzterem um einen unbeabsichtigten, vom autonomen Nervensystem nicht koordinierten Vorgang handelt (Hara et al., 2006). Verminderter Speichelfluss kann als Nebenwirkung zahlreicher Medikamente auftreten (Wynn und Meiller, 2001) – vgl. Abschnitt 2.4.5 – oder als Folge einer Strahlentherapie im Kopf- und Halsbereich (Dreizen et al, 1977). Die Pellikel besteht aus Speichelproteinen, die sich auf Grund elektrostatischer Wechselwirkungen an die Zahnoberfläche anlagern (Skjørland et al., 1995) und kann den Zahn so vor einem direkten Kontakt mit der Säure schützen (Hannig, 1999). Als semipermeable Membran reduziert sie die Herauslösung der Mineralien aus der Zahnoberfläche (Lendenmann et al., 2002). Sie ist jedoch nur bedingt in der Lage den Zahn vor Erosionen zu schützen (Hara et al., 2006). Die unterschiedliche Dicke der Pellikel an verschiedenen Stellen im Zahnbogen ist möglicherweise mit verantwortlich für das ungleichmäßig schnelle Voranschreiten erosiver Defekte in Abhängigkeit ihrer Lokalisation (Amaechi et al., 1999). Die Position des Zahnes innerhalb des Zahnbogens kann die Entstehung von Erosionen auf zwei weitere Arten beeinflussen: Zum einen werden Zähne an verschiedenen Positionen unterschiedlich 18 gut von Speichel erreicht, seine Literaturübersicht Schutzfunktionen kommen somit unterschiedlich stark zum Tragen (Hara et al., 2006). Zum anderen können umgebende Weichgewebe wie Wange und Zunge durch den Kontakt mit erosiv angegriffenen Zahnflächen zusätzlich abrasive Prozesse verursachen (Gregg et al., 2004) – vgl. Abschnitt 2.2. 2.3.5.1.1.3 Verhaltensbezogene Einflüsse Im Rahmen der Entstehung dentaler Erosionen spielt die Kontaktzeit zwischen Zahn und Säure eine wichtige Rolle. Sie wird durch die Art und Weise so wie den Zeitpunkt des Säurekonsums beeinflusst. Es liegt nah, dass ein übermäßiger Genuss von Getränken und Lebensmitteln, welche ein erosives Potential aufweisen, letztlich Erosionen verursacht (Zero und Lussi, 2006). Aber auch auf den ersten Blick weniger offensichtliche Angewohnheiten wie verschiedene Schluck- und Trinkmuster tragen ihren Teil dazu bei. Je nachdem ob ein Getränk nippend, schlürfend oder durch einen Strohhalm in den Mund gelangt, werden unterschiedliche Zähne bzw. Zahnflächen betroffen sein (Edwards et al., 1998; Millward et al., 1997). Wird es zudem nicht sofort herunter geschluckt sondern noch für eine Weile im Mund behalten, kann dies zu einem stärkeren Abfall des pH-Werts führen und das Erosionsrisiko erhöhen (Johansson et al., 2004). Wenn der Säurekonsum abends stattfindet, besteht durch den zu dieser Zeit verminderten Speichelfluss ein doppeltes Risiko Erosionen auszubilden (Zero und Lussi, 2006). Eine gesunde Lebensweise bedeutet oft einen erhöhten Genuss von Obst und Gemüse und somit ein größeres Risiko Erosionen auszubilden. Ins Besondere, wenn es sich um Zitrusfrüchte handelt (Künzel et al., 2000). Dieser Risikogruppe gehören unter anderem Rohkostvegetarier an (Ganss et al., 1999). Genauso wie Menschen, die abnehmen möchten, da Obst und Gemüse Bestandteil zahlreicher Diätpläne sind (Zero und Lussi, 2006). Personen mit einem entsprechenden Gesundheitsbewusstsein weisen zudem häufiger eine überdurchschnittlich gute Mundhygiene auf, welche die Abrasion erosiv erweichter Zahnhartsubstanz vorantreibt (vgl. Absatz 2.2) (Zero, 1996). Gleiches trifft für Patienten mit psychisch bedingten Essstörungen zu (Imfeld und Imfeld, 2005b). 19 Literaturübersicht 2.3.5.1.2 Sport und Beruf Sport Im Rahmen sportlicher Betätigung kommt es zu einem erhöhten Flüssigkeits- und Elektrolytverlust, welcher oft durch spezielle säurehaltige Sport- und/oder kohlensäurehaltige Erfrischungsgetränken ausgeglichen wird. Die nach dem Sport herabgesetzte Speichelfließrate steigert das Risiko einer erosiven Schädigung zusätzlich (Zero und Lussi, 2006). Als Folge sportlicher Betätigung kann außerdem ösophagealer Reflux auftreten (Centerwall et al., 1986). Schwimmer, die sich regelmäßig in Schwimmbecken mit geringem pH-Wert aufhalten (verursacht durch die Chloridzufuhr) weisen ein erhöhtes Erosionsrisiko auf (Centerwall et al, 1986). Die Erosionen finden sich in diesen Fällen generalisiert und können durch eine regelmäßige Kontrolle des Schwimmbadwasser-pH-Werts vermieden werden (Geurtsen, 2000). Eine holländische Arbeitsgruppe berichtete 2005, dass ein pH-Wert über 6,5 jedoch zu einer vermehrten Zahnsteinbildung führt (Scheper et al. 2005). Beruf Es gibt einige wenige Berufe, die mit einem erhöhten Erosionsbefall assoziiert sind. In der Industrie finden sich Bereiche, in denen Arbeiter in besonderem Maße verschiedenen Säuren ausgesetzt sind. Dazu zählen Säure- und Batteriearbeiter, die unter anderem in der Chemieindustrie, Papier- und Zellstoffherstellung und der Erdölgewinnung tätig sind (Ten Bruggen Cate, 1968; Petersen und Gormsen, 1991) Winzer und Weinrichter, die berufsbedingt ihre Zähne regelmäßig Säure in Form von Wein aussetzen, zeigen einen erosiven Zahnhartsubstanzverlust, der sich vor allem an den Ober- und Unterkiefer Frontzähne und Prämolaren zeigt. Mog berichtete, dass Weinrichter täglich bis zu 200 verschiedene Sorten verkosten, wobei der durchschnittliche pH-Wert eines Weines bei 3,0 bis 3,5 liegt (Mok et al., 2001). Die Dauer, die der Wein im Mund verbleibt variiert dabei zwischen ein paar Sekunden und mehreren Minuten. Bereits 5 ml Wein, die zwischen 15 und 45 Sekunden im Mund belassen werden, bewirken einen länger anhaltenden Abfall des intraoralen pH-Werts. Wiederholtes Spülen mit Wein führt zu einer anhaltenden Abschwächung des durch den Speichel gegeben Schutzes, trotz erhöhtem Speichelfluss (Brand et al., 2009). 20 Literaturübersicht 2.3.5.1.3 Mundhygieneprodukte und Medikamente Mundhygieneprodukte Die tägliche Mundhygiene kann eine einfache Maßnahme sein Erosionen vorzubeugen. Aus der Kariesprophylaxe sind verschiedene Fluoride bekannt, die eine schützende Kalziumfluoridschicht (CaF2) auf der Zahnoberfläche ausbilden (Ganss et al., 2004a). Dazu gehören unter anderem Aminfluorid (AmF) und Natriumfluorid (NaF) (Ganss et al., 2008). Diese CaF2-Schicht ist allerdings nicht sehr säure- und abrasionsstabil (Wegehaupt et al., 2009). Des Weiteren scheinen AmF und NaF mit Zunahme der Säurezufuhr immer weniger im Stande wirksam vor Erosionen zu schützen. Ein wirksamer Schutz kann nur durch eine häufige Applikation hochkonzentrierter Fluoridpräparate erreicht werden (Schlueter et al., 2009). Dabei gilt es eine Fluoridintoxikation zu vermeiden. Die wahrscheinlich-toxische Dosis liegt bei 5mg Fpro kg Körpergewicht, die sicher tödliche Dosis zwischen 32 und 64 mg F- pro kg Körpergewicht (Whitford, 1992). In Bezug auf die Erosionsprophylaxe scheinen vor allem Fluoridverbindungen mit polyvalenten Metallionen wie Zinnfluorid (SnF2) und Titantetrafluorid (TiF4) sehr effektiv zu sein (Tezel et al., 2002; Schlueter et al., 2007; Hove et al, 2008). In einigen Studien konnte gezeigt werden, dass zinnfluoridhaltige Verbindungen in der Erosionsprophylaxe Natrium- und Aminfluorid deutlich überlegen sind (Ganss et al., 2008; Hove et al., 2007; Hove et al., 2008; Schlueter et al., 2009,Wiegand et al, 2009). Dies wird durch die Entstehung einer säure- und abrasionsstabilen zinnhaltigen Deckschicht erklärt, die zudem die An- und Einlagerung von CaF2 fördern soll (Young et al., 2006). Ein ähnlicher Mechanismus wird für TiF4 beschrieben: Durch die Einlagerung von Titanionen, die an Stelle von Kalzium eine feste Bindung mit den Phosphatgruppen in den Apatitkristallen eingehen, kann durch TiF4 eine sehr säurestabile Titaniumdioxidschicht auf der Zahnoberfläche ausgebildet werden, die ebenfalls die An- und Einlagerung von CaF2 begünstigen soll (Ribeiro et al., 2006; Meyer-Lueckel et al. 2006). Im Gegensatz zu TiF4 hat SnF2 zwei Vorteile: Als Bestandteil von Mundhygieneprodukten kann es leicht therapeutisch angewandt werden. Bislang ist es noch nicht gelungen TiF4 als Wirkstoff in Zahnpasten oder Mundspüllösungen einzusetzen. Zu dem weist TiF4 einen sehr niedrigen pH-Wert (1 bis 2) auf. Dies kann bei häuslicher Anwendung eine Gefahr für die Gingiva darstellen und zu 21 Literaturübersicht Verätzungen führen. Bei höherem pH-Wert jedoch verliert TiF4 seine Wirksamkeit (Wiegand et al., 2009a; Wiegand et al., 2009b) Es gibt allerdings auch Mundhygieneprodukte, die zur Erosionsausbildung führen können, wenn sie über einen längeren Zeitraum angewendet werden (Pontefract et al., 2001). Beispielsweise solche, die EDTA enthalten. Für die erosive Wirkung wird hier die Fähigkeit der Chelatbildung verantwortlich gemacht (Hellwig und Lussi, 2006; Rytömaa et al., 1989). Eine Studie von Lussi und Jaeggi, in der verschiedene Mundhygieneprodukte auf ihr erosives Potential hin untersucht wurden kam jedoch zu dem Ergebnis, dass lediglich eine einzige fluoridfreie Zahnpasta zu einer verminderten Härte der Schmelzproben führte (Lussi und Jaeggi, 2001). Medikamente Es gibt Medikamente, die bei regelmäßiger Einnahme erosive Defekte bewirken oder zumindest ihre Entstehung unterstützen können. Aspirin (Acetylsalicylsäure) und Vitamin C (Ascorbinsäure) können auf Grund ihrer sauren Eigenschaften die Zähne direkt angreifen. Wenn Aspirin in Form von Kautabletten eingenommen wird, kann es zu einer Haftung in den Fissuren kommen. Die dadurch erhöhte Einwirkzeit steigert das Risiko der Erosionsausbildung zusätzlich (Rogalla er al., 1992). Gleiches gilt für kaubare Vitamin-C-Tabletten (Giunta, 1983). Andere Medikamente lösen laut Packungsbeilage als Nebenwirkungen Erbrechen aus und/ oder setzen die Speichelfließrate herab. Zu diesen Medikamenten gehören unter anderem Beruhigungsmittel, Antihistaminika, Antiemetika sowie Medikamente gegen Parkinson (Atkinson und Wu, 1994; Hellwig und Lussi, 2006). 2.3.5.2 Intrinsische Faktoren Magensaft Magensaft besteht zu einem großen Teil aus Salzsäure und weist einen pH-Wert von etwa 0,9 – 1,5 auf (Young und Tenuta, 2011). Verglichen mit kohlensäurehaltigen Softdrinks wirkt Magensäure deutlich erosiver (Bartlett und Coward 2001). Durch Erbrechen oder Regurgitation kann der saure Mageninhalt in die Mundhöhle gelangen. Typischerweise zeigen sich die erosiven Defekte an den Palatinal- und Inzisialflächen der Oberkieferfrontzähne. Im fortgeschrittenen Stadium können auch an den Prämolaren sowie okklusal 22 der Unterkieferseitenzähne erosive Literaturübersicht Veränderungen festgestellt werden (Bartlett, 2006). Zu erklären ist dies damit, dass die Zunge den Mageninhalt über den Gaumen ins Vestibulum leitet (Lazarchik und Filler, 2000). Somit lässt die Lokalisation erosiver Defekte in gewissem Umfang einen Rückschluss auf die Genese zu (Järvinen et al., 1992). Es ist bekannt, dass organische Bestandteile wie Kollagen die Progression der Erosion hemmen. Der höhere Anteil organischer Bestandteile im Dentin gegenüber Schmelz wird als Begründung dafür gesehen, dass Erosionen im Dentin langsamer voranschreiten (Hara et al., 2005). Magensaft enthält neben Salzsäure auch proteolytische Enzyme, beispielsweise Pepsin bzw. Pepsinogen. Es wird vermutet, dass die damit verbundene Kollagenauflösung die Progression der Erosionen beschleunigt, zumal sich Fluoridierungsmaßnahmen nach Entfernung der kollagenhaltigen Deckschicht als unwirksam herausstellten (Ganss et al., 2004b; White et al., 2001). Krankheitsbilder Die assoziierten Erkrankungen werden in Abschnitt 2.4 erläutert. 2.3.6 Prävention Van Nieuw Amerongen und Veerman stellten 1995 folgende Punkte zur Prävention dentaler Erosionen zusammen: ─ Reduzierung der Säureangriffe pro Tag ─ Verkürzung der Kontaktzeit zwischen Säure und Zahn während des Säurekonsums ─ Erosiv wirkende Getränke neutralisieren, indem man direkt danach nichterosiv bzw. remineralisierend wirkende Getränke trinkt (z.B. Milch oder Wasser) ─ Regelmäßige Fluoridapplikation ─ Tabletten lutschen, die den pH-Wert wieder ansteigen lassen 2.3.7 Therapie Eine umfassende Therapie wird je nach Genese die folgenden Aspekte unterschiedlich stark berücksichtigen. Ziel ist es in jedem Fall die Ursachen nach Möglichkeit auszuschalten und ein Voranschreiten dentaler Erosionen zu vermeiden. 23 Literaturübersicht 2.3.7.1 Kausal Sind die Erosionen Folge einer sauren Ernährung, kann mit Hilfe eines Ernährungsprotokolls eine Nahrungsumstellung mit dem Patienten erarbeitet werden. Es können Fruchtsäfte, die mit Kalzium angereichert sind, empfohlen (Attin et al., 2005) und Menge sowie Häufigkeit der eingenommenen Säuren reduziert werden. Zudem kann auf weniger saure Früchte ausgewichen werden, zum Beispiel Bananen statt Orangen. Einige Lebensmittel zeigen eine anti-erosive Wirkung. Kombiniert mit erosiven Lebensmitteln können sie das Erosionsrisiko reduzieren (vgl. Abschnitt 2.3.5.1.1). Eine ursächliche Medikation kann in Rücksprache mit dem verordnenden Arzt abgesetzt oder umgestellt werden. Lässt sich die Ursache der Erosion auf eine Erkrankung zurückführen (vgl. Abschnitt 2.4), muss diese selbstverständlich behandelt werden. Dazu bedarf es oft einer interdisziplinären Zusammenarbeit mit den entsprechenden Fachkollegen. Um eine Verschlimmerung des oralen Zustands zu vermeiden, können parallel symptomatische bzw. präventive Therapieansätze zum Einsatz kommen. 2.3.7.2 Symptomatisch Symptomatische Behandlungsansätze versuchen in erster Linie eine weitere erosive Schädigung trotz der anhaltenden Säureeinwirkung zu verhindern. Ein effektiver Weg dies zu erreichen ist die Applikation von Dentinadhäsiven (Sundaram et al., 2007; Ganss und Schlüter, 2010). Ihre Haftung auf sklerotischem Dentin ist jedoch deutlich geringer ist als auf gesundem. Es wird vermutet, dass die Tubuli, die auf Grund chemischer und physikalischer Reize, durch sklerotisierende Vorgänge oberflächlich verschlossen werden. Dies verschlechtert die Ausbildung der Tags sowie der Hybridschicht und somit die Haftung der Adhäsive am Dentin (Tay und Pashley, 2004). Eine Vorbehandlung der Zahnfläche mit Stahlfräsen soll, im Vergleich zu diamantierten Schleifkörpern, zu einem besseren Halt führen (Ogata et al., 2001). Oral einzunehmende Antacida werden bei Refluxbeschwerden verschrieben. Sie sollen überschüssige Säure im Magen binden und somit die Beschwerden lindern. Eine finnische Studie aus dem Jahre 1988 zeigt, dass der intraorale pH-Wert deutlich weniger abfällt, wenn das Medikament eine Weile im Mund belassen wird. Diese Art 24 Literaturübersicht der Anwendung kann demnach empfohlen werden, um erosive Prozesse an den Zähnen zu verlangsamen (Meurman et al., 1988). Auch Mundhygieneprodukt zum Schutz vor Erosionen können hier zum Einsatz kommen (vgl. Abschnitt 2.3.5.1.3). Sind die Erosionen bereits so ausgeprägt, dass es zu ästhetischen und funktionellen Beeinträchtigungen gekommen ist, werden konservierende oder prothetische Maßnahmen notwendig. Als Materialien der Wahl gelten Komposite und Keramik. Sie zeigen bezüglich Abrasionsresistenz, Substanzverlust unter sauren Bedingungen, Härteänderung und der Zunahme der Oberflächenrauigkeit die besten Ergebnisse (Lussi und Jaeggi, 2009). Vor allem wenn die okklusalen Flächen der Seitenzähne stark erodiert sind, muss eine Bisshebung zur Rekonstruktion der vertikalen Höhe erfolgen. 2.4 Assoziierte Erkrankungen Es gibt einige schwerwiegende Erkrankungen, die mit regelmäßigem Erbrechen einher gehen. Auf Grund des hohen erosiven Potentials von Magensäure (vgl. Abschnitt 2.3.5.2) kommt es schnell zur Ausbildung dentaler Erosionen. Betroffene Patienten benötigen eine umfassende und fachübergreifende (zahn)ärztliche Betreuung. 2.4.1 Bulimia Nervosa Bulimia Nervosa ist eine suchtartige Essstörung mit den Leitsymptomen Heißhungerattacke und provoziertes Erbrechen. Selbstinduziertes Erbrechen und der (mitunter auftretende) Missbrauch von Abführmitteln sollen eine Gewichtszunahme verhindern (Fairburn und Cooper, 1984; Leitzmann et al., 2009). Die meisten Betroffenen sind zu Beginn der Erkrankung um die 18 Jahre alt (Schmidt und Treasure, 1997). Mit einer Prävalenz von rund 1 bis 3% für junge Frauen und 0,1% für junge Männer (Hoek und van Hoeken, 2003; Imfeld und Imfeld, 2005a) zählt sie neben der Anorexia Nervosa zu den schwerwiegensten Erkrankungen junger Frauen (Hoek, 2006). Durch das viele Erbrechen kommt es zur Ausprägung dentaler Erosionen. Sie gelten als das auffälligste körperliche Merkmal der Erkrankung (Leitzmann et al., 2009). Bis zu 90% der an dieser Essstörung leidenden Menschen weisen diese Form der Zahnschädigung auf (Lifante-Oliva et al., 2008). Therapeutisch unterziehen sich die 25 Literaturübersicht Patienten einer Verhaltenstherapie (Leitzmann et al., 2009). Zusätzlich können Medikamente zum Einsatz kommen, die zu einem verminderten Ruhespeichelfluss führen, zum Beispiel Antidepressiva (Nakash-Eisikovits et al., 2002). Dies erhöht das Risiko der Erosionsentstehung (vgl. Abschnitt 2.3.5.1 – biologische Einflüsse) zusätzlich. Als weiteres körperliches Merkmal gilt eine Vergrößerung der Hauptspeicheldrüsen (Roberts und Li, 1987). Verglichen mit anorektischen Patienten weisen sie einen deutlich instabileren psychischen Zustand auf, der mit einem Rückzug aus dem sozialen Leben und depressiven Phasen einhergeht. Unter bulämischen Patienten findet sich eine erhöhte Selbstmordrate, die teilweise damit begründet wird, dass jede Essattacke als Versagen betrachtet wird (Robb und Smith, 1996). Die Heißhungerattacken treten in der Regel zwei Mal in der Woche auf und gehen mit einem Kontrollverlust einher. Die Betroffenen sind nicht mehr in der Lage zu kontrollieren was und wie viel sie essen. Während einer Essattacke können bis zu 10.000 kcal aufgenommen werden (Bailer et al., 2000). 2.4.2 Reflux Gastrooesophagealer Reflux (GOR) ist allgemein definiert als Zeitraum, in dem der pH-Wert in der Speiseröhre auf unter vier abfällt (Bartlett, 2006). Dies geschieht, indem saurer Mageninhalt durch den unteren Ösophagussphincter in die Speiseröhre aufsteigt. Bei gesunden Menschen passiert dies selten und die Speiseröhre wird durch verschluckten Speichel sowie ihre Peristraltik wieder gereinigt (Orr et al., 19881). Kommt es zu einem immer wieder auftretenden Reflux, spricht man von „gastrooesophageale reflux disease“ (GERD) (Bartlett et al.,1996). Laut einer englische Studie liegt die Prävalenz für Reflux in der Altesgruppe der 20 bis 69 Jährigen bei 29% (Kennedy und Jones, 2000). Als typische Symptome gelten unter anderem Sodbrennen und saures Aufstoßen (Chandra et al., 2004). Bei Letzterem handelt es sich um einen passiven Vorgang, bei dem der saure Mageninhalt durch den oberen Ösophagussphincter in den Rachen bzw. Mundraum gelangt. Dies wird mit der Entstehung dentaler Erosionen in Verbindung gebracht (Bartlett et al., 1996). Reflux kann aber auch völlig unbemerkt auftreten. In diesen Fällen spricht man von „stillem Reflux“. Patienten mit dentalen 26 Erosionen aber unauffälliger Literaturübersicht Erosionsanamnese sollte eine entsprechende Abklärung nahe gelegt werden (Bartlett et al., 1996a). Übergewicht, Alkohol, Kaffee, Schokolade, Zwiebeln, fetthaltiges und gut gewürztes Essen können Reflux fördern (Vitale et al., 1987; Kitchen und Castell, 1991; Hirsch et al., 2003). Eine zuverlässige Methode GERD zu diagnostizieren ist eine 24-Stunden-pH-WertMessung, bei der eine Messsonde in die Speiseröhre eingebracht wird und die Patienten angehalten sind ihr Essverhalten zu dokumentieren (Schindelbeck, 1987; Lussi und Jaeggi, 2009). Das Cornelia de Langs Syndrom ist ein Beispiel für eine komplexe genetische Erkrankung, die unter anderem mit Reflux einhergeht (Grau Carbó et al., 2007). 2.4.3 Weitere Ursachen intrinsisch bedingter Erosionen Xerostomie und Sjögren-Syndrom Wie oben beschrieben spielt Speichel in der Erosionsprophylaxe eine zentrale Rolle (vgl. Abschnitt 2.3.5.1 – biologische Einflüsse). Xerostomie kann als Nebenwirkung diverser Medikamente (Wynn und Meiller, 2001) oder als Folge einer Tumorbehandlung auftreten (Garg und Malo, 1997). Neben einem erhöhten Erosionsrisiko steigt hier auch das Risiko an Karies zu erkranken, da Speichel einen wichtigen Schutzfaktor in der Kariesprävention darstellt (Llena-Puy, 2006). Das Sjögren-Syndrom ist eine Autoimmunerkrankung des Bindegewebes, die zu einer Zerstörung der Tränen- und Speicheldrüsen führt (Kassan und Moutsopoulos, 2004). Kennzeichnend ist eine Symptomtrias: Mundtrockenheit, trockene Augen und trockene Nasen- und Rachenschleimhäute. Es kann als eigenständige Erkrankung aber auch als Teil rheumatischer Erkrankungen wie rheumatoider Arthritis oder Lupus erythematodes auftreten. Frauen sind deutlich häufiger betroffen als Männer (9:1). Üblicherweise bricht die Erkrankung zwischen dem 40. und 60. Lebensjahr aus (Heaton, 1962). Alkoholabusus Robb und Smith beschrieben eine signifikant höhere Prävalenz von Erosionen bei 37 untersuchten Alkoholikern verglichen mit einer Kontrollgruppe, die gleich alt und von gleichem Geschlecht war. Es zeigte sich, dass hauptsächlich die palatinalen Flächen der Oberkieferfrontzähne betroffen waren und, dass dies in den meisten Fällen mit 27 Literaturübersicht einer gastrooesophagealen Refluxerkrankung kombiniert war (Robb und Smith, 1989). Schwangerschaften Hormonell bedingt kann es während der Schwangerschaft zu einem ungewöhnlichen Essverhalten kommen, welches sich jedoch in der Regel nach der Geburt des Kindes wieder normalisiert. Vor allem im ersten Schwangerschaftstrimester kann es zu wiederholten Brechanfällen kommen. Zusätzlich steigt die Anfälligkeit für Reflux (Bartlett, 2006). Menstruationsbeschwerden Es gibt immer wieder Frauen, die während der Menstruation unter regelmäßiger Übelkeit bis hin zum Erbrechen leiden. Über die Jahre können sich an den Zähnen entsprechende erosive Defekte manifestieren (Bassiouny, 2008). 2.5 Antazida 2.5.1 Definition Antazida sind schwache Basen oder Salze schwacher Säuren, die nach oraler Einnahme in der Lage sind Magensäure zu neutralisieren (Mutschler et al., 2008; Karow und Lang-Roth, 2011). Zusätzlich binden sie Gallensäure und vermindern die Aktivität von Pepsin (Wehling, 2005). Sie bewirken jedoch keine Verminderung der Säureproduktion. Neben einer lang anhaltenden Wirkung sind eine hohe Pufferkapazität sowie eine geringe Resorption wünschenswert. Je eingenommener Einzeldosis sollten 30 bis 50 mVal Salzsäure (HCl) gebunden werden können. Maalox 70 mVal entspricht dieser Forderung (Burgis, 2005). Tabelle 5: Auswahl handelsüblicher Antazida Handelspräparat (eingetragenes Warenzeichen) Enthält Gelusil Aluminium-Magnesiumsilicathydrat Maalox, Maaloxan Aluminium- und Magnesiumhydroxid Renni Calzium- und Magnesiumcarbonat Talcid Aluminium-Magnesiumhydroxid-carbonathydrat (Hydrotalcid) Trigastril Aluminium- und Magnesiumhydroxid, Calziumcarbonat Quelle: Mutschler Arzneimittelwirkungen – Lehrbuch der Pharmakologie und Toxikologie. E. Mutschler, G. Geisslinger, H. K. Kroemer, P. Ruth, M. Schäfer-Korting, 9. Auflage, Wissenschaftliche Verlagsgesellschaft mbH Stuttgart, Seite 647 28 Literaturübersicht Als Goldstandard gelten Aluminiumverbindungen. Da diese zu Obstipationen führen, werden sie mit laxierend wirkenden Magnesiumverbindungen kombiniert. Ein weiterer häufiger Bestandteil ist Kalzium. Natriumhydrogencarbonathaltige Antazida gelten heute als obsolet (Mutschler et al., 2008; Burgis, 2005). 2.5.2 Indikation Antazida werden zur Behandlung von Sodbrennen, Gastritis, peptischer Refluxösophagitis und zur Prophylaxe des Stressulkus eingesetzt (Burgis, 2005). Sie sind zur schnellen, symptomatischen Behandlung indiziert. Die Einnahme sollte ein bis drei Stunden nach Nahrungsaufnahme sowie vor dem Schlafengehen erfolgen. Ist eine Senkung der Säureproduktion therapeutisch notwendig, müssen zusätzlich Protonenpumpeninhibitoren und/oder H2-Antagonisten eingesetzt werden. Antazida dienen in diesem Fall nur der akuten Schmerzbehandlung (Mutschler et al., 2008). 2.5.3 Chemie und Wirkungsweise Die Wirkungsweise beruht darauf, dass die basischen Antazida im Magen Protonen binden und somit die Säurekonzentration verringern (Lüllmann et al., 2010). Aluminiumhydroxidhaltige Antacida Aluminiumhydroxid Al(OH3) reagiert im Magen in einer Gleichgewichtsreaktion mit Salzsäure (HCl) Reaktionsprodukte zu Aluminiumchlorid stehen im AlCl3 Gleichgewicht und mit Wasser (H2O). Die Aluminiumhydroxidchlorid (Al(OH)Cl2), Salzsäure (HCl) und Wasser (H2O). Neutralisationsreaktion aluminiumoxidhaltiger Antacida: Al(OH3) + 3 HCL ⇄ AlCl3 + 3 H2O ⇄ Al(OH)Cl2 + HCl + 2 H2O Das entstandene AlCl3 kann weiter reagieren und Phosphat (PO4-) binden. Dazu bedarf es der Reaktionspartner Natriumdihydrogenphosphat (Na2HPO4) und Natriumhydrogenphosphat (NaH2PO4). Es entsteht Aluminiumphosphat (AlPO4). Diese schwerlösliche Verbindung wird mit dem Stuhl ausgeschieden. Als Nebenprodukte entstehen Kochsalz (NaCl) und Salzsäure (HCl) (Reichel et al., 2007). 29 Literaturübersicht Phosphatbindung durch aluminiumhaltige Antacida: 2 AlCl3 + Na2HPO4 + NaH2PO4 → 2 AlPO4 + 3 NaCl + 3 HCl Bei langfristiger Einnahme kann es so zu einem Phosphatmangel mit nachfolgenden Osteopathien kommen (Mutschler et al., 2008; Burgis, 2005). Magnesiumoxidhaltige Antacida Magnesiumoxid (MgO) reagiert im Magen mit Salzsäure (HCl) zu Magnesiumchlorid (MgCl2) und Wasser (H2O). Neutralisation der Magensäure durch Magnesiumoxid MgO + 6 HCl → 3 MgCl2 + 3 H2O Auch Magnesiumchlorid kann in einer Folgereaktion Phosphat binden, welches ebenfalls über den Stuhl ausgeschieden wird. Phosphatbindung durch magnesiumoxidhaltige Antacida: 3 MgCl2 + 2 NaH2PO4 → Mg3(PO4)2 + 4 HCl + 2 NaCl Magnesiumphosphat kann aber auch weiter reagieren, in dem es zwei weitere H+Ionen bindet. Dabei kommt es nicht zu einer Säureausscheidung, lediglich zu einer vorübergehenden Pufferung (Worlitschek, 2008). 2.5.4 Unerwünschte Wirkungen Bei der Einnahme aluminuimhydroxidhaltiger Antazida wird im Gastrointestinaltrakt etwa 1% des Aluminiums resorbiert. In Folge kann es zu einer Form der Enzephalopathie mit Demenz, Sprachstörungen, Krämpfen und anderen Symptomen kommen (Reichel et al., 2007). Allgemein zeigen Antazida einen hemmenden Einfluss auf die Resorption anderer Medikamente, beispielsweise von Eisenpräparaten, Penicillinen, Tetracyklinen und Betablockern. Sie sollten deswegen frühestens zwei Stunden nach Einnahme des Antazidums verabreicht werden (Burgis, 2005; Karow und Lang-Roth, 2011). 30 Material und Methode 3. Material und Methode 3.1 Vorversuch Vor Beginn der eigentlichen Testung erfolgte ein Probelauf. Vier Schmelzproben wurden im bukkalen Bereich einer für den Unterkiefer angefertigten Kunststoffschiene platziert. Die Schiene wurde für knapp drei Stunden getragen, zur Simulation eines Säureangriffs wurde die Schiene für fünf Minuten in 1M Salzsäure eingelegt. Darauf folgend mit Leitungswasser abgespült und anschließend für fünf Minuten in Maalox 70 mVal Suspension (A. Nattermann & Cie, Köln, Deutschland) gelegt. Der Zyklus wurde insgesamt vier Mal durchlaufen. In einem zweiten Durchgang wurde auf die Lagerung in Maalox 70 mVal (A. Nattermann & Cie, Köln, Deutschland) Suspension verzichtet. Vorher und nachher wurde die Mikohärte der Proben bestimmt. 3.2 Aufbau der Studie und Versuchsplan Um die Wirkung von Maalox 70 mVal (A. Nattermann & Cie, Köln, Deutschland) in der Mundhöhle zu Kunststoffschienen für Rinderschmelzproben untersuchen, den und erhielten Oberkiefer. eine fünf In Probanden diese wurden pH-Wert-Messelektrode abnehmbare jeweils vier (Bravo® pH- Überwachungssystem, Medtronic GmbH, Düsseldorf, Deutschland) eingearbeitet. Pro Proband wurden zwei Versuchsperioden durchgeführt, wobei eine Versuchsperiode zwei Tage umfasste. Je Tag wurden die Schienen 16 Stunden am Stück getragen. In der ersten Versuchsperiode wurden die Probanden angehalten alle zwei Stunden eine Minute lang mit Sprite Zero© (The Coca-Cola Company Deutschland – Verkauf, GmbH und Co. KG, Berlin, Deutschland) zu spülen, um einen Säureangriff zu simulieren. Das Spülen sollte mit mehreren Schlucken nacheinander erfolgen. Anschließend wurde ebenfalls eine Minute lang mit Leitungswasser nachgespült. Der erste Spülvorgang erfolgte beim Einsetzen der Schiene. In der zweiten Versuchsperiode wurde das Spülen mit Wasser durch ein einminütiges Spülen mit Maalox 70 mVal Suspension ersetzt (A. Nattermann & Cie, Köln, Deutschland). Die Suspension sollte nach Ablauf der Spülzeit ausgespuckt und auf ein zusätzliches Spülen mit Leitungswasser verzichtet werden. Zum Essen wurde die Schiene entnommen und in Wasser gelagert. Beim Trinken durfte die Schiene im 31 Material und Methode Mund belassen werden. Innerhalb eines Zeitraums von etwa zehn Minuten vor bis zehn Minuten nach dem Spülen sollte auf Essen und Trinken verzichtet werden. Die Schiene wurde in Wasser gelagert, wenn sie nicht getragen wurde. Während der gesamten Versuchszeit wurde der pH-Wert registriert (Bravo® pHÜberwachungssystem, Medtronic GmbH, Düsseldorf, Deutschland). Vor und nach Ablauf einer Versuchsperiode wurde die Härte nach Knop der einzelnen Proben bestimmt. In Abbildung 1 (siehe Seite 33) ist der Versuchsablauf schematisch dargestellt. 3.3 Probenherstellung Bei den zur Gewinnung der Proben erforderlichen Rinderzähne handelte es sich um Unterkieferfrontzähne, die direkt nach dem Schlachten entnommen und dann bis zur Weiterverarbeitung in einer 0,1%igen Thymollösung (Merck, Darmstadt, Deutschland) bei 8°C im Kühlschrank gelagert wurden. In dieser Zeit wurden die bei der Schlachtung entnommenen Hirnbiopsien auf bovine spongiforme Encephalopathie (BSE) hin untersucht. Nur Zähne von Rindern mit einem negativen Befund wurden in der Studie verwendet. Der vestibulären Fläche wurden mit einem diamantierten Trepanbohrer (Gebr. Brasseler, Lemgo, Deutschland) Proben im Durchmesser von 3,5mm entnommen. Es wurde darauf geachtet, die Proben nur in dem Bereich des Zahnes zu entnehmen, der zum Zeitpunkt des Schlachtens bereits durchgebrochen und möglichst sauber war. Immer zwei Schmelzproben wurden gemeinsam in einen Kunststoff zur Herstellung kieferorthopädischer Geräte (Orthocryl Pulver klar, Dentaurum, J.P. Winkelstroeter KG, Ispringen, Deutschland) eingebettet. Die so gewonnenen Kunststoffscheiben wurden anschließend auf einem Objektträger (50x100x1,5mm, Exakt-Apparatebau, Norderstedt, Deutschland) fixiert. Dieser wurde in eine automatische Schleifmaschiene eingespannt (Exakt- Dünnschliffsystem; Exakt Apparatebau, Norderstedt, Deutschland; Tellerschleifer: Knuth-Rother-3, Struers, Willich, Deutschland) und die Proben nacheinander unter Wasserkühlung mit Schleifpapier der Körnungsgrößen 800, 1200, 2400 und 4000 beschliffen und poliert (Silicon Carbide Paper; Struers, Willich, Deutschland). Bevor die in Kunststoffscheiben im Gaumenbereich der Oberkieferseitenzähne mit Klebewachs (Deiberit 502, Hartklebewachs rot, Dr. Böhme und Schöps Dental GmbH, Goslar, Deutschland) fixiert wurden, 32 wurde etwa ein Drittel der Material und Methode Schmelzoberfläche mit Heliobond (Ivoclar Vivadent AG, Schwaan, Lichtenstein) abgedeckt. Rinderfrontzähne Schmelzproben n = 40 Gruppe 1 n = 10 Kunststoffplättchen n = 20 Gruppe 2 n = 10 Mikrohärtemessung (=Ausgangswerte) 1 Minute intraoral Maalox 70 mVal 1 Minute intraoral Wasser 2 Stunden Remineralisation durch Speichel, intraoral Mikrohärtemessung (= Endwerte) Abbildung 1: Schematischer Versuchsaufbau 33 Aufzeichnung des intraoralen pH-Werts 7 Wiederholungen Demineralisation für eine Minute mit Sprite Zero, intraoral Material und Methode 3.4 Schienenherstellung Von jedem Probanden wurden Situationsmodelle angefertigt, auf denen mit dem Erkopress – System 300 TP (Firma Erkodent, Pfalzgrafenweiler, Deutschland) Tiefziehschienen hergestellt wurden. Die verwendeten Kunststoffplatten (Erkodur, Firma Erkodent, Pfalzgrafenweiler, Deutschland) waren 1,0 mm dick. Für den Unterkiefer war eine einfache Tiefziehschiene, die zum Schutz der Zähne getragen werden sollte, ausreichend. Im Oberkiefer wurde am Gaumen auf dem Gipsmodell eine funktionslose pH-Messelektrode (Medtronic GmbH, Düsseldorf, Deutschland) mittels Klebewachs (Deiberit 502, Hartklebewachs, rot, Dr. Böhme und Schöps Dental GmbH, Goslar, Germany) angebracht, die als Platzhalter für die eigentliche Messelektrode diente. Je Schiene kamen zwei Kunststoffplättchen zum Einsatz. 3.5 Probandenauswal Um an der Studie teilzunehmen, mussten die Probanden zwischen 18 und 60 Jahren alt und allgemeinmedizinisch gesund sein. Sie mussten eine normale Mundhygiene aufweisen (d.h. zweimal täglich Zähne putzen) und ihre Speichelflussrate sollte mehr als 0,8 ml/min betragen. Schwangere oder Stillende wurden zur Studie ebenso wenig zugelassen wie Personen, die zum entsprechenden Zeitpunkt erosiv wirkende Medikamente einnahmen. Weitere Ausschlusskriterien waren Mundschleimhauterkrankungen, Xerostomie, Essstörungen, gastroenterale Erkrankungen, eine eingeschränkte Compliance sowie bekannte Allergien gegen in der Studie verwendete Substanzen. 3.6 Bravo® pH-Überwachungssystem Zur kontinuierlichen Aufzeichnung des intraoralen pH-Werts, kam das Bravo® pHÜberwachungssystem (Medtronic GmbH, Düsseldorf, Deutschland) zum Einsatz. Es besteht aus einer Sonde, die den pH-Wert registriert und einem Empfängergerät, das in der Lage ist die alle drei bis fünf Sekunden von der Sonde übermittelten Daten über einen Zeitraum von maximal 48 Stunden aufzuzeichnen. Die Daten können auf einen Computer übertragen und mit dem zugehörigen Programm ausgewertet werden. Für eine problemlose Datenübertragung ist es unbedingt nötig den Empfänger nicht weiter als einen Meter von der Sonde zu entfernen. Um funktionsfähig zu sein, 34 Material und Methode benötigt der Empfänger eine handelsübliche AA/LR6-Batterie. Das Austauschen der Batterie während der Messung hat laut Hersteller keinen negativen Einfluss auf die Kalibrierung der Sonde. Am Empfängergerät befinden sich drei Symptomtasten. Das Drücken einer dieser Tasten schlägt sich in einer farblichen Veränderung der Verlaufskurve des pH-Werts nieder. In der vorliegenden Studie wurden die Tasten verwendet, um zu vermerken wann einer der Probanden ein Getränk zu sich nahm. 3.7 Maalox 70mVal Suspension Maalox 70 mVal (A. Nattermann & Cie, Köln, Deutschland) ist ein zugelassenes, apothekenpflichtiges Medikament, dessen Wirkung auf der Bindung überschüssiger Magensäure beruht. Laut Packungsbeilage ist die Anwendung zur symptomatischen Behandlung bei Sodbrennen, säurebedingten Magenbeschwerden sowie Magenoder Zwölffingerdarmgeschwüren (Ulcus ventriculi oder Ulcus duodeni) freigegeben. Ein Beutel Maalox 70 mVal enthält 10ml. Diese enthalten als arzneilich wirksame Bestandteile Aluminiumoxi) Algeldrat und aus 600 Aluminiumhydroxi-Gel mg Magnesiumhydroxid. (entsprechend Das 900 entspricht mg einer Neutralisationskapazität von 70mVal Salzsäure. Sonstige Bestandteile sind: Sorbitol, Simethicon, Methylcellulose, Saccharin-Natrium, Pfefferminzöl, Zitronensäure, Methyl(4-hydroxybenzonat), Propyl(4-hydroxybenzonat), Wasserstoffperoxid-Lösung und gereinigtes Wasser. Schwangere oder Stillende sollten Maalox 70 mVal Suspension nicht einnehmen, Gleiches gilt für Kinder unter zwölf Jahren. Als Kontraindikation gelten des Weiteren eine eingeschränkte Nierenfunktion, Hypophosphatämie und angeborener FructoseUnverträglichkeit. 3.8 Messverfahren zur Auswertung der Proben Zur Auswertung der Proben wurden die Mirkohärte und die transversale Mikroradiographie (TMR) herangezogen. Zusätzlich wurden die pH-Werte zwischen den Gruppen „Wasser“ und „Maalox 70 mVal“ verglichen. Primärer Endpunkt der Studie war die Bestimmung der Demineralisationsperiode. Die Messung der Schmelzmikrohärte galt als ihr sekundärer Endpunkt. 35 Material und Methode 3.8.1 pH-Wert Die im Rahmen der pH-Metrie gewonnenen und aufgezeichneten Daten wurden mit Hilfe der dazugehörigen Software auf einen Computer übertragen und graphisch dargestellt. Auf der x-Achse war die Zeit, auf der y-Achse der pH-Wert aufgetragen. Das Ablesen der gewünschten Werte wurde durch die Möglichkeit der Parallelverschiebung der Achsen erleichtert. Zur Auswertung werden folgende Werte herangezogen: 1. pH1 = pH-Wert vor Spülbeginn 2. pH2 = pH-Wert nach Spülbeginn (immer den tiefsten Wert) 3. t(0) =Spülzeitpunkt (= Spülbeginn, deutlichen Abfall der Kurve) 4. t(4,5) = Zeitpunkt, an dem der pH-Wert unter 4,5 sinkt 5. t(5,5) = Zeitpunkt, an dem der pH-Wert wieder auf über 5,5 ansteigt 6. t(1) = Zeitpunkt, an dem der Ausgangs-pH-Wert wieder erreicht wird. Sollte dieser nicht wieder erreicht werden, wird der Zeitpunkt bei Erreichen des maximalen Wertes bestimmt. Für die Punkte 4. bis 6. gilt, dass die Kurve oberhalb des entsprechenden Wertes liegen muss. Kurzfristige Peaks bleiben unberücksichtigt. Folgende Werte wurden daraufhin rechnerisch bestimmt: 7. t(4,5) – t(0) = Zeitraum bis zum Beginn der Demineralisation 8. t(5,5) – t(0) = Demineralisationsperiode 9. t(1) – t(0) = Zeit bis zum Erreichen des Ausganswertes 3.8.2 Mikrohärte Jede Probe wurde vor Beginn und nach Abschluss der Versuchsreihe vermessen, wobei jeweils der Mittelwert aus fünf Messungen pro Probe bestimmt wurde. Um die Mikrohärte nach KNOP zu bestimmen, wurden die Proben mit Hilfe eines Prüfkörpers für 30 Sekunden einem Druck F von 1,030 N ausgesetzt (Miniload, Leitz, Wetzlar, Deutschland). Als Prüfkörper fungierte eine Diamantpyramide. Dies führt dazu, dass sich auf der Probenoberfläche rautenförmige Abdrücke bilden, deren Tiefe direkt von der Härte der Oberfläche abhängt. Dabei gilt: Je weicher die Oberfläche, desto größer die Impressionen. Zu beachten ist, dass die Messungen nicht zu nah 36 Material und Methode beieinander durchgeführt werden, damit es nicht zu einer Überlappung der Impressionen kommt. Die Längsachse der Impressionλ wird unter dem Mikroskop bei 500facher Vergrößerung mit Hilfe eines Meßokulars (Leitz, Wetzlar, Deutschland) vermessen. Eine angeschlossene Recheneinheit (RZD-DO, Leitz, Wetzlar, Deutschland) ist in der Lage den ermittelten metrischen Wert in die KNOOP-Härte (KNH) um zurechnen, nach folgender Formel: KHN = 1450,5x10³xF λ² Es gilt: KHN = Knoop Hardness Number in kp/mm² F = die aufgebrachte Kraft in N λ = Länge der Diagonale der Impression des Prüfkörpers auf der Probenoberfläche in µm 3.8.3 Transversale Mikroradiographie Die transversale Mikroradiographie (TMR) ist ein Verfahren zur Bestimmung von Mineralgehalt und Läsionstiefe einer Probe. Im Rahmen der TMR-Auswertung werden aus den Proben Dünnschliffe gewonnen und diese anschießend am PC mikroskopisch beurteilt. Da die Proben dabei kaputt gehen, erfolgte diese Auswertung als letzte. Zur Herstellung der Dünnschliffe wurde der Kunststoff, in dem die Proben eingebettet waren, entfernt. Jede einzelne Probe wurde auf einem Objektträger (50x100x1,5 mm, Exakt-Apparatebau, Norderstedt, Deutschland) befestigt und dabei so platziert, dass die Grenzlinie zwischen der mit Heliobond (Ivoclar Vivadent AG, Schwaan, Lichtenstein) abgedeckten und der exponierten Seite senkrecht zum Objektträger verlief. Anschließend wurden die Proben in einen weiteren Kunststoff (Tecnovit 9100, Heraeus Kulzer GmbH, Wehrheim, Deutschland) eingebettet. Auf dem Objektträger wurde mittels eines spitzen Diamanten sowohl die Probennummer markiert, als auch die Seite gekennzeichnet, auf der die Probe mit Heliobond abgedeckt war. Die Probe wurde in der Mitte, parallel zum Objektträger, zersägt (Diamantbandsäge, ExaktApparatebau, Norderstedt, Deutschland). Und anschließend erneut beschliffen und poliert (Körnungsgrößen 1200, 2400 und 4000, Silicon Carbide Paper; Struers, Willich, Deutschland). Auf der planen Probenfläche wurde ein zweiter Objektträger 37 Material und Methode befestigt. Die Fixierung erfolgte durch Heliobond, das lichtgehärtet wurde. In einem Abstand von 400 bis 500 µm zum zweiten Objektträger wird die Probe erneut gesägt und wieder beschliffen und poliert. Nach dem Polieren sollten alle Proben eine gleichmäßige Dicke von etwa 120 µm und eine plane Oberfläche aufweisen. Die Dicke der so gewonnenen Probenscheibe wurde in der Bügelmessschraube (Mikrometerschraube, Mitutoyo, Messgeräte GmbH, Neuss, Deutschland) bestimmt. Zur Anfertigung des Röntgenbildes wurden die vom Objektträger gelösten Proben an der Dentinseite mit einem ca. einen Millimeter breiten Tesafilmstreifen fixiert und auf einem speziellen halbrunden Plastikträger (TMR-Träger, Inspektor Research Systems BV, Amsterdam, Niederlande) befestigt. Um später zu wissen welche Seite der Probe die mit Heliobond abgedeckte war, wurde diese immer nach links gelegt, wobei die Schmelzseite zur geraden Fläche des Plastikträgers zeigte. Die Anfertigung der Röntgenbilder erfolgt mit einem speziellen Röntgengerät (CuKα – Röntgenquelle, PW 1830/40, Philips, Kassel, Deutschland). Hinter den Proben wurde ein röntgenempfindlicher Film (Kodak high speed holographic film SO-253, Kodak AG, Stuttgart, Deutschland) eingelegt. Anfang und Ende des Films wurden markiert. Die Probe wird parallel zur behandelten Oberfläche und senkrecht zur Schnittfläche von der Röntgenstrahlung (20mA, 20 kV) durchdrungen. Die Belichtung der Proben dauerte zwölf Sekunden. Mit der Probe wird ein fest montierter Aluminiumstufenkeil auf dem Film abgelichtet. Dieser dient bei der Auswertung der Kalibrierung. Die Entwicklung des Filmes erfolgte gemäß den Herstellerangaben. Die Negative wurden am Computer unter Zuhilfenahme eines Mikroskops ausgewertet. Dabei wurden je Probe zwei Bilder angefertigt, einmal für die abgedeckte und einmal für die exponierte Seite der Probe. In allen Fällen wurden der Mineralverlust und die Läsionstiefe bestimmt. 3.9 Statistische Auswertung Zur Bestimmung statistischer Zusammenhänge wurden der Oneway-Anova und der Wilcoxon-Test herangezogen. Die statistische Auswertung erfolgte mit Hilfe des Softwareprogramms SPSS 14.0.1 (SPSS, Chicago, Il, USA) 38 Ergebnisse 4. Ergebnisse 4.1 pH-Werte Die Auswertung der pH-Wert-Messung (Tabelle 6) ergab eine beschleunigte Neutralisation, wenn nach Säureattacken mit Maalox 70mVal gespült wird. Je höher der Ziel-pH-Wert, desto deutlicher war das Ergebnis. Aus den Abbildungen 2 und 3 geht hervor, dass sich der intraorale pH-Wert in den beiden Gruppen Wasser und Maalox vor Versuchsbegin und direkt nach dem einminütigen Spülen mit Sprite Zero© gleicht. Der vorhandene Unterschied ist nicht signifikant (p > 0,001). Tabelle 6: Ergebnisse der pH-Wertmessung 39 Ergebnisse Abbildung 2: Verteilung der Ausgangs-pH-Werte Abbildung 3: Verteilung der pH-Wert direkt nach dem Spülen mit Sprite Zero® 40 Ergebnisse Ein zeitlicher Unterschied zwischen den Gruppen bis zu einem Wiederanstieg des oralen pH-Wertes von 4,5 war nicht zu beobachten. Ohne Spülen mit Maalox 70 mVal wurde dieser Wert nach 85,52 Sekunden (+/- 23,94) erreicht; mit Maalox70mVal-Spülung nach 84,03 Sekunden (+/- 24,07) Für den Ziel-pH-Wert von 5,5 fand sich bereits ein signifikanter Unterschied (p < 0,001). Beim Spülen mit Wasser wurden 134,48 Sekunden(+/- 76,73), beim Spülen mit Maalox 70 mVal nur 88,38 Sekunden (+/- 21,08) benötigt. Noch deutlicher zeigt sich dies bis zur Einstellung des anfänglichen pH-Wertes. In der Wassergruppe waren dafür 682,71 Sekunden (+/925,86) nötig, mit Maalox 70 mVal gelang dies in 113,76 Sekunden (p < 0,001). Die Abbildungen 4 bis 6 stellen dies graphisch dar. Abbildung 4: Verteilung der pH-Werte zum Zeitpunkt t (4,5) 41 Ergebnisse Abbildung 5: Verteilung der pH-Werte zum Zeitpunkt t (5,5) Abbildung 6: Benötigte Zeit zum Erreichen des ursprünglichen pH-Werts in Sekunden 42 Ergebnisse 4.2 Mikrohärte Es konnte gezeigt werden, dass im Vergleich zu einer Spülung mit Wasser beim Spülen mit Maalox 70 mVal die Mikrohärte zunimmt, auch wenn sich nur eine geringe Signifikanz ergab (p = 0,047). In beiden Gruppen waren die Ausgangsbedingungen gleich. Die anfängliche mittlere Mikrohärte betrug für die Wassergruppe rund 280 (+/- 37,19), für die Maaloxgruppe rund 286 KNH (+/- 28,36). Dieser Unterschied ist statistisch nicht signifikant. Die Veränderung der Mikrohärte zeigt Abbildung 7. Abbildung 7: Graphische Darstellung der Veränderung der Mikrohärte 250 Mikrohärte Differenz 200 150 100 50 0 Wasser Maalox Spülmedium 4.3 Transversale Mikroradiographie Mineralverlust Vor Versuchsbegin lag der Mineralverlust der Proben der Gruppe Wasser bei 341,94 (+/- 163,78) und für die Gruppe Maalox bei 439,33 (+/- 262,95). Nach Behandlung der Proben mit den entsprechenden Spülmedien fand sich in der Gruppe Wasser ein Endwert von 402,73 (+/- 272,19). Für Maalox konnte ein Endwert von 352,07 (+/153,44) festgestellt werden. Abbildung 8 stellt den mittleren Mineralverlust graphisch dar. Die Werte zeigen, dass in der Maaloxgruppe der Mineralverlust negativ ist, also eine Zunahme stattgefunden hat. Vergleicht man die beiden Gruppen Wasser und Maalox, so zeigt sich ein signifikanter Unterschied (p<0,5). 43 Ergebnisse Es konnte gezeigt werden, dass das Spülen mit Maalox 70 mVal zumindest nicht zu einer Demineralisation führt, wenn nicht sogar eine Wiedereinlagerung von Mineralien an der exponierten Schmelzoberfläche durch den Speichel unterstützt. Läsionstiefe Die Läsionstiefe betrug zu Begin 9,99 (+/- 6,71) in der Gruppe Wasser und 10,81 (+/- 8,00) in der Gruppe Maalox. Bei Abschluss der Versuchsreihe waren die Werte auf 8,88 (+/- 4,50) in der Gruppe Wasser und auf 10,14 (+/-6,43) in der Gruppe Maalox gefallen. Die Veränderung der Werte betrug -1,12 (+/-6,63) für Wasser und -0,67 (+/-5,82) für Maalox. In Abbildung 9 ist die Veränderung der Läsionstiefe graphisch dargestellt. Weder das Spülen mit Wasser noch das Spülen mit Maalox 70 mVal hatte einen nennenswerten Effekt auf unterhalb der Oberfläche gelegene Schichten. Die statistische Auswertung konnte keinen signifikanten Unterschied in der Veränderung der Läsionstiefe nachweisen. Mittlerer Mineralverlusts Abbildung 8: Graphische Darstellung des mittleren Mineralverlusts Spülung 44 Ergebnisse Mittlere Veränderung der Läsionstiefe Abbildung 9: Graphische Darstellung der Veränderung der Läsionstiefe Spülung 45 Diskussion 5. Diskussion 5.1 Material und Methode 5.1.1 Versuchsaufbau Studiendesign Es ist bekannt, dass kurze aber häufige Säureeinwirkungen bei identischer Gesamteinwirkzeit einen höheren Mineralverlust bedingen als längere aber dafür wenige Säureangriffe (Kirkham et al., 1994). Beim Verzehr saurer Speisen oder dem Genuss säurehaltiger Getränke kommt es über den Tag verteilt zu kurzen aber öfteren Säureangiffen (Meurman und ten Cate, 1996). Patienten, die an chronischem Erbrechen leiden, übergeben sich häufig. So wurde ein Versuchsaufbau mit kurzen (eine Minute) aber häufigeren (acht Mal täglich) Säureangriffen gewählt. Wie einige Übersichtsarbeiten zeigen, ist das Tragen von Applikationsschienen mit eingearbeiteten Schmelzproben ein gängiges Verfahren um die Wirkung eines Agens zum Schutz vor Erosionen in situ zu prüfen (Young und Tenuta, 2011; West et al., 2011). Während der Nicht-Tragezeit sollten die Applikationsschienen feuchtgelagert werden, als Kontrollgruppe empfiehlt sich die Verwendung von Wasser (West et al., 2011). Überlagernde abrasive Prozesse wurden versucht zu vermeiden, indem die Applikationsschienen nicht mechanisch gereinigt wurden. Durch die palatinal-distale Platzierung der Proben, sollten Abrasionen durch das orale Weichgewebe möglichst verhindert werden. Es ist davon auszugehen, dass sich durch die intraoralen Bedingungen eine Plaque ausbilden konnte. Sprite Zero © Das Spülen mit Softdrinks zur Simulation eines Säureangriffs ist eine gängige Praxis (Young und Tenuta, 2011; Wiegand und Attin, 2011). Im vorliegenden Versuchsaufbau wurden die Probanden angehalten mit Sprite Zero© zu spülen. Der pH-Wert von Sprite Zero© wird in der Literatur mit 2,6 (Murrell et al., 2010) bis 3,2 (Lussi und Jaeggi, 2009) angegeben. Für Magensaft wird im nüchternen Zustand ein pH-Wert von 0,8 bis 2 beschrieben (Lussi und Jaeggi, 2009). Der intraorale pH-Wert jedoch fällt auf Grund der Verdünnung der Säure durch den Speichel sowie dessen Pufferkapazität so gut wie nie unter 1,5 (Young und Tenuta, 2011). Für bulämische 46 Diskussion Patienten geben Milosevic et al. den pH-Wert des Erbrochenen mit 2,9 bis 5,0 an (Milosevic et al., 1997). Der pH-Wert im Versuch entspricht damit durchaus reellen Bedingungen. Die Art und Weise das Getränk zu konsumieren kann Enfluss auf die Erosionsentstehung haben (Millward et al., 1997; Edwards et al., 1998). Um Unterschiede im Trink- bzw. Spülverhalten zu vermeiden, wurden die Probanden daher instruiert den Mund gut durchzuspülen und innerhalb der Spülzeit mehrere frische Schlücke zunehmen. Schmelzproben Der chemische Aufbau von Rinderschmelz entspricht dem humaner Zähne (Davidson et al., 1973). Obwohl gezeigt werden konnten, dass sich erosive Vorgänge an bovinem Zahnschmelz weitgehend ähnlich darstellen wie an humanem Zahnschmelz (Meurman und Frank, 1991), ist bekannt, dass boviner Schmelz auf erosive Einflüsse empfindlicher reagiert (Amaechi et al., 1999). Zwischen humanen Weisheitszähnen und Rinderfrontzähnen des Unterkeifers konnte bei kombiniert erosiven-abrasiven Versuchsbedinungen kein Unterschied im Verhalten festgestellt werden (Wegehaupt et al., 2008). Die Verwendung von aus Rinderfrontzähnen gewonnenen Schmelzproben gilt zur Untersuchung erosiver Prozesse als gängiges und in der Literatur viel beschriebenes Verfahren (Young und Tenuta, 2011; Wiegand und Attin, 2011; West et al., 2011). Durch das Beschleifen und Polieren der Schmelzproben wurde die für die Messungen erforderliche plane Oberfläche geschaffen. Allerdings reagiert der polierte Schmelz empfindlicher auf Säureangriffe, als unpolierter, da durch die Bearbeitung die prismenfreie, fluoridreiche und säureresistente oberste Schmelzschicht entfernt wird (Whittaker, 1982; Meurman und Frank, 1991). Intraoral findet sich eine aprismatische Schmelzoberfläche erst nach häufigen erosiven Angriffen (Noack, 1989; Lussi et al., 1991). Patienten mit Essstörungen in Kombination mit chronischem Erbrechen neigen dazu ihre Erkrankung zu verheimlichen (Hazelton und Faine, 1996), sodass es relativ spät zur Diagnosestellung kommt. Es kann demnach davon ausgegangen werden, dass die betroffenen Zahnoberflächen aprismatisch sind. Die Proben wurden palatinal platziert. Ob die Proben anterior oder posterior am Gaumen platziert werden, führt zu keinem signifikanten Unterschied, was die 47 Diskussion Erosionsentstehung anbelangt (Hooper et al., 2007). Bei Patienten, die sich häufig übergeben, werden in erster Linie die palatinalen Flächen erosiv geschädigt (Bartlett, 2006). Eine entsprechende Platzierung der Proben ist also sinnvoll. Insgesamt entspricht der Versuchsaufbau Verhältnissen, wie sie bei Patienten mit chronischem Erbrechen zu erwarten sind. 5.1.2 Messverfahren Mikrohärte Die Bestimmung der Mikrohärte wurde als Testverfahren herangezogen, um zu ermitteln, ob sich De- bzw. Remineralisationsprozesse an der Oberfläche der exponierten Proben abgespielt haben oder nicht. Es handelt sich um ein allgemein anerkanntes Vorgehen, dass bislang in vielen Studien Anwendung fand (Barbour und Rees, 2004; Attin, 2006). Dass ein De- oder Remineralisationsprozess sich in einer Veränderung der Mikrohärte widerspiegelt, konnte 1983 von Featherstone et al. nachgewiesen werden (Featherstone et al., 1983). Bekannt ist auch der Zusammenhang zwischen Abnahme der Mikrohärte und Verlust von Kalzium im Zahnschmelz (Davidson et al., 1974). Für gesunden Zahnschmelz wird eine Mikrohärte von 280 bis 390 KHN angegeben, wenn sie mit einer Kraft von 100g belastet werde (Lussi et al., 2011). Die anfänglichen Mikrohärten der im vorliegenden Versuch verwendeten Schmelzproben erfüllen diese Anforderung. pH-Wert/Bravo-System Die pH-Metrie ist ein für die Diagnose von Refluxerkrankungen anerkanntes Verfahren. Sie stellt eine einfache Methode dar den intraoesophagealen pH-Wert kontinuierlich aufzuzeichnen. Zur Aufzeichnung des intraoralen pH-Wertes kann eine Messsonde palatinal in eine Applikationsschiene eingearbeitet werden (Bartlett et al., 1996a). Das Gerät wurde nach beiliegender Gebrauchsanleitung verwendet. Den Probanden wurde der Umgang mit dem Gerät vorher beigebracht. Transversale Mikroradiographie (TMR) Mikroradiographie beschreibt ein Verfahren zur Auswertung von Röntgenbildern. Seit Beginn der 1960er Jahre besteht die Möglichkeit der quantitativen Beurteilung des 48 Diskussion Mineralgehalts. Dafür entwickelten Angmar et al. einen Aluminiumstufenkeil als Referenz (Angmar et al., 1963). In einem Vergleich verschiedener Mikroradiographien kamen Arends und Ten Bosch zu dem Ergebnis, dass die transversale Mikroradiographie die beste Methode zur Bestimmung des Mineralgehaltes sei (Arends und ten Bosch, 1992). Die TMR fand in zahlreichen Studien zur Untersuchung de- bzw. remineralisierter Zahnsubstanz Anwendung (Amaechi et al, 1999; Laheij et al., 2010). 5.2 Ergebnisse 5.2.1 pH-Wert-Messung Die Ergebnisse der pH-Wert-Messung entsprechen den Erwartungen: Die benötigte Zeit bis zur Neutralisation konnte deutlich verkürzt werden. Meurman et al kamen in einem etwas anderen Versuchsaufbau sogar zu dem Ergebnis, das ein Spülen mit Antacida gar nicht erst zu einem Abfall des intraoralen pH-Werts führt (Meurman et al., 1988). 5.2.2 Mikrohärte Für die Mikrohärte konnte lediglich ein minimal signifikanter Unterschied gezeigt werden, obwohl ein deutlicherer Unterschied erwartet wurde. Eine mögliche Erklärung dafür ist die Überlagerung mit abrasiven Prozessen. Diese können durch das orale Weichgewebe (in vorliegenden Fall die Zunge) verursacht werden (Wiegand und Attin, 2011). Die erweichte Oberfläche reagiert auf die abrasiven Vorgänge empfindlicher (Lussi et al., 1991). Maalox 70mVal führte im Gegensatz zu Wasser zu einer gewissen Remineralisation. Die Ergebnisse der transversalen Mikroradiographie unterstützen diese Vermutung (vgl. Absatz 5.2.3). Patienten mit Essstörungen weisen oft eine übertriebene Mundhygiene auf (Imfeld und Imfeld, 2005b). In diesem Zusammenhang muss in weiteren Studien geprüft werden, ob und wenn ja in welchem Maß Maalox 70 mVal abrasive Prozesse minimieren kann. Auch die Pellikel bzw. die dentale Plaque beeinflussen die Erosionsentstehung. Wenn nun einer der Probanden eine höhere Plaquebildungsrate aufweisen sollte, 49 Diskussion könnte dies sowohl den Einfluss der Säure als auch die Wirkung von Maalox 70 mVal hemmen (Hannig, 1999; Lendenmann et al., 2002). Die Probanden waren angehalten die Applikationsschienen 16 Stunden am Stück zu tragen. Wann innerhalb von 24 Stunden, war ihnen dabei selbst überlassen. Da sich über den Tag verteilt der Speichelfluss verändert, könnte dies einen Einfluss auf die gewonnenen Daten haben (Zero und Lussi, 2006). 5.2.3 Transversale Mikroradiographie Die Ergebnisse der transversalen Mikroradiographie entsprechen den Erwartungen. Die mit Maalox 70 mVal behandelten Proben wiesen im Gegensatz zu den mit Wasser behandelten keinen Mineralverlust auf (Tabellen 11 und 12), während die Läsionstiefe in beiden Gruppen unverändert blieb (Tabelle 15). Erosionen sind ein Oberflächenphänomen (Attin, 2009), demnach entsprechen die Ergebnisse dem heutigen Kenntnisstand. Das die Zahnoberfläche unter dem Einfluss mineralhaltiger Lösungen Mineralien aufnimmt, wurde auch in anderen Studien schon beobachtet, wie eine Übersichtsarbeit zeigt (Lussi et al., 2011). Dass für die Maaloxgruppe sogar ein Mineralgewinn verzeichnet werden konnte, lässt vermuten, dass durch den schnelleren Wiederanstieg des pH-Wertes die Wiedereinlagerung von Mineralien in den Schmelz schneller stattfand und somit der oberflächlich erweichte Schmelz nicht abradiert wurde (Tabelle 12) – vgl. Absatz 5.2.2. 5.3 Fazit Es konnte belegt werden, dass das Spülen mit Maalox 70 mVal nach Säureangriffen sowohl zu einer Verkürzung der Demineralisationsphase als auch zu einer Verbesserung der Remineralisation führt. Antazida sind in der Apotheke rezeptfrei erhältlich. Es besteht die Gefahr, dass Patienten mit Essstörungen bewusst Antazida einsetzen, um die Schädigung ihrer Zähne zu minimieren und somit ihre Erkrankung weiterhin verheimlichen zu können. Da dentale Erosionen als deutlichstes körperliches Merkmal gelten, sind Zahnärzte oft die ersten, die eine entsprechende Verdachtsdiagnose stellen können. Wird dieser Zeitpunkt durch die Eigentherapie dentaler Erosionen hinausgezögert, ist ein helfendes Eingreifen Außenstehender noch schwieriger. 50 Zusammenfassung 6. Zusammenfassung Der Verlust von Zahnhartsubstanz durch erosive Einflüsse ist eine Form der Zahnschädigung, die heute immer häufiger auftritt. Neben sauren Lebensmitteln und Getränken gilt chronisches Erbrechen als Hauptursache. Da bei letzterem meistens eine Grunderkrankung mit ausgeprägter psychischer Komponente vorliegt, erweist sich eine kausale Therapie in der Regel als langwierig und nicht in allen Fällen erfolgreich. Um das Voranschreiten des pathogenen Zahnhartsubstanzverlusts zu vermeiden, muss, zumindest übergangsweise, auf symptomatische Therapien zurück gegriffen werden. Antazida werden zur Behandlung von Refluxerkrankungen eingesetzt. Sie besitzen eine säureneutralisierende Wirkung und sind unter anderem in flüssiger Form erhältlich. Dies legte die Vermutung nah, dass ein Spülen der Mundhöhle mit Antazida nach dem Erbrechen zu einer schnelleren Säureneutralisation mit daraus folgender Verkürzung der Demineralisationsphase führt. Hauptbestandteil vieler Antazida sind Mineralien wie Kalzium und Phosphat. So wurde weiterhin vermutet, dass es außerdem zu einer Unterstützung der Remineralisation kommt. Zur Überprüfung dieser Thesen wurden Probanden angehalten mit Rinderschmelzproben bestückte Kunststoffschienen zu tragen. Zusätzlich wurde eine pH-Wert-Messsonde in die Schiene eingearbeitet. In zwei Versuchsreihen spülten die Probanden mit Sprite Zero zur Simulation eines Säureangriffs; nachfolgend in der ersten Versuchsreihe mit Wasser, in der zweiten mit Maalox 70 mVal. Zur Auswertung wurden neben dem pH-Wert die Mikrohärte und die transversale Mikroradiographie (TMR) herangezogen. Die Ergebnisse zeigen deutlich, dass Maalox 70 mVal die Demineralisationsphase verkürzt. Auch eine im Gegensatz zur Spülung mit Wasser verbesserte Remineralisation konnte nachgewiesen werden. Patienten, die unter chronischem Erbrechen leiden, kann empfohlen werden mit Maalox 70 mVal zu spülen, um die progressive Schädigung dentaler Hartsubstanz durch Magensäure zu minimieren. 51 Literaturverzeichnis 7. Literaturverzeichnis Addy M, Hunter ML (2003) Can tooth brushing damage your health? Effects on oral and dental tissues. Int Dent J 53 (Suppl 3): 177-186. Al-Malik MI, Holt RD, Bedi R (2002) Erosion, caries and rampant caries in preschool children in jeddah, saudi arabia. Community Dent Oral Epidemiol 30: 16-23. Amaechi BT, Higham SM, Edgar WM (1999) Factors influencing the development of dental erosion in vitro: enamel type, temperature and exposure time. J Oral Rehabil 26: 624 - 630. Amaechi BT, Higham SM, Edgar WM, Milosevic A (1999) Thickness of acquired salivary pellicle as a determinat of the sites of dental erosion. J Dent Res 78: 18211828. Angmar B, Carlstrom D, Glas JE (1963) Studies on the ultrastructure of dental enamel. IV. The mineralization of normal human enamel. J Ultrastruct Res 8: 12 - 23. Arends C (1969) Zahnkaries und Speichel. München: Hanser. Arends J, ten Bosch JJ (1992) Demineralization and remineralization evaluation techniques. J Dent Res 71: 924 - 928. Atkinson JC, Wu AJ (1994) Salivary gland dysfunction: causes, symptoms, treatment. J Am Dent Assoc 125: 409-416. Attin T (1999) Erosion und Abrasion von Zahnhartsubstanz - Einflußfaktoren, Pathogenese und Therapie. Dtsch Zahnärzte Kalender 58: 1-31. Attin T (2006) Methods for Assessment of Dental Erosion. Monogr Oral Sci 20: 152 172. Attin T (2009) What distinguishes erosiv hard tooth structure defects from dental caries? Prophylaxedialog 2009 (Spec Iss): 7-9. Attin T, Weiss K, Becker K, Buchalla W, Wiegand A (2005) Impact of modified acidic soft drinks on enamel erosion. Oral Dis 11: 7-12. Bailer U, de Zwaan M, Schussler P (2000) Diagnosis and therapy of eating disorders. Wien Klin Wochenschr 112: 865 - 875. 52 Literaturverzeichnis Barbour ME, Rees JS (2004) The laboratory assessment of enamel erosion: a review. J Dent 32: 591 - 602. Barlette D, Ganß C, Lussi A (2008) Basic erosive wear examination (BEWE). A new scoring system for scientific and clinical needs. Clin Oral Invest 12: 65-68. Bartlett D (2006) Intrinsic causes of erosion. Monogr Oral Sci 20: 119-139. Bartlett DW, Coward PY (2001) Comparison of the erosive potential of gastric juice and a carbonated drink in vitro. J Oral Rehabil 28: 1045-1047. Bartlett DW, Evans DF, Anggiansah A, Smith BGN (1996a) A study of the association between gastro-oesophageal reflux and palatal dental erosion. Br Dent J 181: 125131. Bartlett DW, Evans DF, Smith BGN (1996b) Review: the relationship between gastrooesophageal reflux disease and dental erosion. J Oral Rehabil 23: 289-297. Bassiouny MA (2008) Dental erosion linked to dysmenorrhea. Gen Dent 56: 719-726. Brand HS, Tjoe Fat GM, Veerman EC (2009) The effects of saliva on the erosive potential of three different wines. Aust Dent J 54: 228 - 232. Burgis E (2005) Intensivkurs - Allgemeine und sepzielle Pharmakologie, 3. Auflage. München: Urban und Fischer. Centerwall BS, Armstrong CW, Funkhouser LS, Elzay RP (1986) Erosion of dental enamel among competitive swimmers at a gas-chlorinated swimming pool. Am J Epidemiol 123: 641-647. Chandra A, Moazzez R, Bartlett D, Anggiansah A, Owen WJ (2004) A review of the atypical manifestations of gastroesophageal reflux disease. Int J Clin Pract 58: 41-48. Christensen CM, Navazesh M (1984) Anticipatory salivary flow to the sight of different foods. Appetite 5: 307-315. Coogan MM and Motlekar HB (1996) Salivary and plaque acids in caries active and caries free subjects. J Dent Assoc S Afr 51: 823-827. Critchley M (Hrsg.) (1980) Butterworth's Medical Dictionary. London: Butterworths. 53 Literaturverzeichnis Darby E (1892) Dental erosion and the gauthy diathesis: are they usually associated. Dent Cosmos 4: 629-640. Davidson CL, Boom G, Arends J (1973) Calcium distribution in human and bovine surface enamel. Caries Res 7: 349 - 359. Davidson CL, Hoekstra IS, Arends J (1974) Microhardness of sound, decalcified and etched tooth enamel related to the calcium content. Caries Res 8: 135 - 144. Davies R, Hunter L, Loyn T, Rees J (2008) Sour sweets: a new type of erosive challenge? Br Dent J 203: 1-4. De Menezes Oliveira MA, Torres CP, Gomes-Silva JM, Chinelatti MA, De Menezes FC, Palma-Dibb RG, Borsatto MC (2010) Microstructure and mineral composition of dental enamel of permanent and deciduous teeth. Microsc Res Tech 73: 572-577. Dreizen S, Brown LR, Daly TE, Drane JB (1977) Prevention of xerostomia-related dental caries in irradiated cancer patients. J Dent Res 56: 99-104. Eccles JD (1979) Dental erosion of nonindustrial origin. A clinical survey and classification. J Prosthet Dent 42: 649-653. Edgar WM (1992) Saliva: Its secretion, composition and functions. Br Dent J 172: 305 -312. Edwards M, Ashwood RA, Littlewood SJ, Brocklebank LM, Fung DE (1998) A videofluoroscopic comparison of straw an dcup drinking: the potential influence on dental erosion. Br Dent J 185: 244-249. El Karim IA, Sanhouri NM, Hashim NT, Ziada HM (2007) Dental erosion among 1214 year old school children in Khartoum: a pilot study. Community Dent Health 24: 176-180. Engelen L, de Wijk RA, Prinz JF, van der Bilt A, Bosman F (2003) The relation between saliva flow after different stimulations and the perception of flavor and texture attributes in custard desserts. Physiol Behav 78:165-169. Fairburn CG, Cooper PJ (1984) The clinical features of bulimia nervosa. Br J Psychiatry 144: 238-246. 54 Literaturverzeichnis Fares J, Shirodaria S, Chiu K, Ahamd N, Sherriff M, Bartlett D (2009) A new index of tooth wear. Reproducibility and application to a sample of 18-30-year-old university students. Caries Res 43: 119-125. Featherstone JDB, ten Cate JM, Shariati M, Arends J (1983) Comparison of artificial caries-like lesions by quantitative microradiography and microhardness profiles. Caries Res 17: 385 - 391. Featherstone JDB, Lussi A (2006) Understanding the Chemistry of Dental Erosion. Monogr Oral Sci 20: 66-76. Gallien GS, Kaplan I, Owens BM (1994) A review of non-carious dental cervical lesions. Compend Educ Dent 15: 1366-1372. Gandara BK, Truelove EL (1999) Diagnosis and management of dental erosion. J Contemp Dent Pract 1: 16-23. Ganss C, Klimek J, Brune V, Schürmann A (2004a) Effects of two fluoridation measures on erosion progression in human enamel and dentine in situ. Caries Res 38: 561-566. Ganss C, Klimek J, Giese K (2001) Dental erosion in children and adolescents - a cross-sectional and longitudinal investigation using study models. Community Dent Oral Epidemiol 29: 264-271. Ganss C, Klimek J, Starck C (2004b) Quantitative analysis of the impact of the organic matrix on the fluoride effect on erosion progression in human dentine using longitudinal microradiography. Arch Oral Biol 49: 931-935. Ganss C, Neutard L, van Hinckeldey J, Klimek J, Schlueter N (2010a) Wirksamkeit der elmex EROSIONSSCHUTZ Zahnspülung gegen erosiv bedingte Verluste von Zahnschmelz und Dentin in situ. J Dent Res, online doi 10.1177/0022034510375291. Ganss C, Neutard L, von Hinckeldey J, Klimek J, Schlueter N (2010b) Efficacy of a Tin/Fluoride Rinse: a randomized in situ trail an erosion. J Dent Res, online doi 10.1177/0022034510375291. Ganss C, Schlechtriemen M, Klimek J (1999) Dental erosion in subjects living on a raw food diet. Caries Res 33: 74-80. 55 Literaturverzeichnis Ganss C, Schlüter N (2010) Erosionen der Zahnhartsubstanzen - Prävention und Therapie. Quintessenz 61: 1203-1210. Ganss C, Schlüter N, Hardt M, Schattenberg P, Klimek J (2008) Effect of fluoride compounds on enamel erosion in vitro: a comparison of amine, sodium and stannous fluoride. Caries Res 42: 2-7. Garg AK, Malo M (1997) Manifestations and treatment of xerostomia and associated oral effects secondary to head and neck radiation therapy. J Am Dent Assoc 128: 1128-1133. Gedalia I, Ionat-Bendat D, Ben-Mosheh S, Shapira L (1991) Tooth enamel softening with a cola type drink and rehardening with hard cheese or stimulated saliva in situ. J Oral Rehabil 18: 501-506. Gerlinghoff M, Backmund H (2004) Essstörungen im Kindes- und Jugendalter. Anorexia nervosa, Bulimia nervosa, Binge Eating Disorder. Bundesgesundheitsblatt Gesundheitsforschung Gesundheitsschutz 47: 246 - 250. Geurtsen W (2000) Rapid general dental erosion by gas-chlorinated swimming pool water. Review of the literature and case report. Am J Dent 13: 291-293. Giunta JL (1983) Dental erosion resulting from chewable vitamin C tablets. J Am Dent Assoc 107: 253-256. Grau Carbó J, López Jiménez J, Giménez Prats MJ, Sànchez Molins M (2007) Cornelia de Lange syndrome: a case report. Med Oral Patol Oral Cir Bucal 12: 445448. Gregg T, Mace S, West NX, Addy M (2004) A study in vitro of the abrasive effect of the tongue on enamel and dentine softened by acid erosion. Caries Res 38: 557-560. Grenby TH (1996) Lessening dental erosive potential by product modification. Eur J Oral Sci 104. 221 - 228. Grobler SR, Senekal PJ, Kotze TJ (1989) The degree of enamel erosion by five different kinds of fruit. Clin Prev Dent 11: 23-28. Hannig M (1999) Ultrastructural investigation of pellicle morphogenesis at two different intraoral sites during a 24-h period. Clin Oral Investig 3: 88-95. 56 Literaturverzeichnis Hara AT, Ando M, Cury JA, Serra MC, Gonzalez-Cabezas C, Zero DT (2005) Influence of the organic matrix on root dentine erosion by citric acid. Caries Res 39: 134-138. Hara AT, Lussi A, Zero DT (2006) Biological factors. Monogr Oral Sci 20: 88-99. Harding MA, Whelton H, O'Mullane DM, Cronin M (2003) Dental erosion in 5-year-old Irish school children and associated factors: a pilot study. Community Dent Health 20: 165 - 170. Hazelton LR, Faine MP (1996) Diagnosis and Dental Management of Eating Disorder Patients. Int J Prosthodont 9: 65 - 73. Heaton AM (1962) Sjogren's syndrome. Proc R Soc Med 55: 479-480. Hellwig E, Klimek J, Attin T (2009) Einführung in die Zahnerhaltung. 5. Auflage. Köln: Deutscher Zahnärzte Verlag. Hellwig E, Lussi A (2006) Oral hygiene products and acidic medicines. Monogr Oral Sci 20: 112-118. Hemingway CA, White AJ, Shellis RP, Addy M, Parker DM, Barbour ME (2010) Enamel erosion in dietary acids: inhibition by food proteins in vitro. Caries Res 44: 525-530. Hirsch DP, Mathus-Vliegen EM, Dagli U, Tytgat GN, Boeckxstaens GE (2003) Effect of prolonged gastric distention on lower esophageal sphincter function and gastroesophageal reflux. Am J Gastroenterol 98: 1696-1704. Hoek HW (2006) Incudence,prevalence and mortality of anorexia nervosa and other eating disorders. Curr Opin Psychiatry 19: 389 - 394. Hoek HW, van Hoeken D (2003) Review of the prevalence and incidence of eating disorders. Int J Disord 34: 383-396. Hooper S, Hughes J, Parker D, Finke M, Newcombe RG, Addy M, West N (2007) A clinical study in situ to assess the effect of a food approved polymer on the erosion potential of drinks. J Dent 35: 541 - 546. 57 Literaturverzeichnis Hove LH, Holme B, Young A, Tveit AB (2007) The erosion-inhibiting effect of TiF4, SnF2 and NaF solutions on pellicle-covered enamel in vitro. Acta Odontol Scand 65: 259 - 264. Hove LH, Holme B, Young A, Tveit AB (2008) The protective effect of TiF4, SnF2 and NaF against erosion-like lesions in situ. Caries Res 42: 68-72. Hsu LKG (1983) The aetiology of anorexia nervosa. Psychol Med 13: 231-238. Hsu LKG (1986) The treatment of anorexia nervosa. Am J Psychiatry 143: 573-581. Hughes JA, West NX, Parker DM, von den Braak MH, Addy M (2000) Effects of pH and concentration of citric, malic and lactic acids on enamel, in vitro. J Dent 28. 147152 Imfeld C, Imfeld T (2005a) Essstörungen (I): Allgemeinmedizinische-psychatrische Aspekte. Schweiz Monatsschr Zahnmed 115: 1157 - 1162. Imfeld C, Imfeld T (2005b) Essstörungen (II): Zahnmedizinische Aspekte. Schweiz Monatsschr Zahnmed 115: 1163 - 1171. Imfeld T (1996) Dental erosion. Definition, classification and links. Eur J Oral Sci 104: 151-155. Jaeggi T, Lussi A (1999) Toothbrush abrasion of erosively altered enamel after intraoral exposure to saliva: an in situ study. Caries Res 33: 455-461. Jaeggi T, Lussi A (2004) Erosionen bei Kindern im frühen Schulalter. Schweiz Monatsschr Zahnmed 114: 876-881. Jaeggi T, Schaffner M, Bürgin W, Lussi A (1999) Erosionen und keilförmige Defekte bei Rekruten der Schweizer Armee. Schweiz Monatsschr Zahnmed 109: 1171-1178. Järvinen V, Rytömaa I, Meurman JH (1992) Location of dental erosion in a referred population. Caries Res 26: 391-396. Jensdottir T, Buchwald C, Nauntofte B, Hansen HS, Bardow A (2010) Erosive potential of calcium-modified acidic candies in irradiated dry mouth patients. Oral Health Prev Dent 8: 173-178. Johansson Ak, Johansson A, Birkhed D, Omar R, Baghdadi S, Carlsson GE (1996) Dental erosion, soft-drink intake and oral health in young Saudi men, and the 58 Literaturverzeichnis development of a system for assessing erosive anterior tooth wear. Acta Odontol Scand 54: 369-378. Johansson AK, Lingström P, Imfeld T, Birkhed D (2004) Influence of drinking method on tooth-surface pH in relation to dental erosion. Eur J Oral Sci 112: 484-489. Kaidonis JA, Townsend GC, Richards LC (1992) Abrasion: an evolutionary and clinical view. Aust Prosthet J 6: 9-16. Karow T, Lang-Roth R. (2011). Allgemeine und spezielle Pharmakologie und Toxikologie, 19. Auflage. Kassan SS, Moutsopoulos HM (2004) Clinical manifestations and early diagnosis of Sjögren syndrome. Arch Intern Med 164: 1275 – 1284. Kato MT, Magalhães AC, Rios D, Hannas AR, Attin T, Buzalaf MA (2009) Protective effect of green tea on dentin erosion and abrasion. J Appl Oral Sci 17: 560-564. Kazoullis S, Seow WK, Holcombe T, Newman B, Ford D (2007) Commen dental conditions associated with dental erosion in schoolchildren in Australia. Pediatr Dent 29: 33-39. Kennedy T, Jones R (2000) The prevalence of gastro-oesophageal reflux symptoms in a UK population and the consulation behaviour of patients with these symptoms. Aliment Pharmacol Ther 14: 1589-1594. Keyes PH (1962) Recent Advances in Dental Caries Researche, Bacteriology. Bacteriological Findings and Biological Implications. Ind Dent J 12: 443-464. Kirkham J, Robinson C, Strong M, Shore RC (1994) Effects of frequency and duration of acid exposure on demineralization/remineralization behaviour of human enamel in vitro. Caries Res 28: 9 - 13. Kitchen LI, Castell DO (1991) Rational and efficacy of conservative therapy for gastroesophageal reflux disease. Arch Intern Med 151: 448-454. König KG (1971) Karies und Kariesprophylaxe, 2. Auflage. München: W. Goldmann Verlag. Künzel W, Cruz MS, Fischer T (2000) Dental erosion in Cuban children associated with excessive consumption of oranges. Eur J Oral Sci 108: 104-109. 59 Literaturverzeichnis Laheij AM, van Strijp AJ, van Loveren C (2010) In situ remineralisation of enamel and dentin after the use of an amine fluoride mouthrinse in addition to twice daily brushings with amine fluoride toothpaste. Caries Res 44: 260 - 266. Larsen MJ, Poulsen S, Hansen I (2005) Erosion of the teeth: prevalence and distribution in a group of Danish school children. Eur J Paediatr Dent 6: 44-47. Lazarchik DA, Filler SJ (2000) Dental erosion: predominant oral lesion in gastroesophageal reflux disease. Am J Gastroenterol 95 (8 Suppl): S33-38. Leitzmann C, Müller C, Michel P, Brehme U, Triebel T, Hahn A, Laube H (2009) Ernährung in Prävention und Therapie - Ein Lehrbuch, 3. Auflage. Suttgart: Hippokrates Verlag. Lendenmann U, Grogan J, Oppenheim FG (2002) Saliva and dental pellicel: a review. Adv Dent Res 14: 22-28. Lifante-Oliva C, López-Jornet P, Camacho-Alonso F, Esteve-Salinas J (2008) Study of oral changes in patients with eating disorders. Int J Dent Hygiene 6: 119- 122. Llena-Puy C (2006) The role of saliva in maintaining oral health and as an aid to diagnosis. Med Oral Patol Oral Cir Bucal 11: E449-455. Lüllmann H, Mohr K, Hein L (2010) Pharmakologie und Toxikologie, 17. Auflage. Stuttgart: Thieme. Luo Y, Zeng XJ, Du MQ, Bedi R (2005) The prevalence of dental erosion in preschool children in China. J Dent 33: 115-21. Lussi A, Hellwig E, Zero D, Jaeggi Th (2006) Erosive tooth wear: diagnosis, risk factors and prevention. Am J Dent 19: 319-325. Lussi A, Jaeggi T (2001) The erosiv potential of various oral care products compared to foodstuffs and beverages. Schweiz Monatsschr Zahnmed 111: 274-281. Lussi A, Jaeggie T (2006) Chemical Factors. Monogr Oral Sci 20: 77-87. Lussi A, Jaeggi T (2008) Erosion - diagnosis and risk factors. Clin Oral Invest 12 (Suppl1): 5-13. 60 Literaturverzeichnis Lussi A, Jaeggi T (2009) Dentale Erosionen - Von der Diagnose zurTherapie . Berlin: Quintessenzverlag. Lussi A, Schaffner M, Hotz P, Suter P (1991) Dental erosion in a population of swissadults. Community Dent Oral Epidemiol 19: 286-290. Lussi A, Schlueter N, Rakhmatullina E, Ganss C (2011) Dental Erosion - An Overview with Emphasis on chemical and histopathological Aspects. Caries Res 45 (Suppl 1): 2-12. Magalhães AC, Wiegand A, Rios D, Hannas A, Attin T, Buzalaf MA (2009) Chlorhexidine and green tea extract reduce dentin erosion and abrasion in situ. J Dent 37: 994-998. Mericske-Stern R (2007) Das Abrasionsgebiss bei älteren Menschen - Diagnostik und Strategien. Quintessenz 58: 729-737. Meurman JH, Frank RM (1991) Progression and surface ultrastructure of in vitro caused erosive lesions in human and bovine enamel. Caries Res 25: 81-87. Meurman JH, Kuittinen T, Kangas M, Tuisku T (1988) Buffering effect of antacids in the mouth - a new treatment of dental erosion? Scand J Dent Res 96: 412 - 417. Meurman JH, Ten Cate JM (1996) Pathogenesis and modifying factors of dental erosion. Eur J Oral Sci 199-204. Meyer-Lueckel H, Tschoppe P, Kielbassa AM (2006) Effect of various Ca2+/PO4(3-) concentrations of linseed-based saliva substitutes on enamel in vitro. J Oral Rehabil 33: 760-766. Miller W (1907) Experiments and observations an the wasting of tooth tissue variously. Dent Cosmos 49: 1-25. Miller WD (1899) Die Mikroorganismen der Mundhöhle. Leipzig: Thieme Verlag. Millward A, Shaw L, Harrington E, Smith AJ (1997) Continuous monotoring of salivary flow rate and pH at the surface of the dentition following consumption of acidic beverages. Caries Res 31: 44-49. Millward A, Shaw L, Smith A (1994) Dental erosion in four-year-old children from differing socioeconomic backgrounds. ASDC J Dent Child 61: 263-266. 61 Literaturverzeichnis Milosevic A, Brodie DA, Slade PD (1997) Dental Erosion, oral Hygiene and nutrition in eating disorders. Int J Eat Disord 21: 195 - 199. Milosevic A, Young PJ, Lennon MA (1994) The prevalence of tooth wear in 14-yearold school children in Liverpool. Community Dent Health 11: 83-86. Mok TB, McIntyre J, Hunt D (2001) Dental erosion: In vitro model of wine assessor’s erosion. Australian Dental Journal 46: 263-268. Murrell S, Marshall TA, Moynihan PJ, Qian F, Wefel JS (2010) Comparison of in vitro erosion potentials between beverages available in the United Kingdom and the United States. J Dent 38: 284 - 289. Mutschler E, Geisslinger G, Kroemer HK, Ruth P, Schäfer-Korting M (2008) Mutschler Arzneimittelwirkungen - Lehrbuch der Pharmakologie und Toxikologie, 9. Auflage. Stuttgart: Wissenschaftliche Verlagsgesellschaft mbH Stuttgart. Nakash-Eisikovits O, Dierberger A, Westen D (2002) A multidimensional metaanalysis of pharmacotherapy for bulimia nervosa: summarizing the range of outcomes in controlled clinical trials. Harv Rev Psychiatry 10: 193 - 211. Noack MJ (1989) Erosions of hard tooth substance. Dtsch Zahnarztl Z 44: 517-520. Nunn JH (1996) Prevalence of dental erosion and the implications for oral health. Eur J Oral Sci 104: 156-161. Ogata M, Harada N, Yamaguchi S, Nakajima M, Pereira PN, Tagami J (2001) Effects of different burs on dentin bond strengths of self-etching primer bonding systems. Oper Dent 26: 375-382. Orr WC, Robinson MG, Johnson LF (1981) Acid clearance during sleep in the pathogenesis of reflux esophagitis. Dig Dis Sci 26: 423-427. Packer CD (2009) Cola-induced hypokalaemia: a super-sized problem. Int J Clin Pract 63: 833 - 835. Parry J, Shaw L, Arnaud MJ, Smith AJ (2001) Investigation of mineral waters and soft drinks in realation to dental erosion. J Oral Rehabil 28: 766 - 772. Pearce JM (2004) Richard Morton: origins of anorexia nervosa. Eur Neurol 52: 191192. 62 Literaturverzeichnis Petersen PE, Gormsen C (1991) Oral conditions among German battery factory workers. Community Dent Oral Epidemiol 19: 104-106. Phelan J, Rees J (2003) The erosiv potential of some herbal teas. J Dent 31: S. 241246. Pontefract H, Hughes J, Kemp K, Yates R, Newcombe RG, Addy M (2001) The erosive effects of some mouthrinses on enamel. A study in situ. J Clin Periodontol 28: 319-324. Reichel FX, Mohr K, Hein L, Hickel R (2007) Taschenatlas der Pharmakologie und Toxikologie für Zahnmediziner. Stuttgart: Georg Thieme Verlag KG. Ribeiro CC, Gibson I, Barbosa MA (2006) The uptake of titanium ions by hydroxyapatite particles-structural changes and possible mechanisms. Biomaterials 27: 1749-1761. Robb BG, Smith ND (1989) Dental erosion in patients with chronic alcoholism. J Dent 17: 219-212. Robb ND, Smith BG (1996) Anorexia and bulimia nervosa (the eating disorders): conditions of interest to the dental practitioner. J Dent 24: 7-16. Roberts MW, Li SH (1987) Oral findings in anorexia nervosa and bulimia nervosa: a study of 47 cases. J Am Dent Assoc 115: 407 - 410. Rogalla K, Finger W, Hannig M (1992) Influence of buffered and unbuffered acetylsalicylic acid on dental enamel and dentine in human teeth: an in vitro pilot study. Methods Find Exp Clin Pharmacol 14: 339-346. Rytömaa I, Meurman JH, Franssila S, Torkko H (1989) Oral hygiene products may cause dental erosion. Proc Finn Dent Soc 85: 161-166. Scheper WA, van Nieuw Amerongen A, Eijkman MA (2005) Oral conditoins in swimmers. Ned Tijschr Tandheelkd 112: 147-148. Schiffner U, Micheelis W, Reich E (2002) Erosionen und keilförmige Zahnhalsdefekte bei deutschen Erwachsenen und Senioren. Dtsch Zahnärztl Z 57: 102-106. 63 Literaturverzeichnis Schindelbeck NE (1987) Optimal thresholde, sensitivity, and specificity of longterm pH-metry for the detection of gastroesophageal reflux disease. Gastroenterology 93: 85-90. Schlueter N, Duran A, Klimek J, Ganss C (2009) Investigation of the effect of various fluoride compundes and preparations thereof on erosive tissue loss in enamel in vitro. Caries Res 43: 10 16. Schlueter N, Ganss C, Mueller U, Klimek J (2007) Effect of titanium tetrafluoride and sodium fluoride on erosion progression in enamel and dentine in vitro. Caries Res 41: 141 - 145. Schlueter N, Klimek J, Ganss C (2009) Effect of stanous and fluoride concentration in a mouth rinse on erosive tissue loss in enamel in vitro. Arch Oral Biol 54: 432 - 436. Hove LH, Holme B, Young A, Tveit AB (2008) The protective effect of TiF4, SnF2 and NaF against erosion-like lesions in situ. Caries Res 42: 68-72. Schmidt U, Treasure J (1997) Eating Disorders an the Dental Practitioner. Eur J Prosthodont Rest Dent 5: 161 - 167. Schroeder PL, Filler SR, Ramirez B, Lazarchik DA, Vaezi MF, Richter JE (1995) Dental erosion and acid reflux disease. Ann Intern Med 122: 809-815. Schumacher GH (1997) Anatomie für Zahnmediziner. 3. Auflage. Heidelberg: Hüthig GmbH. Schweizer-Hirt CM, Schait A, Schmid R, Imfeld T, Lutz F, Mühlemann HR (1978) Abrasion des Schmelzes: Eine experimentelle Studie. Schweiz Mschr Zahnheilk 88: 497-529. Skjørland KK, Rykke M, Sønju T (1995) Rate of pellicle formation in vivo. Acta Odontol Scand 53: 358-62. Sognnaes RF, Wolclott RB, Xhonga FA (1972) Dental erosion. I. Erosion-like patterns occuring in association with other dental conditions. J Am Dent Assoc 84: 571-576. 64 Literaturverzeichnis Stephen K, McCrossan J, Mackenzie D, Macfarlane CB, Spieres CF (1980) Factors determining the passage of drugs from blood into saliva. Br Dent Clin Pharmacol 9: 51-55. Sundaram G, Wilson R, Watson TF, Bartlett DW (2007) Effect of resin coating on dentine compared to repeated topical applications of fluoride mouthwash after an abrasion and erosion wear regime. J Dent 35: 814-818. Tay FR, Pashley DH (2004) Resin bonding to cervical sclerotic dentin: a review. J Dent 32: 173-196. Ten Bruggen Cate HJ (1968) Dental Erosion in Industry. Br J Ind Med 25: 249-266. Ten Cate JM, Imfeld T (1996) Dental erosion, summary. Eur J Oral Sci 104: 241-244. Tezel H, Ergücü Z, Onal B (2002) Effects of topical fluoride agents on artificial enamel lesion formation in vitro. Quintessence Int 33: 347-352. Turner CG, Machado LM (1983) A new dental wear pattern and evidence for high carbohydrate consumption in a brazilian archaic skeletal population. Am J Phys Anthropol 61: 125-130. Vitale GC, Cheadle WG, Patel B, Sadek SA (1987) The effect of alcohol on nocturnal gastoresophageal reflux. JAMA 258: 2077-2079. Wegehaupt F, Gries D, Wiegand A, Attin T (2008) Is bovine dentine an appropriate substitute for human dentine in erosion/abrasion tests? J Oral Rehabil 35: 390 - 394. Wegehaupt F, Schneiders V, Wiegand A, Schmidlin PR, Attin T (2009) Influence of two different fluoride compounds and the acquired pellicle on the amount of formed KOH-soluble fluoride and its retention after tooth brushing. Acta Odontol Scand 67: 355 - 259. Wehling M Hrsg (2005) Klinische Pharmakologie. Suttgart: Georg Thieme Verlag KG. West NX, Davies M, Amaechi BT (2011) In vitro and in situ Erosions Models for Evaluating Tooth Substance Loss. Caries Res 45 (suppl): 43 - 52. West NX, Hughes JA, Addy M (2000) Erosion of dentine and enamel in vitro by dietary acids: the effect of temperature, acid character, concentration and exposure time. J Oral Rehabil 27: 875 - 880. 65 Literaturverzeichnis White I, McIntyre J, Logan R (2001) Studies on dental erosion: an in vitro model of root surface erosion. Aust Dent J 46: 203-207. Whitford GM (1992) Acute and chronic fluoride toxicity. J Dent Res 71: 1249 - 1254. Whittaker DK (1982) Structural variations in the surface zone of human tooth enamel observed by scanning electron microscopy. Arch Oral Biol 27: 383 - 392. Wiegand A, Attin T (2011) Design of Erosion/Abrasion Studies - Insights and Rational Cancepts. Caries Res 45 (suppl): 53 - 59. Wiegand A, Bichsel D, Magalhaes AC, Becker K, Attin T (2009) Effect of sodium, amine and stannous fluoride at the same concentration and different pH on in vitro erosion. J Dent 37: 591- 595. Wiegand A, Magalhaes AC, Sener B, Waldheim E, Attin T (2009a) TiF4 and NaF at pH 1.2 but not at pH 3.5 are able to reduce dentin erosion. Arch Oral Biol 54: 790 795. Wiegand A, Waldheim E, Sener B, Magalhaes AC, Attin T (2009b) Comparison of the effects of TiF4 and NaF solutions at pH 1.2 and 3.5 on enamel erosion in vitro. Caries Res 43: 269 - 277. Wiegand A, Müller I, Schnapp JD, Werner C, Attin T (2008) Impact of fluoride, milk and water rinsing on surface rehardening of acid softened enamel. An in situ study. Am J Dent 21: 113-118. Wiegand A, Müller J, Wernd, Attin T (2006) Prevalence of erosive tooth wear and associated risk factors in 2-7-year-old German kindergarten children. Oral Diseases 12: 117-124. Williams JL (1897) A contribution to the study of pathology of enamel. Dent Cosmos 39: 269-353. Worlitschek M (2008) Praxis des Säure-Basen-Haushalts - Grundlagen und Therapie, 6. Auflage. Stuttgart: Karl F. Haug Verlag. Wynn RL, Meiller TF (2001) Drugs and dry mouth. Gen Dent 49: 10-14. Xhonga FA, Valdmanis S (1983) Geographic comparisons of the incidence of dental erosion: a two centre study. J Oral Rehabil 10: 269-277. 66 Literaturverzeichnis Yeh CK, Johnson DA, Dodds MW, Sakai S, Rugh JD, Hatch JP (2000) Association os salivary flow rates with maximal bite force. J Dent Res 79: 1560-1565. Yip HK, Smales RJ, Kaidonis JA (2002) Management of tooth tissue loss from erosion. Quintessence Int 33: 516-520. Young A, Tenuta LMA (2011) Initial Erosion Models. Caries Res 45 (Suppl 1): 33-42. Young A, Thrane PS, Saxegaard E, Jonski G, Rölla G (2006) Effect of stannous fluoride toothpaste on erosion-like lesions: an in vivo study. Eur J Oral Sci 114: 180 183. Zero DT (1996) Etiology of dental erosion-extrinsic factors. Eur J Oral Sci 104: 162177. Zero DT, Lussi A (2005) Erosion - chemical and biological factors of importance to the dental practitioner. Int Dent J 55: 285-290. Zero DT, Lussi A (2006) Behavorial factors. Monogr Oral Sci 20: 100-105. Zipkin J, McClure FJ (1949) Salivary citrate and dental erosion. J Dent Res 28: 613626. 67 Danksagung 8. Danksagung Ich danke Herrn Prof. Dr. Elmar Hellwig für die Überlassung des Themas und Herrn PD Dr. Markus Altenburger für die Betreuung während der letzten Jahre sowie Herrn Prof. Dr. Dr. Rainer Schmelzeisen für die Übernahme des Zweitgutachtens. Des Weiteren danke ich Herrn Dr. Norbert Dreyer so wie Herrn Dr. Frank Hettenhausen für die Motivation und die Korrekturen. 68