1 recherchierte Dokumente
Werbung

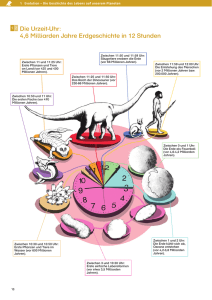
.. WISSENSCHAFT Evolution START IN DER URSUPPE Wie und wann entstand Leben auf der Erde? Was waren die Urbausteine des Lebendigen, und wie wurden sie zu belebter Materie? Molekularbiologen haben begonnen, die Chemie der Urzeugung und die ersten Schritte der Evolution im Labor zu ergründen. Von den Ergebnissen könnte auch die Medizin profitieren. AKG 400 Jahrmillionen habe demnach die Entwicklung der kleinen Wunderwerke gedauert – vielleicht, so mutmaßt der Molekularbiologe vom Howard Hughes Medical Institute in Boulder (Colorado) sei die Evolution der Einzeller noch viel schneller abgelaufen. „Nur 10 Millionen Jahre“, schätzt US-Chemiker Stanley Miller, habe es gedauert vom „Anfang in der präbiotischen Ursuppe bis zu den Vorläufern der Cyanobakterien“, deren versteinerte Überreste in den 3,5 Milliarden Jahre alten Sedimenten in Australien aufgefunden wurden. „Alle chemischen Prozesse, die wir kennen“, doziert der Forschungspionier, „sind schnell“; auch der Vorgang der Urzeugung, meint der Chemieprofessor von der University of California in San Diego, sei im Eiltempo vonstatten gegangen. Nur allmählich bringen die Experten Licht in den dunklen Ursprung des Lebendigen, aus dem die ganze Formenvielfalt von Fauna und Flora hervorgegangen ist. Seit kurzem kommen vor allem aus amerikanischen Forschungslabors in immer schnellerer Folge neue Forschungsresultate, die anzeigen, wie die ersten Biomoleküle entstanden sein könnten und wie sich die ersten lebenden Zellen geformt haben. Mit ausgeklügelten molekularbiologischen Verfahren simulieren amerikanische, aber auch deutsche Forscher derzeit die präbiotische Evolution der ersten Biomoleküle – jenen Prozeß, in dessen Verlauf sich die Bausteine des Lebens zusammenfügten. In ihren Reagenzgläsern wollen die Forscher die Entstehung des Lebens gleichsam im Zeitraffer wiederholen. Im Mittelpunkt dieses Forschungsvorhabens steht eine Klasse von Molekülen, die gleichsam den Motor aller Lebensvorgänge darstellen – die Ribonukleinsäuren (RNS). Bei diesen Schlüsselsubstanzen handelt es sich um die Kopien von Erbinformationen, die Schöpfungsdarstellung: Myriaden von Einzellern wimmelten in den Weltmeeren tockfinster war es, als die Erde geboren wurde. Kein Lichtstrahl durchdrang die dichte Wolke aus Gas und kosmischem Staub, die in rasender Geschwindigkeit um die Sonne rotierte. Tief im Inneren dieses Mahlstroms nahm die Erde vor gut viereinhalb Milliarden Jahren ihre kugelförmige Gestalt an – eine wüste, von mächtigen Vulkanausbrüchen gebeutelte Welt, auf die ein pausenloser Hagel von Gesteinstrümmern niederging. Einige hundert Millionen Jahre kreiste der Planet, gehüllt in heiße Dämpfe, durch die Dunkelheit. Dann begann sich das Chaos zu lichten. Über der Erde ging die Sonne auf. Sie beleuchtete einen Planeten, der kahl und keimfrei seine Bahn zog. Nichts Lebendiges rührte sich in seiner von Dauergewittern durchtosten Atmo- S 156 DER SPIEGEL 26/1995 sphäre. Erst Jahrmillionen später entfaltete sich Leben in den irdischen Urmeeren: Myriaden von Einzellern, womöglich Vorfahren der heutigen Blaualgen, wimmelten in den trüben Gewässern. Wie lange lag der Schöpfungstag, das Datum der Urzeugung, damals schon zurück? Welche chemischen Reaktionen spielten sich in der „Ursuppe“ des Planeten ab, als aus toter Materie Leben entstand und die Evolution in Gang kam? Schon vor 3,5 Milliarden Jahren, soviel ergibt sich aus dem Alter von Fossilienfunden in Australien und Afrika, hatte die Natur die ersten Zellen hervorgebracht – in den urigen Mikroorganismen gab es bereits ein komplexes Zusammenspiel von Erbmolekülen, Stoffwechselkreisläufen und Enzymen. „Wirklich erstaunlich“ findet das der US-Forscher Thomas Cech: Höchstens K. ABBOTT / UNIVERSITY OF COLORADO .. Evolutionsforscher Cech Dilemma von Henne und Ei wir, daß Ribonukleinsäuren beides sein können: Gen und Enzym.“ Seit der Entdeckung von Cech und Altman, die dafür 1989 den Chemie-Nobelpreis erhielten, arbeiten die Evolutionsforscher an einem Szenario der Schöpfung. Als Ausgangspunkt dient ihnen noch immer ein simples Experiment aus dem Jahr 1952, mit dem der Chemiestudent Stanley Miller damals weltweites Aufsehen erregte. Millers Lehrer, der Nobelpreisträger Harold Urey aus Chicago, pflegte seine Schüler in der Chemievorlesung mit einem Exkurs über den Ursprung des Lebens zu traktieren. Student Miller beschloß, die Theorie des Professors im Labor zu überprüfen. Der Chemiker, damals 22, mischte aus Ammoniak, Wasserdampf, Methan und Wasserstoff jene Uratmosphäre, in der nach Ureys Vorstellung vor rund vier Milliarden Jahren das Leben auf der Erde seinen Anfang genommen hat. Sodann setzte er zwei Elektroden in der Mixtur unter Strom und ließ das Gebräu einige Tage köcheln. „Irgendwann im Oktober oder November 1952“, erinnert sich Miller, „hat es funktioniert.“ In seiner Versuchsapparatur waren gleichsam über Nacht Aminosäuren und einige andere Biomoleküle entstanden, die allen Lebewesen als Grundbausteine für Proteine oder als Zwischenprodukte im Stoffwechsel dienen. Nach den Vorstellungen der Evolutionsforscher entstanden aus Purinen und ihren chemischen Verwandten, den Pyrimidinen, zunächst jene vier Bausteine der Nukleinsäuren, die im verschlüsselten Text der Erbinformation als Buchstaben dienen. Aus diesen vier Bausteinen, vermuten die Forscher, entstanden die ersten RNS-Kettenmoleküle. Manche dieser archaischen Genschnipsel besaßen enzymartige Fähigkeiten und begannen, sich selbst zu vervielfältigen – womöglich, im Gencode, der strickleiterförmigen DNS im Zellkern, gespeichert sind. Die RNS-Matrizen dienen in den Zellen als Konstruktionspläne für den Aufbau von Proteinen; zu ihnen zählen auch die Enzyme, die vielerlei Stoffwechselvorgänge vorantreiben und steuern. Auch bei der Herstellung von RNSKopien wirken Enzyme mit – für die Evolutionsforscher, so der US-Biochemiker Thomas Cech, ein „Henne-Ei-Dilemma“: Was war in der molekularen Entwicklung des Lebens zuerst da, die RNS oder das Enzym, das nach dem RNS-Plan aufgebaut wird? Die Rätselfrage blieb für die Gelehrten zunächst unlösbar: Offensichtlich waren alle Lebensformen von Beginn an auf beides angewiesen – auf die RNS-Informationsträger und die für sie zuständigen Enzyme. „Wie konnte das Leben starten ohne RNS-Molekül, das die Information für das Enzym bereithält?“ fragte Erbmoleküle gegen Krebs sich Cech. Tumor-Behandlung mit Ribozymen 1982 fand der Gelehrte eine Antwort. Er entdeckte, 1 daß RNS-Moleküle in der Schädliche Chemie des Lebens eine Boten-RNS Doppelrolle spielen können: In dem Einzeller Tetrahymena hatte er ein sogenanntes Zellkern RibozymRibozym aufgespürt – Teil eiMoleküle 2 nes RNS-Moleküls, das zugleich die Eigenschaften eiRetorten-Gen nes Enzyms besaß. Wenig später fand Cechs Kollege 1 Ribozym-Moleküle werden in Sidney Altman ein weiteres die kranke Zelle eingeschleust natürliches Ribozym im 2 oder von zuvor eingesetzten ReDarmbakterium Escherichia torten-Genen im Zellkern produziert. coli. Cech: „Seither wissen meint der US-Astrophysiker Carl Sagan, „war ein solches, sich selbst nachbildendes, katalytisches RNS-Molekül das erste lebendige Ding in den alten Ozeanen vor etwa vier Milliarden Jahren“. In mehreren Labors arbeiten derzeit amerikanische Moleküldesigner am Nachbau von Urwelt-Ribozymen. Sie lassen dabei die Gesetze von Mutation und Auslese walten. In automatisierten Genretorten komponieren sie aus den Genbausteinen, den Nukleotiden, nach dem Zufallsprinzip RNS-Ketten in beliebiger Zusammensetzung. Diese Prototypen durchlaufen in mehreren Runden eine Vervielfältigungsreaktion, bei der es immer wieder zu Fehlern kommt, zu Mutationen, wie sie auch die Natur hervorbringt. Zwischendurch wird die auf Hunderte von Billionen anschwellende Molekülpopulation auf eine bestimmte Enzymaktivität getestet; nur leistungsfähige Varianten werden aussortiert und dürfen weiter mutieren – Darwinismus im Reagenzglas. Inzwischen haben sich die Evolutionsmaschinen als effektvolle Werkzeuge beim Moleküldesign erwiesen. „Damit können wir das gleiche tun“, behauptet der Ribozym-Experte Gerald Joyce, „was die Natur in vier Milliarden Jahren Evolution geleistet hat.“ Dem US-Forscher Michael Yarus und seinen Kollegen bescherte die neue Molekülbautechnik ein Ribozym, das sich mit der Aminosäure Phenylalanin bestückt. Nobelpreisträger Cech fand dazu einen Gegenspieler – ein Ribozym, das die Eiweißbausteine wieder abspaltet. Beide Vorgänge sind wichtige Schritte bei der Proteinsynthese an den Ribosomen, den Eiweißfabriken aller lebenden Zellen. Der Ribozym-Designer Jack 3 5 4 3 Die Ribozym-Moleküle heften sich an die Boten-RNS von Krebsgenen 4 und zerschneiden die schädlichen Botenmoleküle. 5 Die zerstückelte RNS kann nicht in Krebsproteine übersetzt werden und bleibt unwirksam. DER SPIEGEL 26/1995 157 .. WISSENSCHAFT Nach gleichem Muster wollen die USForscher Flossie Wong-Staal und Arnold Hampel künftig die Virusvermehrung im Blut von HIV-Infizierten bekämpfen. Die Wissenschaftler haben eine RNS-Genschere entwickelt, die das HIV-Erbgut in ungefährliche Fetzen zerlegen kann. In Laborversuchen konnten die Forscher die HIV-Vermehrung nahezu vollständig blockieren. Noch werden die Ribozym-Pharmazeuten von technischen Schwierigkeiten gebremst; ihre RNS-Medikamente sind allzu labil. Vor allem RNS-abbauende Zell-Enzyme, befürchten kritische Fachleute, könnten die Ribozym-Geschosse vernichten, bevor sie ihre Wirkung entfaltet haben. Doch diese Hürde wollen die Moleküldesigner überwinden: Auch die weit- K. WALSH Szostak hat ein Ribozym entwickelt, das zwei RNS-Schnipsel selbsttätig zusammenflicken kann. Was die Forscher sich erträumen, wären RNS-Enzyme aus der Retorte, die sich unbegrenzt selbständig vervielfältigen können – solche Moleküle, meint Ribozym-Forscher Joyce, müßten bereits „als biochemisches Leben“ eingestuft werden. Mittlerweile wollen sich auch die Mediziner der im Labor erzeugten Ribozyme bedienen. Aus dem Molekülarsenal der Vorzeit, so haben sie erkannt, ließen sich schlagkräftige Waffen gegen das RNS-Erbgut von Aids- und Hepatitisviren sowie anderer Erreger schmieden. Auch taugen die RNS-Enzyme womöglich zur Krebsbehandlung (siehe Grafik Seite 157). Chemiker Miller*: Urzeugung im Eiltempo Krebsmetastasen seiner Patienten will der Berliner Tumormediziner Friedhelm Herrmann mit einem Ribozym bekämpfen, das gegen das sogenannte Multidrug-Resistance-Gen (MDR-1Gen ) angeht. Es ist in Tumorzellen, die bisher jeder Chemotherapie hartnäckig widerstehen, besonders aktiv. Herrmanns Medizinerteam plant, den Krebskranken künftig ein Anti-MDRRibozym zu verabreichen. Die RNSScheren sollen sich an die Boten-RNS des MDR-Gens heften und sie zerstükkeln. Die zerteilte Botschaft des MDRGens bliebe für die Eiweißfabriken der Krebszellen unleserlich; der Tumor, seines Schutzschilds beraubt, so das Kalkül der Berliner Mediziner, wäre wehrlos dem Gifttod aus Pharmazeutenhand preisgegeben. * Mit der Nachbildung einer Apparatur zur Simulation der Entstehung von Aminosäuren. aus stabilere Erbsubstanz DNS, haben sie erkannt, kann die Aufgabe eines Enzyms erfüllen. Vorletzte Woche meldete US-Forscher Szostak vom Massachusetts General Hospital in Boston im Fachblatt Nature, seine Evolutionsmaschinen hätten ein künstliches DNS-Enzym ausgespuckt, das zerschnittene DNS-Stücke wieder zusammenfügt. Wenige Monate zuvor hatten Forscher vom Scripps Research Institute in Kalifornien verkündet, es sei ihnen gelungen, DNS, das Genmaterial aller Pflanzen, Tiere und Menschen, als Enzymschere gegen das Erbgut der RNSViren oder schädliche Boten-RNS einzusetzen. Michael Riordan, Präsident einer Gentechfirma in Kalifornien, sieht eine neue Medizinära heraufdämmern – sie werde, schwärmt er, „Nukleinsäuren, die Ursprungsmoleküle des Lebens, als Medikamente nutzen“. Y