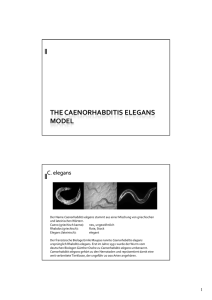
Warum Caenorhabditis elegans
Werbung

Warum Caenorhabditis elegans? VM-Ce1-1 Caenorhabditis elegans - Modellorganismus für einfache multizelluläre Organismen • „How genes might specify the complex structures found in higher organisms is a major unsolved problem of biology“ S. Brenner (1974) VM-Ce1-2 VM-Ce1-3 Übersicht C. elegans als experimenteller Organismus • • • • - Anatomie und Lebenszyklus Genom Konstante Abfolge der Zellteilungen wä während der Entwicklung Genetische Techniken und molekulare Analyse Genetische Analyse verschiedener Entwicklungsprozesse • • • Frü Frühe Embryonalentwicklung Funktion des programmierten Zelltods (Apoptose) Zeitliche Kontrolle von Entwicklungsvorgä Entwicklungsvorgängen wä während der Larvenentwicklung - Beispiel: Genetische Analyse von Signalwegen, die die Vulvaentwicklung kontrollieren - RNAi: Seminarvorträ Seminarvorträge VM-Ce1-4 Anatomie eines ausgewachsenen Tieres Cross section VM-Ce1-5 Fig. C.6a Genom von C. elegans - 97 Mb – sehr klein (2/3 der Größ e von D. melanogaster) Größe melanogaster) Sechs Chromosomen (I-VI) – alle ähnlich groß groß Alle Chromosomen sind holozentrisch (ohne definierte Centromere) Physikalische Karte (Cosmide und YACs) Die Rekombinationsrate variiert beträ beträchtlich ca. 1 Gen alle 5 kb 19.000 Gene Proteins match homologous sequences of other organisms 20% 20% der Protein werden fü für biologische Kernfunktionen benö benötigt (Replikation, Stoffwechsel etc.) Die übrigen Gene werden nur in multizellulä multizellulären Organismen benö benötigt Repetitive Sequenzen – z.B. 7 verschiedene transponierbare Elemente VM-Ce1-6 VM-Ce1-7 Trans-Splicing - - 70% aller mRNAs erhalten eine von zwei “splice-leader”-Sequenzen (SL1 oder SL2) durch Trans-Splicing an das 5’- Ende der mRNA Trans-Splicing findet man in allen Nematoden 25% aller benachbarten Gene werden als Operons transkribiert Durch Trans-Splicing mit dem splice-leader SL2 werden aus dem polycistronischen Transkript Einzelgen-mRNAs produziert VM-Ce1-8 Trans-Splicing in Nematoden VM-Ce1-9 Mechanismus des Trans-Splicing VM-Ce1-10 Anatomie von C. elegans VM-Ce1-11 Lebenszyklus von C. elegans - Hermaphroditen: • • Die ersten 40 Keimzellen entwicklen zu ~150 Spermien die in der Spermatheca deponiert werden Danach wechselt das Geschlecht und die restlichen Keimzellen werden Oozyten VM-Ce1-12 C. elegans Lebenszyklus Fig. C.5b VM-Ce1-13 C. elegans Lebenszyklus VM-Ce1-14 Entwicklung von der Zygote zum ausgewachsenen Tier - 3 Tage Embryonalentwicklung beginnt im Uterus Die Hermaphroditen legen ihre Eier 2 Stunden nach der Befruchtung Blastodermzellen – groß große Zellen als Resultat der ersten Zellteilungen - In der frü frühen Entwicklung ungleiche Teilungen Bis zum 28-Zell-Stadium stehen alle Blastodermzellen mit der Oberflä Oberfläche des Embryos in Verbindung Gastrulation - Im 28-Zell-Stadiu beginnen zwei Schlund Precursorzellen in das Innere einzuwandern Drei Keimschichten (Endoderm, Mesoderm, Ektoderm) Die Larven schlü schlüpfen 14 Stunden nach der Befruchtung Die L1 Larve ist 250µ 250µm lang und besteht aus 558 Zellen • • • • • • - Nächste 50 Stunden: L2, L3, L4 Stadien der Entwicklung, jeweils getrennt durch Hä Häutungen VM-Ce1-15 Embryonalentwicklung in C. elegans Ungleiche Zellteilungen Gastrulation Figure C.5a Vor dem Schlüpfen Larvenähnliche Gestalt VM-Ce1-16 C - 17 Die Enstehungsgeschichte jeder einzelnen Zelle ist bekannt VM-Ce1-18 Zellabstammungs-Diagramm Fig. C.7a VM-Ce1-19 Im Zellteilungsdiagramm erkennt man 6 Gründerzellen, aus denen verschiedene Gewebe und Organe der Erwachsenen hervorgeht VM-Ce1-20 Kultivierung im Labor C.elegans wächst auf Agarplatten und wird mit einem E.coli Bakterienrasen gefüttert. Übertragung mit einem Platindraht Erwachsene Tiere reproduzieren sich innerhalb von 3-4 Tagen Ausgewachsene Tiere lebennoch bis zu 2 Wochen nach der Reproduktion “Dauer”-Larve • • • • Unter Mangelbedingungen arretiert die Larvenentwicklung im Larvenstadium L3 Die Dauerlarve kann bis zu 6 Monate überleben Wenn wieder Nahrung vorhanden ist, wird die Entwicklung wieder aufgenommen Bei Nahrungsmangel wird auch die Alterung aufgehalten VM-Ce1-21 VM-Ce1-22 Kreuzung - Männchen liegen neben den Weibchen bis der fächerförmige Schwanz neben der Vulva liegt Spezielle Struktur wird in die Vulva inseriert Spermien bewegen sich durch die Vulva in den Uterus Die Spermien wandern zu den spermathecae Dort erlangen sie einen Vorteil gegenüber den vorhandenen Spermien und erzeugen Kreuzungsnachkommen VM-Ce1-23 Genetische Analyse - Diploider Organismus Männchen haben nur ein X-Chromosom (XO) Hermaphrodites sind XX Männchen entstehen spontan durch Nondisjunction während der Keimzellbildung • • Sobald Männchen vorhanden sind, entstehen durch Kreuzung weitere Die Hälfte der Nachkommen entstehen aus Spermien, die kein X-Chromosom tragen => XO Männchen VM-Ce1-24 Isolierung von Mutanten - EMS (ethyl methane sulfate) induziert eine hohe Mutationsrate Heterozygote Hermaphroditen produzieren homozygote Nachkommen durch Selbstbefruchtung Aufgrund der Selbstbefruchtung kö können auch Mutationen mit einem starken Effekt (z.B. mit vollstä vollständiger Paralyse der Körpermuskulatur) erhalten werden 1600 Gene auf der Genkarte aus genetischen Screens - • • • - Dumpy (Dpy) – kurz und dick Long (Lon) – lang und dü dünn Unc – unkoordinierte Bewegungen Nomenklatur • • Phä Phänotypbezeichnungen beginnen mit einem Groß Großbuchstaben und sind nicht kursiv Gene und Allele werden mit kleinen kursiven Buchstaben bezeichnet Proteinprodukte werden mit Groß Großbuchstaben gekennzeichnet (z.B., DPY-10) VM-Ce1-25 VM-Ce1-26 Isolierung von Mutanten VM-Ce1-27 VM-Ce1-1 Kultivierung im Labor C.elegans wächst auf Agarplatten und wird mit einem E.coli Bakterienrasen gefüttert. Übertragung mit einem Platindraht Erwachsene Tiere reproduzieren sich innerhalb von 3-4 Tagen Ausgewachsene Tiere lebennoch bis zu 2 Wochen nach der Reproduktion “Dauer”-Larve • • • • Unter Mangelbedingungen arretiert die Larvenentwicklung im Larvenstadium L3 Die Dauerlarve kann bis zu 6 Monate überleben Wenn wieder Nahrung vorhanden ist, wird die Entwicklung wieder aufgenommen Bei Nahrungsmangel wird auch die Alterung aufgehalten VM-Ce1-2 Kreuzung - Männchen liegen neben den Weibchen bis der fächerförmige Schwanz neben der Vulva liegt Spezielle Struktur wird in die Vulva inseriert Spermien bewegen sich durch die Vulva in den Uterus Die Spermien wandern zu den spermathecae Dort erlangen sie einen Vorteil gegenüber den vorhandenen Spermien und erzeugen Kreuzungsnachkommen VM-Ce1-3 VM-Ce1-4 Genetische Analyse - Diploider Organismus - Männchen haben nur ein X-Chromosom (XO) - Hermaphroditen sind XX - Männchen entstehen spontan durch Nondisjunction während der Keimzellbildung • Sobald Mä Männchen vorhanden sind, entstehen durch Kreuzung weitere • Die Hä Hälfte der Nachkommen entstehen aus Spermien, die kein X-Chromosom tragen => XO Mä Männchen VM-Ce1-5 Isolierung von Mutanten - EMS (ethyl methane sulfate) induziert eine hohe Mutationsrate Heterozygote Hermaphroditen produzieren homozygote Nachkommen durch Selbstbefruchtung Aufgrund der Selbstbefruchtung kö können auch Mutationen mit einem starken Effekt (z.B. mit vollstä vollständiger Paralyse der Körpermuskulatur) erhalten werden 1600 Gene auf der Genkarte aus genetischen Screens - • • • - Dumpy (Dpy) – kurz und dick Long (Lon) – lang und dü dünn Unc – unkoordinierte Bewegungen Nomenklatur • • Phä Phänotypbezeichnungen beginnen mit einem Groß Großbuchstaben und sind nicht kursiv Gene und Allele werden mit kleinen kursiven Buchstaben bezeichnet Proteinprodukte werden mit Groß Großbuchstaben gekennzeichnet (z.B., DPY-10) VM-Ce1-6 Isolierung von Mutanten VM-Ce1-7 Klonierung von C. elegans Genen Positional cloning – basierend auf der Lage des Gens im Genom - • - SNPs (Small nuclear polymorphisms) als Marker Identifizierung von Genen • Wiederherstellung des Wildtypphä Wildtypphänotyps durch Injektion von Cosmid-DNA Die Cosmide entsprechen dem Intervall, das durch die Genkartierung identifiziert wurde. • Kandidatengene kö können durch RNAi getestet werden VM-Ce1-8 DNA Transformation - Injektion von DNA in die distalen Gonaden von Hermaphroditen - Die injizierte DNA bildet Arrays (Concatemere), die sich mehr oder weniger stabil vererben - Bestrahlung erhö erhöht die Integrationsrate ins Genom - GFP als Reportergen zeigt transgene Tiere an VM-Ce1-9 Erzeugung von Transposon-Mutanten - Forward genetics • - Begin with mutant phenotype and isolate gene for molecular analysis Reverse genetics • • • Gene of possible developmental interest predicted from genomic DNA sequence Assign function through PCR methods Assign function through RNAi VM-Ce1-10 Mutator Maschine ORF x ORF y ORF z 11 Mutator Maschine 12 RNAi - Ein Enzymkomplex (Dicer) schneidet dsRNA in 22bp Fragmente, die als small interfering RNAs (siRNAs) siRNAs) bezeichnet werden Die siRNAs können sich im Organismus ausbreiten siRNAs werden entwunden und in einen Proteinkomplex (RISC) eingebaut. Dieser Komplex bindet sequenz-spezifisch einzelsträ einzelsträngige mRNA und schneidet diese Zwei mö mögliche Wege: - • • Zerstö Zerstörung von mRNA Amplifikation der siRNA durch RNAabhä abhängige RNA-Polymerase (RdRP) VM-Ce1-13 C. elegans in der postgenomischen Ära - Funktionelle Genomik • - - Identifzierung aller Gene die in bestimmten Stadien exprimiert werden oder deren Expression durch bestimmte Stimuli induziert wird Globale Analyse der Genexpression mit Hilfe von DNA-Chips die geordnete Mikroarrays aller 19.000 Gene enthalten In situ Hybridisierungen zeigen die Expressionsmuster aller Gene während der Entwicklung an VM-Ce1-14 Genetische Analyse der Vulvaentwicklung • 6 Zellen sind an der Vulvaentwicklung beteiligt (P3p – P8p) • P5p-P7p bilden die Vulva als Antwort auf einSignal der Ankerzelle (AC) • • P3p, P4p, P8p bilden zusä zusätzliche Hypodermalzellen VM-Ce1-15 Screen zur Identifizierung von Genen, die an der ACInduktion von P5p, P6p, and P7p beteiligt sind • Suche nach vulvalosen Mutanten Mutanten ohne Vulva produzieren befruchtete Eizellen, aus denen Larven schlü schlüpfen, diesich von der Mutter ernä ernähren (Bag of worms) • Multivulva Mutanten bilden ektopische vulva-artige Strukturen • VM-Ce1-16 Bindung des LIN-3 Liganden an den LET-23 Rezeptor aktiviert einen Signalweg, der die Vulvaentwicklung steuert VM-Ce1-17 Maternaler Effekt - Gene, die fü für die frü frühe Entwcklung des embryonalen Balstoderms benö benötigt werden - Frü Frühe Teilungen benö benötigen Komponenten, die von der Mutter gestellt werden - Vulvalose Hermaphroditen erleichtern die Analyse • • Nachkommen essen die Mü Mütter von innen auf Überlebende F2 Individuen erzeugen mutierte Nachkommen, bei denen die Entwicklung blockiert ist (Bag of dead embryos) VM-Ce1-18 Identifizierung von letalen Mutanten mit maternalem Effekt - Gene, die fü für die frü frühe Entwcklung des embryonalen Balstoderms benö benötigt werden - Frü Frühe Teilungen benö benötigen Komponenten, die von der Mutter gestellt werden - Vulvalose Hermaphroditen erleichtern die Analyse • • Nachkommen essen die Mü Mütter von innen auf Überlebende F2 Individuen erzeugen mutierte Nachkommen bei denen die Entwicklung blockiert ist. VM-Ce1-19 C - 20 Cell-autonomous Determinants must be Distributed to Cells in Which They Act - PAR proteins help direct embryonic polarity (a) wild-type zygotes, P granules initially uniformly distributed, but then localize to posterior part of zygote (b) shortly after fertilization, PAR-2 is found in posterior cortex and PAR-3 in anterior cortex - - - Maternal lethal mutations that produce two-cell embryos with no polarity identify six par genes VM-Ce1-21 Fig. C.13 Inductive Signals Control Cell Fates in Early Embryogenesis - PAR proteins only affect cells that contain them • - Early development also depends on control signals sent between cells to partition Intercellular signaling determines fates of ABa and ABp cells • Figure C.14 Cell autonomous Contact between P2 and ABp enables P2 to send signals to ABp required for proper fate of Abp lineage VM-Ce1-22 Zeitliche Kontrolle während der Larvenentwicklung VM-Ce1-23 Heterochrone Mutationen Führen zu Fehlern im Timing und der Zellbestimmung wä während der Larvalentwicklung Schaltergene: Nullmutanten und dominant aktive Mutanten haben entgegen-gesetzte zeitliche Effekte Lin-14 Deletion verursacht verzö verzögerte Entwicklung Der Zeitpunkt und/oder die Entscheidungen während der Zellteilung sind verä verändert VM-Ce1-24 LIN-14 protein behaves as central clock • Concentration descends from high in L1 animals to a low in L4 animals • Epistasis tests show lin-4 negatively regulates expression of lin-14 by novel mechanism • Lin-4 gene transcript is processed to produce a smaller 22nucleotide RNA complementary to 3! 3! untranslated transcript of lin-14 mRNA • RNAi machinery appears to control LIN-14 concentrations VM-Ce1-25 Genetische Mosaikanalyse - Tiere, die aus Wildtyp und mutanten Zellen zusammengesetzt sind - Chromosomenfragmente werden durch Rö Röntgen- oder gammaStrahlung erzeugt • • - Die Fragment werden als freie extrachromosomale Duplikationen aufrechterhalten Eine rezessive Mutation wird in beide Chromosomen eingefü eingeführt (homozygot) Wenn die Duplikation verlorengeht, entstehen Zellen mit dem mutanten Phä Phänotyp VM-Ce1-26 - Genetisches Mosaik • • • Eine freie Duplikationen trägt das Wildtyp-Allel von lin-12+ in einem mutierten Wurm (lin-12) mrk+ auf der Duplikation im mrk- Hintergrund zeigt den Verlust der lin-12 Duplikation an Mosaik-Analyse zeigt, daß Z1.ppp or Z4.aaa lin12+ Aktivität benötigen um die VU Form anzunehmen VM-Ce1-27 Fig. C.11 Geschlechtsbestimmung in C. elegans C - 28 Programmierter Zelltod - Apoptose VM-Ce1-29 Programmierter Zelltod - Apoptose VM-Ce1-30 C - 31 Trans-Splicing in Nematoden VM-Ce1-32 Bindung des LIN-3 Liganden an den LET-23 Rezeptor aktiviert einen Signalweg, der die Vulvaentwicklung steuert VM-Ce1-33