Studientitel, Nr., Akronym Studie zur Sicherheit, Verträglichkeit
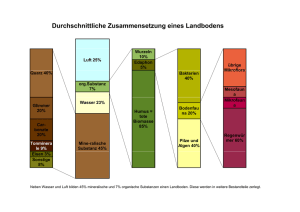
Werbung
Studientitel, Nr., Akronym Studie zur Sicherheit, Verträglichkeit, Antwort Immunsystems und Effektivität der Substanz S-488210 des EudraCT Number: 2011-005014-12 Shionoge Vaccine S-488210 Leiter der Klinischen Prüfung Prüfarzt Kontakt Studienzentrale Herr Dr. Dr. Jan-Dirk Raguse Herr Dr. Dr. Jan-Dirk Raguse Anschrift Tel. Charité - Universitätsmedizin Berlin Campus Virchow-Klinikum Klinik für Mund-, Kiefer- und Gesichtschirurgie Station 4 Mittelallee 2 / Südstraße 8, 3. OG Augustenburger Platz 1 13353 Berlin +49 30 450 555213 Fax +49 30 450 555901 Email Studienziel In dieser Studie sollen die Sicherheit, Verträglichkeit, Antwort des Immunsystems und Effektivität der Substanz S-488210 bei Patienten mit bösartigen, fortgeschrittenen Neubildungen im Kopf-Hals-Bereich (Karzinomen) untersucht werden. Die Verträglichkeit und Effektivität der Substanz S-488210 wird anhand verschiedener Laborparameter, Fragebogen zur Lebensqualität und bildgebender Verfahren (Computertomographie und Kernspintomographie) ermittelt. Behandlung Die Substanz S-488210 besteht aus drei verschiedenen Peptiden (Proteinen). Diese Proteine sind bei zahlreichen bösartigen Erkrankungen im Tumorgewebe verstärkt nachweisbar, während sie in gesundem Gewebe kaum nachweisbar sind. Durch Gabe der Substanz S-488210 erhofft man sich eine Antikörper-Reaktion bei Patienten mit KopfHals-Tumoren. Dies würde eine körpereigene Abwehrreaktion gegenüber dem Tumor bedeuten. Dadurch soll es vor allem bei Patienten, welche nicht auf die Standardtherapie angesprochen haben, zu einer Verbesserung der Lebensqualität und Lebenserwartung kommen. In früheren Studien zu diesen Einzelproteinen und bösartigen Tumoren anderer Organe konnte gezeigt werden, dass die Gabe dieser Substanz einerseits kaum zu wesentlichen Nebenwirkungen bei den Patienten führt und dass sie andererseits z.B. bei Patienten bösartiger Neubildung der Speiseröhre eine gesteigerte Gesamtüberlebensrate bedingt. Die Gabe der Substanz erfolgt subkutan (unter die Haut) und wird einmal wöchentlich vorgenommen. Insgesamt sind in der ersten S. 1 von 2 Phase der Studie (Ermittlung der Sicherheit, Verträglichkeit und Antwort des Immunsystems) mindestens 4 Gaben und in der zweiten Phase (Ermittlung der Effektivität) mindestens 24 Gaben vorgesehen Welche Patienten werden in die Studie aufgenommen? Eingeschlossen werden nur Patienten, die bereits eine Standardtherapie (Operation, Bestrahlung und Chemotherapie mit Cisplatin) für Karzinome im Kopf-Hals-Bereich erhalten haben und dennoch nicht tumorfrei sind. In der ersten Phase der Studie werden zudem nur Patienten eingeschlossen, bei denen anhand von Ergebnissen aus früheren Studien eine Immunantwort zu erwarten ist Wichtigste Einschlusskriterien S. 2 von 2