Sonstiger Bestandteile mit bekannter Wirkung: Natrium, 3,77
Werbung

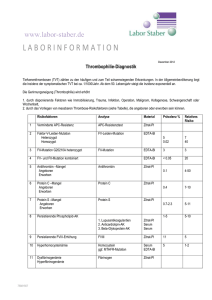
ANTITHROMBIN III KONZENTRAT BAXALTA Zusammenfassung der Merkmale des Arzneimittels= Gebrauchsinformation 1. 1/8 BEZEICHNUNG DES ARZNEIMITTELS ANTITHROMBIN III KONZENTRAT BAXALTA, 500 I.E., Pulver und Lösungsmittel zur Herstellung einer Injektionslösung oder Infusionslösung. ANTITHROMBIN III KONZENTRAT BAXALTA, 1000 I.E., Pulver und Lösungsmittel zur Herstellung einer Injektionslösung oder Infusionslösung. 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Aus humanem Plasma gewonnenes Antithrombin. ANTITHROMBIN III KONZENTRAT BAXALTA wird angeboten als Pulver zur Herstellung einer Injektionslösung oder Infusionslösung und enthält nominell 500 I.E./1000 I.E. aus humanem Plasma gewonnenes Antithrombin je Flasche. Das Produkt enthält etwa 50 I.E./ml (500 I.E./10 ml, 1000 I.E./20 ml) aus humanem Plasma gewonnenes Antithrombin nach Auflösung mit 10 ml/20 ml sterilem Wasser für Injektionszwecke. Der Gehalt (I.E.) wird durch Verwendung der chromogenen Dosierung der Europäischen Pharmakopöe bestimmt. Die spezifische Wirkung von ANTITHROMBIN III KONZENTRAT BAXALTA beträgt mindestens 3 I.E. AT/mg Plasmaproteine. Sonstiger Bestandteile mit bekannter Wirkung: Natrium, 3,77 mg/ml. Vollständige Auflistung der sonstigen Bestandteile siehe, Abschnitt 6.1. 3. DARREICHUNGSFORM Pulver und Lösungsmittel zur Herstellung einer Injektionslösung oder Infusionslösung. ANTITHROMBIN III KONZENTRAT BAXALTA liegt in Form einer hellgelben bis hellgrünen festen, bröckeligen Substanz oder eines Pulvers vor. Osmolarität: nicht weniger als 240 mosmol/kg, pH: 6,0 – 7,5. 4. KLINISCHE ANGABEN 4.1. Anwendungsgebiete Der Antithrombin-Mangel kann angeboren oder im Rahmen einer großen Vielfalt klinischer Störungen erworben sein. Ein erworbener Antithrombin-Mangel kann auf einen erhöhten Verbrauch oder auf einen Proteinverlust oder aber auf eine mangelhafte Antithrombin-Synthese zurückzuführen sein. Die Verabreichung von ANTITHROMBIN III KONZENTRAT BAXALTA ist angezeigt bei Patienten mit einer Antithrombin-Aktivität im Plasma unter 70 % des normalen Wertes, für die Prophylaxe und die Behandlung von thrombotischen und thromboembolischen Störungen. Die Antithrombin-Infusionslösungen können in folgenden klinischen Situationen angezeigt sein: • chirurgische Eingriffe oder Schwangerschaft und Geburt bei Patienten mit angeborenem Antithrombin-Mangel; • unangemessenes Ansprechen oder Fehlen des Ansprechens auf eine Heparintherapie; • Vorhandensein oder Risiko einer disseminierten intravaskulären Gerinnung (z.B. mit Polytrauma, septischen Komplikationen, Schock, Präeklampsie und sonstigen Störungen in Verbindung mit einer akuten disseminierten intravaskulären Gerinnung); • Vorhandensein oder Risiko einer Thrombose bei Patienten mit nephrotischem Syndrom oder entzündlicher Erkrankung des Intestinaltraktes; Version 7.0 (QRD 3.0) ANTITHROMBIN III KONZENTRAT BAXALTA Zusammenfassung der Merkmale des Arzneimittels= Gebrauchsinformation 2/8 • chirurgischer Eingriff oder Blutungen bei Patienten mit schwerer Leberinsuffizienz und insbesondere, wenn die Patienten mit Konzentraten von Koagulationsfaktoren behandelt werden. 4.2. Dosierung und Art der Anwendung Der Behandlungsbeginn muss von einem Arzt überwacht werden, der Erfahrung in der Behandlung von Patienten mit einem Antithrombin-Mangel hat. Dosierung Im Falle eines angeborenen Mangels muss die Dosierung individuell angepasst werden, unter Berücksichtigung thromboembolischer Ereignisse in der Familienanamnese, gegenwärtiger klinischer Risikofaktoren und Laborauswertungen. Die Dosierung sowie die Dauer der Substitutionsbehandlung bei erworbenem Mangel hängen vom Antithrombin-Plasmaspiegel, von Hinweisen für eine erhöhte Antithrombin-Produktion, von der zugrunde liegenden Ursache und dem Schweregrad des klinischen Zustandes des Patienten ab. Die zu verabreichende Menge und die Verabreichungshäufigkeit müssen stets auf der klinischen Wirksamkeit und auf den Laborbestimmungen des einzelnen Patienten beruhen. Die Anzahl an verabreichten Antithrombin-Einheiten wird in Internationalen Einheiten angegeben (I.E.), die sich auf den aktuellen WHO-Standard von Antithrombin beziehen. Die Antithrombin-Aktivität im Plasma wird entweder als Prozentsatz (relativ zum normalen menschlichen Plasma) oder in Internationalen Einheiten (relativ zum Internationalen Standard für Antithrombin im Plasma) angegeben. Eine Internationale Einheit (I.E.) der Antithrombin-Aktivität entspricht der Menge an Antithrombin, die in 1 ml normalem Humanplasma enthalten ist. Die Berechnung der erforderlichen Antithrombin-Dosis basiert auf dem empirischen Befund, dass 1 Internationale Einheit (I.E.) Antithrombin pro kg Körpergewicht die Antithrombin-Plasmaaktivität um etwa 2 % erhöht. Die Initialdosis wird mit folgender Formel berechnet: erforderliche Einheiten = Körpergewicht (kg) x (gewünschter – aktueller Antithrombin-Aktivität [%]) x 0,5 Die ursprüngliche, zu erreichende Antithrombin-Aktivität hängt von der klinischen Situation ab. Wenn die Indikation für die Antithrombin-Substitution nachgewiesen ist, muss die Dosierung ausreichend hoch sein, um die gewünschte Antithrombin-Aktivität zu erreichen und aufrechtzuerhalten. Die Dosierung muss auf der Basis der Laborwerte der Antithrombin-Aktivität bestimmt und kontrolliert werden; diese sind mindestens zweimal pro Tag durchzuführen, bis die Lage des Patienten stabil ist, und anschlieβend einmal pro Tag, vorzugsweise unmittelbar vor der nächsten Infusion. Die Dosisanpassung muss den Anzeichen eines erhöhten Antithrombin-Umsatzes (je nach Laborkontrolle) sowie der klinischen Entwicklung Rechnung tragen. Während der Behandlungsdauer muss eine Antithrombin-Aktivität von über 80 % aufrechterhalten werden, es sei denn, klinische Besonderheiten sprechen für einen anderen effektiven Spiegel. Die gebräuchliche Initialdosis im Falle eines angeborenen Mangels sollte zwischen 30 und 50 I.E./kg liegen. Besondere Patientengruppen Sowohl die Dosierung als auch die Verabreichungshäufigkeit und die Behandlungsdauer müssen den biologischen Parametern und der klinischen Situation angepasst werden. Kinder und Jugendliche Die Sicherheit und Wirksamkeit von ANTITHROMBIN III KONZENTRAT BAXALTA bei pädiatrischen Patienten wurde in klinischen Studien zu Baxalta nicht erwiesen. Jedoch ist die Anwendung von Lösungen mit Antithrombin III bei pädiatrischen Patienten in der medizinischen Version 7.0 (QRD 3.0) ANTITHROMBIN III KONZENTRAT BAXALTA Zusammenfassung der Merkmale des Arzneimittels= Gebrauchsinformation 3/8 Fachliteratur belegt. Art der Anwendung Hinweise zur Rekonstitution des Arzneimittels vor der Verabreichung, siehe Abschnitt 6.6. Das Mittel muss intravenös verabreicht werden. Die maximale Verabreichungsgeschwindigkeit liegt bei 5 ml pro Minute. 4.3. Gegenanzeigen Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile. In der Krankengeschichte bekannte heparininduzierte Thrombozytopenie. 4.4. Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung Wie bei jedem intravenös verabreichten proteinhaltigen Präparat können allergische Überempfindlichkeitsreaktionen auftreten. Die Patienten müssen daher während der gesamten Infusionsdauer streng kontrolliert und sorgfältig beobachtet werden, um jegliche Symptome zu erfassen. Die Patienten sollten über die möglichen Frühzeichen von Unverträglichkeitsreaktionen aufgeklärt werden, wie zum Beispiel Nesselausschlag, generalisierte Urtikaria, Engegefühl in der Brust, Atemnot, Blutdruckabfall und Anaphylaxie. Die Patienten sollten ihren Arzt kontaktieren, wenn diese Symptome nach der Verabreichung auftreten. Die Behandlung des Schocks erfolgt nach den Regeln der modernen Schocktherapie. Standardmaßnahmen zur Verhinderung von Infektionen, die durch aus menschlichem Blut oder Plasma hergestellten Arzneimitteln übertragen werden können, schließen die Auswahl der Spender, die Testung der Einzelspenden und der Plasmapools auf spezifische Infektionsmarker und die Durchführung effektiver Herstellungsschritte zur Inaktivierung/Abtrennung von Viren mit ein. Trotzdem sind bei der Anwendung von aus menschlichem Blut oder Plasma hergestellten Arzneimitteln Infektionskrankheiten durch Übertragung von Erregern nicht völlig auszuschließen. Dies gilt ebenfalls für unbekannte oder neu auftretende Viren und für andere Pathogene. Diese Maßnahmen werden für umhüllte Viren wie z.B. HIV, HBV und HCV sowie für das nicht umhüllte Virus HAV für wirksam erachtet. Diese Maßnahmen können gegebenenfalls bei manchen nicht umhüllten Viren, wie z.B. Parvovirus B19, eingeschränkt wirksam sein. Infektionen durch Parvovirus B19 können bei Schwangeren (foetale Infektion) und Personen mit Immundefekten oder gesteigerter Erythropoese (z.B. hämolytische Anämie) zu schweren Erkrankungen führen. Wird ein aus menschlichem Plasma hergestelltes Antithrombin regelmäßig/wiederholt verabreicht, müssen geeignete Impfungen (Hepatitis A und B) in Betracht gezogen werden. Im Interesse des Patienten wird dringend empfohlen, jede Verabreichung von ANTITHROMBIN III KONZENTRAT BAXALTA mit Produktnamen und Chargenummer (lot) zu dokumentieren, um die Verbindung zwischen Patient und Produktcharge herstellen zu können. Klinische und biologische Überwachung bei gleichzeitiger Antithrombin- und Heparintherapie: • Zum Anpassen der Heparindosis und zur Vermeidung einer exzessiven Hypokoagulabilität sollte das Ausmaß der Antikoagulation (aPTT, falls möglich Anti-FXa-Aktivität) regelmäßig, mit kurzen Intervallen und insbesondere in den ersten Minuten/Stunden nach Beginn der AntithrombinTherapie engmaschig kontrolliert werden. Aufgrund des Risikos der Verminderung der Antithrombin-Spiegel durch verlängerte Behandlung mit unfraktioniertem Heparin ist zur individuellen Dosisanpassung die tägliche Bestimmung der Antithrombin-Spiegel erforderlich. Dieses Arzneimittel enthält 3,77 mg Natrium pro ml. Dies sollte bei Patienten unter natriumarmen kontrollierten Diät beachtet werden. Version 7.0 (QRD 3.0) ANTITHROMBIN III KONZENTRAT BAXALTA Zusammenfassung der Merkmale des Arzneimittels= Gebrauchsinformation 4/8 Kinder und Jugendliche Die Sicherheit und Wirksamkeit von Antithrombin III Konzentrat Baxalta bei pädiatrischen Patienten wurde in klinischen Studien zu Baxalta nicht erwiesen. Jedoch ist die Anwendung von Lösungen mit Antithrombin III bei pädiatrischen Patienten in der medizinischen Fachliteratur belegt. Daten aus klinischen Studien und systematischen Übersichtsarbeiten über die Verwendung von Antithrombin III bei der Behandlung von Frühgeborenen in der nicht genehmigten Indikation „Atemnotsyndrom des Neugeborenen (IRDS)“ deuten auf ein erhöhtes Risiko für intrakranielle Blutungen und Mortalität hin, bei gleichzeitig fehlendem Nachweis von positiven Wirkungen in dieser Patientenpopulation. 4.5. Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen Heparin: Die Antithrombin-Substitution während der Verabreichung von Heparin in therapeutischen Dosen erhöht das Blutungsrisiko. Die Wirkung von Antithrombin wird durch Heparin erheblich verstärkt. Die Halbwertszeit von Antithrombin kann aufgrund der beschleunigten Antithrombin-Elimination unter gleichzeitiger Heparintherapie stark vermindert sein. Deshalb muss eine gleichzeitige Verabreichung von Antithrombin und Heparin bei Patienten mit erhöhtem Blutungsrisiko klinisch und biologisch überwacht werden. 4.6. Fertilität, Schwangerschaft und Stillzeit Es gibt nur beschränkte Erfahrungen hinsichtlich der Sicherheit der humanen Antithrombin-Produkten bei Anwendung in der Schwangerschaft bei den Menschen. Die Unbedenklichkeit von ANTITHROMBIN III KONZENTRAT BAXALTA bei schwangeren oder stillenden Frauen wurde nicht in kontrollierten klinischen Prüfungen nachgewiesen. Daher sollte ANTITHROMBIN III KONZENTRAT BAXALTA bei Frauen mit Antithrombin-Mangel in der Schwangerschaft und Stillzeit nur bei eindeutiger Indikationsstellung angewendet werden. Dabei ist zu berücksichtigen, dass aufgrund der Schwangerschaft bei diesen Patientinnen das Risiko für thromboembolische Ereignisse erhöht ist. 4.7. Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen ANTITHROMBIN III KONZENTRAT BAXALTA hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen. 4.8. Nebenwirkungen Zusammenfassung des Sicherheitsprofils Es sind keine Nebenwirkungen im Laufe der klinischen Studien beobachtet worden. Überempfindlichkeitsreaktionen oder allergische Reaktionen (eventuell zusammen mit einem Angioödem, Brennen und Kribbeln an der Injektionsstelle, Frösteln, Rötungen, generalisierter Nesselsucht, Kopfschmerzen, Juckreiz, niedrigem Blutdruck, Lethargie, Übelkeit, Unruhe, beschleunigtem Herzrhythmus, Beklemmungsgefühl in der Brust, Ameisenlaufen, Erbrechen und pfeifender Atmung) sind gelegentlich beobachtet worden und können in bestimmten Fällen zu einer schweren Anaphylaxe (einschlieβlich Schock) führen. In seltenen Fällen wurde Fieber beobachtet. In seltenen Fällen kann eine durch Heparin ausgelöste autoimmune Thrombozytopenie (Typ II) auftreten. Es können Blutplättchenzählungen unter 100 000/µl oder eine Verringerung der Blutplättchenzählung um 50 % beobachtet werden. Nach der Markteinführung von ANTITHROMBIN III KONZENTRAT BAXALTA wurden folgende Version 7.0 (QRD 3.0) ANTITHROMBIN III KONZENTRAT BAXALTA Zusammenfassung der Merkmale des Arzneimittels= Gebrauchsinformation 5/8 Nebenwirkungen berichtet: Tremor, Hitzewallung. Tabellarische Zusammenstellung der Nebenwirkungen Die Nebenwirkungen sind gemäß den MedDRA-Systemorganklassen (SOC) sowie sofern möglich gemäß dem Schweregrad aufgeführt. Die Häufigkeiten sind wie folgt definiert: sehr häufig (≥1/10); häufig (≥1/100, <1/10); gelegentlich (≥1/1.000, <1/100); selten (≥1/10.000, <1/1.000); sehr selten (<1/10.000); nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar). Häufigkeiten der Nebenwirkungen MedDRASystemorganklassen Erkrankungen des Blutes und des Lymphsystems Erkrankungen des Immunsystems Erkranku ngen des Nervensy stems Häufigkeit der Nebenwirkungen MedDRA-Terminologie Selten Thrombozytopenie Überempfindlichkeitsreaktionen oder allergische Reaktionen (die Angioödem, Brennen und und Kribbeln an der Injektionsstelle, Schüttelfrost, Rötung, generalisierte Urtikaria, Kopfschmerzen, Pruritus, Hypotonie, Lethargie, Nausea, Agitiertheit, Tachykardie, Brustenge, Ameisenlaufen, Erbrechen und Giemen) Gelegentlich Tremor* Nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar) Gefäßerkrankungen Hitzewallung* Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Fieber Nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar) Selten * Nebenwirkungen, die nach der Markteinführung berichtet wurden Kinder und Jugendliche Die Sicherheit und Wirksamkeit von ANTITHROMBIN III KONZENTRAT BAXALTA bei pädiatrischen Patienten wurde in klinischen Studien zu Baxalta nicht erwiesen. Jedoch ist die Anwendung von Lösungen mit Antithrombin III bei pädiatrischen Patienten in der medizinischen Fachliteratur belegt. Für Hinweise zur viralen Sicherheit, siehe Abschnitt 4.4. Meldung des Verdachts auf Nebenwirkungen Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung anzuzeigen. Version 7.0 (QRD 3.0) ANTITHROMBIN III KONZENTRAT BAXALTA Zusammenfassung der Merkmale des Arzneimittels= Gebrauchsinformation Belgien Föderalagentur für Arzneimittel und Gesundheitsprodukte Abteilung Vigilanz EUROSTATION II Victor Hortaplein, 40/40 B-1060 BRUSSEL Website: www.fagg-afmps.be E-Mail: [email protected] 4.9. 6/8 Luxemburg Direction de la Santé – Division de la Pharmacie et des Médicaments Villa Louvigny – Allée Marconi L-2120 Luxembourg Site internet: http://www.ms.public.lu/fr/activites/pharmaciemedicament/index.html Überdosierung Symptome durch Überdosierung mit Antithrombin sind nicht bekannt. 5. 5.1. PHARMAKOLOGISCHE EIGENSCHAFTEN Pharmakodynamische Eigenschaften Pharmakotherapeutische Gruppe: Antithrombotika: Heparin-Gruppe. ATC-Code: B01AB02 Antithrombin, ein Glykoprotein mit einem Molekulargewicht von 58 kD und 432 Aminosäuren, gehört in die Gruppe der Serpine (Serin-Protease-Inhibitor). Es ist einer der wichtigsten natürlichen Hemmer der Blutgerinnung. Die am stärksten gehemmten Faktoren sind Thrombin und Faktor Xa, aber auch die Faktoren der Kontaktaktivierung, des intrinsischen Systems und der VIIa/Tissue Faktor Komplex. Die AntithrombinAktivität wird durch Heparin erheblich verstärkt, wobei die antikoagulatorischen Effekte von Heparin vom Vorhandensein von Antithrombin abhängen. Antithrombin enthält zwei funktionell wichtige Bereiche. Der eine enthält das reaktive Zentrum und stellt die Spaltungsstelle für Proteinasen wie Thrombin, eine Vorbedingung zur Bildung eines stabilen ProteinaseInhibitor-Komplexes, dar. Der zweite ist eine Glykosaminoglykan bindende Domäne und ist für die Interaktion mit Heparin und ähnlichen Substanzen, die die Hemmung von Thrombin beschleunigen, verantwortlich. Die gerinnungshemmenden Enzymkomplexe werden durch das retikuloendotheliale System eliminiert. Die Antithrombin-Aktivität bei Erwachsenen liegt zwischen 80–120%, die Spiegel bei Neugeborenen zwischen 40 und 60%. 5.2. Pharmakokinetische Eigenschaften Pharmakokinetikstudien von Antithrombin zeigten eine mittlere biologische Halbwertszeit von etwa 3 Tagen. Bei gleichzeitiger Therapie mit Heparin kann die Halbwertszeit auf etwa 1,5 Tage verkürzt sein. Bei sehr starkem Verbrauch kann sich die Halbwertszeit auf wenige Stunden verkürzen. 5.3. Präklinische Daten zur Sicherheit Humanes Antithrombin ist ein normaler Bestandteil des menschlichen Plasmas. Untersuchungen am Tier zur Toxizität nach einmaliger Verabreichung sind für den Patienten wenig aussagekräftig. Toxizitätsuntersuchungen am Tier mit wiederholten Verabreichungen sind aufgrund der Antikörperbildung gegen das fremde (menschliche) Protein undurchführbar. Es gibt keine Hinweise auf eine embryo-fötale Toxizität oder ein karzinogenes oder mutagenes Potential. 6. PHARMAZEUTISCHE ANGABEN Version 7.0 (QRD 3.0) ANTITHROMBIN III KONZENTRAT BAXALTA Zusammenfassung der Merkmale des Arzneimittels= Gebrauchsinformation 6.1. 7/8 Liste der sonstigen Bestandteile Pulver: • • • • Glukose; Natriumchlorid; Natriumcitrat.2H2O; Tris (hydroxymethyl)aminomethan. Lösungsmittel: • steriles Wasser für Injektionszwecke. 6.2. Inkompatibilitäten Das Arzneimittel darf, außer mit den unter Abschnitt 6.6 aufgeführten, nicht mit anderen Arzneimitteln gemischt werden. 6.3. Dauer der Haltbarkeit Das lyophilisierte Produkt hat eine Haltbarkeitsdauer von 3 Jahren. Da das Produkt kein Konservierungsmittel enthält soll ANTITHROMBIN III KONZENTRAT BAXALTA nach Rekonstitution unverzüglich verwendet werden. 6.4. Besondere Vorsichtsmaßnahmen für die Aufbewahrung Im Kühlschrank lagern (2°C – 8°C). Nicht einfrieren. In der Originalverpackung, vor Licht geschützt aufbewahren. Arzneimittel für Kinder unzugänglich aufbewahren. 6.5. Art und Inhalt des Behältnisses Die Flaschen mit lyophilisiertem Antithrombin sind aus Kalk-Natron-Glas, mit silikonbeschichteter Oberfläche, hydrolytische Klasse II. Die Flaschen mit dem Lösungsmittel (steriles Wasser für Injektionszwecke) sind aus Borosilikatglas, hydrolytische Klasse I. Dei Verschlüsse der Flaschen mit dem Produkt und der Flaschen mit dem Lösungsmittel sind aus Kautschuk. ANTITHROMBIN III KONZENTRAT BAXALTA ist erhältlich in Packungsgrößen mit 500 I.E. Antithrombin/10 ml Lösungsmittel und 1000 I.E. Antithrombin/20 ml Lösungsmittel. Jede Packung enthält auch: • 1 Transfernadel; • 1 Filternadel; • 1 Belüftungsnadel; • 1 Einwegnadel; • 1 Infusionsset. Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht. 6.6. Besondere Vorsichtsmaßnahmen für die Beseitigung und sonstige Hinweise zur Handhabung ANTITHROMBIN III KONZENTRAT BAXALTA soll erst unmittelbar vor der Verabreichung aufgelöst werden. Version 7.0 (QRD 3.0) ANTITHROMBIN III KONZENTRAT BAXALTA Zusammenfassung der Merkmale des Arzneimittels= Gebrauchsinformation 8/8 Nur das Infusionsset darf verwendet werden. Der gesamte Vorgang der Rekonstitution muss unter Beachtung aseptischer Techniken erfolgen. Danach soll die Lösung unverzüglich verwendet werden (da die Lösung keine Konservierungsmittel enthält). Vor Verabreichung soll das rekonstituierte Produkt auf sichtbare Partikel oder Verfärbung überprüft werden. Die Lösung muss klar und leicht opalisierend sein. Trübe Lösungen oder solche mit Niederschlag sind zu verwerfen. Nicht verwendete, gelöste Produkte oder Abfälle sind gemäß den geltenden Vorschriften zu entsorgen. Rekonstitution der lyophilisierten Substanz 1. Das verschlossene Fläschchen mit dem Lösungsmittel (steriles Wasser für Injektionszwecke) auf Raumtemperatur (maximal 37°C) erwärmen. 2. Die Schutzkappen der Fläschchen mit dem Konzentrat und mit dem Lösungsmittel entfernen (Abb. A) und die beiden Gummistopfen desinfizieren. 3. Die Schutzkappe der Transfernadel durch Drehen und Ziehen an der einen Seite entfernen (Abb. B). Mit der ungeschützten Nadel in den Gummistopfen des Fläschchens mit dem Lösungsmittel stechen (Abb. C). 4. Die Schutzkappe am anderen Ende der Transfernadel entfernen und dabei darauf achten, das ungeschützte Ende der Nadel nicht zu berühren. 5. Das Fläschchen mit dem Lösungsmittel umdrehen, und das ungeschützte Ende der Transfernadel in den Gummistopfen des Fläschchens mit dem Konzentrat stechen (Abb. D). Durch die Luftleere im Fläschchen mit dem Konzentrat wird das Lösungsmittel angesaugt. 6. Zugleich die Nadel und das Fläschchen mit dem Lösungsmittel vom Fläschchen mit dem Konzentrat entfernen (Abb. E). Durch Schütteln oder leichtes Drehen des Fläschchens mit dem Konzentrat wird der Lösungsvorgang beschleunigt. 7. Nach vollständigem Auflösen des Konzentrats die beigepackte Belüftungsnadel (Abb. F) einstechen, um den Schaum zu entfernen, der sich eventuell gebildet hat. Die Belüftungsnadel entfernen. Abb. A Abb. B Abb. C Abb. D Abb. E Abb. F Abb. G Intravenöse Injektion 1. Die Schutzkappe der beigepackten Filternadel durch Drehen und Ziehen entfernen. Die Nadel auf eine sterile Einwegspritze aufsetzen. Die Lösung in die Spritze aufziehen (Abb. G). 2. Die Filternadel von der Spritze entfernen, und die Lösung mittels der beigepackten Einwegnadel (oder mittels des beigepackten Infusionssets) langsam intravenös injizieren (maximale Injektionsgeschwindigkeit: 5 ml/Min.). Infusion Im Falle einer Infusion das beigepackte Einweg-Infusionsset mit adäquatem Filter verwenden (maximale Infusionsgeschwindigkeit: 5 ml/Min.). Version 7.0 (QRD 3.0) ANTITHROMBIN III KONZENTRAT BAXALTA Zusammenfassung der Merkmale des Arzneimittels= Gebrauchsinformation 7. 9/8 INHABER DER ZULASSUNG Baxalta Innovations GmbH, Industriestrasse 67, A-1221 Wien, Österreich 8. ZULASSUNGSNUMMERN ANTITHROMBIN III KONZENTRAT BAXALTA, 500 IE, Pulver und Lösungsmittel zur Herstellung einer Injektionslösung oder Infusionslösung: BE273971. ANTITHROMBIN III KONZENTRAT BAXALTA, 1000 IE, Pulver und Lösungsmittel zur Herstellung einer Injektionslösung oder Infusionslösung: BE274005. Verschreibungsstatus Verschreibungspflichtig 9. DATUM DER ERTEILUNG DER ZULASSUNG/VERLÄNGERUNG DER ZULASSUNG Datum der Erteilung der Zulassung: 11. Juli 2005 Datum der letzten Verlängerung der Zulassung: 11. Juli 2010. 10. STAND DER INFORMATION Das Zulassungsdatum: 02/2017 Version 7.0 (QRD 3.0)