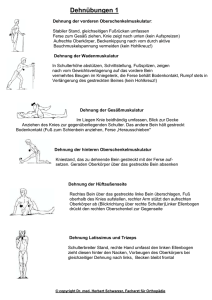
Koronare Herzerkrankungen sind eine der häufigsten
Werbung

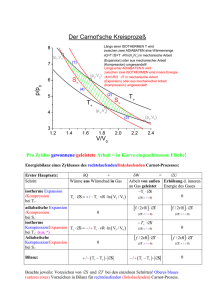
EIN MODIFIZIERTES SYNTHETISCHE-APERTUR-VERFAHREN ZUR KORREKTUR GEOMETRISCHER ARTEFAKTE IN DER INTRAVASKULÄREN ULTRASCHALL-ELASTOGRAPHIE Christian Perrey*, Wilko Wilkening, Bernhard Brendel und Helmut Ermert Lehrstuhl für Hochfrequenztechnik, Ruhr-Universität Bochum, Deutschland * [email protected] I. EINLEITUNG Koronare Herzerkrankungen sind eine der häufigsten Todesursachen in den westlichen Industrieländern. Als besonders gefährlich werden instabile (‚weiche’) Plaques angesehen, die an 80 bis 90% aller akuten Koronarereignisse beteiligt sind. Der kathetergestützte Intravaskuläre Ultraschall (IVUS) ist der derzeitige Goldstandard zur Beschreibung morphologischer Veränderungen der Koronargefäße, ermöglicht jedoch keine eindeutige Differenzierung von stabilen und instabilen Plaques. Letztere weisen im Vergleich zu kalzifizierten Koronarplaques jedoch unterschiedliche mechanische Eigenschaften auf, die mit der Methode der UltraschallElastographie visualisert werden können. Bei diesem Verfahren wird das zu untersuchende Gewebe durch Blutdruckschwankungen radial komprimiert und die daraus resultierende Dehnung anhand mehrerer, bei unterschiedlichen Kompressionszuständen aufgenommener Ultraschallbilder geschätzt. Es existieren verschiedene Algorithmen zur Elastographie mit Intravaskulärem Ultraschall [2, 3], die Verschiebung und Dehnung des Gewebes in Richtung des Schallstrahls durch Kreuzkorrelation schätzen. Die Kompression der Gefäßwände erfolgt in axialer Richtung, ausgehend von der Lumenmitte. Wenn der Schallwandler sich nicht in der Mitte des Gefäßlumens befindet, erfolgt die Kompression nicht parallel zu den Schallstrahlen, was zu systematischen Fehlern bei der Dehnungsschätzung führt [3]. Die bei IVUS verwendeten Schallwandler besitzen zirkulare Wandler-Arrays, eine Fokussierung der Schallstrahlen erfolgt nach dem Prinzip der Synthetischen Apertur (SAFT). In dieser Arbeit wird ein modifiziertes Rekonstruktionsverfahren vorgestellt, das bei exzentrischen Wandlerpositionen erlaubt, die Schallstrahlen in radialer Richtung, also parallel zur Kompression des Gewebes, zu rekonstruieren und die systematischen Fehler bei der Schätzung zu vermeiden. Zur Verifikation des Verfahrens werden Schallfeldsimulationen durchgeführt, bei denen der Schallwandler an verschiedenen Positionen innerhalb eines zylindrischen Gefäßes positioniert wird. II. METHODEN Für die Schätzung der Dehnungsverteilung werden hochfrequente Ultraschalldaten verwendet, die vor und nach einer Kompression des Gewebes aufgenommen werden. Durch diese Kompression treten in den Fortschritte der Akustik - DAGA 2002, Bochum, S. 687-688. - 687 - Echosignalen lokale Verschiebungen auf, die anhand von Kreuzkorrelationsmethoden geschätzt werden können. Der Phasenverlauf der Kreuzkorrelation zweier Signale weist an der Stelle des Betragsmaximums eine Nullstelle auf, die iterativ mit dem Newton’schen Verfahren bestimmt werden kann. Die Dehnung wird aus der Verschiebung durch Bildung der Ableitung berechnet. Katheter P2 Schallstrahl C M R Ko ale adi mp d α P1 ion d´ s res Lumen Lumenmitte Abb. 1: Fehler in der Verschiebungsschätzung aufgrund des Winkels zwischen Schallstrahl und radialer Kompression Bei Untersuchungen mit IVUS ist der Schallwandler wie in Abb. 1 gezeigt oft exzentrisch innerhalb des Gefäßes positioniert. Wenn der Druck innerhalb des Lumens steigt, wird das (bei den folgenden Simulationen als homogen angenommene) Gewebe komprimiert und so radial verschoben. Die dabei geschätzte Verschiebung eines Gewebselementes d’ ist geringer als die tatsächliche Verschiebung d aufgrund des Winkels α zwischen der Richtung der Kompression und dem Ultraschallstrahl [3]. Nur wenn der Schallwandler in der Lumenmitte positioniert wird, tritt ein solcher systematischer Fehler nicht auf. Fokussierung mit Synthetischer Apertur Die verwendeten Schallwandler besitzen 64 auf dem Katheterumfang (1.2 mm) angeordnete Arrayelemente. Das zur Bildrekonstruktion verwendete Verfahren ist in [1] beschrieben. Es handelt sich um ein multistatisches Rekonstruktionsverfahren, bei dem eine Aperturbreite von 14 Elementen gewählt wurde. Sende- und Empfangselemente werden anhand eines Multiplexers sukzessive umgeschaltet, es werden 64 ×14 = 896 verschiedene Signale aufgenommen, aus denen durch phasen- richtige Überlagerung ein Ultraschallbild rekonstruiert wird. Bei der hier vorliegenden Geometrie kann die Position des Schallwandlers innerhalb des Lumens anhand des Ultraschallbildes durch Detektion der Gefäßkontur bestimmt werden. Mit Kenntnis dieser Position können aus den unfokussierten Daten wie in Abb. 2 gezeigt Schallstrahlen in radialer Richtung rekonstruiert werden. Die Ergebnisse nach erfolgter Refokussierung der Schallstrahlen sind in Abbildung 4 dargestellt. Die Dehnungsverteilung weist keinen winkelabhängigen Fehler mehr auf. Der weiße Kreis in der Mitte deutet den Ursprung der Schallstrahlen an, die Katheterposition ist weiterhin exzentrisch. weich y C α P1 hart γ M 15 mm β Abb. 4: Korrigiertes B-Bild und Elastogramm eines simulierten Gefäßes bei einer 40% exzentrischen Katheterposition x III. DISKUSSION Die Simulationen belegen, dass eine exzentrische Katheterposition bei der Abbildung der Dehnung mit IVUS zu systematischen Fehlern führt. Es wurde gezeigt, dass diese Fehler durch geeignete Refokussierung der Ultraschallsignale mit einem modifizierten SAFT-Ansatz korrigiert werden können. Die Anwendbarkeit dieser Methode zur Korrektur der Dehnungsabbildung In Vivo muss jedoch im weiteren untersucht werden, da die Gefäßwände keine regelmäßigen Konturen aufweisen und in ihren mechanischen Eigenschaften inhomogen sind. Abb. 2 Geometrie der geänderten SAFT Rekonstruktion Um einen von der Lumenmitte M ausgehenden radialen Strahl zu rekonstruieren, muss für jeden Punkt die entsprechende Subapertur sowie der Abstand zum Kathetermittelpunkt bestimmt werden (Winkel α und Abstand CP1 ). Bei bekannter Katheterposition, bestimmt durch den Winkel γ und den Abstand MC , können α und CP1 durch einfache geometrische Berechnungen ermittelt werden. Alle Signale der so bestimmten Apertur werden dann mit entsprechenden Laufzeitverzögerungen überlagert, was für jede Position des Schallstrahls durchgeführt wird. LITERATURHINWEISE [1] ERGEBNISSE Abbildung 3 zeigt das simulierte Ultraschallbild eines homogenen Gefäßes sowie die zugehörige grauwertkodierte Dehnungsverteilung. Die Position des Schallwandlers ist durch einen weißen Kreis angedeutet. Die geringere Dehnung bei 3 bzw. 9 Uhr wird durch den zuvor beschriebenen geometrischen Fehler bei exzentrischer Katheterposition hervorgerufen. [2] [3] weich M. O'Donnell, M. J. Eberle, D. N. Stephens, J. L. Litzza, K. San Vicente and B. M. Shapo, "Synthetic Phased Arrays for Intraluminal Imaging of Coronary Arteries", " IEEE Trans. Ultrason. Ferroelec., Freq. Cont., Vol. 44, No.3, pp. 714-721, 1997 C. Perrey, G. Braeker, W. Bojara und H. Ermert, „Ein Elastographie-System zur Charakterisierung koronarer Plaques mit intravaskulärem Ultraschall“, Biomedizinische Technik, Band 46, Ergänzungsband 1, S. 66-67, 2001 C.L De Korte, E. I. Cespedes, and A. F. W. Van der Steen, ” Influence of catheter position on estimated strain in intravascular elastography”, IEEE Trans. Ultrason. Ferroelec., Freq. Cont., Vol. 46, No.3, pp. 616-625, 1999 Ein Beitrag aus dem Kompetenzzentrum Medizintechnik Ruhr (KMR), Bochum, gefördert vom BMBF, Aktenzeichen: 13N8079 hart 15 mm Abb. 3: B-Bild und Elastogramm eines simulierten Gefäßes bei einer 40% exzentrischen Katheterposition. Fortschritte der Akustik - DAGA 2002, Bochum, S. 687-688. - 688 -