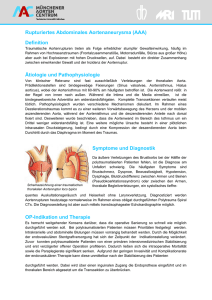
Magnetresonanztomographische Nachuntersuchung nach
Werbung

Zentrum für Chirurgie Klinik für Herz-, Thorax- und Gefäßchirurgie Ärztlicher Direktor: Prof. Dr. med. Andreas Liebold Magnetresonanztomographische Nachuntersuchung nach endovaskulärer Therapie der akuten traumatischen Aortenruptur Dissertation zur Erlangung des Doktorgrades der Medizin der Medizinischen Fakultät der Universität Ulm Stephan Trumpp Diepholz 2017 Amtierender Dekan: Prof. Dr. rer. nat. Thomas Wirth 1. Berichterstatter: Prof. Dr. Orend 2. Berichterstatter: Prof. Dr. Rasche Tag der Promotion: 04.05.2017 Inhaltsverzeichnis Abkürzungsverzeichnis III 1. Einleitung 1 1.1 Die akute traumatische Aortenruptur 1 1.2 Pathomechanismus und Lokalisation der traumatischen 2 Aortenruptur 1.3 Therapie der traumatischen thorakalen Aortenläsion: 3 konventionelle versus endovaskuläre Operation 1.4 Komplikationen nach thorakaler endovaskulärer 5 Aortenchirurgie 1.5 Postoperative Nachuntersuchungen mittels 7 Computertomographie 1.6 Ziele der Arbeit 9 2. Material und Methoden 10 2.1 Patientenkollektiv 10 2.2 Bildgebende Verfahren: Computertomographie 11 2.2.1 Einführung 11 2.2.2 Bilderzeugung 13 2.2.3 Bildkomponenten 15 2.3 18 Bildgebende Verfahren: Magnetresonanztomographie 2.3.1 Einführung 18 2.3.2 Bilderzeugung 21 2.4 22 Implantierte Endoprothesen I 2.5 Erhebung des Bildmaterials bei computer- und 24 magnetresonanztomographischen Nachuntersuchungen 2.6 Relevante Artefaktbildung und qualitative Darstellung der 28 betrachteten Endoprothesen im Vergleich 2.7 Planimetrische Vergleichsmessungen der computer- und 35 magnetresonanztomographischen Datensätze 2.8 Statistische Testverfahren 38 3. Ergebnisse 40 3.1 Alters- und Geschlechtsverteilung 40 3.2 Manuelle Vergleichsmessungen der Stentdurchmesser 40 3.3 Manuelle Vergleichsmessungen der Stentdurchmesser 43 nach landmarkenbasierter Registrierung durch 3DSlicer 3.4 Manuelle Vergleichsmessungen der registrierten 47 Bilddatensätze durch einen unabhängigen Korrektor 4. Diskussion 52 5. Zusammenfassung 59 6.Literaturverzeichnis 61 7. Appendix 68 8. Danksagung 71 9. Lebenslauf 72 II Abkürzungsverzeichnis A. Arteria Abb. Abbildung Angio Angiographie ASCS Acute Stent Compression Syndrome ATAR Akute traumatische Aortenruptur Bsp. Beispiel bzgl. bezüglich bzw. beziehungsweise ca. circa CE contrast enhanced CI confidence interval CT Computertomographie d.h. das heißt dist. Distal EKG Elektrokardiogramm ePTFE expanded Polytetrafluoroethylene etc. et cetera et al. et alii EVAR endovascular aortic repair eventl. Eventuell FFS Feet-First-Supine FLASH Fast-Low-Angle-Shot Gl Gleichung III h Hora HF Hochfrequenz HU Hounsfield Unit ICD implantable cardioverter-defibrillator Kg Kilogramm KM Kontrastmitte Lig. Ligamentum max. maximal Mhz Megahertz min. Minute mind. Mindestens MIT Massachusetts Institute of Technology ml Milliliter mm Millimeter MR magnetresonanz MRI Magnetic Resonance Imaging MRT Magnetresonanztomographie ms Millisekunde mSV Millisievert NFS Nephrogene Systemische Fibrose Nr. Nummer o.g. oben genannt OR Odds Ratio PC Personal Computer Prox. Proximal IV ROI Region of Interest s Sekunde SCT Spiral-CT SHT Schädel-Hirn-Trauma SIRS Systemic Inflammatory Response Syndrome SNR Signal-to- Noise-Ratio sog. so genannt SSFP Steady-State-Free-Precession Sv Sievert TAA Thorakales Aortenaneurysma TAAA Thorakoabdominales Aortenaneurysma TAG Excluder Bezeichnung für Stentprothese TAR Traumatische Aortenruptur TEVAR Thoracic Endovascular Aortic Repair USA United States of America U.S. United States Vgl. Vergleich vs. versus z.B. zum Beispiel 3D dreidimensional V 1. Einleitung 1.1 Die akute traumatische Aortenruptur Die akute traumatische thorakale Aortenruptur ist nach letalen Kopfverletzungen die zweithäufigste Todesursache bei Patienten nach erlittenem Dezelerationsoder stumpfem Thoraxtrauma [50]. In Zahlen bedeutet dies eine Inzidenz von ca. 8.000 solcher Unfallopfer pro Jahr (Nordamerika) [15]. Die Mortalitätsrate solcher Aortenverletzungen liegt bei über 90% [47]. Bei erlittener kompletter thorakaler Aortenruptur verstirbt der Patient meist am Unfallort aufgrund eines hämorrhagischen Schocks mit konsekutiver respiratorischer und kardialer Insuffizienz. zunehmender Durch stetige technischer Verbesserungen Innovationen in der bezüglich Notfallrettung sowie Fahrsicherheit (z.B. Sicherheitsgurt, Airbag) seitens der Automobilindustrie ist die Zahl der Patienten, welche lebend ein Traumazentrum erreichen, in den letzten Jahrzehnten kontinuierlich angestiegen [43, 55]. Unbehandelt erliegt nahezu jeder 2. Patient seinen Verletzungen innerhalb der ersten 24 Stunden [38, 29]. Patienten, welche sofort einer notfallmäßigen operativen/konservativen Therapie unterzogen wurden, zeigten dennoch eine Gesamtmortalität zwischen 20% bis 35% [48, 51]. Meist handelt es sich bei solch schweren Verletzungen um polytraumatisierte Patienten nach erlittenem Verkehrsunfall (Auto-/Motorradunfall) oder Stürzen aus großer Höhe. Laut Studienlage beträgt der Patientenanteil, welcher ursächlich in einen Autounfall involviert war, zwischen 70% bis 80% [16, 14, 10]. Hierbei handelt es sich wiederum meist um Männer mittleren Alters (70%-81%) mit einem Durchschnittsalter zwischen 31 bis 41 Jahren [16, 10]. -1- 1.2 Pathomechanismus und Lokalisation der traumatischen Aortenruptur (TAR) Die akute traumatische Aortenruptur/-dissektion ist hauptsächlich Folge eines kombinierten Kompressions-Dezelerationstraumas (z.B. frontaler Autounfall). Hierbei kommt es zu einer durch die Dezeleration bedingte zentrifugale Krafteinwirkung auf den Aortenabschnitt (proximale im Bereich Aorta des Lig. descendens). arteriosum Der befestigten Aortenisthmus wird schlagartig übermäßig gestreckt. Eine weitere Krafteinwirkung auf den Aortenisthmusbereich findet sich bei erfolgter Thorax-/Abdomenkompression durch eine aufwärtsgerichtete Bewegung des Mediastinums [55, 7]. Gleichzeitig wird das Herz zwischen Sternum und Wirbelsäule so stark komprimiert, dass es zu einer dramatischen Erhöhung des aortalen Blutdrucks kommt. Es wird weiter angenommen, dass es weiterhin zu einer Einklemmung der Aorta deszendenz im Bereich des Hiatus aorticus kommt, wodurch der Blutabfluss behindert wird. Dies trägt zusätzlich zur Entstehung eines plötzlichen aortalen Blutdruckanstiegs bei (Wasserhammer Effekt) [55]. Hinzu kommt, dass die strukturellen Unterschiede der Aortenwand im Isthmusbereich gegenüber des aszendierenden bzw. deszendierenden thorakalen Aortenabschnitts möglicherweise ebenfalls eine Rolle spielen [53]. Beim Trauma wird die Isthmusregion, welche sich zwischen der fixierten Aorta deszendenz und dem nach kranial bewegenden Herzen/Aortenbogen befindet, hohen Dreh- und Zugkräften ausgesetzt. Bei zusätzlich immens erhöhten Blutdruckverhältnissen kann es dann zur aortalen Ruptur im Isthmusbereich kommen. Der Aortenisthmus ist sozusagen die „Achillessehne“ der thorakalen Aorta. 85% 95% der traumatischen thorakalen Aortenläsionen finden sich in diesem Bereich direkt distal der A. subclavia sinistra [14, 32, 34]. Dieser Bereich wird auch als „loco typico“ der Aortenruptur bezeichnet. -2- Therapie 1.3 der traumatischen thorakalen Aortenläsion: konventionelle versus endovaskuläre Operation Seit vielen Jahren ist die offene chirurgische Therapie ein etabliertes Verfahren zur Behandlung des TAA/TAAA sowie der TAR. Je nach Lokalisation wird bei der TAR der Aorta aszendenz oder des Aortenbogens die operative Versorgung über eine mediane Sternotomie durchgeführt. Bei Verletzungen im Bereich des Anfangsteils der Aorta deszendenz („loco typico“) wird der Thorax über eine linksposterolaterale Thorakotomie eröffnet. Dies geschieht in Rechtsseitenlagerung sowie Einlungenbeatmung. Abhängig von der Ausdehnung der Verletzung wird die Aorta proximal und distal davon abgeklemmt und entweder direkt End-zu-End anastomosiert (clamp-and-sew Technik) oder, falls nötig, eine Rohrprothese interponiert. Heutzutage ist eine Operation in einfacher Abklemmtechnik jedoch nur bei kleineren Defekten (Coarctatio, Isthmusstenosen) vertretbar, da bei Überschreiten einer 30 min. aortalen Abklemmzeit ohne sonstige präventive Maßnahmen (Hypothermie, Linksherzbypass) die Gefahr einer irreversiblen spinalen Ischämie exponentiell ansteigt und nach 60 min. zu 95% neurologische Folgeschäden entstehen [31]. Das postoperative Paraplegierisiko hängt hauptsächlich von der aortalen Abklemmzeit, Ausdehnung der Aortenruptur, des Patientenalters, einer eventl. bestehenden Niereninsuffizienz [8, 58] sowie der perioperativen Hypotension ab. Durch Abklemmen der thorakalen Aorta kommt es zu einem gesteigerten zerebralen Blutfluss sowie einem ansteigenden intrakraniellen Druck. Letztlich führt dies zu einer Druckerhöhung im Spinalkanal. Im weiteren Verlauf wird diese aufgrund eines reperfusionsbedingten Gewebeödems verstärkt. Spinalmarködem und ansteigender Druck im rigiden Spinalkanal führen somit zu einer Druckschädigung des gesamten Rückenmarks und zum Zusammenbruch der Mikrozirkulation [19]. Die fehlende distale Aortenperfusion durch thorakales Crossclamping führt zusätzlich zu einer Ischämie aller inneren Organe. Hierdurch kommt es zur Entwicklung eines SIRS [24]. Sehr wahrscheinlich ist eben jener Vorgang ein wesentlicher Faktor bei der postoperativen Entwicklung eines Einzel- bzw. Multiorganversagens. Trotz verschiedener Überwachungsmaßnahmen (Liquordrainage, Neuromonitoring) des intrakraniellen/intraspinalen Drucks sowie unterschiedlicher -3- Operationstechniken (Shuntverfahren, extrakorporale Zirkulation) besteht auch heute noch ein Paraplegierisiko zwischen 2.3% bis 25.5% [47, 9]. Mit Hilfe der Herz-Lungen-Maschine sind zwar niedrigere Paraplegieraten zu erzielen, aufgrund der Vollheparinisierung besteht jedoch bei den polytraumatisierten Patienten ein stark erhöhtes Blutungsrisiko mit einer erhöhten Mortalitätsrate im Vergleich zu verschiedenen Shunttechniken ohne Antikoagulantienzusatz [9]. Bei den meisten Patienten nach TAR bestehen zusätzlich multiple Lungenkontusionen. Bei Einlungenbeatmung kann es hier bereits intraoperativ zu einer dramatischen respiratorischen Insuffizienz kommen. Die Eröffnung des Thorax bietet Keimen ebenfalls die Möglichkeit, für weitere pulmonale oder systemische infektiöse Komplikationen zu sorgen [28, 49]. Im Gegensatz zur offen chirurgischen Therapie liefert TEVAR seit Mitte der 1990er Jahre vielversprechende Ergebnisse [17, 20, 27] und sollte daher als primäre Therapie favorisiert werden. Mit einer kleinen Inzision im Bereich der Leistenregion wird die A. femoralis communis punktiert. Anschließend erfolgt die Anlage einer Schleuse, über die dann das Einführen eines Stentgrafts in das Gefäß ermöglicht wird. Unter Durchleuchtung kann nun der entsprechende Stentgraft mit Hilfe eines Führungsdrahts an die Rupturstelle geführt, richtig positioniert und entfaltet werden. In einem Reviewartikel berichteten Lettinga et al. über eine Gesamtmortalität bei 132 Patienten bezüglich des offen chirurgischen Verfahrens von 18.9%. Unter TEVAR wurde die Gesamtmortalität bei 73 Patienten mit lediglich 4% angegeben [37]. Xenos et al. zeigten in einer Meta-Analyse, welche insgesamt 17 nicht randomisierte Kohortenstudien von 2003 bis 2007 beinhaltete, eine ebenfalls deutlich reduzierte Gesamtmortalität (OR 0.44; 95% CI, 0.25-0.78; P = .005) bei der endoluminalen Therapie der traumatischen Aortenruptur. Insgesamt waren 589 Patienten beteiligt. 389 wurden offen operiert, 220 wurden einer TEVAR unterzogen. 16 der 17 Studien beinhalteten Daten bezüglich des postoperativen Paraplegierisikos. Hier wurden 215 Patienten mittels Endograft und 333 offen chirurgisch behandelt. Auch hier sah man ein signifikant niedrigeres Risiko bei der -4- endoluminalen Gruppe (OR 0.32; 95% CI, 0.1-0.93; P = .037) [70]. Ein Jahr später (2009) veröffentlichte dieselbe Forschungsgruppe eine Aktualisierung der eben erwähnten Studie mit ähnlichen Ergebnissen [71]. Die reduzierte Gesamtmortalität sowie das geringere Paraplegierisiko bei TEVAR sind auf die minimalinvasive, endovaskuläre Operationstechnik zurückzuführen. Insgesamt liegt eine kürzere Operationszeit vor, in der das Auftreten von Komplikationen aufgrund von Begleitverletzungen reduziert wird. Die Vermeidung einer extrakorporalen Zirkulation macht den Einsatz von Heparin überflüssig. Intraabdominale Blutungen, ein Schädel-Hirn-Trauma (SHT) oder multiple Frakturen stellen somit keine relative Kontraindikation für eine frühe Behandlungsstrategie des meist lebensbedrohlichen Allgemeinzustands mehr dar. Des Weiteren besteht bei zusätzlicher Milz- und/oder Leberruptur die Möglichkeit einer kombinierten Therapie, bestehend aus TEVAR und einer therapeutischen Embolisation blutender intraabdominaler Organe. Patienten mit pulmonalen Schäden profitieren ebenfalls von der fehlenden Notwendigkeit einer Thorakotomie [37]. 1.4 Komplikationen nach thorakaler endovaskulärer Aortenchirurgie Neben den multiplen Vorteilen, welche die TEVAR gegenüber einer offen chirurgischen Intervention bei der TAR bietet, dürfen mögliche Komplikationen, die durch eine endoluminale Stentgraftimplantation verursacht werden, keinesfalls vernachlässigt werden. Gerade bei diesen Patienten spielt das meist jüngere Lebensalter eine entscheidende Rolle. Der Aortenbogen stellt sich häufig mit scharfem Winkel zwischen auf- und absteigendem aortalen Schenkel dar. Hier kann es schwierig werden, für eine ordentliche Ankerzone zu sorgen, in der der Stentgraft eng an der Aortenwand anliegt. Steht die Prothese ins Lumen über und bildet nun mit der aortalen Wand einen triangulären Raum, besteht die Gefahr eines akuten Stentkompressionssyndroms (ASCS) mit möglichem totalen Prothesenkollaps [46] sowie der Entstehung eines „Endoleaks“. -5- Bei ca. 9% der Pateinten tritt nach TEVAR ein sog. „Endoleak“ oder eine distale Embolisation auf [30]. Einen kurzen Überblick der Klassifikation der Endoleckagen bietet Abbildung 1. Abbildung 1: Klassifikation der Endoleckagen nach Implantation einer endovaskulären Stentprothese [33] Bei den Endoleckagen sind 4 verschiedene Typen nach Ursache und Lokalisation zu unterscheiden. Undichte Stellen im Bereich der proximalen oder distalen Ankerzonen bzw. an bestehenden Übergangszonen zweier aneinander gekoppelter Endoprothesen (Endoleak Typ1 oder 3) bergen weiterhin eine Rupturgefahr des (Pseudo-)Aneurysmasacks und müssen umgehend mittels „overstenting“ verschlossen werden [33]. Ferner stellt die Prothesenmigration eine Gefahr dar. Ursächlich hierfür ist eine zunehmende Vergrößerung des Aortendurchmessers. Im Laufe eines Lebens vergrößert sich der Aortendurchmesser um ca. 1.5 mm alle 10 Jahre [25]. Somit könnte es bei den meist jungen Patienten mit zunehmendem Alter zu einer Lockerung der Ankerzonen kommen. Hinzu kommt, dass der Endograft ständiger wechselnder dynamischer Kräfte ausgesetzt ist, welche ebenfalls zu Konformationsänderungen an der Prothese führen können. Die o.g. Endoleaks können hierbei selbstverständlich ebenfalls entstehen. -6- 1.5 Postoperative Nachuntersuchungen mittels Computertomographie Bei der endovaskulären Therapie der TAR existieren bis heute keine validen Langzeitergebnisse randomisierter prospektiver Studien. Neben all den Vorteilen in der Akutphase gegenüber der klassischen offenen chirurgischen Therapie müssen die Ergebnisse dieser Technik kontinuierlich kontrolliert werden, um mögliche Langzeitkomplikationen frühzeitig zu erkennen. Derzeit ist das jährlich durchgeführte Spiral-Thorax-CT mit Kontrastmittel bei den bildgebenden Verfahren die optimale Vorgehensweise (Goldstandart). Bei einer einzigen Thorax-CT Aufnahme ist der Patient einer effektiven Dosis ionisierender Strahlung von ca. 7mSv ausgesetzt. Zu beachten ist, dass der Einheit Sv bereits alters- und geschlechtsspezifisch gemittelte Gewebewichtungsfaktoren zugrunde gelegt wurden. Statistisch (berechnet auf die U.S. amerikanische Gesamtbevölkerung) kann eine Strahlungsexposition von 10mSv bei 1 von 1000 Patienten im Laufe seines weiteren Lebens bereits ein solides Tumorleiden auslösen [2]. Ein 40jähriger Patient, welcher sich über 30 Jahre einer jährlichen Kontroll-CT Untersuchung unterziehen musste, wäre einer kumulativen Strahlendosis von ca. 210mSv innerhalb dieses Zeitraums ausgesetzt, wodurch er ein signifikant erhöhtes malignes Tumorrisiko hätte [44]. Alternativ wäre wünschenswert. Vermeidung hierzu die Fehlende nephrotoxischer sichere Anwendbarkeit ionisierende jodhaltiger einer MR-Bildgebung Strahlungsbelastung Kontrastmittelgabe sowie die steigern die Attraktivität der MR-Bildgebung zusätzlich. Aufgrund der durchschnittlich meist jungen Patienten, welche eine thorakale Aortenruptur überleben konnten, ist die fehlende Strahlenbelastung, bei bisher mindestens einer jährlichen Kontrolluntersuchung, daher von besonderer Bedeutung und sollte so gering wie möglich gehalten werden. Derzeit angewendete MR-Kontrastmittel sind für ihre Sicherheit bekannt. Übelkeit, Veränderung des Geschmackssinns sowie Urtikaria sind gelegentliche Nebenwirkungen, von denen in der Vergangenheit berichtet wurde. Allerdings wurde 2006 ein kausaler Zusammenhang zwischen Gd3+-basierenden -7- Kontrastmitteln (gadoliniumhaltige KM wie z.B. Omniscan, OptiMARK) und der Entwicklung einer nephrogenen systemischen Fibrose (NFS) bei Patienten mit einer fortgeschrittenen Nierenerkrankung nachgewiesen [21, 42]. Aktuell wird angenommen, dass das Risiko, an einer NSF zu erkranken, in Zusammenhang mit den physiochemischen Eigenschaften des Chelatkomplexes steht. Hierbei spielt die Freisetzung von Gadolinium-Ionen eine Rolle. Die Entwicklung einer NSF nach Verwendung von Kontrastmitteln mit zyklischer Struktur (z.B. Dotarem, Gadovist, ProHance) wurde bisher nicht nachgewiesen. Krankheitsfälle traten ebenfalls bisher keine auf. Das Erkrankungsrisiko einer NSF kann somit durch die Verwendung zyklisch strukturierter Kontrastmittel vermieden werden. Eine Langzeitanwendung ist daher ebenfalls problemlos möglich. Bei unserem Patientenkollektiv wurden die MR-Untersuchungen unter Verwendung von Magnevist (linear-ionische Struktur) durchgeführt, welches bezüglich der Entwicklung einer NSF ebenfalls verantwortlich sein kann. Bisher sind jedoch nur sehr wenige Fälle bekannt. Magnevist gehört zu den am häufigsten verwendeten Kontrastmitteln bei der Magnetresonanztomographie. Kontraindikationen bezüglich unseres Patientenkollektivs bestanden keine. -8- 1.6 Ziele der Arbeit Ziel der Arbeit ist es, die Anwendbarkeit der MRT als planimetrisches diagnostisches Mittel bei Nachkontrollen im Vergleich zur CT Standarddiagnostik zu prüfen. In diesem Zusammenhang stellen sich folgende Fragen: - Kann die MRT vergleichbares Bildmaterial zur CT erbringen, d.h. ist der Stentgraft eindeutig zu sehen (Lagebeurteilung des Stents) und von den benachbarten anatomischen Strukturen (z.B. Anliegen an der Aortenwand) klar abzugrenzen? - Sind somit auch planimetrische Messungen (z.B. Sagittal- und Transversaldurchmesser) möglich? - Stellen MRT typische Artefaktbildungen der untersuchten Endoprothesen ein Problem bei der Auswertung des Bildmaterials dar? - Sind Komplikationen (z.B. Endoleaks) nach TEVAR ebenso effektiv mittels MRT Diagnostik frühzeitig zu erkennen? -9- 2. Material und Methoden 2.1 Patientenkollektiv In der Klinik für Herz- Thorax- und Gefäßchirurgie der Universität Ulm wurden seit 1999 bis 2008 ca. 40 Patienten mittels transfemoraler Stentgraftimplantation bei ATAR innerhalb 24h nach Ereignis therapiert. Aus diesem Patientenkollektiv konnten insgesamt 21 Patienten (14 Männer, 7 Frauen; Durchschnittsalter: 39,1 Jahre; Standardabweichung: +/- 16,9) für die vorliegende Vergleichsstudie einbezogen werden. Alle Patienten erlitten eine traumatische Aortenruptur im Übergansbereich des Aortenbogen und der Aorta deszendenz, dem sog. „loco typico“, welcher bei einem Dezelerationstrauma hohen Dreh- und Zugkräften ausgesetzt ist. In über 90% der Fälle handelte es sich um Verkehrsunfälle mit frontalen Fahrzeugkollisionen. 13 Patienten wurde eine thorakale Endoprothese der Firma Gore TAG® (Gore Associated GmbH, Putzbrunn Germany) implantiert, 8 Patienten wurden mittels eines Stentgraft der Firma Medtronic (Medtronic World Medical, Sunrise, FL, USA) Modell Valiant® behandelt Zur Nachuntersuchung wurden alle Patienten nach erfolgter Operation den nach Goldstandard üblichen regelmäßigen bildgebenden Verfahren mittels SCT mit Kontrastmittel unterzogen. Zusätzlich wurde hierbei im Rahmen unserer Studie weiteres Bildmaterial der Endoprothese durch eine MRT (3D Angiogramm der thorakalen Aorta mit und ohne Kontrastmittel) erhoben. Dies erfolgte zwischen dem 8. und 2417. Tag nach Intervention. Folgende Einschlusskriterien lagen vor: - Thorakale traumatische Aortenrupturen, welche mittels endovaskulärem Stentgraft in der Klinik für Herz-, Thorax- und Gefäßchirurgie Universitätsklinik Ulm versorgt wurden, unabhängig von der Zeit zwischen Implantation und Nachuntersuchung. - Patienten im Alter von 18-70 Jahre - Einverständniserklärung des Patienten nach Aufklärung - 10 - Folgende Ausschlusskriterien waren gegeben: - Das Vorliegen einer Schwangerschaft oder unsichere Kontrazeption - Nicht einwilligungsfähige Patienten - Patienten/Probanden mit kardialer Instabilität (eingeschränkte linksventrikuläre Pumpfunktion, akuter Myokardinfarkt < 7 Tage, dekompensierte Herzinsuffizienz) - Patienten/Probanden mit ausgeprägter Klaustrophobie - Patienten/Probanden mit Herzschrittmacher oder implantierten Defibrillatoren (ICD) - Patienten/Probanden mit Metallsplitterverletzungen der Augen oder MRTinkompatiblen metallischen Einschlüssen oder Implantaten - Patienten/Probanden mit großflächigen Tätowierungen - Patienten/Probanden mit nicht entfernbaren Piercings - Patienten/Probanden, die an einer anderen Studie teilnehmen - Mitarbeiter der Studie Das Studienprotokoll wurde durch eine unabhängige Ethikkommission der Universität Ulm geprüft und akzeptiert (15.05.2008; Az. 24/08). Alle Probanden wurden ausführlich und umfassend informiert und erteilten ihr schriftliches Einverständnis. 2.2. Bildgebende Verfahren: Computertomographie 2.2.1 Einführung Im Jahr 1972 wurde die Computertomographie erstmalig von Godfrey Hounsfield in Zusammenarbeit mit Allan M. Cormack als weiteres bildgebendes Verfahren in der Humanmedizin eigesetzt. Hounsfield`s Idee war es, im Gegensatz zum konventionellen Röntgen, überlagerungsfreie Schichtaufnahmen zu erhalten. Röntgenstrahlen sollten hierzu multiaxial aus verschiedenen Projektionswinkeln das zu untersuchende Objekt durchdringen und die daraus resultierende Signalabschwächung von einem direkt gegenüberliegenden Detektor registriert werden. Ein Computer, welcher mit dem Detektor in Verbindung steht, sollte dann nach vorgegebenen Algorithmen diese „Datensätze“ weiter zu verwertbarem - 11 - Bildmaterial umwandeln. Abbildung 2: Prinzip einer CT-Messung 1972: Röntgenstrahl durchleuchtet Objekt in unterschiedlichen Abtastwinkeln (Translations- und Rotationsbewegung) zur Bestimmung der Schwächungskoeffizienten [63]. Heutzutage befinden sich mehrheitlich Mehrzeilen–Spiral-Computertomographen der 3. Generation in klinischem Einsatz. Dies sind sog. Rotate-Rotate Geräte. Dabei rotieren die Strahlungsquelle und die Detektorzeile kontinuierlich synchron um das Untersuchungsobjekt, während sich der Lagerungstisch stetig nach kranial bewegt. Hochwertige, artefaktarme 3D-Rekonstruktionen bei geringer Scanzeit sind hierdurch möglich. Abbildung 3: Prinzip der Computertomografie eines Rotate-Rotate Computertomographen mit Strahlenquelle und Strahlendetektoren, die synchron um den Patienten rotieren. Während dieser Rotation werden kontinuierlich Daten aufgezeichnet [13]. - 12 - Ein solches Gerät besteht im Wesentlichen aus einem elektromotorisch beweglichen Patientenlagerungstisch, einem Computer, einem Bedienpult mit Auswerteeinheit, einem Monitor, und dem Gantry (=„Fassöffnung“; kurzer Ringtunnel). Hier befinden sich die Röntgenröhre sowie mehrere Detektoren. Aufgrund einer fächerförmig erzeugten Röntgenstrahlung mittels eines Schlitzkollimators ist eine zusätzliche Translationsbewegung von Strahlungsquelle und Detektor nicht mehr notwendig. Es können somit dennoch flächenhafte Röntgenbilder vom Untersuchungsobjekt gewonnen werden. 2.2.2 Bilderzeugung Bei einer CT-Aufnahme bewegt sich eine Hochleistungsröntgenröhre kreisförmig um den Patienten und durchleuchtet diesen mit fächerförmiger Röntgenstrahlung. Diese durch das Untersuchungsobjekt abgeschwächte Strahlungsenergie wird von gegenüberliegenden Detektoren registriert. Die hier entstehenden Messwerte werden als Projektion bezeichnet. Mehrere Projektionen aus unterschiedlichen Durchleuchtungswinkeln lassen sich nun mit Hilfe des Computers zu einem Schichtbild rekonstruieren. Bei homogenen Körpern liegt der detektierten Attenuation folgende Gleichung zu Grunde: [Gl. 1] Der Abschwächungskoeffizient berechnet sich aus [Gl. 1] zu: [Gl. 2] Dabei entspricht der Anfangsintensität des Röntgenstrahls, welcher ein homogenes Gewebe der Länge mit konstantem Abschwächungskoeffizienten durchdringt. Die Abschwächung des Röntgenstrahls verhält sich exponentiell. - 13 - homogenes Objekt Intensität Röntgenstrahl Distanz Abbildung 4: homogenes Objekt (graues Oval) wird von Röntgenstrahl (dicker schwarzer Pfeil) durchdrungen. Diagramm zeigt die exponentiell abfallende Anfangsintensität I0 über eine gegebene Distanz x. Da der Mensch jedoch nicht aus einer einzigen homogenen Masse besteht, sondern aus einer Abfolge nacheinander auftretender verschiedener Gewebearten mit unterschiedlichen Abschwächungskoeffizienten der Berechnung der Röntgenintensität und Längenmaßen , liegt folgende Formel zu Grunde: ∑ [Gl. 3] ∑ [Gl. 4] Das Bildrekonstruktionsverfahren, welches bei der CT zur Anwendung kommt, wird „gefilterte Rückprojektion“ genannt. Diese bedient sich der logarithmierten Werte und berechnet die Funktion (x,y). Die hieraus errechneten Abschwächungskoeffizienten werden als analoge Grautöne nach der sog. Hounsfield-Skala bildlich dargestellt. Damit erhält man ein Abbild der abgetasteten Körperquerschnittsfläche, auf dem die unterschiedlich absorbierenden Strukturen digital aus diskreten Bildelementen dargestellt werden können. - 14 - Abbildung 5: Durchgang eines Nadelförmigen Röntgenstrahls durch den Körper; I0=Anfangsintensität ; µ1-4 = N=unterschiedliche Abschwächungskoeffizienten; Δl=Schichtlänge; schwarzer Pfeil=Richtung des Röntgenstrahls [11]. Zur Berechnung der Schnittbilder sind mehrere 1000 Projektionen notwendig. Pro Detektorschicht und Umlauf werden etwa 800 bis 1000 Projektionen zu je 6001200 Messwerten akquiriert. Jeder Punkt eines Objekts muss aus einem Winkelintervall der Länge 180° oder mehr gemessen werden. Abbildung 6: Aus den gemessenen Intensitäten werden die Schwächungskoeffizienten berechnet [64]. µ1-9= Schwächungskoeffizienten, S1-12= gemessene Intensitäten 2.2.3 Bildkomponenten Bei der Computertomographie werden aus Projektionen Schichtbilder berechnet, bei denen jedes einzelne Pixel (Bildelement) einen Gewebeteil darstellt. Zur Bildberechnung wird das Schichtbild in eine Matrix bestehend aus Pixeln eingeteilt. Weiter wird die Schichtdicke bestimmt, welche zwischen 1 mm und 12 - 15 - mm liegen kann. Die hieraus entstandenen Volumenelemente werden Voxel genannt. Eine solche Bildmatrix besteht meist aus 512 x 512 oder 1024 x 1024 Schichtdicke Volumenelementen. Schichtlänge Schichtbreite Abbildung 7: Schematische Darstellung der einzelnen Bildelemente. y=Schichtlänge, x= Schichtbreite, z= Schichtdicke Jedem Pixel mit entsprechendem Röntgenschwächungskoeffizienten µ wird nun eine spezifische Graustufe zugewiesen. Die Einheit dieser zugeordneten Dichtewerte wurde nach Godfrey Hounsfield (HU = Hounsfield Unit) benannt. - 16 - CT-Zahl Spalte1 Spalte2 Spalte3 Spalte4 1000 800 80 geronnenes Blut (70-80) kompakter Knochen (250 600 1000) 70 Leber (50-70) 400 60 frisches Blut (50-60) 200 spongiöser Knochen (50 -200) 50 Pankreas (30-50) 0 Wasser Fett (100) -200 40 graue Substanz (40-45) weiße Substanz (30-35) 30 Niere (20-40) -400 20 -600 10 Lunge (500-900) -800 0 Liquor (0-10) -1000 Luft Hounsfield Skala Tabelle 1: Hounsfield-Skala für verschiedene Gewebearten. Diese werden mittels Computer bei der Computertomographie in verschiedenen Graustufen dargestellt; CT= Computertomographie Die Berechnung der einzelnen Graustufen wird dabei immer relativ zu Wasser (HU= 0) und Luft (HU= -1000) nach folgender Formel durchgeführt: CT-Zahl = 1000 [Gl. 5] - 17 - 2.3 Bildgebende Verfahren: Magnetresonanztomographie 2.3.1 Einführung Die Magnetresonanztomographie oder Kernspintomographie basiert grundlegend auf dem physikalischen Zusammenhang zentrale Effekt der Element Kernspinresonanz. ist das Das Wasserstoffatom, in diesem welches in Fettverbindungen, sowie als Molekül mit Sauerstoff in Form von Wasser, hauptsächlich in menschlichem Gewebe vorkommt. Im Vergleich zu anderen röntgenbasierenden Verfahren wie der Computertomographie besitzt die Magnetresonanztomographie einen besonders hohen Weichteilkontrast. Das liegt unter anderem an einem sehr guten Signal-zu-Rauschen Verhältnis (engl.: SNR = signal-to-noise ratio) beim MRT. Zum besseren Verständnis kann man sich hierzu ein leises Flüstern in mitten einer lauten Menschenmenge vorstellen. Das Flüstern entspricht hierbei dem Signal, die Menschenmenge einem störenden Rauschen. Mittels unterschiedlicher Methoden wird bei einer MRT nun versucht, dieses Signal möglichst deutlich warzunehmen und gleichzeitig die Störgeräusche abzuschwächen. Hierzu kann z.B. die magnetische Feldstärke deutlich erhöht werden (z.B: Ultra-Hochfeld MR mit 7 Tesla). Das MR-Signal wächst hier quadratisch mit der Magnetfeldstärke, wohingegen das Rauschen nur linear zunimmt. Verschiedene Filterungsprozesse finden hier ebenso Anwendung wie das Anheben des Signals durch eine verlängerte Stimulationszeit oder eine Verringerung der Schichtdicke. Der Wasserstoffkern besteht aus einem Proton, das aufgrund seines „Spins“ ein magnetisches Dipolmoment µ besitzt. Bei einer MRT wird der menschliche Körper einem starken statischen Magnetfeld ausgesetzt. In der klassischen Approximation richten sich die Protonen der Wasserstoffatome unter einem bestimmten Winkel parallel oder antiparallel zu diesem aus. Die Summe aller ausgerichteten magnetischen Momente resultiert in einem makroskopischen magnetischen Moment M, welches entlang der Magnetfeldachse des äußeren magnetischen Feldes ausgerichtet ist (longitudinale Magnetisierung Mz). - 18 - Abbildung 8: Paramagnetismus von Wasserstoff ohne (rechts) und mit (links) angelegtem starkem äußeren Magnetfeld. Rot-Grüne Trapezformen = Wasserstoff, N=Nordpol; S= Südpol; schwarze Pfeile= Richtung äußeres Magnetfeld [69]. Das neu hinzugewonnene magnetische Moment M kann aufgrund seiner longitudinalen Ausrichtung entlang des externen statischen Magnetfeldes jedoch nicht berechnet werden. Durch Applizieren eines Hochfrequenzpulses mit der Resonanzfrequenz = 42.6MHz/T orthogonal zum statischen Magnetfeld lässt sich die initial longitudinal ausgerichtete Magnetisierung um die entsprechende Achse drehen. Wird die longitudinale Kernmagnetisierung (konventionsgemäß in z-Richtung verlaufend) komplett in die xy-Ebene gedreht (transversale Magnetisierung), so spricht man von einer 90° Anregung. Sobald die Longitudinalausrichtung verlassen wird, rotiert die transversale Magnetisierung Mxy in der xy-Ebene mit der Larmorfrequenz abhängig von der äußeren Magnetfeldstärke T ( ( = gyro-magnetisches Verhältnis). . Die Frequenz ist ) und vom jeweiligen Atomkern Protonen haben somit bei einer Magnetfeldstärke von 1 Tesla eine Präzessionsfrequenz von 42,6 Mhz. Die hier zugrunde liegende Formel wird Larmorgleichung genannt. = Die rotierende [GL.6] Magnetisierung induziert eine elektrisch messbare Wechselspannung in einer Spule senkrecht zum Hauptmagnetfeld. Ihre Amplitude ist proportional zur transversalen Magnetisierung [45]. - 19 - z N Pr äzessionsfr equenz um Bo z.B. Bo = 1 Tesla Vo = 42,6 MHz m agnet isches Mom ent M Pr ot on Bo " Spin" y S x Abbildung 9: ⃑⃑⃑⃑ und gestrichelte Linien= Richtung des longitudinalen (statischen) Magnetfeldes; = Präzessionsfrequenz in Megahertz (MHz); = Magnetfeldstärke in Tesla; N = Nordpol; S= Südpol; x-, y- ,z- = Raumkoordinate. Nach Abschaltung des hochfrequenten Wechselfelds verringert sich die transversale Magnetisierung, da die Wasserstoffatome nun wieder zu ihrer longitudinalen statischen Magnetfeldausrichtung tendieren. Diese Relaxation besitzt eine charakteristische Abklingzeit welche wiederum abhängig ist von der jeweiligen chemischen Verbindung und molekularen Umgebung der beobachteten Wasserstoffkerne (T1-Relaxation). Somit können wir unterschiedliche Gewebearten ihrem charakteristischen Signal nach zuordnen und mit Hilfe eines Computers eine Bildberechnung mit unterschiedlichen Graustufen durchführen. - 20 - 2.3.2 Bilderzeugung Grundlage der Bilderzeugung in der MRT sind die unterschiedlichen Kernspinrelaxationszeiten der Wasserstoffkerne in verschiedenen Gewebearten nach Anregung durch eine transversale Kernmagnetisierung. Diese messbaren Relaxationszeiten sind zusätzlich von der angelegten Magnetfeldstärke sowie dem verwendeten Kontrastmittel abhängig. Man unterscheidet hauptsächlich zwischen der longitudinalen Relaxationszeit ( sowie der transversalen Relaxationszeit ( ). Die ) -Zeit, auch „Spin-Gitter- Relaxationszeit“ genannt, ist die Zeit, welche das angeregte Teilchen benötigt, um die zuvor aufgenommene Energie an seine Umgebung („Gitter“) abzugeben und sich wieder in den Ausgangszustand (Ausrichtung an longitudinales Magnetfeld) zu begeben. Tabelle 2 zeigt Beispiele für die gewebsspezifischen Relaxationszeiten in Millisekunden (ms). Relaxat ionspr ozesse Bereich Gewebe 1,5 T 1,0 T 0,2 T T2 Gehirn Graue Weissse Liquor Tum or Ödem 921 ( m s) 787 3000 957- 1073 1090 813 ( m s) 683 2500 871- 1055 975 495 ( m s) 390 1200 629- 864 627 101 ( m s) 92 1500 103- 121 113 Leber Norm al Tum or 493 905 423 857 229 692 43 84 Milz Norm al 782 683 400 62 Niere Norm al Tum or 652 907 589 864 395 713 58 83 Tabelle 2: gewebespezifische Relaxationszeiten bei unterschiedlichen Feldstärken in Millisekunden (ms); T (rot) = Tesla; ms = Millisekunde; T2 (blau) = transversale Relaxationszeit - 21 - Unter der -Zeit, auch Spin-Spin-Relaxationszeit genannt, versteht man den Verlust der zuvor phasensynchronen Kreiselbewegungen der Atomkerne. Dies geschieht nach Abschalten des HF(Hochfrequenz)-Signals aufgrund sich gegenseitig aufhebender inter- und intramolekularer Dipolwechselwirkungen und hat eine messbare Abnahme der Transversalmagnetisierung zur Folge. Gewebe, welches eine Transversalmagnetisierung relativ lange aufrechterhalten kann (z.B. Wasser), stellt sich in -gewichteten Aufnahmen hell dar. Bei einer klinischen MRT-Untersuchung werden meist angefertigt. In der Regel zeigen - und -Sequenzen -gewichtete Sequenzen Stoffe mit kurzer (z.B. Fett, Knochenmark) hell wobei sich der Kontrast invers proportional zu konstant zum Gewebe ergibt. In proportional zur gewichteten Sequenzen ist die Signalintensität konstant zum Gewebe. Mit Hilfe verschiedener linear ortsabhängiger Magnetfelder (Gradientenfelder) wird nun eine Ortskodierung erzeugt, wonach sich das emittierte HF-Signal räumlich zuordnen lässt. Die Schichtselektionsgradienten, Gradientenfelder bestehen Phasenkodiergradienten aus und einem einem Frequenzkodiergradienten. Alle 3 Gradienten zusammen ermöglichen eine räumliche Kodierung des Signals. Ein Computer kann dann mit Hilfe einer FourierTransformation ein zweidimensionales Bild berechnen. 2.4. Implantierte Endoprothesen Bei der Auswahl der implantierten Endoprothesen wurden folgende Kriterien berücksichtigt. Wichtig waren hierbei die aktuelle Verfügbarkeit sowie die Größe der Prothesen. Zusätzlich bestanden auch persönliche Präferenzen der einzelnen Operateure. Zum einen wurde die thorakale Gore TAG® Endoprothese der Firma GORE (W.L, Gore Associated GmbH, Putzbrunn Germany) verwendet, zum anderen der Medtronic Valiant® Stentgraft der Firma Medtronic (Medtronic World Medical, Sunrise, FL, USA). Beide Stents besitzen ein Nitinol-Stützgerüst bestehend aus einer Nickel-Titan-Legierung. Dieses ist gut gewebeverträglich und bildet die - 22 - Grundlage für eine optimale Formbarkeit sowie Formerhaltung nach vollzogener Implantation. An den proximalen und distalen Prothesenenden befinden sich Goldbänder (Gore TAG®) oder Platin-Iridium-Drähte (Medtronic Valiant®) zur perioperativen röntgenologischen Lagekontrolle. Die Rohrwandung der Gore TAG® Prothese besteht aus einem expandiertem Polytetrafluorethylengewebe (ePTFE). Im Gegensatz dazu wurde beim Medtronic Valiant® ein monofilament Polyestergewebe verwendet. In beiden Fällen dient die Rohrwandung der Schienung der Rupturstelle sowie der vollständigen Wiederherstellung des physiologischen Blutflusses. Am proximalen Ende des Medtronic Valiant® überlappt das Drahtgerüst seinen Polyestermantel ein wenig. Dies dient der zusätzlichen Positionserhaltung. Ein Federring soll peri-und postoperativ vor „Infolding“ Phänomenen schützen. Der Medtronic Valiant® sowie die Gore TAG® Prothese sind beide für Magnetfeldstärken bis zu 3 Tesla zugelassen. Abbildung 10: links: Gore TAG® thorakale Endoprothese [61]; rechts: Medtronic thorakaler Stentgraft Valiant® [12] - 23 - Abbildung 11: implantierte Gore TAG® thorakale Endoprothese [62] 2.5. Erhebung des Bildmaterials bei computer- und magnetresonanztomographischen Nachuntersuchungen Alle Patienten wurden weiterhin der nach Goldstandard empfohlenen regelmäßigen Nachuntersuchungen unterzogen. Diese bestanden neben einer ausführlichen Anamnese und einer klinischen Untersuchung aus einer Angio-CT der thorakalen Aorta, welche an der Universität Ulm, Abteilung für Radiologie, durchgeführt wurde. Hierzu bediente man sich eines 64-Zeilen Spiral-CT (Brilliance 64, Philips Medical Systems, The Netherlands) bei einer Bildauflösung von 0,6x 0,6 x 0,9mm³ und einer Schichtdicke von 4 mm. Dabei wurde ein Volumen von 90ml/Kg jodhaltigem Röntgenkontrastmittel (lomeprol© 400, Bracco, Milan, Italy) mit einer Injektionsgeschwindigkeit von 4,5 ml/s appliziert. Die Patienten wurden für die Untersuchung in der FFS (Feet First-Supine) Position gelagert, d.h. sie wurden in Rückenlage mit den Füßen voraus in Geräterichtung - 24 - positioniert. Es wurden Schnittbilder in der axialen, sagittalen und koronaren Körperebene angefertigt. Abbildung 12: Sagittales Schnittbild eines Angio-Computertomogramms mit Kontrastmittel. Klar erkennbar ist das sehr hell bis weiß erscheinende Drahtgerüst der in der Aorta descendens eingebrachten Endoprothese mittig im Bild (Hier: Gore TAG® Endoprothese) Bei der Bildbetrachtung wurde primär nach möglichen Komplikationsfolgen wie Endoleaks, Strebenbrüche im Metallskelett oder einer Stentmigration Ausschau gehalten sowie der allgemeine Gefäßstatus der thorakalen Aorta und ihrer Abgänge beurteilt. Im weiteren Verlauf der Nachuntersuchung wurden die Patienten einer MRT unterzogen. Diese wurde mittels einem 1.5 T Philips Gyroscan Intera (© Philips Medical Systems, Best, The Netherlands), mit Power Trak 6000 Gradientenspule (23 mT/m; 219 μs Anstiegszeit) durchgeführt. Die Signalerfassung erfolgte mit einer für das Herz geeigneten, aus 5 oder 32 Elementen bestehenden PhaseArray Spule. Ein angelegtes Vektorkardiogramm ermöglichte die getriggerte Synchronisation von Herzzyklus und Datenakquisition. Neben Atemanhaltemanövern und atemnavigierten Akquisitionen diente dies zur weiteren - 25 - Reduktion von Bewegungsartefakten in der ROI (Region of Interest) und somit einer besseren Bildqualität. MR-(CE-)Angiographie der Aorta Zur ersten Orientierung und Lokalisation der aortalen Endoprothese wurden ebenfalls Schichtbilder in axialer, transversaler und koronarer Ebene hergestellt (Abbildung 16: Angio-Sequenz). Hierbei bediente man sich einer für Bewegungsanalysen von Myokard gängigen 3D SSFP (Steady-State-Free Precession)-Sequenz, welche sich im Vergleich zu anderen FLASH (Fast LowAngle-Shot)-Gradientenechosequenzen durch kürzere Akquisitionszeiten bei höherem Kontrast- und Signal-Rausch-Verhältnis auszeichnet [59]. Somit ist es möglich, die Endoprothese in ihrer Position dreidimensional ohne stärkere Bewegungsartefakte (Blutfluss, Myokardbewegung) zu betrachten. Die Akquisitionszeit betrug 15 Sekunden bei Atmungsstopp. Nachfolgend wurden unter Kontrastmittelgabe (Magnevist, Schering, Germany) weitere, spezielle angiographische Schnittbilder des linksventrikulären Ausflusstraktes, der Aorta ascendens, des Aortenbogens und der thorakalen Aorta descendens in parasagittaler Ebene angefertigt (Abbildung 15: CE-Angio = Contrast-Enhanced Angiography). Die Aufnahmen erfolgten nach Gabe einer gewichtsadaptierten Gesamtdosis (ml/Kg) Kontrastmittel bei einer Injektionsgeschwindigkeit von 4ml/s. Das Kontrastmittel diente hierbei zur besseren Gefäßdarstellung und Abgrenzung gefäßnaher Strukturen der thorakalen Aorta und ihrer Abgänge. - 26 - Abbildung 13: einliegende Endoprothese im Bereich der Aorta descendens; links: parasagittaler computertomographischer Schnitt; rote Pfeile: weißes Stentgerüst; rechts: gleiche Schnittebene bei gleichem Patienten, hier magnetresonanztomographisches Schnittbild ohne Kontrastmittel; grüne Pfeile: aufgrund der Signalauslöschung im Magnetresonanztomographen erscheint der Stent schwarz und ist klar von der Gefäßwand abzugrenzen. Funktions-CINE-MRT Zur weiteren dynamischen Untersuchung des Stentgraft während eines Herzzyklus wurde mit Hilfe eines angelegten EKG durch retrospektives Gating die Herzbewegung über insgesamt 40 Herzzyklen mit der Datenakquisition (SSFP mehrschichtige Akquisitionstechnik) synchronisiert (CINE). Dabei werden wie bei einem kinematographischen Film („cine“) in schneller Folge Schnittbilder an derselben Stelle erzeugt. Mehrfache Atemstillstandsmanöver wurden zusätzlich zur Artefaktreduktion durchgeführt. Diese Aufnahmen erfolgten proximal, zentral und distal des Stentgraft, jeweils orthogonal zur Mittellinie desselben. Eine detaillierte Übersicht der einzelnen MRT-Sequenzen bietet Tabelle 3. - 27 - Magnetresonanztomographische Akquisitionsparameter Angio CE-Angio CINE 300 x 300 x 150 400 x 360 x 84 380 x 347 x 6 1,8 x 1,8 x 1,5 1,0 x 1,7 x 4,0 1,2 x 1,2 x 6,0 Echo-Zeit(ms) 1,9 1,3 1,7 Repetitions-Zeit (ms) 3,8 4,9 3,4 Flip-Winkel (°) 90 40 60 Turbo Faktor 39 N/A 14 Herzphasen 1 1 40 Akquisitionszeit (ms) 149 N/A 23 Scan Dauer (s) 217 21 11 Gesichtsfeld (mm) Auflösung (mm) Tabelle 3: Magnetresonanztomographische Akquisitionsparameter; Angio = Angiographie; CEAngio = Contrast Enhanced (kontrastmittelverstärkte) Angiographie, CINE= kinematographisches Bewegungsprotokoll, mm = Millimeter, s = Sekunde, ms = Millisekunden, min = Minuten, (°) = Grad, N/A = not applicable (nicht zutreffend); (Gesichtsfeld= Sichtfeld des Gerätes; Auflösung = Auflösung des verwendeten Tomographen in allen 3 Ebenen, Echo Zeit = Zeit von der Anregung des Kernspins bis zur Messung, Repetitions-Zeit = Zeit zwischen 2 Anregungen; Flip Winkel = Anregungswinkel im Vergleich zum Hauptmagnetfeld; Turbo Faktor = Anzahl der Echos, die aus einer Messung gemessen werden; Akquisitionszeit= Dauer bis zum Bilderwerb 2.6. Relevante Artefaktbildung und qualitative Darstellung der betrachteten Endoprothesen im Vergleich Artefaktbildung der MR-Datensätze Die in der vorliegenden Arbeit untersuchten Endoprothesen besitzen alle ein Nitinol-Stützgerüst und gelten somit im Allgemeinen als gut MR-kompatibel [50]. Zu den hier relevanten Artefaktbildungen gehören Abschirmungsartefakte, Suszeptibilitätsartefakte sowie Bewegungs- und Flussartefakte. Die nachfolgende Abbildung zeigt eine direkte Gegenüberstellung einer thorakalen Endoprothese, dargestellt mittels einer nativen (links) und Kontrastmittel - 28 - verstärkten, T1-gewichteten MRI-Aufnahme (rechts). In der nativen SSFP (Steady State Free Precession) Aufnahme ist ein Signalverlust im Bereich des proximalen Stentlumens zu beobachten. Hierbei handelt es sich höchstwahrscheinlich um ein Abschirmungsartefakt, hervorgerufen durch eine Radiofrequenzabschirmung durch den Stent selbst. Dabei kommt es einerseits zu einer Reduktion der eindringenden Signalstärke, andererseits werden ausgehende Signale aus dem inneren Gefäßlumen durch den Stent abgeschirmt und somit von der Empfängerspule nur noch in erniedrigter Intensität empfangen [6]. Die native SSFP Aufnahme zeigt eine bessere Abgrenzung des Stentgerüsts von der Gefäßwand im Vergleich zu seinem Pendant auf der rechten Seite. Man könnte daher annehmen, dass eine bestehende Dislokation eines Endografts bei dieser Aufnahmetechnik besser zu erkennen wäre. Abbildung 14: (links) native und (rechts) kontrastmittelverstärkte magnetresonanztomographische Aufnahme. Offene Pfeile zeigen die Abgrenzung des Stentgraft links besser als rechts, wobei die Signalhomogenität innerhalb der Aorta (geschlossener Pfeil links) rechts besser dargestellt wird. Unter Suszeptibilität versteht man vereinfacht ausgedrückt die Magnetisierbarkeit von Materialien innerhalb eines Magnetfeldes. Aufgrund unterschiedlicher Suszeptibilitäten von Materialien (z.B. Endoprothesen, Blut, verschiedene - 29 - Gewebearten) kommt es zu Phasendifferenzen welche zu einer Signalauslöschung führen können. Diesen Effekt macht man sich bei der suszeptibilitätsgewichteten Bildgebung auch zu Nutze, um z.B. kleinste Hirnblutungen oder Eisenablagerungen zu erkennen [22]. Suszeptibilitätsartefakte treten entgegen der hier verwendeten Endoprothesen häufiger bei der Darstellung von eisenhaltigen Stents auf und sind abhängig vom Ort, der Magnetfeldfrequenz und der vorangegangenen Magnetisierung. Bewegungsartefakte durch willkürliche Körperbewegungen konnten durch vorherige Aufklärung der Patienten bezüglich der Einnahme einer konstanten Körperhaltung während der Bildgebung deutlich reduziert werden [1]. Atemanhaltemanöver halfen ebenfalls, Bewegungsartefakte zu reduzieren. Dank der Funktions-MR Scans konnte unscharfes Bildmaterial durch Flussartefakte besonders in der Aorta ascendens meist vermieden bzw. deutlich reduziert werden. Bei Patienten mit leicht obstruktiv einliegenden Stentgrafts konnten Flussartefakte identifiziert werden. Diese wiesen somit ebenfalls auf eine erhöhte Flussgeschwindigkeit in diesem Bereich hin. Ein Beispiel zeigt Abbildung 15. Abbildung 15: Qualitative Visualisierung von Flussartefakten (schwarze und weiße Pfeile bei 90 und 130ms) während der End-Diastole a) und der Systole b,c). Zeitangaben in ms sind relativ zur vorausgegangenen R-Zacke im Elektrokardiogramm gemessen. ms= Millisekunde. - 30 - Artefaktbildung der CT-Datensätze Bei der computertomographischen Darstellung der Endoprothesen sind ebenfalls neben Bewegungsartefakten im Wesentlichen Strahlungsaufhärtungs- und Teilvolumenartefakte zu nennen. Bei der Strahlungsaufhärtung erhöht sich die durchschnittliche Photonenenergie mit zunehmender Eindringtiefe der Röntgenstrahlung. Dabei werden die energetisch „kleineren“ Photonen nach jeder durchdrungenen Gewebeschicht mehr gestreut als energetisch höherwertige Photonen. Aufgrund der heute verwendeten Detektoren, Gesamtphotonenenergie welche messen, nur eine stellen sich Mittelung in der der auftreffenden Bildrekonstruktion Aufhärtungsartefakte als dunkle, hypodense Bereiche dar [52]. Bei Teilvolumenartefakten kommt es aufgrund stark unterschiedlich detektierten Röntgenschwächungskoeffizienten innerhalb eines Voxels zu Streifenbildung im CT-Bild. In der vorliegenden Arbeit sind vor allem Bereiche mit sehr hohem unterschiedlichem Kontrast angrenzender Strukturen (z.B. Metall und Gewebe) davon betroffen. Teilvolumenartefakte oder Abtastartefakte können durch feinere Abtastung oder geringer gewählte Schichtdicken vermieden werden [65]. Höhere Pitch Einstellungen verursachen deutlichere Artefaktbildung. Die Bildqualität sowie die Abgrenzung des Stentgerüsts von seiner Umgebung verbessern sich zunehmend durch eine geringere Kollimation. Die Größe der stentbedingten Artefaktbildung sowie die Sichtbarkeit des Lumens ist prinzipiell auch von unterschiedlich verwendetem Stentmaterial sowie des Stentdesigns der einzelnen Hersteller abhängig [40]. Qualitativer Bildvergleich Bei allen Patienten konnte der Stentgraft in mindestens mittelmäßig guter Bildqualität dargestellt werden. Dadurch konnten verwertbare planimetrische Messungen durchgeführt werden. Einen direkten Vergleich zwischen MRI- und CT-Scans sowie der Bilder untereinander bietet Abbildung 16. - 31 - Abbildung 16: Native Magnetresonanztomographie- (a-c) und Computertomographieaufnahmen (d-f) mit dargestelltem aortalem Stentgraft. Aufgrund der unterschiedlichen Aufnahmmethoden erscheinen die Endografts in der Magnetresonanztomographie schwarz und in der Computertomographie weiß leuchtend - 32 - Ein grober Verlust morphologischer Bildinformation konnte bei beiden bildgebenden Verfahren ausgeschlossen werden. Aufgrund der geminderten räumlichen Auflösung der MR-Scans und der entstandenen Signalauslöschungen in der Nähe des Stentgerüsts scheint eine deutlichere Abgrenzung des Endografts von der Gefäßwand bei den CT-Scans besser möglich zu sein. Bezüglich der Lagebeurteilung der Endoprothesen zeigten die MR- und CT-Scans vergleichbar gute Bilder. Aufgrund der teilweise engen Aortenbögen zeigte die Mehrzahl der Patienten (n=11) kleinere, der Gefäßwand nicht anliegende Stentabschnitte (Abb. 16 b, e). 8 Patienten wiesen sogar große, nicht anliegende Stentbereiche auf (Abb. 16 c, f). Nur bei 2 Patienten konnte eine optimale Stentlage beschrieben werden (Abb. 16 a, d). Bei allen KM verstärkten MRI Aufnahmen konnte eine ausreichende Bildqualität zur Berechnung einer Volumenvisualisierung erreicht werden. Ein Beispiel zeigt Abbildung 17. - 33 - Abbildung 17: Kontrastmittelverstärkte magnetresonanztomographische Volumenvisualisierung eines Endograft der thorakalen Aorta (a,c) im Vergleich zur Computertomographie (b,d). Der Stent ist in der magnetresonanztomographischen Aufnahme nicht direkt sichtbar. Die Stentposition kann nur anhand der irregulären Verformungen an der Aortenoberfläche erahnt werden. Im Vergleich zum CT-Scan (Abb. 17 b,d) kann aufgrund unterschiedlicher Darstellungsmechanismen der Endograft im MR-Scan (Abb. 17 a,c) nur anhand der unregelmäßigen Oberflächenstruktur der Aorta erahnt werden, wogegen der - 34 - CT- Scan ein direktes Abbild des Stentgerüsts erkennen läßt. Dennoch ist eine solche MR-Volumenvisualiserung für die erste Einschätzung nach erfolgter Stentimplantation bezüglich der Gefäßmorphologie durchaus als geeignet anzusehen. 2.7. Planimetrische Vergleichsmessungen der computer- und magnetresonanztomographischen Datensätze Zu Beginn der Arbeit wurden manuelle planimetrische Messungen beider Bilddatensätze (CE-Angio CT/MRT) aller Patienten durchgeführt. Jedem Patienten konnte somit ein MRT- und ein CT-Bilddatensatz des zu vermessenden implantierten Stentgrafts zugeordnet und verglichen werden. Für die Messungen bediente man sich der dem Magnetresonanztomographen zugehörigen Bedienungssoftware Philips Extended Workspace© 2.6.3.2“ (Philips Medical Systems, Netherlands). Gemessen wurden die Stentdurchmesser im proximalen, mittleren und distalen Stentabschnitt. Hierfür boten parasagittale Schnittbilder einen guten Gesamtüberblick des aortalen Stentverlaufs. Die manuelle Einstellung erforderte ein möglichst mittig getroffenes Schnittbild der rohrförmigen Aorta bei der CT und der MR-Bildgebung. Zusätzlich war es wünschenswert, möglichst markante anatomische Merkmale vorzufinden, anhand derer sich beide Datensätze in vergleichbare Schnittebenen einstellen ließen. Es wurden dann 3 Messlinien, orthogonal zu einer zuvor ebenfalls manuell bestimmten „Centerline“ in den jeweiligen Abschnitten gewählt. Als Anfangs- und Endpunkt der Messstrecke wurde bei den CT-Aufnahmen jeweils vom Zentrum des weiß leuchtenden Metallsignals des Stentgerüsts bis zu seinem gegenüberliegenden Pendant gemessen. Bei den MR-Aufnahmen wurde das Zentrum der Signalauslöschung des Stentgerüsts gewählt. Bei Pateinten mit einem eher irregulären Aortenverlauf gestalteten sich die Messungen allgemein schwieriger. Auf die Ergebnisse der rein manuellen Bildeinstellungen und Messungen wird im Abschnitt 3 dieser Arbeit nochmals gesondert eingegangen. - 35 - Abbildung 18: Bsp. Zweier komplett manuell gemessener Datensätze, welche sich in etwa derselben Scan-Schicht befinden. Links: parasagittaler Computertomographie-Schnitt; Rechts: parasagittaler Magnetresonanztomographie-Schnitt; grüne Linie: Centerline; rote Linien: orthogonal zur Centerline gemessene Durchmesser jeweils im proximalen, mittleren und distalen Abschnitt des Endograft. Anwendung von 3DSlicer Im weiteren Verlauf der Arbeit musste die Vorgehensweise angepasst werden. Grund hierfür war die nicht reproduzierbare Lagerung der Patienten während der verschiedenen computer- und kernspintomographischen Scandurchläufe. Eine rein manuelle Datenverarbeitung war daher nicht möglich. Deshalb kam die Computersoftware 3DSlicer Vers. 3.4.1.0 zum Einsatz. Das „open source“ Programm wurde zur Analyse und Visualisierung medizinischen Bildmaterials vom Surgical Planning Laboratory am Brigham & Women`s Hospital (Boston, Massachusetts, USA) in Zusammenarbeit mit dem MIT Computer Science and Artificial Intelligence Laboratory (Cambridge, Massachusetts, USA) entwickelt. Mit Slicer war eine Registrierung zweier CT und MR-Bilddatensätze eines Patienten anhand gesetzter anatomischer Landmarken möglich. Hierfür kamen anatomische Merkmale des Mediastinums (z.B. Aorta ascendens, A. pulmonalis dextra et sinistra, Truncus Pulmonalis, Atrium cordis sinistrum etc.) in Frage, welche sich bei jedem einzelnen Patienten in den verschiedenen Ebenen als Landmarken eigneten. Auch die Endoprothese selbst wies häufig entsprechende - 36 - Merkmale auf (z.B. starke Krümmung der Endoprothese, Ausbuchtungen des Drahtgitters aufgrund eines vorbestehenden Aneurysmas), die sich als Landmarkenpunkte gut eigneten. Die Software führte anhand der Landmarken eine affine Transformation der Schnittbilder durch. Somit wurde mit Hilfe von Rotations-, Translations- und Skalierungsberechnungen eine weitgehend optimale Kongruenz der für die Messungen wichtigen Stentabschnitte erreicht. Eine manuelle Bestimmung der Durchmesser konnte anschließend nach bereits beschriebener Vorgehensweise erfolgreich durchgeführt werden. Eine zusätzliche Vermessung der Stentumfänge war für die vorliegende Arbeit nicht mehr notwendig. Die registrierten Datensätze wurden von einem erfahrenen Korrektor nachgemessen. Abbildung 19: Computertomographie (links) und Magnetresonanztomographie (rechts) in sagittalem Schnitt nach Platzierung einiger Landmarken (rot F1-4; siehe Beschriftung im Bild) und vor der Registrierung durch 3D Slicer. - 37 - 2 1 Abbildung 20: Beispiel einer Messung nach erfolgter Registrierung zweier Datensätze. Hierbei wird eine direkte Überlagerung der registrierten Bilddatensätze dargestellt. Computertomographie (rote 1), Magnetresonanztomographie (rote 2), rote Linie: Trennlinie bzw. Übergang von Computertomographie nach Magnetresonanztomographie, LP-1-6 (blau): gegenüberliegende Messpunkte der jeweiligen Magnetresonanz- Durchmesser. 2.8. Statistische Testverfahren Die Datenerfassung und -verarbeitung erfolgte mit Microsoft Excel 2007 (Microsoft, Redmond, WA) sowie mit IBM SPSS Statistics Software. Die erhaltenen Parameter wurden als absolute Maßzahlen, Mittelwerte und Standardabweichungen angegeben. Mittels Balken- und Punktwolkendiagramm wurden die Durchschnittswerte bzw. Einzelmessungen anschaulich dargestellt. Als statistischer Signifikanztest wurde ein zweiseitiger gepaarter Student`s T-Test mit einer max. Irrtumswahrscheinlichkeit von 5% durchgeführt. Mittels Regressionsanalyse wurde die Errechnung einer Regression in Form einer Regressionsgeraden bzw. –funktion dargestellt. Zusätzlich wurde mittels Pearson- 38 - Korrelation Auskunft über den Grad des linearen Zusammenhangs der Messdaten gegeben. Der Rangkorrelationskoeffizient nach Spearman wurde ebenfalls berechnet, da dieser einerseits nicht von vornherein annimmt, dass die Beziehung der Variablen linear ist und andererseits eventuell vorhandene, extrem abweichende Werte, aufgrund der Rangberechnung nicht so sehr ins Gewicht fallen. Bland-Altman Diagramme wurden zur Beurteilung und zum Vergleich der einzelnen Messmethoden untereinander (Intra-Technik Variabilität) sowie zum Methodenvergleich der ursprünglichen Messungen gegenüber den Kontrollmessungen (unabhängiger Beobachter) erstellt. Hier sollte dann auf eine Inter-Observer Variabilität geachtet werden. - 39 - 3. Ergebnisse 3.1. Alters- und Geschlechtsverteilung An der vorliegenden Vergleichsstudie nahmen insgesamt 21 Patienten teil. Hierunter befanden sich 14 Männer und 7 Frauen im Alter zwischen 20 und 79 Jahren Das Durchschnittsalter betrug 39,1 Jahre. 7 männlich Anzahl der Patienten 6 weiblich 5 4 3 2 1 0 20-30J 31-40J 41-50J 51-60J >60J Alter in Jahren Abbildung 21: Alters- und Geschlechtsverteilung von 21 Patienten nach erlittener traumatischer Aortenruptur und erfolgter transfemoraler Stentgraftimplantation durch die Herz- Thorax- und Gefäßchirurgie der Universität Ulm der Jahre 1999-2008. J=Jahre Wie aus Abbildung 21 deutlich zu erkennen ist kam der größte Anteil der Patienten aus der Gruppe der 20-30-jährigen. In fast allen Altersgruppen lag der männliche Patientenanteil deutlich über dem weiblichen. 3.2. Manuelle Vergleichsmessungen der Stentdurchmesser Gemessen wurden die Stentdurchmesser an insgesamt 3 unterschiedlichen Stentabschnitten jeweils proximal, der Stentmitte sowie am distalen Ende mittels - 40 - der Bedienungssoftware des 1.5 T Philips Gyroscan Intera Magnetresonanztomographen (© Philips Medical Systems, Best, The Netherlands) der Universität Ulm. Die Stentdurchmesser wurden definiert als orthogonal zur Centerline gemessene Strecken, wobei der Anfangs- und Endpunkt innerhalb des Stentgerüsts liegt (siehe Abb. 20). Die Ergebnisse wurden in Millimeter angegeben. Hierbei entstanden insgesamt 6 Messungen pro Patient, jeweils 3 für die MR- und 3 bei den CT-Datensätzen. Um vergleichbare Werte zu erhalten wurde bei jedem Patienten versucht, anhand anatomischer Merkmale eine nahezu identische parasagittale Schichtaufnahme zwischen den CT- und MR-Datensätzen manuell einzustellen. Das nachfolgende Balkendiagramm gibt einen Überblick der erhaltenen Durchschnittswerte des jeweiligen Stentabschnitts. durchschnittliche Durchmesserlänge in mm 35 Ø MR 30 Ø CT 25 20 15 10 5 0 23,7 24,1 D1 (mm) 26,6 25,2 22,7 D2 (mm) Messbereiche der Aortenstents 21,7 D3 (mm) Abbildung 22: Balkendiagramm aller manuell gemessenen Aortenstentdurchmesser der untersuchten Patienten im Durchschnitt mit ihren jeweiligen Standartabweichungen. Es wurde jeweils proximal, mittig und distal gemessen. D1= proximal; D2= Mitte; D3= distal mm=Millimeter; Ø=Durchschnitt; MR=Magnetresonanztomographie; Vertikale CT=Computertomographie; Linien in den jeweiligen Balken = Standartabweichungen. - 41 - In Tabelle 4a des Appendix findet sich eine Übersicht aller exakt gemessenen Einzelwerte. Alle Messwerte aus Tabelle 4a wurden in einem Punktwolkendiagramm (Abb. 23) dargestellt. Stentdurchmesser MR [mm] 35,00 30,00 25,00 y = 0,7415x + 5,6083 R² = 0,703 P = 0,04 20,00 15,00 10,00 10,00 15,00 20,00 25,00 30,00 35,00 40,00 Stentdurchmesser CT [mm] Abbildung 23: Punktwolkendiagramm der rein manuell eingestellten und gemessenen Aortenstentdurchmesser (Tabelle 4a) der computertomographischen (horizontale Achse) und der magnetresonanztomographischen untersuchten Patienten; mm=Millimeter, (vertikale schwarze Achse) Messungen diagonale aller Linie=Trendlinie, MR=Magnetresonanztomographie, CT=Computertomographie, y=Steigung der Trendlinie (Regressionsfunktion), x=Platzhalter für beliebigen Wert auf der X-Achse, R²=Bestimmtheitsmaß (Bildet sich aus dem Quadrat des Korrelationskoeffizienten), P=Signifikanzwert (P-Wert). Anhand des hierbei entstehenden Verteilungsmusters der Punktwolke ließ sich eine hohe Übereinstimmung zwischen den CT- und MR-Messungen bereits bildlich erahnen. In Zahlen ausgedrückt berechnete sich die Pearson-Korrelation - 42 - (Korrelationskoeffizient) positiv mit 0,84 (p< 0,01) und zeigte somit eine bestehende signifikante Korrelation, wobei steigende CT-Durchmesser auch steigende MR-Durchmesser zur Folge hatten. Des Weiteren wurde der Rangkorrelationskoeffizient nach Spearman mit einem positiven Wert von 0,78 (p<0,01) berechnet. Der nachfolgend für jedes manuell gemessene Datenpaar durchgeführte zweiseitige gepaarte Student`s T-Test ergab jedoch einen P-Wert (Signifikanzwert) von Irrtumswahrscheinlichkeit 0,04. von Bei einer 5% (α=0,05) angenommenen wurde die maximalen Nullhypothese (Stentdurchmesser sind gleich groß) somit widerlegt. Die durchschnittliche Differenz der Stentdurchmesser jedes Datenpaares (CT/MR) lag bei 0,7 +/- 2,6 mm. Daraufhin wurde die Messmethode geändert, wie im folgenden Kapitel beschrieben. 3.3 Manuelle Vergleichsmessungen der Stentdurchmesser nach landmarkenbasierter Registrierung durch 3DSlicer Als Ursache der statistisch signifikanten Werte wurde die ungenügend reproduzierbare Lagerung jedes einzelnen Patienten während der Scandurchläufe angenommen. Somit ergaben sich durch variierende Schnittwinkel keine optimalen Vergleichsschnittebenen der eingelegten Endoprothesen zwischen den MR- und CT-Datensätzen. Unter diesen Voraussetzungen war das Bildmaterial nur eingeschränkt vergleichbar und für diese Arbeit unzureichend präzise. Mithilfe der PC- Software 3DSlicer Vers. 3.4.1.0 konnten wir dieses Problem jedoch lösen. Neben anderen Anwendungsmöglichkeiten bietet 3DSlicer die landmarkenbasierte Registrierung von Bilddatensätzen im dreidimensionalen Raum. Diese wurde vor weiteren Vergleichsmessungen bei jedem Patienten für das jeweilige Bilddatenpaar mit Fokus auf die thorakale Endoprothese durchgeführt. Aufgrund dieses Zwischenschritts erhielten wir anschließend optimal ausgerichtete und vergleichbare Schnittebenen beider Bilddatensätze. Eine Übersicht der ersten durchgeführten Messungen nach erforderlicher Registrierung bietet Abbildung 24. - 43 - durchschnittliche Durchmesserlänge in mm 30 Ø MR 25 Ø CT 20 15 10 5 0 21,9 21,9 23,2 D1(mm) 22,9 22,1 D2 (mm) 21,9 D3 (mm) Messbereiche der Aortenstents Abbildung 24: Balkendiagramm aller manuell gemessenen Aortenstentdurchmesser der untersuchten Patienten im Durchschnitt mit ihren jeweiligen Standartabweichungen nach erfolgter Registrierung durch 3DSlicer. Es wurde jeweils proximal, mittig und distal gemessen. D1= proximal; D2= Mitte; D3= distal; mm=Millimeter, Ø=Durchschnitt, CT=Computertomographie; MR=Magnetresonanztomographie; Vertikale Linien in den jeweiligen Balken=Standardabweichungen. In Tabelle 4b des Appendix dieser Arbeit sind alle Einzelmessungen noch einmal gesondert aufgeführt. Diese wurden ebenfalls anhand eines Punktwolkendiagramms (Abb. 25) veranschaulicht. - 44 - Stentdurchmesser MR [mm] 40 35 30 25 y = 0,9356x + 1,2725 R² = 0,9429 P= 0,20 20 15 10 10 15 20 25 30 35 40 Stentdurchmesser CT [mm] Abbildung 25: Punktwolkendiagramm der Aortenstentdurchmesser (Tabelle 4b) der computertomographischen (horizontale Achse) und der magnetresonanztomographischen (vertikale Achse) manuellen Messungen aller untersuchten Patienten nach vorheriger landmarkenbasierter Registrierung durch 3DSlicer; mm=Millimeter; schwarze diagonale Linie=Trendlinie, MR=Magnetresonanztomographie, CT=Computertomographie, y=Steigung der Trendlinie (Regressionsfunktion), x=Platzhalter für beliebigen Wert auf der X-Achse, R²=Bestimmtheitsmaß (Bildet sich aus dem Quadrat des Korrelationskoeffizienten), P=Signifikanzwert (P-Wert). Der errechnete Korrelationskoeffizient nach Pearson lag bei 0,97 (p<0,01) und bewies somit eine sehr hohe Korrelation zwischen den beiden Datenreihen. Der Rangkorrelationskoeffizient nach Spearman ergab einen Wert von 0,96 (p<0,01). Anhand der positiven Verteilungsmusters im Punktwolkendiagramm (Abbildung 25) ist hier der Unterschied zur rein manuellen Messung gut zu beobachten. Jedem gemessenen Wert auf der horizontalen X-Achse (CT) kann ein in etwa gleich großer Wert auf der Y-Achse (MRI) zugeordnet werden. Nach durchgeführtem zweiseitigem gepaartem Student`s T-Test ergab sich bei einem angenommenen Signifikanzniveau von α=0,05 ein P-Wert von 0,20. Die Nullhypothese konnte somit bestätigt werden. - 45 - Obwohl die unterschiedlich großen Durchmesser statistisch nicht signifikant waren, konnten rückblickend leicht vergrößert gemessene MR-Stentdurchmesser festgestellt werden. Die Intra-Technik Variabilität beschreibt hier den durchschnittlich gemessenen Unterschied der Durchmesserlängen jedes Messpaares (MR/CT). Dieser lag hier bei nur -0,17 +/- 1,1 mm. Ein Bland-Altman Diagramm (Abb. 26) wird hierzu nachfolgend aufgeführt. Differenz in mm Y X Anzahl der Messpaare Abbildung 26: Bland-Altman Diagramm zur Intra-Technik Variabilität. Es beschreibt hier den durchschnittlich gemessenen Unterschied der Aortenstentdurchmesser jedes Messpaares (schwarze waagrechte Linie) sowie alle Einzeldifferenzen jedes Messpaares (schwarze Punkte). Die Y-Achse zeigt die Differenzwerte jedes Messpaares (Magnetresonanztomographie/Computertomographie) in mm aller Aortenstentdurchmesser eines Patienten; Die X-Achse zeigt die Anzahl der Messpaare (insgesamt 63); Waagrechte schwarze Linie in der Mitte: Mittelwert der Differenzen; rote Linien: Grenzen des 95% Konfidenzintervalls. - 46 - 3.4. Manuelle Vergleichsmessungen der registrierten Bilddatensätze durch einen unabhängigen Korrektor Die erhaltenen registrierten Bilddatensätze wurden anschließend noch einmal von einem zweiten unabhängigen Korrektor vermessen. Die hieraus gewonnenen Messwerte sind in Tabelle 4c des Appendix enthalten. Auch hier wurden die Ergebnisse gemittelt und im folgenden Balkendiagramm mit den jeweiligen Standartabweichungen (Abb. 27) dargestellt. durchschnittliche Durchmesserlänge im mm 30 Ø MR 25 Ø CT 20 15 10 5 21,7 0 21,7 23,1 D1 (mm) 23,1 22 D2 (mm) 21,8 D3 (mm) Messbereiche der Aortenstents Abbildung 27: Balkendiagramm aller, durch einen Korrektor gemessenen Aortenstentdurchmesser der untersuchten Patienten im Durchschnitt mit ihren jeweiligen Standartabweichungen nach erfolgter Registrierung durch 3DSlicer. Es wurde jeweils proximal, mittig und distal gemessen. mm=Millimeter, Ø=Durchschnitt, CT=Computertomographie; MR=Magnetresonanztomographie; Vertikale Linien in den jeweiligen Balken=Standartabweichungen. Die gemessenen Daten (Tabelle 4c) wurden ebenfalls mittels Punktwolkendiagramm (Abb. 28) veranschaulicht. - 47 - 40 Stentdurchmesser MR [mm] 35 30 25 y = 0,9895x + 0,1616 R² = 0,94 P= 0,58 20 15 10 10 15 20 25 30 35 Stentdurchmesser CT [mm] Abbildung 28: Punktwolkendiagramm der Aortenstentdurchmesser (Tabelle 4c) der computertomographisch (vertikale Achse) (horizontale Messungen Achse) durch und einen magnetresonanztomographischen Beobachter nach vorheriger landmarkenbasierter Registrierung durch 3DSlicer; mm=Millimeter; schwarze diagonale Linie=Trendlinie, MR=Magnetresonanztomographie, CT=Computertomographie, y=Steigung der Trendlinie (Regressionsfunktion), x=Platzhalter für beliebigen Wert auf der X-Achse, R²=Bestimmtheitsmaß (Bildet sich aus dem Quadrat des Korrelationskoeffizienten), P=Signifikanzwert (P-Wert). Der Pearson Korrelationskoeffizient errechnete sich mit 0,97 (p<0,01). Der Rangkorrelationskoeffizient nach Spearman ergab 0,97 (p<0,01). Nach durchgeführtem zweiseitigem gepaartem Student`s T-Test ergab sich bei einem angenommenen Signifikanzniveau von α=0,05 ein P-Wert von 0,58. Auch hier konnte die Nullhypothese somit bestätigt werden. Die Intra-Technik Variabilität lag hier bei -0,07 +/- 1 mm. Ein Bland-Altman Diagramm (Abb. 29) wird hierzu ebenfalls nachfolgend aufgeführt. - 48 - Differenzwerte in mm Y X Anzahl der Messpaare Abbildung 29: Bland-Altman Diagramm der intra-Technik Variabilität des Korrektors. Es beschreibt hier den Aortenstentdurchmesser durchschnittlich gemessenen Unterschied jedes Messpaares (schwarze waagrechte Linie) sowie alle Einzeldifferenzen jedes Messpaares (schwarze Punkte). Die Y-Achse zeigt Differenzwerte der jedes Messpaares in die Millimeter (Magnetresonanztomographie/Computertomographie) aller Aortenstentdurchmesser eines Patienten; Die X-Achse zeigt die Anzahl der Messpaare (insgesamt 63); Waagrechte schwarze Linie in der Mitte: Mittelwert der Differenzen; rote Linien: Grenzen des 95% Konfidenzintervalls. Zum weiteren Vergleich der Inter-Observer Variabilität wurden folgende BlandAltman Diagramme berechnet. Abbildung 30 zeigt die Differenzen aller gemessenen CT-Durchmesser der ersten Messreihe im Vergleich zu den CTMessungen des Korrektors. Der Mittelwert der Differenzen lag bei -0,03 +/- 0,84 mm (p=0,77). - 49 - Differenzwerte in mm Y X Anzahl der Messpaare Abbildung 30: Bland-Altman Diagramm der Inter-Observer Variabilität der computertomographischen Messungen der Aortenstentdurchmesser. Es zeigt die Differenzen aller manuell gemessenen Computertomographiedurchmesser der ersten Messreihe im Vergleich zu den Computertomographiemessungen des Korrektors nach erfolgter Registrierung durch 3DSlicer. Die Y-Achse zeigt die Differenzwerte jedes Computertomographie-Messpaares in Millimeter der Originalmessung und der Nachkontrolle (Korrektor). Die X-Achse zeigt die Anzahl der Messpaare (insgesamt 63); waagrechte schwarze Linie in der Mitte: Mittelwert der Differenzen; rote Linien: Grenzen des 95% Konfidenzintervalls. Abbildung 31 bildet abschließend das Pendant für die jeweiligen MR-Messungen der beiden Beobachter. Hier lag der Mittelwert bei -0,13 +/- 1 mm (p=0,3). - 50 - Differenzwerte in mm Y X Anzahl der Messpaare Abbildung 31: Bland-Altman Diagramm der Inter-Observer Variabilität der magnetresonanztomographischen Messungen der Aortenstentdurchmesser. Es zeigt die Differenzen aller manuell gemessenen Magnetresonanztomographiedurchmesser der ersten Messreihe im Vergleich zu den Magnetresonanztomographiemessungen des Korrektors nach erfolgter Registrierung durch 3DSlicer. Die Y-Achse zeigt die Differenzwerte jedes magnetresonanztomographischen Messpaares in Millimeter der Originalmessung und der Nachkontrolle (Korrektor); Die X-Achse zeigt die Anzahl der Messpaare (insgesamt 63); waagrechte schwarze Linie in der Mitte: Mittelwert der Differenzen; rote Linien: Grenzen des 95% Konfidenzintervalls. - 51 - 4. Diskussion Transluminal eingebrachte endovaskuläre Stentgrafts werden zunehmend bei der Behandlung des thorakalen Aortenaneurysmas sowie der akuten traumatischen Aortenruptur verwendet. Diese Patienten profitieren im Vergleich zur offen chirurgischen Therapie von einer deutlich niedrigeren perioperativen Mortalität aufgrund des minimal invasiven Vorgehens und dem damit verbundenen geringeren auftreten postoperativer Komplikationen [67]. In der vorliegenden Arbeit wurden insgesamt 21 Patienten untersucht, davon 14 Männer und 7 Frauen mit einem Durchschnittsalter von ca. 39 Jahren. Bei allen 21 Patienten wurden insgesamt 378 planimetrische Einzelmessungen durchgeführt. Pro implantierten Stentgraft wurde anhand der vorhandenen MR- und CTBilddatensätze je 6 Mal proximal, mittig sowie am distalen Ende der Endoprothesendurchmesser bestimmt. Wir erhielten somit 2 Gruppen verschiedener Messwerte, welche sich einerseits aus den MRT-Bildern zum anderen aus den CT-Bildern der Endoprothese zusammensetzten. Nachfolgend wurden die erhaltenen Werte miteinander verglichen und auf ihre Signifikanz geprüft. Um eine mögliche Anwendbarkeit der MRT gegenüber der CT im Rahmen notwendiger Follow-ups nach TEVAR zu prüfen, war die qualitative Bewertung des vorhandenen Bildmaterials notwendig. Hierzu wurde in Kapitel 1.6 bereits folgende Fragestellung formuliert: Kann die Magnetresonanztomographie vergleichbares Bildmaterial zur Computertomographie erbringen, d.h. ist der Stentgraft eindeutig zu sehen (Lagebeurteilung des Stents) und von den benachbarten anatomischen Strukturen (z.B. Anliegen an der Aortenwand) klar abzugrenzen? Wie in der vorliegenden Arbeit bereits mehrfach veranschaulicht wurde, ist eine Ergebnisbeurteilung nach TEVAR bei verwendetem MR-kompatiblem Stentgraft (Nitinolgerüst) durch eine zeitlich aufgelöste MRT in 3D SSFP (Steady-State-Free - 52 - Precession)-Sequenz möglich. Im untersuchten Patientenkollektiv konnte die MRBildgebung erfolgreich abgeschlossen werden. Das Stentgerüst verursachte bei der MRT einen Signalverlust, welcher den Stent in der axialen Ebene als schwarzen Ring gut sichtbar darstellte und vom inhomogenen Gefäßlumen abgrenzte. Die thorakalen Endoprothesen konnten hierbei mindestens mit mittelmäßig bis guter Bildqualität erkannt werden. Bei komplett an der Aortenwand anliegenden Endoprothesen gestaltete sich eine genaue Abgrenzung des Stentgerüsts von der Aortenwand anfänglich als etwas schwierig. Nicht komplett anliegende Stents oder ins Aortenlumen ragende Stentenden sind jedoch ohne Einschränkung gut abgrenzbar zur Umgebung gewesen. Unsere Ergebnisse bezüglich einer qualitativen Beurteilbarkeit aortaler Nitinolstents bei der MR-Bildgebung sind mit anderen Arbeiten vergleichbar. So beschreiben Weigel et al. ebenfalls eine überwiegend gut sichtbare Stentkonfiguration ohne fundamental einschränkende Artefaktbildung im Vergleich zur CT Diagnostik nach TEVAR. Allen 11 Patienten wurde ein vergleichbarer Medtronic Talent Endograft, bestehend aus einem Nitinol-Stützgerüst sowie einer Rohrwandung aus Polyester, implantiert. Das Stentgerüst war hier ebenfalls vom inhomogen signalverstärkten Gefäßlumen gut abzugrenzen. Die Lokalisation der Stentgrafts konnte bei der MR-Bildgebung im Vergleich zur CT-Bildgebung daher problemlos durchgeführt werden [67]. Andere Arbeiten sprechen trotz unterschiedlich angewandter MR- Akquisitionsparameter und MR-Sequenzen in vitro und in vivo von mindestens durchschnittlicher bis exzellenter Bildqualität der dargestellten Nitinolstents [35, 57, 9, 4]. Zu den entscheidenden Faktoren scheint hierbei eine gute MRKompatibilität durch nahezu fehlenden Ferromagnetismus des Stentmaterials zu gehören. Nitinol, eine Nickel-Titan Legierung, eignet sich daher besonders gut. Suszeptibilitätsartefakte treten bei Nitinolstents bei Standartfeldstärken von 1,5 Tesla in deutlich geringerem Umfang auf. Im Gegensatz dazu wird die Beurteilung von Stentgrafts, welche aus einem Stahl- oder Kobaltgerüst bestehen, als sehr schwierig beschrieben [36]. Bei ausreichender Bildqualität der untersuchten Endografts formulierten wir folgende Fragestellung: - 53 - Sind somit auch planimetrische Messungen (z.B. Sagittal- und Transversaldurchmesser) möglich? Genaue planimetrische Messungen des sagittalen Stentdurchmessers konnten bei allen Patienten in jeweils 3 verschiedenen Stentpositionen (Proximal, Mitte, Distal) erfolgreich durchgeführt werden. Rein manuelle, vergleichbare Messungen waren jedoch aufgrund der nicht exakt reproduzierbaren Lagerungsmöglichkeit der Patienten zur CT- bzw. MR-Bildgebung nicht möglich. Die Nullhypothese (Stentdurchmesser sind gleich groß) wurde hier wiederlegt. Daher wurden die Bilddatensätze vorab registriert und so möglichst exakt aufeinander abgebildet. Die Registrierung erfolgte in der vorliegenden Arbeit bei jedem Patienten landmarkenbasiert. Der Registrierungsvorgang erwies sich im Verlauf als unerlässlich und führte zu sehr genauen und vergleichbaren Messergebnissen der Stentdurchmesser trotz unterschiedlichen Bildmaterials. Die Nullhypothese konnte dann bestätigt werden. Vergleichbare Arbeiten hierzu finden sich leider kaum. Weigel et al. beschreiben die manuelle Messung des minimalen und maximalen Stentgraftlumendurchmessers bei 11 Patienten nach TEVAR. Die Bildbeurteilung sowie die manuelle Vermessung der CT- und MR-Bilddatensätze wurden hierbei durch 2 Radiologen durchgeführt. Genaue Messprotokolle werden in diesem Zusammenhang jedoch nicht genannt. Weder die Vermessungsebene noch die genauen Anfangs- und Endpunkte der planimetrischen Messungen sind angegeben. Der durchschnittliche Längenunterschied zwischen den Stentgraftlumina der CT- und MRT-Datensätze wurde mit weniger als 1 mm angegeben. Weitere Signifikanztests oder Bland-Altman Diagramme zur Veranschaulichung der berechneten intra- und inter-Observer Variabilitäten werden nicht aufgeführt [67]. Ayuso et al. untersuchten 28 Patienten nach EVAR auf der Suche nach Endoleaks während des Follow-ups mittels CT- und MR-Angiographie. 27 Patienten wurden aufgrund eines abdominellen, ein Patient aufgrund eines thorakalen Aortenaneurysmas behandelt. Allen Patienten wurde ein Nitinolstent implantiert. Weiter wurden die maximalen Durchmesser der gefundenen Endoleaks der CT- 54 - und MR-Datensätze manuell gemessen und miteinander verglichen. Der durchschnittliche Maximaldurchmesser der im CT gesehenen Endoleaks lag bei 56,7 mm (Range: 39 – 93mm), bei den MR-Bildern lag dieser bei 58,8mm (Range: 37 – 96mm). Im statistischen Vergleich der Durchschnittswerte beider Bilddatensätze wurde der P-Wert mit 0,165 berechnet [4]. Hilfiker et al. nahmen in Vitro Vergleichsmessungen unterschiedlicher Endografts (Kobalt basiert, Nitinol oder Edelstahl) vor. Die Lumendurchmesser waren definiert als orthogonal zur Stent-Längsachse gemessene Strecken, welche ihren Anfangsund Endpunkt innerhalb der halbmaximalen oder minimalen Signalintensität hatten. Zur Bildgebung wurden KM verstärkte 3D Gradientenechosequenzen mittels einem 1,5 T MRT (Signa EchoSpeed; GE Medical System, Milwaukee, Wis) mit einer antero-posterior phased-array Oberflächenspule erzeugt. Die erhaltenen Messungen wurden dann mit den tatsächlich bekannten Durchmesserangaben des Herstellers des jeweiligen Endografts verglichen. Leider wurde hier auf die absolute Angabe der gemessenen Werte verzichtet, da der Fokus der Arbeit auf der Messbarkeit des Gefäßlumens innerhalb unterschiedlicher Endografts im Hinblick auf sich darstellenden Bildartefakten lag. Nitinolstents stellten sich am artefaktärmsten dar. Die hierbei gemessenen Durchmesser waren 0-20% kürzer im Vergleich zur Herstellerangabe [26]. Bei unseren Ergebnissen waren minimal vergrößerte MR-Messungen im Vergleich zu den CT-Messungen auffällig, welche jedoch nicht signifikant waren. Bei Beobachter 1 war dies häufiger der Fall als bei Beobachter 2. Ursache hierfür ist sehr wahrscheinlich eine niedrigere räumliche MR-Auflösung und die häufig etwas verschwommene Darstellung des Stentgerüsts. Die stattfindende Signalauslöschung des Stentgerüsts bei den MR-Datensätzen stellt sich im Vergleich zu den CT-Aufnahmen somit als etwas breitere Linie dar. Gemäß unserem Messprotokoll, welches die Messungen der Durchmesseranfangs- und endpunkte innerhalb des Stentgerüsts zu bestimmen vorsieht, lässt einen personenbezogenen Spielraum im Zehntelmillimeter- bis Millimeterbereich zu. Hier könnte es sich um einen personenbezogenen systematischen Methodenfehler handeln, welcher sich in der Intra- und Inter-Observervariabilität wiederspiegelt. Die beobachteten Differenzen zwischen CT- und MR-Durchmesser lagen jedoch weit unter den bisher veröffentlichten Angaben bezüglich einer reproduzierbaren Quantifizierung von CT-Scans [54, 39]. Richtigkeit und Präzision konnten aufgrund - 55 - der erfolgten Registrierung der Datensätze deutlich gesteigert werden, was die errechneten Mittelwerte und Standartabweichungen belegen. Bezüglich der Inter-Observer Variabilität der CT-Datensätze lagen wir mit -0,03 +/- 0,84 mm (p=0,77) ebenfalls deutlich unter vergleichbaren Angaben gegenwärtiger Literatur [56, 68]. Für die MR-Datensätze zeigten sich ähnlich exakte und reproduzierbare Vergleichsmessungen mit einem durchschnittlichen Unterschied von -0,13 +/- 1 mm (p=0,3). Vergleichende Arbeiten konnten hierzu leider keine gefunden werden. Aktuell lassen sich Arbeiten bezüglich manueller MR- und CT- Vergleichsmessungen einzelner Stentdurchmesser nach TEVAR anhand der gering vorhandenen Literatur nur teilweise miteinander vergleichen. Neben unterschiedlicher Aquisitionsprotokolle der MR- und CT-Datensätze sowie unterschiedlich verwendeter Endografts gibt es ebenso wenig einheitliche Messprotokolle der einzelnen Beobachter. MRT geeignete Endografts sind aufgrund ihrer geringen Neigung zur Artefaktbildung für genaue planimetrische Messungen wünschenswert [67]. Bezüglich der vorliegenden Arbeit wurde daher folgende Fragestellung formuliert: Stellen MRT typische Artefaktbildungen der untersuchten Endoprothesen ein Problem bei der Auswertung des Bildmaterials dar? MR-typische Artefaktbildung von Endoprothesen (hauptsächlich Suszeptibilitätsund Abschirmungsartefakte) wird in der gegenwärtigen Literatur unterschiedlich bewertet. Für die kontrastmittelverstärkte MR-Angiographie scheinen nicht ferromagnetische Stentgrafts (z.B. Nitinol- Platinum- oder Kobaltstentlegierungen) am besten geeignet zu sein. Wang et al. berichten bezüglich getesteter NitinolPlatinum– oder Kobaltstentgrafts über nur unerheblich auftretende Suszeptibilitätsartefakte. Im Gegensatz dazu zeigten Edelstahlstents einen kompletten Signalverlust, ohne verwertbares Bildmaterial zu erbringen. Variabel zeigte sich der Signalverlust (14 -77%) aufgrund unterschiedlich schwer auftretender Abschirmungsartefakte der stahlfreien Stentgrafts [66]. Nicht ferromagnetisches, jedoch leitfähiges Material kann Hochfrequenzströme - 56 - induzieren, welche ebenfalls zu verzerrtem Bildmaterial führen können [18]. Ein gutes Gefäßlumensignal ist abhängig von der Stentgeometrie, der relativen Orientierung zur magnetischen Feldrichtung sowie der Legierung des Stentgerüsts [36]. Des Weiteren wird die Neigung zur Artefaktbildung durch die magnetische Feldstärke, der Echozeit sowie der Orientierung zum Auslesegradienten beeinflusst. Gawenda et al. untersuchten 8 unterschiedliche abdominale Endografts, darunter waren 2 Edelstahl- sowie 5 Nitinol- und 1 Elgiloystentgerüst. Diese wurden jeweils von 4 unabhängigen Beobachtern (3 Radiologen, 1 Gefäßchirurg) auf ihre Anwendbarkeit nach MR-Akquisition im Vergleich zu den jeweiligen CT-Bilddatensätzen bewertet. Lediglich 3 Nitinolprothesen konnten vergleichbares MR-Bildmaterial liefern [18]. Andere Autoren kommen zu dem Ergebnis das Stahl – sowie Nitinolstents aufgrund ihrer Artefaktbildung nicht geeignet wären, um einen intraluminalen Stenosegrad im Bereich der Arteria iliaca communis verlässlich anzugeben [41]. In der vorliegenden Arbeit konnten alle Endoprothesen systematisch vermessen werden. Artefaktbildung war bei den ausschließlich im Bereich der thorakalen Aorta implantierten Nitinolstents zwar vorhanden, es ergaben sich hieraus jedoch keine gravierenden Probleme bzgl. der durchzuführenden planimetrischen Messungen der Stentdurchmesser. landmarkenbasierten Registrierung Auch durch bei 3D der zuvor durchgeführten Slicer war unterschiedliche Artefaktbildung kein limitierender Faktor. Das Programm arbeitete hier problemlos. Optimierte MR-Einstellungen konnten eine übermäßige Artefaktbildung bei gleichzeitig ordentlichem SNR bereits von vorne herein auf ein Minimum reduzieren. Als Beispiel sind hier EKG-getriggerte Funktions-MR-Scans zu nennen zur Reduktion von Bewegungsartefakten. Durchschnittlich betrug die Akquisitionsdauer ca. 30 Minuten und wurde von den Patienten gut toleriert. - 57 - Abschließend ist noch folgende Frage zu diskutieren: Sind Komplikationen (z.B. Endoleaks) nach TEVAR effektiv mittels MRT Diagnostik frühzeitig zu erkennen? Die aktuelle Literatur legt hier einen deutlichen Vorteil zu Gunsten der MR nahe. Bei Patienten nach EVAR zeigten Habets et al., dass durchgeführte MR-Scans eine weitaus höhere Sensitivität bei der Früherkennung von Endoleaks im Vergleich zur CT besitzen [23]. In der vorliegenden Arbeit war im Vorfeld bei keinem unserer Patienten ein Endoleak dokumentiert worden. Während unserer MR-Scans konnte ebenfalls kein Endoleak entdeckt werden. Eine Aussage ist daher diesbezüglich nicht möglich. - 58 - 5. Zusammenfassung Gegenüber dem Goldstandard der Computertomographie (CT) zeichnet sich die Magnetresonanztomographie (MRT) neben der rein statischen Bilddarstellung der thorakalen Endoprothese funktionellen gerade durch Informationsgewinnung aus. die zusätzliche Hierbei stehen Möglichkeit der besonders die Stentdynamik sowie die Visualisierung der hämodynamischen Auswirkungen auf die Endoprothese im Vordergrund. Begrenzende Faktoren beim magnetresonanztomographischen Einsatz sind hauptsächlich magnetresonanztomographisch inkompatible Stentgrafts oder andere künstliche Implantate. Hierbei kann es neben massiven Bildartefakten auch zu einem kompletten Signalverlust wichtiger Bereiche bei den Bilddatensätzen kommen. Darüber hinaus könnten ferromagnetische Endografts innerhalb dieser starken magnetischen Wechselfelder erhitzen oder sogar ihre Position ändern. Allerdings ist die Mehrzahl der heutzutage verwendeten Endografts für magnetresonanztomographische Untersuchungen geeignet und kann daher bedenkenlos einer magnetischen Feldstärke von mindestens 1,5 Tesla ausgesetzt werden. Bei den meisten Knochenverletzungen unserer vor, Multitraumapatienten welche ebenfalls mittels lagen multiple Metallimplantaten osteosynthetisch versorgt werden mussten. Keiner dieser Patienten musste aus Sicherheitsgründen von unserer Studie ausgeschlossen werden oder zeigte unverwertbares Bildmaterial. Bei dem erhobenen Datenmaterial ist auf das Fehlen von Langzeitergebnissen hinzuweisen. Die untersuchten Patienten zeigten weiter keinerlei Komplikationen nach einer thorakalen endovaskulären Aortenreparatur (TEVAR). Endoleaks traten nicht auf. An der Studie nahmen ausschließlich Patienten mit erlittener thorakaler Aortenruptur im Übergangsbereich zwischen Aortenbogen und Aorta deszendenz teil. Das Patientenkollektiv, bestehend aus Patienten mit solch schwerwiegenden, meist tödlich verlaufenden Verletzungen, ist daher als klein zu betrachten. Eine Empfehlung zur ausschließlichen Verwendung der MR-Technologie nach TEVAR kann daher nicht ausgesprochen werden. Allerdings bietet das Beurteilungsmöglichkeiten MRT-Verfahren der implantierten zusätzliche umfangreiche Stentgrafts. Planimetrische - 59 - Messungen sowie die Erfassung der Stentbewegung innerhalb des Organismus sind bei der MRT ohne den Einsatz ionisierender Strahlung und nephrotoxischer Kontrastmittelgabe möglich und machen diese daher zu einer sehr attraktiven Alternative zum gängigen Goldstandard der CT während des weiteren Follow-up nach TEVAR. - 60 - 6. Literaturverzeichnis 1. Ali SH, Modic ME, Mahmoud SY, Jones SE: Reducing clinical MRI motion degradation using a prescan patient information pamphlet. AJR Am J Roentgenol 200: 630-4 (2013) 2. American College of Radiology http://www.acr.org/~/media/ACR/Documents/AppCriteria/RadiationDoseAs sessmentIntro.pdf (15.11. 2016) 3. Attar S, Cardarelli MG, Downing SW, Rodriguez A, Wallace DC, West RS, McLaughlin JS: Traumatic aortic rupture: recent outcome with regard to neurologic deficit. Ann Thorac Surg 67: 959-64; discussion 964-5 (1999) 4. Ayuso JR, de Caralt TM, Pages M, Riambau V, Ayuso C, Sanchez M, Real MI, Montaña X: MRA is useful as a follow-up technique after endovascular repair of aortic aneurysms with nitinol endoprostheses. J Magn Reson Imaging 20: 803-10 (2004) 5. Baqué P, Serre T, Cheynel N, Arnoux PJ, Thollon L, Behr M, Masson C, Delotte J, Berdah SV, Brunet C: An experimental cadaveric study for a better understanding of blunt traumatic aortic rupture. J Trauma 61: 58691 (2006) 6. Bartels LW, Bakker CJ, Viergever MA: Improved lumen visualization in metallic vascular implants by reducing RF artifacts. Magn Reson Med 47: 171-80 (2002) 7. Lehrbuch Ben-Menachem Y, Handel SF: The Mechanism of Injury. Angiography in Trauma. A work atlas. London WB Saunders, S. 25-46 (1981) 8. Biglioli P, Spirito R, Porqueddu M, Agrifoglio M, Pompilio G, Parolari A, Dainese L, Sisillo E: Quick, simple clamping technique in descending thoracic aortic aneurysm repair. Ann Thorac Surg 67: 1038-43; discussion 1043-4 (1999) 9. Cejna M, Loewe C, Schoder M, Dirisamer A, Hölzenbein T, Kretschmer G, Lammer J, Thurnher S: MR angiography vs CT angiography in the follow-up of nitinol stent grafts in endoluminally treated aortic aneurysms. Eur Radiol12: 2443-50 (2002) - 61 - 10. Cook J, Salerno C, Krishnadasan B, Nicholls S, Meissner M, KarmyJones R: The effect of changing presentation and management on the outcome of blunt rupture of the thoracic aorta. J Thorac Cardiovasc Surg 131: 594-600 (2006) 11. Lehrbuch Drössel O: Bildgebende Verfahren in der Medizin. Springer Berlin Heidelberg , S.111, Abb. 4.7 (2000) 12. Fa. Medtronic Bild eines Medtronic Valiant Endograft (genehmigt 23.04.2015) 13. Fa. Siemens Healthcare GmbH http://www.medizinischestrahlung.de/verfahren-der-medizinischenbildgebung/bildgebende-verfahren-mitrontgenstrahlung/computertomografie-ct/ (Abdruck mit freundlicher Genehmigung der Fa. Siemens Healthcare GmbH 14.04.2015) 14. Fabian TC, Richardson JD, Croce MA, Smith JS Jr, Rodman G Jr, Kearney PA, Flynn W, Ney AL, Cone JB, Luchette FA, Wisner DH, Scholten DJ, Beaver BL, Conn AK, Coscia R, Hoyt DB, Morris JA Jr, Harviel JD, Peitzman AB, Bynoe RP, Diamond DL, Wall M, Gates JD: Prospective study of blunt aortic injury: Multicenter Trial of the American Association for the Surgery of Trauma. J Trauma 42: 374-80; discussion 380-3 (1997) 15. Fattori R, Celletti F, Descovich B, Napoli G, Bertaccini P, Galli R, Gavelli G, Pierangeli A: Evolution of post-traumatic aortic aneurysm in the subacute phase: magnetic resonance imaging follow-up as a support of the surgical timing. Eur J Cardiothorac Surg 13: 582-6; discussion 586-7 (1998) 16. Feczko JD, Lynch L, Pless JE, Clark MA, McClain J, Hawley DA: An autopsy case review of 142 nonpenetrating (blunt) injuries of the aorta. J Trauma 33: 846-9 (1992) 17. Fernandez V, Mestres G, Maeso J, Domínguez JM, Aloy MC, Matas M: Endovascular treatment of traumatic thoracic aortic injuries: short- and medium-term Follow-up. Ann Vasc Surg 24: 160-6 (2009) 18. Gawenda M, Gossmann A, Krüger K, Zaehringer M, Hahn M, Wassmer G, Brunkwall J: Comparison of magnetic resonance imaging and computed tomography of 8 aortic stent-graft models. J Endovasc Ther 11: 627-34 (2004) - 62 - 19. Gawenda M, Zähringer M, Görg C, Südkamp M, Haupt WF, Koebke J, Brunkwall J: Das Dilemma der spinalen Ischämie: Interdisziplinäre Strategien zum Schutz vor spinaler Ischämie bei Aortenchirurgie. Dtsch Arztebl 102: A 201–208 ( 2005) 20. Go MR, Barbato JE, Dillavou ED, Gupta N, Rhee RY, Makaroun MS, Cho JS: Thoracic endovascular aortic repair for traumatic aortic transection. J Vasc Surg 46: 928-33 ( 2007) 21. Grobner T: Gadolinium – a specific trigger for the development of nephrogenic fibrosing dermopathy and nephrogenis systemic fibrosis?. Nephrol Dial Transplant 21: 1104-1108 (2006) 22. Haacke EM, Xu Y, Cheng NYC, Reichenbach JR: Susceptibility Weighted Imaging (SWI). Magn Reson Med 52: 612–618 (2004) 23. Habets J, Zandvoorte HJA, Reitsma JB, Bartels LW, Moll FL, Leinere T, van Herwaardene JA: Magnetic Resonance Imaging is More Sensitive than Computed Tomography Angiography for the Detection of Endoleaks after Endovascular Abdominal Aortic Aneurysm Repair: A Systematic Review. Eur J Vasc Endovasc Surg 45: 340-50 (2013) 24. Hanssen SJ, Derikx JP, Vermeulen Windsant IC, Heijmans JH, Koeppel TA, Schurink GW, Buurman WA, Jacobs MJ: Visceral injury and systemic inflammation in patients undergoing extracorporeal circulation during aortic surgery. Ann Surg 248:117-125 ( 2008) 25. Hartley MC, Langan EM, Cull DL, Taylor SM, Carsten CG, Blackhurst DW: Evaluation of the diameter of the proximal descending thoracic aorta with age: implications for thoracic aortic stent grafting. Ann Vasc Surg 23: 639-44 (2009) 26. Hilfiker PR, Quick HH, Debatin JF: Plain and covered stent-grafts: in vitro evaluation of characteristics at three-dimensional MR angiography. Radiology 211: 693-7 (1999) 27. Hoffer EK, Forauer AR, Silas AM, Gemery JM: Endovascular stent-graft or open surgical repair for blunt thoracic aortic trauma: systematic review. J Vasc Interv Radiol 19: 1153-64 ( 2008) 28. Jahromi AS, Kazemi K, Safar HA, Doobay B, Cinà CS: Traumatic rupture of the thoracic aorta: cohort study and systematic review. J Vasc Surg 34: 1029-34 ( 2001) 29. Jamieson WR, Janusz MT, Gudas VM, Burr LH, Fradet GJ, Henderson C: Traumatic rupture of the thoracic aorta: third decade of experience. Am J Surg 183: 571-5 (2002) - 63 - 30. Jonker FH, Giacovelli JK, Muhs BE, Sosa JA, Indes JE: Trends and outcomes of endovascular and open treatment for traumatic thoracic aortic injury. J Vasc Surg 51: 565-71( 2010) 31. Katz NM, Blackstone EH, Kirklin JW, Karp RB: Incremental risk factors for spinal cord injury following operation for acute traumatic aortic transection. J Thorac Cardiovasc Surg 81: 669-74 (1981) 32. Kodali S, Jamieson WR, Leia-Stephens M, Miyagishima RT, Janusz MT, Tyers GF: Traumatic rupture of the thoracic aorta. A 20-year review: 1969-1989. Circulation 84:III40-6 (1991) 33. Kortmann H, Johnsen F: Elf Jahre Erfahrung mit der endovaskulären Aortenrekonstruktion. Hamburger ÄBl 60: 520 (2006) 34. Kpodonu J, Wheatley GH, Ramaiah VG, Diethrich EB: Endovascular management of a thoracic aortic disruption following failure of deployment of a parachute. Interact Cardiovasc Thorac Surg 6: 823-4 (2007) 35. Krämer SC, Wall A, Maintz D, Bachmann R, Kugel H, Heindel W: 3.0 Tesla magnetic resonance angiography of endovascular aortic stent grafts: phantom measurements in comparison with 1.5 Tesla. Invest Radiol 39: 413-7 (2004) 36. Lenhart M, Voelk M, Manke C, Nitz WR, Strotzer M, Feuerbach S, Link J: Stent Apearance at Contrast-enhanced MR Angiography: in vitro Examination with 14 stents. Radiology 217:173-8 (2000) 37. Lettinga-van de Poll T, Schurink GW, De Haan MW, Verbruggen JP, Jacobs MJ: Endovascular treatment of traumatic rupture of the thoracic aorta. Br J Surg 94: 525-33 (2007) 38. Lin PH, Bush RL, Zhou W, Peden EK, Lumsden AB: Endovascular treatment of traumatic thoracic aortic injury--should this be the new standard of treatment? J Vasc Surg 43: 22A-29A ( 2006) 39. Lu TL, Rizzo E, Marques-Vidal PM, Segesser LK, Dehmeshki J, Qanadli SD: Variability of ascending aorta diameter measurements as assessed with electrocardiography-gated multidetector computerized tomography and assisted diagnosis software. Interact Cardiovasc Thorac Surg 10: 217-21 (2010) 40. Maintz D, Fischbach R, Juergens KU, Allkemper T, Wessling J, Heindel W: Multislice CT angiography of the iliac arteries in the presence of various stents: in vitro evaluation of artifacts and lumen visibility. Invest Radiol 36: 699-704 (2001) - 64 - 41. Maintz D, Kugel H, Schellhammer F, Landwehr P: In vitro evaluation of intravascular stent artifacts in three dimensional MR angiography. Invest Radiol 36: 218-24 (2001) 42. Marckmann P, Skov L, Rossen K, Dupont A, Damholt MB, Heaf JG, Thomsen HS: Nephrogenic systemic fibrosis: suspected causative role of gadodiamide used for contrast-enhanced magnetic resonance imaging. J Am Soc Nephrol17: 2359-2362 (2006) 43. McGwin G Jr, Metzger J, Rue LW: The influence of side airbags on the risk of head and thoracic injury after motor vehicle collisions. J Trauma 56: 512-6; discussion 516-7 (2004) 44. Miller LE: Potential long-term complications of endovascular stent grafting for blunt thoracic aortic injury. ScientificWorldJournal 2012: 897489 (2012) 45. Nitz WR http://www.physik.uniregensburg.de/studium/medphys/Nitz/MRT_hndout_ UR_SS2014_v12red.pdf (21.04.2015) 46. Orend KH, Zarbis N, Schelzig H, Halter G, Lang G, Sunder-Plassmann L: Endovascular treatment (EVT) of acute traumatic lesions of the descending thoracic aorta--7 years' experience: Eur J Vasc Endovasc Surg 34: 666-72 ( 2007) 47. Parmley LF, Mattingly TW, Manion WC, Jahnke EJ Jr: Nonpenetrating traumatic injury of the aorta. Circulation ;17: 1086-101 (1958) 48. Plummer D, Petro K, Akbari C, O'Donnell S: Endovascular repair of traumatic thoracic aortic disruption. Perspect Vasc Surg Endovasc Ther 18: 132-9 (2006) 49. Razzouk AJ, Gundry SR, Wang N, del Rio MJ, Varnell D, Bailey LL: Repair of traumatic aortic rupture: a 25-year experience. Arch Surg 135: 913-8; discussion 919( 2000) 50. Reddy VS: Endovascular approaches for traumatic thoracic aortic injury: immediate versus delayed therapy. J Trauma 62: S23 ( 2007) 51. Riesenman PJ, Brooks JD, Farber MA: A review of 100 consecutive cases of acute blunt traumatic thoracic aortic injury to the descending thoracic aorta. J Vasc Surg 56: 1274–1280 (2012) 52. Schlegel W, Bille J: Medizinische Physik 2: Medizinische Strahlenphysik. Springer Berlin Heidelberg New York, S. 261-263 ( 2002) 53. Shah CS, Hardy WN, Mason MJ, Yang KH, Van Ee CA, Morgan R, Digges K: Dynamic biaxial tissue properties of the human cadaver aorta. Stapp Car Crash J 50: 217-46 ( 2006) - 65 - 54. Shimada I, Rooney SJ, Farnati PA: Reproducibility of thoracic aortic diameter measurement using computed tomographic scans. Eur J Cardiothoracic Surg 16: 59-62 (1999) 55. Siegel JH, Smith JA, Siddiqi SQ: Change in velocity and energy dissipation on impact in motor vehicle crashes as a function of the direction of crash: key factors in the production of thoracic aortic injuries, their pattern of associated injuries and patient survival. A Crash Injury Rese. J Trauma57: 760-77; discussion 777-8 ( 2004) 56. Singh K, Jacobsen BK, Solberg S, Bønaa KH, Kumar S, Bajic R, Arnesen E: Intra- and interobserver variability in the measurements of abdominal aortic and common iliac artery diameter with computed tomography. The Tromsø study. Eur J Vasc Endovasc Surg 25: 399-407 (2003) 57. Stavropoulos SW, Charagundla SR: Imaging techniques for detection and management of endoleaks after endovascular aortic aneurysm repair. Radiology 243: 641-55 (2007) 58. Svensson LG, Crawford ES, Hess KR, Coselli JS, Safi HJ: Experience with 1509 patients undergoing thoracoabdominal aortic operations. J Vasc Surg 17: 357-68; discussion 368-70 (1993) 59. Thelen M, Erbel R, Kreitner KF: Bildgebende Kardiodiagnostik. Thieme Verlag, S. 106-107 (2010) 60. von Oppell UO, Dunne TT, De Groot MK, Zilla P: Traumatic aortic rupture: twenty-year metaanalysis of mortality and risk of paraplegia. Ann Thorac Surg 58: 585-93 (1994) 61. W.L. Gore & Associates. Picture of a Gore TAG Endoprothesis. (genehmigt 09.07.2015) 62. W.L. Gore & Associates. Picture of a Gore TAG Endoprothesis in Vivo. (genehmigt 09.07.2015) 63. Lehrbuch WA Kalender: Cumputed Tomography. Publicis Publishing Erlangen, 3. Auflage, S. 27, Bild 1.5 ( 2011) 64. Lehrbuch WA Kalender: Cumputed Tomography. Publicis Publishing Erlangen, 3. Auflage, S. 28, Bild 1.6 ( 2011) 65. Lehrbuch WA Kalender: Cumputed Tomography. Publicis Publishing Erlangen, 3. Auflage, S. 151-152 (2011) - 66 - 66. Wang Y, Truong TN, Yen C, Bilecen D, Watts R, Trost DW, Prince MR: Quantitative evaluation of susceptibility and shielding effects of nitinol, platinum, cobalt-alloy, and stainless steel stents. Magn Reson Med 49: 972-6 (2003) 67. Weigel S, Tombach B, Maintz D, Klotz S, Vestring T, Heindel W, Fischbach R: Thoracic aortic stent graft: comparison of contrastenhanced MR angiography and CT angiography in the follow-up: initial results. Eur Radiol 13: 1628-34 (2003). 68. Wever JJ, Blankensteijn JD, van Rijn JC, Broeders IA, Eikelboom BC, Mali WP: Inter- and intraobserver variability of CT measurements obtained after endovascular repair of abdominal aortic aneurysms. AJR Am J Roentgenol 175: 1279-82 (2000). 69. Wikipedia https://de.wikipedia.org/wiki/Magnetismus#/media/File:Paramagnetism_wit h_and_without_field.svg (08.07.2015) 70. Xenos ES, Abedi NN, Davenport DL, Minion DJ, Hamdallah O, Sorial EE, Endean ED: Meta-analysis of endovascular vs open repair for traumatic descending thoracic aortic rupture. J Vasc Surg 48: 1343-51 (2008) 71. Xenos ES, Minion DJ, Davenport DL, Hamdallah O, Abedi NN, Sorial EE, Endean ED: Endovascular versus open repair for descending thoracic aortic rupture: institutional experience and meta-analysis. Eur J Cardiothorac Surg 35: 282-6 (2009) - 67 - 7. Appendix Manuell eingestellte und gemessene Stentdurchmesser der MR- und CT-Datensätze Patient Nr. MRT 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 D1 (prox.) in mm 28,10 29,50 20,80 22,60 23,40 22,30 23,40 24,60 20,50 27,80 19,10 28,00 27,40 30,80 22,60 23,20 23,60 21,80 22,20 14,40 22,50 CT D2 (Mitte) in mm 25,70 27,40 27,50 30,20 22,40 24,60 20,60 32,10 30,10 26,90 26,20 31,50 36,40 31,20 18,90 25,20 25,60 26,10 25,20 15,10 30,60 D3 (dist.) in mm 18,70 23,10 20,30 23,30 15,50 22,40 15,40 27,20 24,60 26,90 24,60 26,10 29,90 27,90 15,60 23,60 22,20 25,10 24,50 11,90 27,30 D4 (prox.) in mm 29,20 24,90 23,70 25,70 21,30 21,70 20,70 23,50 24,90 24,40 23,50 29,90 25,00 28,00 21,90 25,00 25,10 23,50 21,00 15,70 27,20 D5 (Mitte) in mm 22,60 24,40 24,70 26,90 19,10 21,00 24,40 28,80 33,40 25,70 24,70 33,60 33,70 31,70 20,70 23,60 22,60 24,60 22,60 13,80 28,30 D6 (dist.) in mm 21,90 23,20 18,00 19,20 18,50 19,60 17,90 24,20 22,90 24,10 22,90 27,80 26,60 26,30 18,60 20,60 19,50 22,30 22,50 13,90 24,50 Tabelle 4a: Übersicht der rein manuell eingestellten und gemessenen Aortenstentdurchmesser der magnetresonanztomographischen und computertomographischen Datensätze aller Patienten; mm = Millimeter; D1-6 = Stentdurchmesser, Nr. = Nummer, prox. = proximal, dist. = distal, MRT = Magnetresonanztomographie, CT = Computertomographie - 68 - 1. Messung der mit 3DSlicer registrierten und manuell gemessenen Stentdurchmesser Patient Nr. MRT 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 D1 (prox.) in mm 22,30 26,90 18,80 17,50 24,80 17,20 20,90 17,90 25,10 22,00 13,80 29,10 26,10 20,50 22,10 20,00 16,90 27,00 16,60 21,80 32,10 CT D2 (Mitte) in mm 22,90 25,90 16,00 18,40 33,80 20,50 20,60 21,30 27,10 23,30 15,60 26,50 27,50 17,90 23,10 20,10 24,80 33,90 17,90 23,10 28,00 D3 (dist.) in mm 23,90 23,90 23,20 18,30 22,80 17,60 25,20 22,20 24,50 20,90 13,40 27,50 26,70 16,70 22,10 19,70 22,70 26,00 20,10 22,10 24,10 D4 (prox.) in mm 23,10 27,10 19,30 17,20 23,70 16,60 20,90 18,50 25,30 19,30 13,50 28,70 25,10 22,90 22,10 19,50 16,60 26,20 18,20 22,00 33,10 D5 (Mitte) in mm 24,10 25,90 16,90 17,90 32,00 19,30 20,20 22,40 26,40 22,80 15,20 26,20 25,20 19,10 22,30 18,40 23,80 34,50 18,50 22,20 28,30 D6 (dist.) in mm 24,30 24,50 23,40 20,20 22,40 17,20 24,10 21,50 24,10 18,90 14,10 26,30 24,30 19,00 22,00 18,90 22,40 25,80 18,80 22,50 25,30 Tabelle 4b: Übersicht der 1. Messung der mit 3DSlicer registrierten und manuell gemessenen Aortenstentdurchmesser der magnetresonanztomographischen und computertomographischen Datensätze aller Patienten; mm = Millimeter; D1-6 = Stentdurchmesser, Nr. = Nummer, prox. = proximal, dist. = distal, MRT = Magnetresonanztomographie, CT = Computertomographie - 69 - 2. Messung (Beobachter) der mit 3DSlicer registrierten und manuell gemessenen Stentdurchmesser Patient Nr. MRT 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 D1 (prox.) in mm 23 26,50 19,00 17,30 24,30 18,50 20,40 19,00 25,20 22,00 14,00 28,00 25,20 20,80 21,20 20,00 16,40 26,50 17,10 21,00 31,20 CT D2 (Mitte) in mm 24,50 24,50 16,20 18,60 33,10 19,30 21,00 22,30 25,50 23,20 15,10 28,90 25,10 19,00 22,70 20,60 24,80 32,80 18,50 22,70 26,60 D3 (dist.) in mm 24,80 23,80 23,00 18,30 23,10 18,20 24,30 23,50 25,40 21,50 13,50 27,10 24,90 16,50 22,30 20,00 19,40 27,50 20,40 21,70 22,20 D4 (prox.) in mm 22,60 25,60 19,10 17,10 24,30 16,60 21,00 17,80 24,70 20,50 13,50 27,30 25,40 22,50 21,90 19,30 16,20 26,50 17,40 22,30 33,10 D5 (Mitte) in mm 24,80 26,30 16,50 18,00 32,70 19,40 20,30 23,00 25,70 23,20 14,90 27,10 25,60 20,00 22,10 20,00 23,20 34,00 19,80 23,40 26,10 D6 (dist.) in mm 23,60 24,20 23,20 20,10 22,90 16,90 24,50 23,00 24,60 20,50 14,00 27,10 25,00 18,30 22,30 19,00 19,90 25,80 17,70 20,20 24,80 Tabelle 4c: Übersicht der 2. Messung (Beobachter) der mit 3DSlicer registrierten und manuell gemessenen Aortenstentdurchmesser der magnetresonanztomographischen und computertomographischen Datensätze aller Patienten; mm = Millimeter; D1-6 = Stentdurchmesser, Nr. = Nummer, prox. = proximal, dist. = distal, MRT = Magnetresonanztomographie, CT = Computertomographie - 70 - Danksagung aus Gründen des Datenschutzes entfernt - 71 - Lebenslauf aus Gründen des Datenschutzes entfernt - 72 - Lebenslauf aus Gründen des Datenschutzes entfernt - 73 - Lebenslauf aus Gründen des Datenschutzes entfernt - 74 -