AB 1 Abbaubare Polymere in der Medizin Datum „Hydrolytischer
Werbung

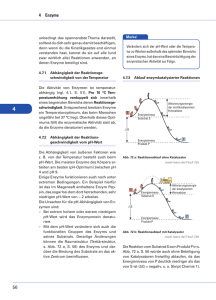
Online - Ergänzungen Arbeitsblätter AB 1 Abbaubare „Hydrolytischer Polymere in Abbau“ der Medizin Datum Bei der Hydrolyse einer Polymerkette findet entweder eine Kettenspaltung an zufälligen Stellen innerhalb der Polymerkette oder die Abspaltung einer Wiederholungseinheit an einem der beiden Kettenenden statt. Polymerart und Länge der Ketten bestimmen den bevorzugten Angriffspunkt. a) b) Abb. 1: Spaltung der Polymerketten an a) zufälligen Stellen oder b) von den Kettenenden aus. Aufgaben: 1. Vervollständigen Sie die Tabelle. Polymer hydrolysierbare Bindung Spaltprodukte nach Hydrolyse - Strukturformeln O R'' Polyamid R' N H Amid-Bindung O O Polyanhydrid R' O R'' Anhydrid-Bindung 2. Beschreiben Sie anhand der Abb. 1a) und Abb. 1b) den jeweiligen Ablauf der Spaltung der Polymerketten. Abbaubare Polymere in der Medizin AB 2 Datum „Enzymatischer Abbau“ Einige abbaubare Polymere werden nur sehr langsam hydrolytisch abgebaut. Der Abbau dieser Polymere kann jedoch durch die Mitwirkung von Enzymen erheblich beschleunigt werden. Was sind Enzyme? Enzyme, sogenannte „Biokatalysatoren“, sind Proteine oder Proteinkomplexe, die biochemische (Stoffwechsel-) Reaktionen in Organismen beschleunigen. Sie werden in sechs verschiedene Enzymklassen eingeteilt, die sich wiederum in Unterklassen aufteilen. Das hierfür verwendete System beruht auf der IUBMB, der „International Union of Biochemistry and Molecular Biology“ (vergleichbar mit der IUPAC in der Chemie). Jedem Enzym wird dabei ein Zahlencode zugeordnet, der die Funktion und Zugehörigkeit des Enzyms erklärt. Am Abbau beteiligte Enzyme gehören zu den Hydrolasen (z.B. Esterasen, Peptidasen) und Oxidoreduktasen (z.B. Oxidasen). Durch Hydrolasen findet eine wasserabhängige Spaltung und durch Oxidasen eine oxidative Spaltung mit Hilfe von Sauerstoff statt. Enzyme sind substratspezifisch und greifen in der Regel nur an bestimmten Stellen in einer Polymerkette an. Die Ursache hierfür liegt im aktiven Zentrum des Enzyms begründet, das spezifisch bestimmte Sequenzen eines Substrates (hier Sequenzen von Wiederholungseinheiten in Polymeren) bindet. Abb. 1: Schematische Darstellung der Spaltung einer Polymerkette (blau) durch ein Enzym (rot) Die Sequenzen mit den spaltbaren Bindungen innerhalb des Polymers müssen jedoch für das Enzym erreichbar sein. Hilfreich hierfür ist eine hohe Flexibilität der Polymerkette. In der Regel bauen Enzyme aufgrund ihrer Größe polymerbasierte Probekörper von außen nach innen ab. Nur bei porösen Strukturen könnten Enzyme direkt in das Innere eines Probekörpers gelangen. Herausragende Flächen (Unebenheiten) werden bevorzugt attackiert. Die Spaltung von Kohlenstoff-Kohlenstoff-Bindungen unter Einwirkung der Enzyme von Mikroorganismen wie Bakterien und Pilzen spielt nur eine geringe Rolle. Aufgaben: 1. Fertigen Sie eine Vorlage für eine Filmstreifensequenz mit mindestens vier Teilbildern an, mit der der makroskopische Abbau von Polymerprobekörpern durch Enzyme von außen nach innen dargestellt wird. O O O H H OH n PCL O O OH n PPDO -caprolacton) [PCL] durch das Enzym Lipase (eine fettspaltende Hydrolase) erfolgt schneller als der von Poly(p-dioxanon) [PPDO]. Erklären Sie. AB 3 Abbaubare Polymere in der Medizin Datum „Oberflächenabbau“ Oberflächenabbau findet bei hydrolytisch abbaubaren Polymeren dort statt, wo die Diffusion von Wassermolekülen in die Polymermasse langsamer erfolgt als die Hydrolyse der Bindungen in der Polymerkette. Der Probekörper wird von außen nach innen abgebaut und immer kleiner. Dieser Vorgang kann modellhaft mit dem Abschälen einer Zwiebel verglichen werden. Die Geschwindigkeit des Oberflächenabbaus ist vor allem von dem Oberflächen-zu-Volumen-Verhältnis abhängig. Ein scheibenförmiges Polymer wird daher schneller vollständig abgebaut, als ein kugelförmiges Polymer mit der gleichen Masse. Polymere, die Oberflächenabbau zeigen, werden in der Medizin als Matrix für Systeme, die für eine kontinuierliche, kontrollierte Wirkstoffabgabe dienen, verwendet. Einen Oberflächenabbau zeigen z.B. Polyanhydride. Abb. 1: Modell des zeitlichen Verlaufs des Oberflächenabbaus eines Polymers und der Diffusion der Kettenfragmente. Ein Beispiel für eine solche Anwendung ist das Wirkstofffreisetzungssystem Gliadel®, das zur Behandlung von Tumorerkrankungen eingesetzt wird. Die Depotfunktion kommt dadurch zustande, dass der Wirkstoff in ein speziell entwickeltes Copolymer [Abb. 2] aus der Gruppe der Polyanhydride eingebracht wird. Abb. 2: Polyanhydrid in Gliadel® - ein Copolymer aus 20mol-% 1,3-bis(pCarboxyphenoxy)-propan)- Einheiten (dunkelbraun) und 80mol-% Sebacinsäure- Einheiten (orange); Kurzform: Poly(CPP-co-SA) In experimentellen Untersuchungen zum Oberflächenabbau von Polymeren konnte für die Masse m des gesamten Probekörpers der in Abbildung 3 dargestellte zeitliche Verlauf ermittelt werden. Die drei Probekörper (A, B und C) weisen ein unterschiedliches Oberflächen-zu-Volumen-Verhältnis auf. Abb. 3: Masse-Zeit-Diagramm Aufgaben: 1. Zeichnen Sie in das Masse-Zeit-Diagramm den ungefähren Kurvenverlauf für ein Polymer, das Oberflächenabbau zeigt und dessen Oberfläche größer ist als die von Polymer A ist. 2. Poly(CPP-co-SA) wird durch Oberflächenabbau und nicht zeitgleich im gesamten Polymerkörper hydrolytisch abgebaut. Erläutern Sie anhand der Abbildung 2. AB 4 Abbaubare Polymere in der Medizin Datum „Abbau in der Masse“ Beim Abbau in der Masse von hydrolytisch spaltbaren Polymeren erfolgt die Diffusion von Wasser in den Probenkörper schneller als der Abbau. Der Abbau findet daher an annähernd allen Stellen der Probenkörper etwa gleich schnell statt. Vereinzelte Spaltungen im Inneren des Polymerkörpers führen möglicherweise bereits zu wasserlöslichen Fragmenten. Eine Diffusion dieser kürzeren Ketten aus der Polymerprobe kann jedoch nicht erfolgen, weil die umgebenden Polymerketten noch nicht weit genug abgebaut wurden, um ein Entweichen aus dem Inneren zu ermöglichen. Einen Abbau in der Masse zeigen z.B. aliphatische Polyester. Abb. 1: Modell des zeitlichen Verlaufs des Abbaus in der Masse eines Polymers Fäden aus biologisch abbaubaren Polyestern, die in der Medizin als Nahtmaterial eingesetzt werden und nicht mit einer Folgeoperation entfernt werden müssen, zeigen einen Abbau in der Masse. Bei einem Einsatz solcher Polymere als Träger für Wirkstoffe, kann es allerdings zum „Burst-Effect“ kommen. Hierbei wird ein im Inneren der Polymermatrix befindlicher Wirkstoff in großen Mengen und innerhalb einer relativ kurzen Zeitspanne freigesetzt, wenn die Hülle des Polymers vollständig aufbricht und die im Inneren bereits gespaltenen Fragmente zusammen mit dem Wirkstoff hinausdiffundieren können. In experimentellen Untersuchungen zum Abbau in der Masse von hydrolysierbaren Polymeren konnten für die Masse m des gesamten Polymerprobekörpers und das Zahlenmittel der molaren Masse M die zeitlichen Verläufe ermittelt werden, die in Abb. 1 und Abb. 2 dargestellt sind. Abb. 1: Masse-Zeit-Diagramm Aufgabe: 1. Interpretieren Sie die Diagramme mit Hilfe der Textinformationen. Abb. 2: mittlere Molare Masse– Zeit - Diagramm Abbaubare Polymere in der Medizin Info Datum „Hydrolytischer Abbau“ Ein bedeutender Prozess beim Abbau von polymerbasierten Biomaterialien ist die Bindungsspaltung mittels Hydrolyse. Die Hydrolyse ist eine chemische Reaktion, bei der eine Verbindung durch Wasser gespalten wird (hydro: Wasser, lyse = Lösung, Spaltung). Die hydrolytische Abbaubarkeit kann dadurch erreicht werden, dass die Polymerketten in ihrem Rückgrat (siehe Abb. 1) Heteroatome enthalten, die Bestandteil hydrolysierbarer funktioneller Gruppen sind. Zu den Heteroatomen gehören Sauerstoff- und Stickstoff-Atome. Nur wenn polare Bindungen vorhanden sind, ist eine Hydrolyse möglich. Beispiele für polymere Stoffklassen, die hydrolysierbare Bindungen in der Hauptkette enthalten sind z. B. Polyester, Polyanhydride, Polyorthoester und Polyamide. Abb. 1: Verzweigte Polymere; mit Hauptkette (blau) und Seitenketten (grün) Ob eine Elektronenpaarbindung polar oder unpolar ist, wird über die Elektronegativitätsdifferenz (EN) der an der Bindung beteiligten Atome ermittelt. Bei zwei gleichartigen Atomen ist EN gleich „Null“, weil beide die gleiche Elektronegativität besitzen. Bei verschiedenartigen Atomen ist EN größer als “Null”, wobei das Atom mit der höheren Elektronegativität die Bindungselektronen stärker an sich zieht und deswegen partiell negativ () geladen wird. Bei dem anderen Atom entsteht eine positive Partialladung (+). Das Wasser-Molekül ist aufgrund der Elektronenverschiebung zum Sauerstoff-Atom und seiner gewinkelten Struktur eine polare Verbindung [Abb. 2]. Elektronegativität (EN) von Sauerstoff: 3,5 Elektronegativität (EN) von Wasserstoff: 2,1 Abb. 2: Strukturformel eines Wasser-Moleküls mit angedeuteter Elektronenverschiebung Die Hydrolyse eines Polyesters findet meist säure- oder basenkatalysiert statt. Bei einer hydrolytischen Spaltung im alkalischen Milieu greift im ersten Schritt ein Hydroxid-Ion als Nukleophil an dem partiell positiv geladenen KohlenstoffAtom der zu spaltenden Bindung an. Im sauren Milieu kommt es zuerst zu einer Anlagerung eines Protons an dem partiell negativ geladenen Sauerstoff-Atom der Carbonyl- Gruppe. Im Anschluss daran erfolgt die eigentliche Hydrolyse, also die Bindungsspaltung durch die Reaktion mit einem Wassermolekül. Nach der Abspaltung und somit Rückgewinnung des Katalysators (H+ oder OH--Ion) entstehen zwei Spaltprodukte. Ein Spaltprodukt trägt die Hydroxy- Gruppe und das andere im sauren Milieu eine Carboxyl- [vergl. Abb. 3] und im basischen Milieu eine Carboxylat- Gruppe. O O R2 R1 + O H H H O Polyester R1 Wasser H R2 O O Polyester-Fragment mit endständiger Carboxylgruppe Abb. 3: Beispiel für die Hydrolyse einer Ester-Bindung + Polyester-Fragment mit endständiger Hydroxygruppe