4 Enzyme 56 - Medi
Werbung

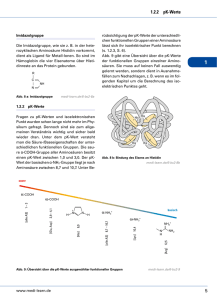
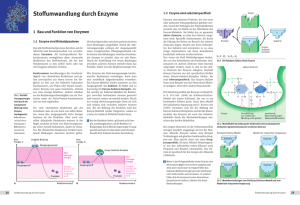
4 Enzyme unbedingt das spannendste Thema darstellt, solltest du dich sehr genau damit beschäftigen, denn wenn du die Kinetikgesetze erst einmal verstanden hast, kannst du sie auf alle (und zwar wirklich alle) Reaktionen anwenden, an denen Enzyme beteiligt sind. 4.7.1 4 Abhängigkeit der Reaktionsgeschwindigkeit von der Temperatur Die Aktivität von Enzymen ist temperaturabhängig (vgl. 4.1, S. 51). Pro 10 °C Temperaturerhöhung verdoppelt sich innerhalb eines begrenzten Bereichs deren Reaktionsgeschwindigkeit. Entsprechend besitzen Enzyme ein Temperaturoptimum, das beim Menschen ungefähr bei 37 °C liegt. Oberhalb dieses Optimums fällt die enzymatische Aktivität steil ab, da die Enzyme denaturiert werden. 4.7.2 Verändern sich der pH-Wert oder die Temperatur zu Werten außerhalb des optimalen Bereichs eines Enzyms, hat das eine Beeinträchtigung der enzymatischen Aktivität zur Folge. 4.7.3 Ablauf enzymkatalysierter Reaktionen Aktivierungsenergie der nichtkatalysierten Hinreaktion S Abb. 72: Reaktionsab- medi-learn.de/7-bc2-72 Energieniveau lauf ohne KaSubstrat S talysator G Abhängigkeit der Reaktionsgeschwindigkeit vom pH-Wert Die Abhängigkeit von äußeren Faktoren wie z. B. von der Temperatur besteht auch beim pH-Wert. Die meisten Enzyme des Körpers arbeiten am besten (pH-Optimum) zwischen pH 4 und pH 9. Einige Enzyme funktionieren auch noch unter extremen Bedingungen. Ein Beispiel hierfür ist das im Magensaft enthaltene Enzym Pepsin, das sogar bei dem dort herrschenden, sehr niedrigen pH-Wert von ~ 2 arbeitet. Die Ursachen für die pH-Abhängigkeit von Enzymen sind: – Bei extrem hohem oder extrem niedrigem pH-Wert wird das Enzymprotein denaturiert. – Mit dem pH-Wert verändern sich auch die funktionellen Gruppen des Enzyms und seines Substrats. Derartige Änderungen können die Raumstruktur (Tertiärstruktur, s. Abb. 72 a, S. 56) des Enzyms und darüber die Bindung des Substrats an das aktive Zentrum beeinflussen. 56 – Merke! Energieniveau Produkt P P Abb. 72 a: Reaktionsablauf ohne Katalysator medi-learn.de/7-bc2-72a S Energieniveau Substrat S Aktivierungsenergie der katalysierten Hinreaktion G P Energieniveau Produkt P Abb. 72 b: Reaktionsablauf mit Katalysator medi-learn.de/7-bc2-72b Die Reaktion vom Substrat S zum Produkt P in s. Abb. 72 a, S. 56 würde auch ohne Beteiligung von Katalysatoren freiwillig ablaufen, da das Energieniveau von P deutlich niedriger als das von S ist (∆G = negativ, s. a. Skript Chemie 1).