1) Legierungen: Eine Legierung ist eine homogene Mischung, aus
Werbung

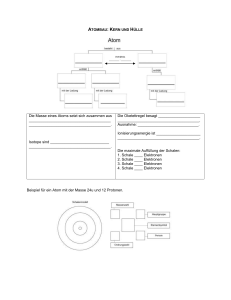
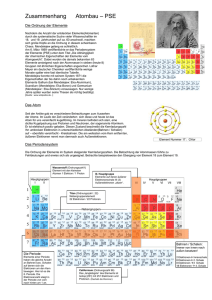
1) Legierungen: Eine Legierung ist eine homogene Mischung, aus verschiedenen Metallen. Durch diese Verbindung werden die Eigenschaften des neuen Metals verbessert. - Messing: Kupfer und Zink Bronze: Kupfer und Zinn Woodmetall: Blei Zinn 2) Es gibt keine richtigen oder falschen Modelle, nur für den jeweiligen Zweck ein brauchbares Modell! Demokrit: Atom = kleinste, unteilbare Einheit jeder stofflichen Dinge Dalton: Kugelförmig, gleichmäßig, undurchdringbar, kleinste teil, Streuversuch Röntgen: X- oder Röntgenstrahlen, Strahlen durchdringen alles ausser Blei Thomson: Elektron, wesentlich geringere Masse als Atom, Rusinenkuchenmodell, Elektronen bewegen sich um den Kern Becquerel: Entdeckung unerklärlicher Strahlung die alles durchdringt Curie: Verständnis der radioaktiven Strahlen, Photoplatte im Tresor Rutherford: radioaktives Material sendet 3 Strahlenarten aus, α, β und γ Strahlen, Streuversuch mit Goldfolie 3) Nach dem Wissensstand der damaligen Zeit erwartete Rutherford, dass die Atome wie Tennisbälle, die man gegen eine wand wirft, zurück geworfen werden. Doch von etwa 100.000 Teilchen wurden nur einige wenige abgeleitet. Woraus Rutherford geschlossen hat, dass Atome keine Starren kugeln sind, sondern ihre Masse nur im viel kleineren Kern hat. Und der Raum um den Kern leer ist. (Kern ca. Stecknadel, Hülle Durchmesser 200m). Eine Alpha Strahlen wurden jedoch trotzdem abgeleitet, da sie in die nähe des kerns kamen und von dort abgelenkt wurden. (Positive Alpha teilchen, positiver kern.) 4) Niels Bohr leitete daraus ab, dass ein Atom aus mehreren Schalten besteht und die Elektronen auf diesen Schalen um den Kernkreisen, ähnlich wie die Planeten um die Sonne. Die Fliehkräfte die dabei entstehen heben sich durch die Anziehungskraft des Kerns auf. Wenn die Außenelektronen eines Stoffes erwärmt werden haben sie den Drang, ihre Schale zu wechseln. Sie nehmen dabei Energie auf. Beim erneuten Wechseln, auf ihre Ursprungsschale geben sie die Energie in Form von farbigem Licht wieder ab. Licht wird in mehreren Farben abgegeben, die Farbpalette reicht von Infrarot bis Ultraviolett. - Infrarot = langwelliger, energieärmer Ultraviolett = kurzwelliger, energiereicher Jeder Stoff hat einen eigenen Chemischen Fingerabdruck, der sich z.B. durch erwärmen und spektroskopieren nachweisen lässt. - Li = roter strich, orangener Strich Na = gelber Strich 5)Bohrsche Postulate: - es gibt maximal 7 Schalen Schalennummer n=1 bis n=7 Jede Schale kann nur eine bestimme Höchstzahl an Elektronen aufnehmen 2 x n² Die jeweilige Äußere Schale kann höchstens 8 Außenelektronen aufnehmen Die vollständige Auffüllung der inneren Schalen erfolgt nach der Besetzung der äußeren Schale mit zunächst 2 Elektronen Das Auffüllen erfolgt von innen nach außen 6) Isotope Atome mit gleicher Kernladungszahl und unterschiedlicher Neutronenzahl nennt man Isotope. - obere Zahl = Massenzahl (Protonen + Neutronen) untere Zahl = Ordnungszahl = Protonen = Elektronen = Kernladungszahl Buchstabe = Elementsymbol für das chemische Element …







![Kugelwolkenmodell (KWM) der Atomhülle [c/ A. Schill]](http://s1.studylibde.com/store/data/006026842_2-f7ef645afd4f19b760ad28335b8d24ad-300x300.png)
