2.1.7 Defibrillatoren - Ihre Homepage bei Arcor
Werbung

Brandenburgische Technische Universität Cottbus; Tragbare Elektronik und Rechentechnik Bachelor-Studiengang: Informations- und Medientechnik Bachelor-Arbeit Thema: Medizintechnische Wearables: Genesis, Stand und Perspektiven Erstprüfer: Juniorprofessor. Dr. – Ing. A. Böger Ronny Dietrich Matrikel-Nr. 9912825 Florian-Geyer-Strasse 8 03099 Kolkwitz 0355 / 287243 E-Mail: [email protected] Datum: 23.10.2006 1 Bachelorarbeit Name: Ronny Dietrich Studiengang: Informations- und Medientechnik Matrikelnummer: 9912825 Betreuerin: Prof. Dr.-Ing. Astrid Böger; Juniorprofessor Tragbare Elektronik und Rechentechnik; Fakultät 3 / LG 3a Thema Medizintechnische Wearables: Genesis, Stand und Perspektiven Beschreibung Die Bachelorarbeit „Medizintechnische Wearables: Genesis, Stand und Perspektiven widmet sich der ausführlichen Aufbereitung des vorhandenen Wissens zu tragbaren medizintechnischen Geräten von ihrer Erfindung bis zum heutigen Stand technologischer Entwicklungen und verbindet dies mit einem Ausblick auf zukünftige Trends und Perspektiven. Dabei werden vor allem mobile medizinische Anwendungen als Ergebnis der Miniaturisierungsprozesse vergangener Jahre analysiert. Auf der Grundlage von umfangreichen Recherchearbeiten werden die historischen Entwicklungsverläufe ausgewählter medizinischer Geräte herausgearbeitet und im Rahmen der Bedeutung von Wearables für die Medizintechnik bewertet. Außerdem erfolgt eine definitorische Auseinandersetzung zum Begriff Wearables. Im Ergebnis erfolgt eine entsprechende Klassifizierung im Bereich Medizintechnik. Ziel ist es, eine weitgehende Systematisierung medizinischer Wearables aus heutiger Sicht vornehmen zu können. Zur Vertiefung des vor allem theoretisch orientierten ersten Teils werden ausgewählte Wearables mit unterschiedlichem Reifegrad hinsichtlich ihrer Akzeptanz als moderne Wearable-Technik untersucht. Hierbei werden sowohl klassische Charakteristika als auch neue Bewertungsansätze mit einbezogen. Die Auswahl erfolgt hinsichtlich der Schwerpunkte Verfügbarkeit und Bekanntheitsgrad bei den Anwendern. Im Vordergrund steht die kritische Auseinandersetzung der Nutzer hinsichtlich der Chancen und Risiken neuer medizinischer oder Gesundheitsanwendungen. Welche Akzeptanz erfahren neue tragbare Technologien im präventiven, privaten und häuslichen Umfeld? Dabei wird die zentrale Frage diskutiert, in wieweit Wearables einen Paradigmenwechsel im Gesundheitssystem hervorrufen können. Zum Abschluss der Bachelorarbeit werden mögliche Perspektiven von medizintechnischen Wearables aufgezeigt sowie ein Ausblick in die Zukunft gegeben. 2 Inhaltsverzeichnis 1. EINLEITUNG ................................................................................................................. 5 1.1 WEARABLES – TRAGBARE ELEKTRONIK ALLGEMEIN ................................................... 5 1.1.1 GESCHICHTE................................................................... ...................................5 1.1.2 DEFINITION .................................................................... ...................................7 1.1.3 PHYSISCHE UMSETZUNG.................................................................................... 9 1.1.4 ANWENDUNGSBEREICHE...................................................................................10 1.2 WEARABLES IN DER MEDIZINTECHNIK ....................................................................... 11 2. GENESIS........................................................................................................................ 13 2.1 HISTORISCHER ENTWICKLUNGSVERLAUF AUSGEWÄHLTER MEDIZINTECHNISCHER ........ GERÄTE ...................................................................................................................... 13 2.1.1 HERZSCHRITTMACHER................................................................................... .14 2.1.2 THERMOMETER ............................................................................................... 20 2.1.3 STETHOSKOP ................................................................................................... 25 2.1.4 EEG - ELEKTROENZEPHALOGRAFIE ................................................................ 30 2.1.5 EMG - ELEKTROMYOGRAFIE .......................................................................... 35 2.1.6 EKG - ELKETROKARDIOGRAFIE ...................................................................... 36 2.1.7 DEFIBRILLATOREN .......................................................................................... 49 2.1.8 PULSMESSGERÄTE ........................................................................................... 54 2.1.9 BLUTDRUCKMESSGERÄTE ............................................................................... 58 2.1.10 HÖRGERÄTE .................................................................................................... 63 2.1.11 BRILLEN .......................................................................................................... 71 2.1.12 PROTHESEN ..................................................................................................... 79 2.2 ZUM STAND DER TECHNIK ......................................................................................... 85 2.2.1 SENSATEX SMART SHIRT ................................................................................ 85 2.2.2 BLUETHOOTH - EKG -T-SHIRT ....................................................................... 88 2.2.3 LIFEVEST WEARABLE DEFIBRILLATOR ........................................................... 90 3 3. EMPIRISCHE UNTERSUCHUNGEN....................................................................... 92 3.1 BESCHREIBUNG DER EMPIRISCHEN UNTERSUCHUNG .................................................. 93 3.1.1 ZIELSETZUNG .................................................................................................. 93 3.1.2 ABGRENZUNG DER UNTERSUCHUNG ............................................................... 94 3.1.3 ANGEWANDTE ERGEBUNGSMETHODEN UND VORGEHEN ................................ 94 3.2 UNTERSUCHUNGSOBJEKT ........................................................................................... 96 3.2.1 „DOKTOR MOUSE“ ............................................................................................. 96 3.3 ERGEBNISSE ............................................................................................................. 102 3.3.1 ERGEBNISSE DER ANWENDERBEFRAGUNG - ALLGEMEIN ................................. 102 3.3.2 ERGEBNISSE DER ANWENDERBEFRAGUNG - GRUPPE 1 ..................................... 106 3.3.3 ERGEBNISSE DER ANWENDERBEFRAGUNG - GRUPPE 2 ..................................... 111 3.3.4 ERGEBNISSE DER SELBSTTESTS ........................................................................ 115 3.4 SCHLUSSFOLGERUNGEN DER EMPIRISCHEN UNTERSUCHUNG ................................... 116 4. AUSBLICK, VISIONEN UND PERSPEKTIVEN .................................................. 119 5. FAZIT ........................................................................................................................... 120 EIDESSTATTLICHE ERKLÄRUNG .......................................................................... 121 LITERATURVERZEICHNIS ....................................................................................... 122 ABBILDUNGSVERZEICHNIS .................................................................................... 127 ANHANG ......................................................................................................................... 134 4 1. Einleitung 1.1. Wearables – Tragbare Elektronik allgemein 1.1.1 Geschichte Wearables sind technologische Zusatzgeräte, die unterstützende Funktionen, wie beispielsweise die Verbesserung der menschlichen Sinne, haben. Derartige Ideen sind keine Erscheinungen der Neuzeit, sondern traten schon viel früher auf. So beschrieb schon Robert Hooke 1665 in seinem Werk Micrographia „augmented senses“ 1 - erweiterte Sinneswahrnehmungen: "The next care to be taken, in respect of the Senses, is a supplying of their infirmities with Instruments, and as it were, the adding of artificial Organs to the natural...and as Glasses have highly promoted our seeing, so 'tis not improbable, but that there may be found many mechanical inventions to improve our other senses of hearing, smelling, tasting, and touching." 1762 erfand John Harrison den ersten nutzbaren Schiffs-Chronometer im Taschenuhrformat. Er diente zur genauen und zuverlässigen Bestimmung von geographischen Längengraden. 1907 beauftrage der Flugzeugpilot Alberto Santos-Dumont den Juwelier Louis Cartier mit der Konstruktion der ersten Armbanduhr. Das erlaubte Santos-Dumont während des Fliegens die freihändige Nutzung der Uhr. Der amerikanische Ingenieur Vannevar Bush erkannte schon frühzeitig die aufkommende und exponentiell wachsende Informationsflut und entwickelte deshalb 1945 das Konzept des Memex (Memory Extender). Dabei handelt es sich um einen fiktiven Analogrechner, in Form eines Schreibtisches, der mit elektromechanischen Kontrollen, Mikrofilmgeräten und Bildschirmen ausgestattet ist. Dieses Gerät dient als erweitertes Gedächtnis, das der Benutzer als persönliche Bibliothek zur Speicherung und Wiederabrufung von Büchern, Aufzeichnungen, Gesprächen etc. benutzen kann. 1960 ließ sich Morton Heilig ein stereophonisches Head Mounted Display (HMD) zum Fernsehgebrauch patentieren. Zwei Jahre später folgte sein Patent für den Sensorama Simulator, ein Echtheits-Simulator mit Lenkstangen, binokularen Displays, stereophonen Lautsprechern, Kaltluftgebläse und einer olfaktorischen Ausgabevorrichtung. Ed Thorp und Claude Shannon vom MIT (Massachusetts Institute of Technology) stellten 1966 ihre Erfindung des ersten Wearable Computers vor, der beim Roulette zur Vorhersage des Ergebnisses benutzt werden konnte. Es war ein zigarettenschachtelgroßer Analogcomputer mit 4 Knöpfen. Eine weitere Erfindung in diesem Jahr war das erste computerbasierte HMD (Head-Mounted-Display) von Ivan Sutherland. Es bestand aus zwei CRTs (Cathode Ray Tube) mit halbversilberten Spiegeln, die die Bilder zu den Augen des 1 Quelle: http://www.media.mit.edu/wearables/lizzy/timeline.html#1665 5 Nutzers reflektierten. Befestigt wurden sie an den Ohren des Trägers. Das eigentliche Rechnersystem war über dem Kopf des Nutzers angebracht, wodurch der Erfindung der Name „Damoklesschwert“ zuteil wurde. 1976 konstruierte Hubert Upton einen analogen Wearable Computer mit einem an Brillengläser befestigtem Display („eyeglass-mounted display“), zur Unterstützung des Lippenlesens. Mit Hilfe von Hoch- und Tiefpassfiltern konnte dieser Computer die Art der gesprochenen Laute bestimmen. Zu deren visuellen Darstellung waren Leuchtdioden so an die Brillengläser montiert, dass unterschiedliche Laute die Gläser unterschiedlich beleuchteten. Ein Jahr später stellte Douglas Engelbart die erste einhändig zu bedienende Tastatur vor. 1977 entwickelte C.C. Collins des Smith-Kettlewell Institutes eine tragbare „camera-totactile“ Weste für Blinde. Das System wog um die 2 kg und bestand aus einer am Kopf angebrachten Kamera („head-mounted camera“), die Bilder in 1024 Punkte zerlegte und einem 10 Zoll großen quadratischen Tastrasterfeld auf der Weste, auf dem die Bilder entsprechend taktil sichtbar gemacht werden konnten. Eudaemonic Enterprises konstruierte 1978 einen digitalen Wearable Computer in einem Schuh zur Vorhersage von Rouletteergebnissen. 1981 entwickelte Steve Mann ein Rucksack-Computersystem zur Steuerung fotografischer Ausrüstung (Blitzlichter, Kameras und andere Fotosysteme). Als Anzeige diente ein auf einem Helm befestigter Kamera-Bildsucher-CRT. Versorgt wurde das komplette System mit Bleisäurebatterien. Im Jahr 1991 präsentierte Doug Platt seinen schuhkartongroßen „Hip-PC“, welcher mit einem 286 XT Modul arbeitete. Als Bildschirm fungierte hier ein „Private Eye HMD“ 2. Die Eingabe erfolgte mittels Agenda Palmtop, der am Gürtel des Nutzers befestigt war. 1993 entwickeln Steve Feiner, Blair MacIntyre und Doreè Seligmann von der Columbia Universität das „KARMA10 augmented reality system“. Bei diesem System trägt der Benutzer ein Private Eye über einem Auge. Wenn der Träger seine Umwelt nun mit beiden Augen betrachtete nahm er gleichzeitig die Anzeige des Private Eyes sowie seine Umwelt wahr. Es entstand ein Überlagerungseffekt. So könnte beispielsweise bei der Betrachtung eines Druckers gleichzeitig dessen Bedienungsanleitung via Private Eye angezeigt werden. Ermöglicht wurde dies mit an Gegenständen angebrachten Sensoren zu deren Lokalisation. Beim „Forget-Me-Not“-System, das 1994 von Mik Lamming und Mike Flynn entwickelt wurde, handelte es sich um einen Wearable Computer, der die Interaktion von Menschen und Geräten aufnahm und für eine spätere Verwendung abspeicherte. Über kabellose Transmitter kommunizierte dieses System mit der intelligenten Raumausstattung und konnte somit auch auf Fragen wie „Wer kam durch die Tür als ich mit Marc am Telefon sprach?“ reagieren. Noch im selben Jahr stellten Edgar Matias und Mike Ruicci ihren „wirst computer“ (Armbandcomputer) mit einem „half-QUERTY keyboard“ vor. 1994 übertrug die von Steve Mann entworfene Wearable Wireless Webcam Bilder von einer am Kopf montierten Kamera über Amateur-TV-Frequenzen direkt ins WWW. Die Übertragung und Darstellung der Aufnahmen auf einer Webpage waren beinahe in Echtzeit. 2 Das Private Eye Display von Reflection Technology nutzt eine Reihe von LEDs und einen schnell vibrierenden Spiegel, um die Illusion eines Volltextdisplays zu kreieren. 6 Im Jahr 1996 tagte der erste größere Workshop „Wearables in 2005“, wobei sämtliche Industrie-, Universitäts- und Militärvisionäre zusammenkamen. Die erste akademische Konferenz (IEEE International Symposium on Wearable Computers) fand 1997 in Cambridge, Massachusetts, statt. Seitdem lädt das IEEE Symposium jährlich zum Thema Wearables ein. Auch kommerzielle Firmen, wie beispielsweise Xybernaut, tragen zur Weiterentwicklung von Wearables bei. So entwickelte das Unternehmen 1999 das erste anwendungsfähige WearableSystem. Im Kapitel 2.2. werden einige aktuelle Systeme beschrieben. 1.1.2 Definition „Wearable Computing ist das Forschungsgebiet, das sich mit der Entwicklung von tragbaren Computersystemen (Wearable Computern) beschäftigt. Ein Wearable Computer wiederum ist ein Computersystem, das während der Anwendung am Körper des Benutzers befestigt ist. Wearable Computing unterscheidet sich von der Verwendung anderer mobiler Computersysteme dadurch, dass die hauptsächliche Tätigkeit des Benutzers nicht die Benutzung des Computers selbst, sondern eine durch den Computer unterstützte Tätigkeit in der realen Welt ist.“ 3 Der Begriff „Wearable Computing“ bezeichnet demnach eine neue Form der MenschMaschine-Kommunikation und umfasst dabei nicht nur die Miniaturisierung und die Integration von Computern in Kleidung, sondern beschreibt auch ein ganz neues Verständnis hinsichtlich der Funktionalität dieser Computer für den Menschen. Ein Wearable Computer ist nämlich kein herkömmlicher mobiler Arbeitsplatz, sondern er stellt dem Nutzer jederzeit einen unsichtbaren, intelligenten und persönlichen Assistenten zur Verfügung, der die verschiedensten Aufgaben zu bewältigen vermag. Sei es als Arzt, Kommunikations- oder Informationsschnittstelle. Ein Wearable ist ein System, welches sowohl Informationen aus der Umwelt als auch Informationen vom Benutzer selbst berücksichtigt und somit kontextsensitiv ist. Ursprünglich stammt das Wort „Wearable“ aus dem Englischen und bezeichnet streng genommen nichts weiter, als am Körper getragene Technik (auch: Wearable Electronics). Schon in der Vergangenheit tauchten mit Brillen oder Taschenuhren erste Vorreiter moderner Wearable-Systeme auf. Heutzutage versteht man unter einem Wearable-System eine Vielzahl von Kleinstcomputern mit unterschiedlichen Funktionen, die ohne Benutzung der Hände dauerhaft am Körper getragen und verwendet werden können. Die Kommunikation zwischen den einzelnen Komponenten (Recheneinheiten, Sensoren, Ein- und Ausgabeeinheiten, Netzwerke) erfolgt drahtlos oder über in die Kleidung eingewebte Kabel. Wearable-Systeme können dem Nutzer also verschiedene Dienste nach dem „anytime, anything, anywhere“ Prinzip zur Verfügung stellen, wie z.B. Kommunikationsdienste – Mobilfunktelefonie. Damit ein System als tragbar/wearable bezeichnet werden darf, muss es konkrete Charakteristika aufweisen. B. J. Rhodes definierte sie wie folgt: 4 3 4 Wearables müssen aus der Bewegung heraus benutzt werden können. Quelle: http://de.wikipedia.org/wiki/Wearable_Computing Quelle: http://www.tzi.de/~ruegge/PDF-Dateien/THEALIT_01_Ohne_Bilder.pdf 7 Wearables können durch gesprochene Sprache o.ä. kontrolliert werden, so dass beide Hände frei sind für andere Aufgaben. Wearables sind mit Sensoren zur Wahrnehmung der physikalischen Umwelt ausgestattet. Wearables sind immer funktionsbereit und versorgen den Benutzer autonom mit Informationen. Wearables nehmen kontinuierlich Daten auf und sind permanent im Einsatz. Steve Mann, ein Wegbereiter des Wearable Computing, formulierte ebenfalls konkrete Eigenschaften für Wearable-Systeme in Form von 6 Attributen.5 1. Unmonopolizing: Das Wearable-System darf während seiner Benutzung nicht die gesamte Aufmerksamkeit des Nutzers beanspruchen, so dass er sich gleichzeitig auch anderen Dingen zuwenden kann. Der Benutzer darf nicht von seiner Außenwelt abgeschnitten sein. Das Wearable-System hat sich immer den Anforderungen der realen Welt unterzuordnen. 2. Unrestrictive: Der Benutzer muss das System uneingeschränkt, unabhängig von Ort, Zeit und ausgeübter Tätigkeit, nutzen können. 3. Observable: Das System kann immer die Aufmerksamkeit des Benutzers erlangen. 4. Controllable: Der Benutzer hat jederzeit die volle Kontrolle über das WearableSystem. Automatische Prozesse müssen vom Benutzer widerrufen werden können 5. Attentive: Die Umgebung des Benutzers sowie der Zustand des Benutzers selbst soll zu jedem beliebigen Zeitpunkt aufmerksam, multimodal und multisensorisch vom System erfasst und kontrolliert werden können. 6. Communicative: Das Wearable-System hat jederzeit die Fähigkeit mit anderen außerhalbliegenden Medien zu kommunizieren. Abb. 1: Signalflüsse zwischen Mensch und Maschine nach Steve Mann 5 Quelle: http://www.cs.albany.edu/~maniatty/teaching/ubicomp/class02/lectnotes.pdf 8 Beim Wearable Computing spielt jedoch nicht nur die Leistungsfähigkeit und Leistungsbereitschaft der Miniaturcomputer eine zentrale Rolle, sondern auch die Ein- und Ausgabegeräte sowie deren Anordnung. Außerdem ist die Gestaltung von adaptiven Schnittstellen von enormer Bedeutung, damit der Interaktionsaufwand für den Benutzer so gering wie möglich gehalten wird. Grundsätzlich werden Wearables in 2 Kategorien eingeteilt. Zum einen können sie den Benutzer mit einer Art technischer Verbesserung ausstatten – Personal Enhancement (PE) und zum anderen können sie den Benutzer bei der Erreichung eines bestimmten Zieles unterstützen –Personal Assistent (PA). 1.1.3 Physische Umsetzung Eine der bedeutsamsten Aufgaben bei der Konzeption eines Wearables stellt deren physische Realisierung dar. Abhängig vom Einsatzort und der Anwendung eines Wearable-Systems muss eine Art und Form der Umsetzung gefunden werden, die den Gebrauch im jeweiligen Bereich ermöglicht. Generell lassen sich 3 große Realisierungsrichtungen unterscheiden, die nun im Folgenden näher betrachtet werden sollen. Geräte zum Umschnallen/ Anlegen /“Anziehen“ Zu dieser Kategorie zählen unter anderem die ersten Prototypen von Wearables, aber auch viele neue Entwicklungen, bei denen es sich um Zusatzkomponenten handelt, die man bewusst nicht in die Kleidung integriert. Solche Geräte werden dann von außen am Körper angebracht. Beispiele hierfür sind sogenannte „onhandPCs“, die man wie Armbanduhren trägt und am Handgelenk oder Unterarm befestigt. Aber auch größere Gerätschaften, die mittels Gürtel oder Rucksäcke getragen werden, fallen mit in diese Gruppe. Ein Beispiel dafür ist der „Voltaic – Solar Backpack“ 6 für die mobile Energieversorgung. Derartige Ansätze zur Gestaltung von Wearables lassen zwar die Entwicklung von leistungsfähigeren Produkten zu und sind aufgrund der nicht fest in die Kleidung integrierten Technik sehr einfach erweiterbar, haben aber dennoch entscheidende Nachteile für den realen Einsatz, vor allem aus optischen und ergonomischen Gründen. In Textilien und Kleidungsstücke integrierte Systeme Durch die zunehmenden Fähigkeiten der Forschung und Entwicklung, Technik immer kleiner gestalten zu können, ist man in der Lage, Wearable-Systeme direkt in handelsübliche Textilien zu integrieren. So können Mikrochips, Verbindungsleitungen, Ein- und Ausgabegeräte komplett in den Stoff mittels spezieller Webetechniken eingearbeitet werden. Mit diesem Verfahren fallen auch die optischen und ergonomischen Probleme weg, so dass es sich dann tatsächlich um intelligente Kleidung handelt, die jedermann überall kaufen und in gewohnter Art und Weise verwenden kann. Ein Beispiel hierfür ist ein in die Kleidung integrierter MP3-Player von Infineon. 7 6 7 Quelle: http://www.voltaicsystems.com/bag_backpack.shtml Quelle: http://www.golem.de/0204/19543.html 9 Integration im Körper / menschlichen Gewebe Diese letzte Realisierungsrichtung von Wearables findet sich in der direkten Implantation in den menschlichen Körper wieder. Dabei werden technologische Kleinstgeräte in das lebende Gewebe eingepflanzt. Darunter fallen beispielsweise Systeme wie Herzschrittmacher oder das „Braingate“ 8 der US Firma Cyberkinetics. Beim „Braingate“ handelt es sich um einen Mikrochip, der direkt in das Gehirn eines 25 jährigen Querschnittsgelähmten implantiert wurde. Dieser Chip ermöglicht es ihm E-Mails abzurufen, Fernsehprogramme zu steuern und Computer zu spielen. Inwiefern und ob sich derartige Entwicklungen dauerhaft im Businessoder Consumerbereich durchsetzen werden ist ungewiss. Anders sieht es da im medizinischen Bereich aus. Dort wächst der vermehrte Einsatz von Implantaten. 1.1.4 Anwendungsbereiche Nahezu jeder Berufszweig nutzt heutzutage die Computertechnologie um mit deren Hilfe effizienter, kosteneffektiver und schneller die gesteckten Unternehmensziele erreichen zu können. So stehen vielen Arbeitnehmern und Arbeitgebern bei der Ausübung verschiedenster Tätigkeiten Computer unterstützend zur Seite. Dies gilt auch für mobile Arbeiten, bei denen sich Wearable Computer als optimale Lösung zur Arbeitsunterstützung anbieten. Denn durch ihre vielfältigen Einsatzmöglichkeiten stellen sie ein enormes Innovationspotential für viele Branchen aber auch für private Zwecke dar. So umfassen potentielle Einsatzgebiete von Wearable-Systemen die gesamte Breite der klassischen Wirtschaftssektoren - von der Dienstleitung über die Industrie bis hin zur Landwirtschaft - sowie den gesamten Consumerbereich. Erste Wearable Systeme wurden bereits für folgende Bereiche entwickelt: Logistik Produktion, Montage, Konstruktion Instandhaltung: Inspektion, Wartung, Instandsetzung Medizin Tourismus / Kultur Umwelt / Landwirtschaft Unterhaltung / Journalismus Krisen- und Katastrophenmanagement Militär / Sicherheit Facility Management. Auf nähere Erläuterungen und konkrete Beispiele für die einzelnen Anwendungsbereiche, mit Ausnahme der Sparte „Medizin“ (siehe Abschnitt 1.2), wird hier verzichtet, da es den Rahmen der Einleitung sprengen würde und nicht Gegenstand dieser Bachelorarbeit ist. 8 Quelle: http://www.spiegel.de/wissenschaft/mensch/0,1518,323079,00.html 10 1.2 Wearables in der Medizintechnik Besonders großes Potential für den Einsatz von Wearable-Systemen steckt im medizinischen Sektor. Wearables übernehmen dort schon heute erfolgreich die verschiedensten Aufgaben (Monitoring, Prävention etc.) und werden zukünftig sicherlich noch in weitere Aufgabenbereiche der Medizin vorstoßen. Wearable-Systeme sind hier in 2 große Bereiche zu unterteilen, nämlich in Wearables zur Unterstützung von Verwaltung und Personal und in Patienten-Wearables. Schwerpunkt dieser Bachelorarbeit sind die Patienten-Wearables. 1. Patienten-Wearables Patienten-Wearables sind zum einen überwachende Systeme zur medizinischen Vor- und Nachsorge (Monitoring) und zum anderen Systeme, die in der Lage sind, Aufgaben defekter Körperfunktionen zu übernehmen. Überwachende Systeme werden vom Patienten am Körper getragen oder sind direkt in die Alltagskleidung integriert. Sie ermöglichen eine allgegenwärtige Kontrolle der Vitalfunktionen (Puls, Blutdruck, Körpertemperatur etc.) und sind bei Notfällen mit der Fähigkeit ausgestattet, Hilfe zu alarmieren - so wie beispielsweise das „Smart Shirt“ von Sensa-Tex (siehe Abschnitt 2.2.1). Aufgrund dieser Möglichkeiten werden solche Systeme deswegen hauptsächlich bei Sportlern, kranken oder gesundheitlich gefährdeten Menschen eingesetzt. Zum Beispiel profitieren Menschen mit chronischen Krankheiten wie einer Herzschwäche sehr von solchen technischen Errungenschaften. Sie können rund um die Uhr mit einem mobilen, portablen EKG überwacht werden, das bei Herzunregelmäßigkeiten Alarm auslöst und völlig autonom den Arzt informiert. Dadurch erlangen Patienten ein ganz neues Gefühl der Sicherheit und können wie gewohnt ihrem Alltagsgeschehen nachgehen. Wearable-Systeme, die zur Heilung oder zur Übernahme von defekten Körperfunktionen bzw. Körperorganen entwickelt und eingesetzt werden, sind der andere Teil von PatientenWearables. Hierzu zählen beispielsweise Hörgeräte, Herzschrittmacher und Prothesen. Herzschrittmacher werden dabei direkt in das menschliche Gewebe implantiert und steuern die regelmäßige Herztätigkeit. Es ist auch möglich, Herzschrittmacher mit Defibrillatoren auszustatten, die bei Notfallsituationen, in denen es um das Überleben des Patienten geht und somit jede Sekunde zählt, automatisch versuchen die reguläre Herztätigkeit des Patienten wiederherzustellen. Selbst Gehörlosen und Sehbehinderten kann mit Wearable-Systemen geholfen werden. Zwar sind Gehörlose in der Lage mit der Gebärdensprache gut miteinander zu kommunizieren, aber für die meisten anderen Menschen ist sie unverständlich. Deshalb wird an Geräten geforscht, die die Gebärdensprache in die gewöhnliche Muttersprache des Landes übersetzen können. Einen ersten Prototyp dafür entwickelte Thad Starner 9. Thad Starner war es auch, der für seine stark sehbehinderte Großmutter ein Wearable-System konstruierte, das Bilder so vergrößert oder deren Lichtintensivitäten verstärkt, dass sie wieder lesen konnte. 10 Auch Steve Mann konstruierte eine Weste für sehbehinderte Menschen, die mit einem Radar arbeitete und den Trägern durch Vibrationen die eigene Position mitteilte. Dadurch wurde es 9 http://en.wikipedia.org/wiki/Thad_Starner http://www.monitor.co.at/monitor/598/story/drescode.html ; Die medialisierte Wirklichkeit 10 11 ihnen möglich, sich ohne Hilfe von Dritten in ihrer Umgebung zurechtzufinden. Forschungen auf diesen Gebieten stehen hier allerdings noch am Anfang. 2. Wearables zur Unterstützung von Verwaltung und Personal Das Monitoring von Patienten findet heute fast ausschließlich in den Krankenhäusern oder Arztpraxen statt. Dies soll sich in Zukunft schon allein aus Kostengründen heraus ändern. Dann tragen Patienten im Alltag miniaturisierte und integrierte Monitoring-Systeme, die ununterbrochen Patientendaten sammeln und sie bei Bedarf an den Klinikcomputer schicken. Der behandelnde Arzt kann diese dann mittels einer von ihm getragenen Armtastatur jederzeit abrufen und Änderungen wie Notizen etc. vornehmen. Ähnlich könnte es auch bei einer Visite im Krankenhaus vonstatten gehen. Patientendaten könnten hier direkt während der Visite durch den Arzt über die Armtastatur aktualisiert werden. In diesem Zusammenhang eröffnet sich das Feld der digitalen Krankenakte. Durch die digitale Verwaltung von Patientendaten sowie deren ständige Aufnahme mit Hilfe von Wearable-Systemen stehen jedem behandelnden Arzt und jedem medizinischen Personal sämtliche Patienteninformationen jederzeit und überall zur Verfügung – abgerufen werden sie durch Wearable-Systeme, die das medizinische Fachpersonal ständig bei sich trägt. Besonders in Notfallsituationen kann dies von lebensrettender Bedeutung sein. Rettungssanitäter können mittels der am Unfallort erhobenen Patientendaten die digitale Krankenakte des Patienten aktualisieren. Somit haben die Mediziner im Krankenhaus die Möglichkeit durch Abfrage der aktualisierten Krankenakte bereits vor Eintreffen des Patienten im Krakenhaus eine Diagnose zu stellen und entsprechend Vorbereitungsmaßnahmen zu treffen. Dadurch kann eine schnellere Hilfe gewährleistet werden. Aber auch bei der häuslichen Pflege durch Pflegepersonal kann die digitale Krankenakte sinnvoll eingesetzt werden. Das Pflegepersonal kann sich mit ihr vor Ort patientenbezogene Informationen beschaffen, wie z.B. spezielle Behandlungshinweise, und Patientendaten ändern. Wie anhand dieses Abschnittes leicht zuerkennen ist, ergeben sich zahlreiche Vorteile für den Einsatz von Wearable-Systemen im medizinischen Bereich. Die Wichtigsten davon sind: die allgegenwärtige, kostengünstige Überwachung, Vorsorge und Nachsorge von Patienten die schnelle Benachrichtigung bei Notfallsituationen durch das Wearable selbst und die gesundheitlich unterstützenden Funktionen, wie z.B. die Kontrolle und Korrektur der allgemeinen Herzrhythmustätigkeit. Nachfolgend werden noch zwei Anwendungsbeispiele für Wearable-Systeme (PatientenWearables) im medizinischen Bereich aus einer Studie über „Technologische und anwendungsorientierte Potenziale mobiler, tragbarer Computersysteme“ vorgestellt und bewertet. Die Studie selbst wurde an der Universität Bremen im Technologie-Zentrum Informatik mit Unterstützung des Unternehmens Xybernaut 11 und der Landesinitiative zur verstärkten Informations- und Mediennutzung „bremen in t.i.m.e.“ 12 verfasst. Eine entsprechende grafisch tabellarische Darstellung der aufgezeigten Beispiele ist im Anhang (Abbildung 1 & 2) wiederzufinden. 11 12 http://www.xybernaut.com/ http://www.bremerarbeit.de/_gruen/index.php?rubric=Bremen+in+t.i.m.e. 12 VibraVest Die „VibraVest“ ist ein Wearable-System, das blinden Menschen bei der Orientierung in ihrer Umwelt helfen soll. Es besteht aus einem Wearable Computer mit Radar-Sensoren sowie einem in eine Weste integrierten taktilen Display. Die Radar-Sensoren nehmen Gegenstände in der näheren Umgebung des Westenträgers wahr, die ein Softwareprogramm in entsprechende Vibrationen umsetzt. Je nach Vibration kann der Träger der Weste die Entfernung, die Geschwindigkeit und die Richtung von Objekten auf taktiler Ebene erkennen. Die „VibraVest“ erlaubt blinden Menschen also eine freie und vor allem sichere Bewegung im Alltag, ohne auf die Mithilfe von Dritten angewiesen zu sein. NOAH Vest Um veraltete und langsame Kommunikations- und Dokumentationstechniken im Bereich des Rettungsdienstes zu ersetzten, wurde eine spezielle Weste, die „NOAH Vest“, entwickelt. Sie ist mit einem Modem, einem besonderen Touchscreen für Ein- und Ausgaben, einer Batterie und einer Main-Unit für Prozessorarbeiten ausgestattet. Mit dieser Ausstattung erlaubt sie den Rettungssanitätern bei Notfallsituationen eine umgehend digitale und somit weitestgehend verlustfreie Informationsübertragung (Unfallhergang, Zustand der Unfallopfer etc.) zum Krankenhaus und reduziert Zeitverluste, die lebensrettend sein können. Des Weiteren wird durch den Einsatz der „NOAH Vest“ die Qualität der Dokumentation mit Hilfe spezieller Softwareprogramme erheblich gesteigert. Mit der „NOAH Vest“ können demnach viele der im Zielkrankenhaus benötigten Daten, erhoben durch die Kommunikation und Dokumentation vor Ort, zeitnah und wohl strukturiert übermittelt werden. Durch diesen geschaffenen Zeitvorsprung im Gegensatz zur üblichen Vorgehensweise wird Patienten eine schnellere und präzisere Hilfe gewährleist, die über Leben und Tod entscheiden kann. 2. Genesis 2.1. Historischer Entwicklungsverlauf medizintechnischer Geräte ausgewählter In dem nun folgenden Kapitel wird der Entwicklungsverlauf einiger ausgewählter medizinischer Instrumente und Geräte näher betrachtet. Die Auswahl erfolgte nicht willkürlich, sondern beruht zum einen auf der konstruierten Fragestellung - „Bei welchen medizinischen Geräten/Instrumenten könnte sich in deren Entwicklungsverlauf die Entstehung eines Wearables abzeichnen?“ - und zum anderen auf dem Schwerpunkt dieser Bachelorarbeit (Patienten-Wearables; siehe Abschnitt 1.2). Nach ausgiebigen Literaturstudien fiel die Wahl der zu untersuchenden Geräte auf, 1. Herzschrittmacher, 2. Thermometer, 3. Stethoskope, 4. Elektroenzephalographen, 5. Elektromyographen, 6. Elektrokardiographen, 13 7. Defibrillatoren, 8. Pulsmessgeräte, 9. Blutdruckmessgeräte, 10. Hörgeräte, 11. Brillen und 12. Prothesen. Bei den Recherchearbeiten für die einzelnen Instrumente waren in der Literatur immer wieder Unstimmigkeiten bezüglich der Jahresangaben zu finden. So wurden in manchen Quellen Erfindungen früher oder später datiert als in anderen. Bei solchen Fällen wurden stets die Jahreszahlen übernommen, die in der Mehrheit auftraten. Die Entwicklungsgeschichte der o.g. Geräte wurde durch viele herausragende Neuerungen und Ideen geprägt. Einige davon waren essentiell für deren weitere Entwicklung, andere wiederum gerieten schon nach kürzester Zeit wieder in Vergessenheit. Deswegen konzentrieren sich die kommenden Abschnitten auf die wichtigsten und bedeutsamsten Erfindungen jener Zeit. 2.1.1 Herzschrittmacher Der Herzschrittmacher wurde für Patienten entwickelt, deren Herz zu langsam oder zu unregelmäßig schlägt und den menschlichen Körper deshalb nicht mit ausreichend Blut versorgen kann. Der Herzschrittmacher ist ein medizinisches, elektronisches Gerät, das aus einem miniaturisierten Schaltkreis und einer Kompaktbatterie besteht. Die Verbindung zwischen Schrittmacher und Herz wird durch eine bzw. zwei Elektrode(n) hergestellt. Die Elektrode ist ein sehr dünner, elektrisch isolierter Draht, der im rechten Vorhof oder in der rechten Herzkammer verankert wird. Er stellt die Herzaktivität fest, leitet die Informationen an den Herzschrittmacher weiter, der dann durch einen elektrischen Impuls von rund 3 Volt für eine Zeitdauer von etwa 0,5 Millisekunden automatisch die Herzfrequenz des Patienten an die gegebene Situation (z.B. schlägt das Herz bei erhöhter Körperbelastung schneller und bei Schlaf langsamer) anpassen kann. Dadurch zieht sich das Herz zusammen und Blut wird in den Kreislauf gepumpt. Neuere Schrittmacher haben darüber hinaus noch weitere Funktionen. Sie können einen Herzblock 13 zwischen Vorhof und Kammer überbrücken, sie können Herzrhythmusstörungen des Trägers aufzeichnen und in einer Datenbank speichern, sie können durch Überstimulation Vorhofrhythmusstörungen vermeiden helfen, sie verfügen über ein hochauflösendes intrakardiales EKG, das in Echtzeit am Monitor des Arztes zu sehen ist, sie verfügen über ein Home-Monitoring-System etc. Durch all diese o.g. Eigenschaften ist ein Herzschrittmacher zu einem vollständigen am Körper tragbaren Computersystem geworden – einer Wearable-Applikation. Grundsätzlich gibt es 3 verschiedene Arten von Herzschrittmachern: externe (nichtinvasive) Schrittmacher, passagere Schrittmacher und permanente Schrittmacher. Externe Schrittmacher sind große aufklebbare Elektroden, über die durch die Haut regelmäßig 13 Herzblock: Blockierung oder Verzögerung der Erregungsausbreitung im Erregungsleitungssystem des Herzens. 14 Stromstösse gegeben werden, um das Herz stimulieren. Sie sind nur im Notfall sinnvoll. Passagere Schrittmacher werden über eine Vene mit einer Elektrode in das rechte Herz eingebunden. Über eine von außen angeschlossene Batterie und ein Steuerungssystem wird dann das Herz stimuliert. Diese Methodik ist nur für wenige Tage sinnvoll, da sonst Infektionsgefahr besteht. Bei permanenten Schrittmachern wird eine Reizelektrode mit Batterie in den Brustkorb des Patienten operiert, um das Herz je nach Bedarf zu stimulieren. Ein moderner Herzschrittmacher hat heutzutage eine Funktionsdauer von 6 bis 12 Jahren. Meilensteine in der Entwicklung von Herzschrittmachern Im Jahr 1855 behandelte der französische Neurologe Armand-Duchenne eine Tachyarrhythmie 14-Patientin mit der „elektrischen Hand“ - zwei von außen aufgelegte Plattenelektroden. Dadurch gelang es ihm ihre zu hohen Herzfrequenzen zu senken und den regelmäßigen Pulsschlag wiederherzustellen. Gegen Ende des 19. Jahrhunderts um 1882 schaffte es Geh.-Rat Prof. Dr. Hugo Wilhelm von Ziemssen erstmals, Herzaktionen von außerhalb beliebig zu steuern. Ausschlaggebend für diesen Durchbruch war jedoch das Fehlen einiger Rippen bei der Patientin in der Herzregion. 1927 berichtete Arzt Marmorstein als Erster über eine erfolgreiche transvenöse Stimulation des rechten Vorhofs und Ventrikels 15 mit einer unipolaren, bipolaren und tripolaren Elektrode. Fünf Jahre darauf, 1932 beschrieb der New Yorker Arzt Hyman ein Gerät zur elektrischen Herzreizung durch periodische Stromimpulse. Das Gerät bestand aus einem Gleichstromgenerator mit Stromunterbrecher und einer bipolaren Nadelelektrode zur transthorakalen 16 Punktion des rechten Vorhofs. Diese erste Variante eines Herzschrittmachers wog 7,2 kg und musste alle 6 Minuten neu aufgeladen werden Der erste Herzschrittmacher, gebaut von dem kanadischen Elektrotechniker John Hopps im Jahre 1950, gab von außerhalb des Körpers elektrische Impulse durch die Haut an das Herz ab. Er war groß, klobig und unhandlich. Nachfolgende Geräteentwicklungen wurden zwar immer kleiner, arbeiteten jedoch noch von außerhalb und bezogen ihren Strom aus der Steckdose. Dadurch wurde die Bewegungsreichweite des Patienten, in Abhängigkeit der Länge des vorhandenen Stromkabels, stark eingeschränkt. 14 Tachyarrhythmie beschreibt eine schnelle und unregelmäßige Herztätigkeit. Herzhauptkammer 16 Transthorakal: durch den Thorax (Körper) 15 15 Abb. 2: erster externer Herzschrittmacher 1957 erfand Earl Bakken den ersten batteriebetriebenen externen Herzschrittmacher, der mit Transistoren arbeitete. Abb. 3 : Earl Bakkens Herzschrittmacher Im folgenden Jahr, 1958, entwickelten der Techniker Rune Elmqvist und der Chirurg Ake Senning (Firma Siemens&Halske) den ersten voll implantierbaren Herzschrittmacher mit myokardialen Elektroden 17. Dieser Schrittmacher bestand aus 20 diskreten Bauteilen und hatte einen Durchmesser von 5,6 cm, war 1,9 cm dick und wo ca. 180 g. Er arbeitete mit 2 Volt und einer Impulsdauer von 1,5 ms. Seine Funktionsdauer betrug um die 3 Stunden. Nachfolgende Geräte dieser Art hielten schon 2 Tage. Die Stromversorgung wurde über Nickel-Kadmium Akkus realisiert, die durch Induktionsspulen von außerhalb des Körpers wieder aufgeladen werden konnten. Somit entfiel die zuvor nachteilige Reichweiteneinschränkung. Dem ersten Patienten dieses ersten Herzschrittmachers, Arne Larsson, wurden im Laufe seines Lebens noch 22 weitere Geräte eingesetzt. 17 Myokardiale Elektroden: Elektrodenkopf ist über ein Gewinde in den Herzmuskel eingeschraubt 16 Abb. 4: erster implantierter Herzschrittmacher 1960 entwickelten und implantierten William Chardack und Wilson Greatbatch verbesserte Herzschrittmacher, welche sich durch besseres Material und längere Akkulaufzeiten auszeichneten, bei zwei Kindern und acht älteren Patienten mit Herzrhythmusstörungen. Durch den Einsatz von Quecksilberoxid-Zink-Akkumulatoren betrug die maximale Funktionsdauer etwa 24 Monate. Dadurch mussten diese Geräte nicht mehr von außerhalb aufgeladen werden. Abb. 5: Medtronic Chardack-Greatbatch Herzschrittmacher Die erste erfolgreiche Implantation eines Herzschrittmachers (Chardack-Greatbatch 5850) in Deutschland gelang Prof. Dr. Heinz-Joachim Sykosch im Jahre 1961. Dieser Schrittmacher war faustgroß und wog 300g. 1962 baute Wilson Greatbatch den ersten Prototyp eines Zweikammerschrittmachers. Dieser erlaubte eine Synchronisation zwischen Vorhof und Ventrikel bei Herzrhythmusstörungen. Zweikammerschrittmacher arbeiten grundsätzlich mit 2 Elektroden (Sonden), je eine für die Haupt- und Vorkammer. Vorherige Schrittmacher waren nur Einkammersysteme, bei denen dann auch nur eine Elektrode zum Einsatz kam. Im selben Jahr wurden erste Sonden, die direkt durch die Vene ins Herz gebracht werden konnten, entwickelt. Dadurch erübrigten sich bisherige Verfahren, wobei dem Patienten unter Vollnarkose der Brustkorb geöffnet werden musste. 17 Lagergren kombinierte dann im Jahr 1963 den transvenösen 18 Zugang der Elektroden mit der Implantation eines batteriebetriebenen Aggregates unter die Haut (vorhofgesteuerter Schrittmacher). Ein Jahr nach dem ersten Prototyp eines Zweikammerschrittmachers, kam es zum ersten Einsatz dieser Systeme. Im Gegensatz zu den bisher festfrequenten Schrittmachern, die pausenlos elektrische Impulse abgaben, entwickelte Castellanos im Jahr 1964 den ersten Bedarfsschrittmacher nach dem Demand-Prinzip. Hier erfolgt die Impulsabgabe nur bei unregelmäßigem oder bei aussetzendem Herzschlag. Diese Entwicklung war die Grundlage der modernen Herzschrittmachertherapie. 1969 erfand Berkovits die ersten Zweikammersysteme (bifokale Schrittmacher), die eine koordinierte Vorhof- und Ventrikelstimulation ermöglichten. Um 1970 kam es zur Entwicklung und Implantation von Schrittmachern, die mit atombetriebenen Energiequellen arbeiteten und sich durch eine einwandfreie Funktionsweise auszeichneten. Jedoch wurde die Nutzung dieser Geräte, weil der Umgang mit ihnen aus strahlenrechtlichen Gründen sehr umständlich war, ziemlich bald auch wieder eingestellt. Mit der Erfindung der ersten implantierbaren Lithium-Iod-Batterie im Jahr 1972 durch Wilson Greatbatch erhöhte sich die Funktionsdauer der Herzschrittmacher deutlich und löste die bisherigen Zink-Quecksilber Batterien sowie alternative Energiekonzepte (z.B. atombetriebene Schrittmacher) ab. Der große Nachteil damaliger Schrittmacher war es, dass sie nur so arbeiteten wie es die Techniker in der Fabrik eingestellt hatten. Erst durch Entwicklung der programmierbaren Herzschrittmacher wurde es möglich, beispielsweise die Geschwindigkeit oder die Energie seiner Impulse durch von außen angelegte elektromagnetische Funkwellen zu verändern. 1974 setzte Camilli erstmals einen frequenzadaptiven Schrittmacher ein, bei dem das System auf Veränderungen des pH-Wertes im Blut, als Parameter veränderlicher körperlicher, und damit auch kardialer Belastung des Schrittmachers, reagiert. 1976 wurden antitachykarde Systeme entwickelt und implantiert. Sie dienten speziell zur Behandlung von zu schnellen Herzfrequenzen. Im Jahr 1979 wandte man zum ersten Mal die Telemetrie an, um den Batteriezustand oder die Elektrodenfunktionen ohne chirurgischen Eingriff überprüfen zu können. Das von Michael Mirowski 1966 entwickelte Konzept des implantierbaren Kardioverters wurde 1980 realisiert und bei einem Patienten am St. John’s Hopkins Medical Center in Baltimore, MD, USA, angewandt. Es sollte dem plötzlichen Herztod aufgrund von Herzrhythmusstörungen vorbeugen. Durch die Konstruktion von atemfrequenzgesteuerten und frequenzadaptierenden Herzschrittmachern im Jahr 1983 waren die Schrittmacher nun in der Lage, eigenständig die Stimulationsfrequenz je nach Körperaktivität des Trägers anzupassen. 1986 kamen erste Herzschrittmachern mit Temperatursensoren hervor, da sich bei Belastung zahlreiche physiologische Parameter u.a. die zentralvenöse Bluttemperatur verändern. Somit 18 eine Elektrodeneinführung durch die Vene 18 könnte die Stimulationsfrequenz des Herzschrittmachers kann anhand dieser Daten gesteuert werden. Im Jahr 1992 wurde der erste Herz-Kreislauf-Schrittmachers, der mittels „Closed Loop Stimulation“ komplett in die natürliche Regulierung des Systems integriert werden konnte, eingesetzt. Dieser Schrittmacher erkannte sowohl physische als auch mentale Belastungen (veränderte Gefühlslage) und führte dementsprechende Stimulationsfrequenzanpassungen durch. 1995 gelang die Konstruktion eines speziellen Zweikammerschrittmachers mit nur einer Elektrode. Nach der Entwicklung der Einkammer- und Zweikammersysteme kam 1999 erstmals die Dreikammerstimulation (Dreikammersysteme - biventrikulärer Herzschrittmacher) zum Einsatz. Sie zeichnete sich durch eine zeitgerechte Stimulation des rechten Vorhofs und der beiden Herzkammern aus und diente zur Behandlung von Patienten mit schwerer Herzinsuffizienz. Im Universitätsklinikum Heidelberg implantierte man 2003 weltweit erstmalig einen Schrittmacher, der beide Herzkammern synchronisiert und von zu Hause aus überwachbar ist (Home Monitoring System). Die aufgezeichneten kardialen Patientendaten werden per Mobilfunk über ein mobiles Patientengerät an die Servicezentrale des Herstellers Biotronik übermittelt und bei Anfrage des Arztes per Fax an diesen übertragen. Heute: Moderne Schrittmacher wiegen um die 20 g und sind etwa so groß, wie ein 5-DM Stück. Sie lassen sich nach dem NBG-Code in mehrere Gruppen (Stimulationsort, Wahrnehmungsort, Betriebsart, Frequenzadaption und multifokale Stimulation) einteilen, die jeweils mit maximal 5 Buchstaben abgekürzt sind. Abhängig vom Bedarf des Patienten werden Einkammer-, Zweikammer- oder Dreikammersysteme (intern sowie extern) verwendet. Abb. 6: moderne interne Herzschrittmacher Prognose: Die Herzschrittmachertechnik (Hardware) wird zunehmend optimiert (z.B. längere Funktionsdauer) und miniaturisiert. Aufgrund der Multiprogrammierbarkeit der Schrittmachersysteme, gibt es eine bessere Adaption an die verschiedenen Belastungen. Im Idealfall kann zukünftig der realistische physiologische Zustand des Patientenorganismus wiederhergestellt werden. 19 2.1.2 Thermometer Thermometer sind Messgeräte zur Erfassung von Temperatur und Temperaturschwankungen. Je nach Aufbau (messbare Temperaturbereiche, Skaleneinteilung etc.) und/oder verwendetem Sensor werden sie in verschiedenen Bereichen zur Temperaturmessung eingesetzt. Thermometer lassen sich in unterschiedliche Kategorien einteilen, zu denen beispielsweise Berührungsthermometer, die direkt mit dem Messstoff in Berührung kommen, Ausdehnungsthermometer, mit denen die Temperatur durch Messen der Längen- oder Volumenänderung eines Körpers bestimmt wird, z.B. QuecksilberFieberthermometer, Bimetallthermometer, die sich die unterschiedlichen Ausdehnungskoeffizienten von Bimetallen zur Nutze machen, Halbleiterthermometer und Widerstandsthermometer, bei denen die Temperatur über die Temperaturabhängigkeit des elektrischen Widerstandes ermittelt wird, gehören. Die Entwicklung des Thermometers wurde besonders zu Beginn ihrer Ära stark von anderen wissenschaftlichen Forschungen und Erkenntnissen aus Philosophie, Physik und Chemie beeinflusst. Auf dem Weg hin zur ihrer Vervollkommnung durchlief sie verschiedene Stadien, wobei eines einer besonderen Bedeutung zu Teil wurde und den Kern in der Thermometerentwicklung darstellte. Nachdem die Grundform des Thermometers durch viele Experimente weitestgehend festgelegt war, kam es über viele Jahrzehnte hinweg immer wieder zu ständigen Veränderungen bzgl. der Skaleneinteilung, Fixpunkte und Flüssigkeiten. In den jeweiligen Zeiträumen etablierten sich demnach unterschiedliche Thermometerstandards, so dass einheitliche Messungen so gut wie unmöglich waren. Einige von den im Laufe der Zeit entwickelten Standards sind uns auch noch bis heute erhalten geblieben. Dazu zählen zum Beispiel Celsius und Fahrenheit. Nachfolgend werden nun die bedeutsamsten Entdeckungen und Forschungen rund um das Thermometer beschrieben. Meilensteine in der Entwicklung des Thermometers Das älteste bekannteste Instrument zur Temperaturmessung datiert um 120 v. Chr. stammt von Heron von Alexandria. Dieses Gerät – das Thermoskop 19 - besaß noch keine Skala zum Ablesen der gemessenen Temperatur. 19 Ein nicht geeichtes wärmeempfindliches Instrument, das Temperaturveränderungen anzeigt. Thermoskope bildeten die Ausgangsbasis zur Entwicklung der Thermometrie bzw. Thermodynamik. 20 Abb. 7: Thermoskop von Heron von Alexandria Galileo Galilei wird das erste neuzeitliche Gerät zur Temperaturmessung zugeschrieben - ein offenes Luftthermoskop aus dem Jahre 1592. Es bestand aus einem Glaskolben mit einer aufgesetzten Glasröhre, die mit ihrem offenen Ende in ein Vorratsgefäß taucht. Jedoch waren auch mit diesem Apparat noch keine präzisen und genauen Messungen möglich, da die Messergebnisse je nach Luftdruck stark variierten. Die Körpertemperaturmessung mit dem Galilei’schen Thermoskop erwies sich ebenfalls als ungenau und sehr zeitraubend. Abb. 8: Galileis Thermoskop Einige Jahre später ca. 1611 entwickelte Santorio unabhängig von Galileis Erfindung ein ähnliches Thermometer zur Körpertemperaturmessung. Es war wie eine Glaskugel geformt, die der Patient im Mund hielt und von der aus sich eine lange schlangenförmige Röhre zu einer mit Wasser gefüllten Schüssel erstreckte. Je höher die Körpertemperatur des Patienten war, desto tiefer fiel der Wasserspiegel im Rohr. 21 1631 gelang dem Arzt Jean Rey die Konstruktion des ersten geschlossenen Flüssigkeitsthermometers. Durch dieses geschlossene System konnten nun vom Luftdruck unabhängige Temperaturmessungen vorgenommen werden, wodurch es die Genauigkeit von Galileis Thermoskop übertraf. Da die Flüssigkeit die Rey in seinem Thermometer verwendete Wasser war, gelangen ihm jedoch keine Messungen von Kältegraden. Durch die Entwicklung der ersten Weingeistthermometer um 1640 gelang eine präzisere Temperaturanzeige, die vor allem wegen des niedrigeren Gefrierpunktes von Alkohol noch bis zu bestimmten Kältegraden funktionierte. Die unterschiedliche Reinheit der verwendeten Alkohole, führte aber auch hier zu ungenauen und uneinheitlichen Messergebnissen. Großherzog Ferdinand II. von Toskana aus dem Hause der Medici entwickelte 1654 das „Florentiner - Flüssigkeitsthermometer“, ein Alkoholthermometer aus versiegeltem Glas, mit einer Skaleneinteilung von 50 Einheiten. Dieses Thermometer gab es später aber auch noch in anderen Ausführungen, die sich u.a. in ihrer Skaleneinteilung voneinander unterschieden. Die 50-teiligen Thermometer konnten im Gegensatz zu den anderen Arten jedoch fast gleich gehend angefertigt werden und ihre Kalibrierung erfolgte durch den Vergleich mit anderen Geräten. Bisherige Thermometer enthielten noch keinerlei Referenzpunkte. Abb. 9: 50-teiliges Thermometer „Florentine Little“ Zu Beginn des 18. Jahrhunderts kam man auf die Idee, die Wärmeausdehnung von Metallen zur Temperaturmessung zu verwenden. Des Weitern nahm Isaac Newton 1701 die erste Festlegung von Fixpunkten bzw. Referenzpunkten vor. Er entschied, den Nullpunkt auf den Gefrierpunkt von Wasser zu legen sowie den von menschlichem Blut auf 12°. Dadurch konnten Thermometer nun anhand von Fixpunkten auf den Temperaturskalen untereinander kalibriert werden. Newton verwendete seinerseits Leinöl als Thermometerflüssigkeit, das im 22 Vergleich zu Wasser über einen größeren Temperaturbereich flüssig blieb. Zwei Jahre darauf 1703 entwickelte Guillaume Amontons eines der ersten Gasthermometer mit konstantem Volumen. 1715 baute der Danziger Glasbläser David Fahrenheit ca. 60 cm lange Quecksilberthermometer, die allesamt in ihrer Anzeige übereinstimmten und entwickelte seine eigene Temperaturskala. Als Fixpunkte wählte er den Gefrierpunkt des Wassers bei +32° und den Siedepunkt des Wassers bei + 212°. Abb. 10: frühes Quecksilberthermometer Während Fahrenheit wie erwähnt Quecksilber als Füllung für sein Thermometer benutzte, konstruierte der Franzose Rene-Antoine Ferchault de Réaumur 1730 ein ähnliches Thermometer mit einer Alkoholfüllung (Weingeist). Er legte jedoch mit 0° (Gefrierpunkt des Wassers) und 80° (Siedepunkt des Wassers) neue Fixpunkte für die Temperaturmessung mit seinem Thermometer fest und unterteilte seine Skala in 80 gleiche Gradabstufungen. Die Temperaturmessergebnisse waren aber noch ziemlich ungenau, da der verwendete Weingeist kein lineares Volumenausdehnungsverhalten aufwies. 23 Aufgrund der Unzulänglichkeit des Alkohols bei höheren Temperaturen kehrte der schwedische Astronom Anders Celsius um 1742 zum Quecksilberthermometer zurück. Celsius führte bei seinem Thermometer eine neue und besser zu handhabende Skaleneinteilung von 100 Einheiten ein. Dies ermöglichte unter der Festlegung eines bestimmten Luftdrucks eine universelle Temperaturmessung, so dass Temperaturen auf der ganzen Welt miteinander verglichen werden konnten. Als neue Fixpunkte zur Kalibrierung des Thermometers wählte er 100° als Gefrierpunkt des Wassers und 0° als Siedepunkt des Wassers. Drei Jahre darauf, 1745, kalibrierten Daniel Ekström und Carl von Linnè die Fixpunkte von Celsius neu, woraufhin der Gefrierpunkt des Wassers bei 0° und der Siedepunkt des Wassers bei 100° lag. Mit diesen Fixpunkten und der Skaleneinteilung von Celsius ist dieses Thermometer in dieser Form noch bis heute das gebräuchlichste Instrument für die wissenschaftliche und damit auch für die ärztliche Thermometrie. 1800 entwickelte A.L. Breguet ein Bimetallthermometer, das einen erweiterten Messbereich zur Bestimmung höherer Temperaturen besaß. Im selben Jahr baute der Liverpooler James Currie ein Thermometer zur Körpertemperaturmessung mit gebogenem Ende, so dass der Arzt, der hinter dem Patienten stand, das Messergebnis optimal ablesen konnte. Zu Ehren von Anders Celsius wurde 1948 bei der 9. Generalkonferenz für Maß und Gewicht festgelegt, die Temperaturskala in Celsius-Skala umzubenennen. Sir Clifford Allbutt stellte 1866 ein etwa 15 cm langes Fieberthermometer her, bei welchem der Quecksilberfaden durch Kontraktion unterbrochen wurde, so dass auf diese Weise die Maximaltemperatur abgelesen werden konnte. Aus dieser Idee entstand allmählich das heutige Fieberthermometer mit Quecksilber. 1871 konstruierte Werner von Siemens das erste PlatinWiderstandsthermometer. Abb. 11: Thermometer mit Réaumur-Skala 24 Heute: Durch den Aufschwung der Chemie und Technik ist das heutige Thermometer zu einem der wichtigsten Messinstrumente überhaupt geworden. Es sind Messungen von bis zu 1/1000 °C möglich, weshalb es auch in vielen Gebieten, wie zum Beispiel in der Medizin oder der Meteorologie Anwendung findet. Aufgrund der leichten Zerbrechlichkeit und der hochgiftigen Flüssigkeit Quecksilber haben digitale Thermometer Quecksilberthermometer, speziell im medizinischen Bereich, ersetzt. Abb. 12: modernes digitales Fieberthermometer Prognose: Weitere Verbesserungen der Messtechnik sowie deren Miniaturisierung wird es ermöglichen winzige Fieberthermometer in Alltagsgegenstände, wie z.B. Kleidung zu integrieren. Dadurch kann eine permanente Überwachung der Körpertemperatur garantiert werden. 2.1.3 Stethoskop Das Stethoskop dient bei ärztlichen Untersuchungen als Diagnosegerät, mit dem der Arzt Körpergeräusche, vor allem jedoch Herztöne, Lungen- und Darmgeräusche sowohl abhören als auch gleichzeitig beurteilen kann. Das Abhören eines Organs mit einem Stethoskop wird in der Medizin selbst als Auskultation (lateinisch: auscultare – (eifrig) zuhören, horchen) bezeichnet. Das Stethoskop, eine noch relativ junge Erfindung des frühen 19. Jahrhunderts, dient aber nicht nur zur klaren Filterung von Körpergeräuschen, sondern soll auch die Distanz zum kranken Patienten wahren, um einer möglichen Ansteckung vorzubeugen. Stethoskope lassen sich in zwei Typen unterscheiden, nämlich in akustische und elektronische Stethoskope. Akustische Stethoskope sind heutzutage die gängigsten und bestehen aus den drei Grundelementen Ohrbügel, Schlauch und Schalltrichter/Bruststück/Kopf. Im Schalltrichter befindet sich zur Aufnahme von Geräuschen eine Membran, die durch solche in Schwingung versetzt wird. Die dadurch entstehenden Schallwellen bahnen sich ihren Weg durch den Schlauch zum Ohrbügel, der mittels so genannter „Oliven“ die Gehörgänge des Arztes abdichtet, um ein frühzeitiges Entweichen des Schalls zu vermeiden. Mit einem speziellen Trichter im Bruststück werden die Schallwellen noch zusätzlich verstärkt. Elektronische Stethoskope basieren nicht wie Akustische auf physikalischen Phänomenen, sondern sind in der Lage, den Schall mittels zusätzlicher elektronischer Systeme gezielt zu verstärken, Umgebungsgeräusche herauszufiltern und wahrgenommene Töne aufzuzeichnen. Stethoskope dieser Art sind bisher noch kaum verbreitet. 25 Meilensteine in der Entwicklung des Stethoskops Erste Schritte zur Entdeckung des Stethoskops machte etwa in der Mitte des 18. Jahrhunderts um 1761 Leopold Auenbrugger. Er erkannte, dass durch Abklopfen/Abhören des Brustkorbes (Perkussion 20) innere Erkrankungen wesentlich besser diagnostiziert werden können. Im Jahr 1808, rund 40 Jahre nach der Entdeckung von Auenbrugger, veröffentlichte dann der Pariser Arzt Jean Nicolas Corvisart eine Schrift über die Perkussion. Dadurch verhalf er der Perkussion zur allgemeinen Anerkennung als wichtiges diagnostisches Hilfsmittel. Während der Perkussion hörte der Arzt mit seinem Ohr direkt den Körper des Patienten ab. Den entscheidenden Geistesblitz, der zur Entwicklung des Stethoskops führte, hatte 1816 der französische Arzt Dr. Renè Thèophile Hyacinthe Laennec. Er formte erstmals eine Rolle aus Papier, um Herztöne von Patienten abzuhören, da die Perkussion zur Diagnose allein oftmals nicht ausreichte. Es wird vermutet, dass Laennec aufgrund der enormen Leibesfülle seiner Patienten auf diese Idee kam. Später ersetze er diese Papierrolle durch ein Holzrohr und nannte sein Instrument Stethoskop (griechisch: stethos, skopein = Brust, beobachten). Das erste Stethoskop für ein Ohr bestand aus einer 32 mm langen und 36 mm dicken Eichenholzrolle mit einem Gewicht von 230 Gramm. Nachfolgende Instrumente wurden stetig leichter, handlicher und brachten vor allem bessere akustische Ergebnisse. Laennec gilt aufgrund dieser Erfindung als Vater der Auskultation. Abb. 13: Nachbildung des Stethoskops von Laennec Laennecs Schüler Pierre Adolph Piorry fügte 1826 dem ursprünglichen Stethoskop ein großes flaches Ohrstück hinzu, das die Ohrmuschel besser abdecken sollte, um so die gehörten Schallwellen präziser in den Gehörgang zuleiten. Außerdem empfahl er die Verwendung einer kleinen flachen Elfenbeinplatte, die er als Plessimeter bezeichnete und die auf den Brustkorb des Patienten aufgelegt, dem klopfenden Finger als Anschlagfläche diente. Etwa zur gleichen Zeit kam aus England dann jedoch der Vorschlag, der sich bis heute durchgesetzt hat, einen Finger der anderen Hand des Untersuchers als Anschlagpunkt zu verwenden. 20 In der Medizin bezeichnet die Perkussion ein von Leopold Auenbrugger eingeführtes Verfahren, bei dem der Körper zur Diagnose abgeklopft wird. 26 1829 verbesserte Dr. Charles Williams das Laennec-Stethoskop, indem er es in 2 Teile zerlegte und als Material Guttapercha 21 einsetzte. Ein Gelenk verband diese beiden Teile, so dass es sich in verschiedene Winkel drehen ließ. Das ermöglichte dem Arzt beim Abhören eine bequemere Körperhaltung. Der englische Arzt Nicholas Comins entwickelte im selben Jahr ein Stethoskop mit einem langen flexiblen Tubus, da vor allem Frauen Untersuchungen mit dem herkömmlich kurzen Stethoskop als peinlich und unsittlich empfanden. Der New Yorker Arzt George P. Camman erschuf im Jahr 1850 ein binaurales Stethoskop für beide Ohren. Die ersten Stethoskope dieser Art waren hauptsächlich aus Stahl, mit Ohrteilen aus Elfenbein und Brustteilen aus Ebenholz in zwei verschiedenen Größen (variabel aufsteckbar). Die Schläuche bestanden aus Guttapercha und später aus Gummi. Abb. 14: binaurales Stethoskop von Camman Im Jahr 1868 baute Scott Alison das Differentialstethoskop bestehend aus zwei separaten Bruststücken, wobei die Schläuche jeweils an ein Ohr angelegt werden mussten. Dies ermöglichte den Vergleich der wahrgenommenen Geräusche von jedem Ohr. Das Stethoskop wurde zum Sinnbild eines wissenschaftlichen Arztes. 21 Der eingetrocknete Milchsaft der im malaiischen Raum heimischen Palaquium Bäume. 27 Abb. 15: Alisons Differentialstethoskop Die Arbeit des Italieners Aurelio Bianchi an einem komplexen Stethoskop mit einer Wasserdichtung, welches sich im praktischen Umfeld jedoch als unbrauchbar herausstellte, bildete 1884 die Grundlage für ein Patent, das der amerikanische Ingenieur R.C. M. Bowles für ein einfaches modernes Membranenbruststück einreichte. Durch aufwändige Untersuchungen und vielen Erfahrungen beim Umgang mit dem Stethoskop zeigte es sich immer mehr, dass sowohl ein Trichter als auch eine Membran zum optimalen Abhören eines Patienten erforderlich sind. Howard Sprague entwickelte deshalb 1926 das erste kombinierte Bruststück, wobei er einen Trichter mit einer Membran bespannte. Dieses Grundelement ist uns, wenn auch in deutlich weiterentwickelter Form, noch bis heute erhalten geblieben. 1958 konstruierte der britische Kardiologe Dr. Aubrey Leatham eine neuartige Form des Stethoskops. Sein Instrument enthielt neben der Kombination von Membran- und Trichterstethoskop, einen zusätzlich kleineren Trichter innerhalb des Ersten. Durch einen Hebelmechanismus konnte nun der eigentliche Trichter mit dem Kleineren erweitert werden, wodurch eine einfachere und akkuratere Auskultation von Kindern machbar wurde. Amplivox entwickelte 1961 ein elektronisches Stethoskop, das sich die neue kleinere Vakuumröhrentechnologie zunutze machte. Das Gerät entsprach jedoch nicht den Anforderungen der Ärzte und musste den herkömmlichen Stethoskopen wieder weichen. Im gleichen Jahr fertigte der amerikanische Kardiologe Dr. David Littmann im Gegensatz zu Vorgängergeräten ein rationalisierteres, leichtgewichtigeres und binaurales Stethoskop mit Schlauch an. Die Vorteile dieser Erfindung waren ein leichtes Gewicht, Flexibilität und ausgezeichnete akustische Eigenschaften. Littmanns Stethoskop war somit einer der wichtigsten Meilensteine in der Entwicklung des Stethoskops. 28 Abb. 16: Stethoskop nach Littmann Heute: Stethoskope kommen heutzutage in fast jeder medizinischen Einrichtung für das Abhören von Patienten zum Einsatz. Dabei werden derzeit fast ausschließlich nur akustische Stethoskope, die sich physikalische Phänomene zunutze machen, um Körpergeräusche besser wahrnehmen zu können, benutzt. Elektronische Stethoskope „Digital Stethoskop“ hingegen sind gerade erst auf dem Vormarsch. Abb. 17: elektronisches Stethoskop Prognose: Zukünftig werden digitale Stethoskope den Markt erobern, da sie schlichtweg leistungsfähiger als ihre akustischen Konkurrenten sind. Mit der Weiterentwicklung der Technik im Allgemeinen wird es auch hier möglich sein, Stethoskope soweit zu miniaturisieren, dass sie in Kleidung miteingebunden werden könnten. Dies würde ein automatisches Abhören von Körpergeräuschen für Vorbeugung, Nachsorge etc. ermöglichen. Der zuständige Arzt könnte dann die dadurch ermittelten Daten bei Bedarf über eine zentrale medizinische Sammelstelle abrufen. Voraussichtlich wird Stethoskopen im Bereich Wearables jedoch nur eine geringe Bedeutung zu Teil werden, da der Auswertungsaufwand der aufgenommenen Körpergeräusche zu umständlich und kompliziert sein würde. 29 2.1.4 EEG - Elektroenzephalografie Die Elektroenzephalografie ist eine Methode um elektrische Gehirnströme zu messen. Diese Gehirnströme werden durch physiologische Vorgänge innerhalb einzelner Gehirnzellen, die durch ihre elektrischen Zustandsänderungen zur Informationsverarbeitung des Gehirns beitragen, hervorgerufen und sind an der Kopfoberfläche abgreifbar. Die gemessenen elektrischen Spannungen werden dann mit einem geeigneten Gerät verstärkt und auf einem Monitor in Form von Hirnstromwellen angezeigt. Der Arzt kann dann anhand der Frequenzen und der Amplituden der Hirnstromwellen Aussagen über die Gehirnaktivität und den Bewusstseinszustand ableiten. Die grafische Darstellung der gemessenen Hirnströme heißt Elektroenzephalogramm. Damit Gehirnströme aufzeichnet werden können, werden dem Patienten ca. 30 Elektroden auf der Kopfhaut angebracht. Ein EEG dauert etwa 30 Minuten, aber es sind auch EEGMessungen bis zu 24 Stunden möglich. Dabei wird dem Patienten ein tragbares EEG-Gerät angelegt, das die Hirnströme über festsitzende oder festgeklebte Elektroden aufnimmt und abspeichert. Sämtliche EEG-Untersuchungen sind ungefährlich, schmerzlos und beliebig oft wiederholbar. „Grundsätzlich gibt es zwei Arten der EEG-Technologie. Das konventionelle und das Computer-EEG. Unter einem konventionellen EEG werden EEG-Geräte verstanden, die mit direkt schreibenden Registriersystemen arbeiten und eine EEG-Buch erzeugen. Das EEGBuch besteht aus ca. 120 registrierten Papierseiten von EEG-Signalen über die Dauer von ca. 20 Minuten. Dagegen bezeichnet man Systeme, die ein EEG auf elektronische Datenträger wie Laserplatten („Optical disk“) abspeichern und die registrierten Signale auf einem PCMonitor zur Darstellung bringen als Computer-EEG. Um ein Elektroenzephalogramm aufzuzeichnen, werden Elektroden, ein Vorverstärker (Differenzverstärker) und ein EEGGerät mit Verstärker und Schreib- oder Speichersystemen benötigt.“ 22 Abb. 18: modernes digitales EEG-System mit 32 Kanälen 22 Quelle: http://www.file-commander.de/projektarbeit.htm 30 Die Entwicklung der Elektroenzephalografie nahm schon in der Antike mit der primitiven Hirnforschung ihren Anfang. Viele Gelehrte und Wissenschaftler (z.B. Hippokrates, Herophilos, Erasistratos und Claudius Galenus) experimentierten dort mit Leichen, um ihre anatomischen Kenntnisse auch im Bereich des Gehirns zu erweitern. Erst mit der Entdeckung der Nervenzellen um 1677 durch den Holländer Antoni van Leeuwenhoek begann man, die Komplexität des Gehirns zu erahnen, womit das Interesse der Wissenschaftler stetig anstieg. Etwa 250 Jahre später, um 1929, wurde dann das erste menschliche EEG aufgenommen. In den folgenden 60 Jahren gab es zahlreiche Verbesserungen und Weiterentwicklungen in der Technologie zur Ableitung, Verstärkung und Analyse des EEG. Weitreichende Fortschritte in der Aufklärung der elektrophysiologischen Vorgänge, die der Wellenform des EEG zugrunde liegen, ergaben sich in den letzen 20 Jahren. Meilensteine in der Entstehung der Elektroenzephalografie Erste Entdeckungen, die den Weg der Elektroenzephalografie ebneten, machte 1840 Emil Du Bois-Reymond. Er stellte fest, dass Aktivitäten peripherer Nerven zu Spannungsänderungen im näheren Umfeld führen (stetiger Wechsel zwischen Ruhepotential und Aktionspotential). Dem Liverpooler Arzt Richard Caton gelang es 1875 erstmals, diese elektrischen Spannungsänderungen auf dem freiliegenden Kortex 23 von Tieren (Affen und Kaninchen) zu messen. Dabei verwendete er ein Thomson-Spiegelgalvanometer (Abschnitt 2.1.6). 1888 entdeckte der polnische Wissenschaftler Adolf Beck regelmäßige elektrische Muster im zerebralen Kortex von Kaninchen und Hunden. Schon zu dieser Zeit vor den bahnbrechenden Arbeiten des deutschen Neurologen und Psychiaters Hans Berger 24 studierte Beck die elektrische Aktivität des Gehirns bei Tierversuchen und gelang größtenteils, wie später festzustellen war, zu denselben Ergebnissen wie Berger. Die Unterlagen des russischen Physiologen Pravdich-Neminski enthalten vermutlich die weltweit erste illustrierte Aufzeichnung einer elektrischen Hirnaktivität um 1911. Das „Electrocerebrogram“, wie er es nannte, wurde an Hunden mit Hilfe des Fadengalvanometers von Einthoven vermessen (Abschnitt 2.1.6). Das Jahr 1929 war wohl eines der bedeutsamsten in der Entwicklung der Elektroenzephalografie. Der Jenaer Psychiater Hans Berger publizierte die von ihm 1924 erstmals durchgeführte Elektroenzephalografie mit Silbernadelelektroden beim Menschen das erste menschliche Elektroenzephalogramm. Dabei registrierte er mit Hilfe von Verstärkern und Messgeräten (Berger verwendete sowohl Lippmanns Kapillargalvanometer als auch Einthovens Fadengalvanometer) die Aktionsstromtätigkeit des Gehirns und entdeckte dabei die Alpha 25- und Beta 26-Wellen. Natürlich stand man trotz dieses Durchbruchs noch 23 Großhirnrinde, eine vor allem beim Menschen besonders groß entwickelte Struktur, die nochmals unterteilt werden kann in Bereiche mit unterschiedlicher Funktion, z.B. auditiver Kortex (Hörrinde), visueller Kortex (Sehrinde) etc. 24 Hans Berger gilt als Entdecker des Elektroenzephalogramms. Er entwickelte eine Methode zur Ableitung von menschlichen Hirnströmen. (Quelle: http://de.wikipedia.org/wiki/Hans_Berger) 25 Als Alpha-Welle wird ein Signal im Frequenzbereich zwischen 8 und 12 Hat bezeichnet. Ein verstärkter Anteil von Alpha-Wellen wird mit leichter Entspannung assoziiert. 31 am Anfang in der Entwicklung von EEG-Systemen. So arbeitete Berger beispielsweise, aufgrund mangelndem Wissens und technischen Defiziten noch mit zu großen Elektroden. Sie erlaubten keine detaillierten Aufnahmen der elektrischen Hirnaktivität, um beispielweise Tumore oder epileptische Zentren erkennen zu können. Abb. 19: das erste von H. Berger aufgenommene Elektroenzephalogramm Abb. 20: Bergers EEG-Aufnahmesystem um 1926 1932 erfand Jan Friedrich Tönnies den Differenzverstärker und konstruierte das erste direkt schreibende Multikanal-EEG-Gerät, bei welchem die gemessenen Hirnströme direkt mit einem Messschreiber auf Endlospapier geschrieben werden konnten. Durch den Differenzverstärker wurde es nun möglich, die sehr kleinen Hirnströme, die man über die Kopfhaut abgriff, soweit zu verstärken, dass verbesserte Auswertungsmöglichkeiten von Elektroenzephalogrammen zur Verfügung standen. 26 Beta-Wellen nehmen einen Frequenzbereich zwischen 14 und 30 Hz ein. Beta-Wellen treten nur unter der Einwirkung von Sinnesreizen oder bei geistiger Tätigkeit auf. 32 Abb. 21: direkt schreibendes Multikanal-EEG-Gerät Zwei Jahre darauf, 1934 hielt die nächste Revolution auf dem Gebiet der Verstärkertechnik ihren Einzug. B.H.C. Matthew entwickelte den Differentialverstärker mit dem die Gewinnung von bioelektrischen Signalen, einschließlich der Hirnströme, stark erleichtert wurde. Im folgenden Jahr gelang der Nachweis der Delta 27-Wellen. Im Jahr 1936 richtete das „Massachusetts General Hospital“ das erste EEG-Labor ein. Im gleichen Jahr erkannte der britische Wissenschaftler William Gray Walter, dass mit einer größeren Anzahl von Elektroden, die zudem noch kleiner als Bergers waren, viel bessere Messergebnisse erzielt werden könnten und dadurch die Lokalisierung von Tumoren und anderen Krankheiten möglich wurde. Da Walter seine Forschungen im Bereich der Elektroenzephalografie stetig vorantrieb, verwundert es nicht, dass er schließlich 1943 die Theta 28-Wellen entdeckte. Der erste in Europa industriell hergestellte 4-Kanal-Elektroenzephalograph von der Firma Schwarzer wurde 1946 ausgeliefert. Ein Jahr später kam es zur Gründung der „American EEG Society“. 1957 machte der Wissenschaftler William Gray Walter mit der Entwicklung des Toposkops sowie der dazugehörigen Technologie für dessen Anwendung, der EEG –Topographie, erneut auf sich aufmerksam. Das Gerät bestand aus 22 Kathodenstrahlröhren (CRT), woran wiederum je ein Elektrodenpaar befestigt war. Sämtliche Elektroden wurden in einer konkreten geometrischen Anordnung auf der Kopfhaut des Patienten angebracht, so das nun jede Kathodenstrahlröhre in der Lage war, die Intensität der elektrischen Hirnstromwellen einzelner Gehirnbereiche zu ermitteln und diese simultan als Elektroenzephalogramm auf einem speziellen Bildschirm darzustellen. Mit Hilfe dieser Technologie erkannte Walter schnell, dass Hirnstromwellen in unterschiedlicher Weise, zu unterschiedlichen Zeiten und in 27 Als Delta-Wellen werden Hirnwellen mit niedrigen Frequenzen von 0,5 bis 4 Hz bezeichnet. Delta-Wellen sind typisch für die traumlose Tiefschlafphase. 28 Theta-Wellen sind Signale im Frequenzbereich zwischen 3 und 8 Hz. Sie sind typisch für die Einschlafphase, Wachträumen, Hypnose, aber auch tiefe Entspannung und Meditation. 33 unterschiedlichen Teilen des Gehirns variieren. Anhand dieser Erkenntnisse konnte er dann die Funktionen der Alpha und Beta-Wellen exakt beschreiben. Walters Toposkop war jedoch sehr kompliziert und kostspielig, weshalb es sich trotz seiner enormen Vorteile in der Diagnostik nicht durchsetzen konnte. Erst in den 80er Jahren mit der Einführung schnellerer und kompakter Computer kam es zur Wiedergeburt dieses Instruments, das bis heute noch in ähnlicher Form weltweit zum Einsatz kommt. Durch die sich langsam verbreitende Digitaltechnik wurde 1988 das weltweit erste digital arbeitende EEG-Gerätes mit thermosensitiver Aufzeichnung und Signalübertragung mittels Lichtwellenleiter konstruiert. 1998 wurde der erste in Deutschland gefertigte Elektroenzephalograph für den Einsatz im Kernspintomographen gebaut. Heute: Die Elektroenzephalografie wird heute zu klinischen Diagnosen von schweren Kopfverletzungen, Gehirntumoren, zerebralen Infektionen, Epilepsie und degenerativen Krankheiten des Nervensystems eingesetzt. Sie findet aber auch Anwendung in der modernen Schlafmedizin. Gegenwärtige kommerzielle EEG-Geräte arbeiten zur Aufnahme von Hirnstromaktivitäten mit ca. 21 Kanälen (Elektrodenanzahl), obwohl weitaus mehr möglich wären. Dies würde jedoch im Vergleich zu dem erwartenden Informationsgewinn einen enormen methodischen und apparativen Mehraufwand bedeuten und wäre somit unökonomisch. Einige Labore hingegen nutzen zu besonderen Forschungszwecken teilweise bis zu 60 Kanäle. Neben normalen Kurzzeituntersuchungen von etwa 30 Minuten können EEG-Geräte auch zu Langzeituntersuchungen (24 Stunden) eingesetzt werden. Dabei kommen dann mobile Wireless-EEG-Systeme zum Einsatz, bei denen beispielsweise die gesamte Elektronik in einem Golfcap 29 integriert ist. Abb. 22: modernes Computer-EEG 29 Quelle: http://www.futurehealth.org/wireless_eeg.htm 34 Abb. 23: Wireless-EEG Prognose: Zukünftige EEG-Instrumentarien werden aufgrund ihrer Miniaturisierung unauffällig in die Kleidung integriert, so dass der Träger seinen alltäglichen Aufgaben in gewohnter Art und Weise nachgehen kann. Des Weiteren ist es vorstellbar, dass man Schnittstellen zwischen dem menschlichen Gehirn und dem Computer (Brain Computer Interface) entwickelt, bei denen Elektroenzephalografen die Gehirnströme des Menschen aufnehmen um sie zur Analyse an ein lernfähiges Computersystem zu übertragen. Dort werden aus den ausgewerteten Daten Steuerungssignale für angeschlossene Systeme generiert. Träger eines solchen Brain Interfaces sind dann in der Lage, per Gedanken Geräte in ihrer unmittelbarer Körpernähe zu kontrollieren. 2.1.5 EMG - Elektromyografie Die Elektromyografie ist eine Methode der medizinischen Elektrodiagnostik. Dabei misst man mit Hilfe von Oberflächen- oder Nadelelektroden Aktionspotentiale der Muskelzellen, die durch die Aktivität der Körpermuskulatur entstehen. Bei dieser Untersuchung werden die bipolaren Oberflächen- oder Nadelelektroden in einen Muskel eingestochen bzw. äußerlich auf einem Muskel angebracht. Die elektrischen Ströme in den Muskeln werden so sowohl im Ruhezustand als auch bei Anspannung gemessen. Die dann von den Elektroden aufgenommenen elektrischen Potentiale des Muskels werden über ein Oszilloskop als Wellenmuster angezeigt. Veränderungen des Wellenmusters können Hinweise auf mögliche Muskel- oder Nervenerkrankungen geben. Es werden also Folgen von muskulären Nervenschädigungen erkannt und Muskelerkrankungen diagnostiziert. Dabei handelt es sich hauptsächlich um neuromuskuläre Erkrankungen wie beispielsweise primäre Muskelerkrankungen oder unvollständige Lähmungen der Muskulatur. Eine besondere Form der Elektromyografie ist das Messen der Nervenleitgeschwindigkeiten (NLG). Hier wird gemessen wie schnell die Nerven elektrische Impulse weiter leiten können. Aus dem Vergleich mit Normalwerten ergeben sich dann Hinweise auf Art und Ort einer Schädigung des Nervens der untersucht wurde. Bei dieser Art der Messung werden Nerven mit kurzen Stromstössen gereizt, wodurch das Reizantwortpotential ermittelt werden kann. Die Nervenleitgeschwindigkeit ergibt sich somit aus dem Quotienten von Weg- und Zeitdifferenzen. Die Messung der NLG ist in allen Fällen von neurogenen Schädigungen bzw. Erkrankungen der Muskulatur von Bedeutung. Die Elektromyografie lässt sich in zwei Subkategorien einteilen, in das klinische und das kinesiologische EMG. Während beim klinischen EMG hauptsächlich mit Nadel- und 35 Drahtelektroden gearbeitet wird, um die Potentiale einzelner motorischer Einheiten messen zu können, beschäftigt sich das kinesiologische EMG, das meist mit Oberflächenelektroden agiert, primär mit der Funktion und der Koordination von Muskeln bei unterschiedlichen Bewegungsabläufen und Positionen. Meilensteine in der Entstehung der Elektromyografie Aufzeichnungen aus dem Jahr 1666 dokumentieren erste Erkenntnisse über die Muskulatur von Lebewesen. So beschrieb F. Redi als erster Wissenschaftler, dass Muskeln elektrische Potentiale generieren. 1780 entdeckte Luigi Galvani durch Experimente mit präparierten Froschschenkeln die Kontraktion von Muskeln unter Einfluss statischer Elektrizität. Nach dieser ersten zufälligen Entdeckung stellte Galvani systematische Beobachtungen an und bemerkte, dass die Froschbeine auch zuckten, wenn er sie mit zwei unterschiedlichen Metallen berührte. Galvani zog aus seinen Untersuchen damals jedoch den falschen Schluss. Er vermutete, dass die elektrische Spannung, die die Kontraktion der Froschmuskeln bewirkte, vom Froschgewebe selbst erzeugt worden sei und nannte sie „animalische Elektrizität“. Erst 1799 widerlegte Alessandro Volta aus Padua Galvanis Theorie der „animalischen Elektrizität“. Er erkannte, dass der elektrische Stromfluss in Galvanis Experiment nicht vom Froschbein selbst erzeugt wurde, sondern durch den leitenden Kontakt der zwei unterschiedlichen Metalle (Kupfer und Eisen). Im Jahr 1838, knapp 60 Jahre nach Galvanis Versuchen, bewies Carlo Matteucci, Professor der Physik, bei Forschungsarbeiten, ebenfalls mit Froschschenkeln, das biologisches Gewebe wie Nerven und Muskeln durch willkürliche Kontraktionen geringe elektrische Ströme erzeugen. Schließlich war es Emil Du Bois-Reymond der 1840 die Ursache dieser elektrischen Ströme im Ruhepotential eines Muskels, das sich durch Kontraktion verändert, sah. Die Potentialänderung nannte er Aktionspotential. Neun Jahre später leitete Du Bois-Reymond dann als Erster diese elektrische Signale von einem menschlichen Muskel ab, um sie mit einem von ihm entwickelten, besonders empfindlichen Galvanometer, dem„Multiplikator“, zu messen. Zur Untersuchung der Handgreifmuskulatur entwickelte Piper um 1907 die ersten Metalloberflächenelektroden, um elektrische Ströme über die Haut abzunehmen. Bei seinen Experimenten verwendete er neben diesen Elektroden auch ein Kraftmessgerät und einen Galvanometer. 36 Abb. 24: Oberflächenelektroden 1922 kamen Herbert Gasser und Joseph Erlanger auf die Idee, die 1897 entwickelte Braunsche Röhre 30 anstatt des Galvanometers zu verwenden, um so Elektrizität, die von der Muskulatur ausging, sichtbar zu machen. Nachfolgende Messungen wurden daraufhin leichter und vor allem präziser. Abb. 25: Braunsche Röhre Neben sämtlichen Erfindungen diverser Geräte, die die Entwicklung der Elektromyografie vorantrieben, gab es auch zahlreiche theoretische Forschungen im Bereich der Körpermuskulatur, die einen großen Anteil an der o.g. Entwicklung hatten. So entwarfen beispielsweise Sherrington und Liddell 1925 ihr Konzept der motorischen Einheit, das wesentlich zum Verständnis der Entstehung von registrierten elektrischen Signalen beitrug. Mit der Einführung der konzentrischen Nadelelektrode im Jahr 1929 durch Adrian und Bronk, wurde es nun möglich, die von einzelnen bzw. wenigen Muskelfasern erzeugten elektrischen Signale direkt zu erfassen. Dies lies eine genauere Diagnose von Erkrankungsursachen zu. 30 Die Kathodenstrahlröhre oder auch Braunsche Röhre (engl. cathode ray tube, kurz CRT) ist eine Elektronenröhre zur Erzeugung von Elektronenstrahlen, mit der sich u. a. schnell ändernde Spannungen und Ströme auf einem Fluoreszenzschirm sichtbar machen lassen. 37 Abb. 26: konzentrische Nadelelektrode 1934 revolutionierte B.H.C. Matthew mit der Erfindung des Differentialverstärkers die Verstärkertechnik zur Gewinnung von bioelektrischen Signalen. Einen der ersten Elektromyographen mit einer 35 mm Aufnahmekamera und einem Lautsprecher konstruierten 1946 Huddleston und Golseth. Abb. 27: Elektromyograph von Huddleston & Golseth Im Jahr 1960 wurden die ersten stabilen Silber-Chlorid-Oberflächenelektroden für das kinesiologische EMG entwickelt. Das besondere dieser Elektrodenart ist, dass sie nicht polarisierbar sind und deshalb ein unverfälschtes Messergebnis liefern können. Heute: Moderne EMG-Geräte basieren auf denselben Komponenten wie EMG-Geräte älterer Herkunft (Eingabeterminal, Verstärker, Filter, visuelle und/oder auditive Ausgabegeräte, Elektroden), erlauben aber eine bessere und zuverlässigere Diagnose, wodurch steigende Heilungschancen erreicht werden. Das EMG dient heutzutage nicht nur zur Diagnose von Muskelerkrankungen, sondern auch zum Studium komplexer Bewegungsabläufe im Bereich Physiotherapie oder der Sportmedizin. Gegenwärtige EMG-Geräte gibt es in verschiedenen Ausführungen: komplexe EMG-Systeme in medizinischen Laboren kleine tragbare EMG-Geräte für Belastungs- oder Langzeituntersuchungen sowie zur dauerhaften Überwachung 38 wireless EMG-Geräte Abb. 28: tragbares EMG-Gerät Prognose: Tragbare und miniaturisierte EMG-Systeme werden in Kleidungsstücke, als Hilfsmittel zur schnellen Diagnose von Muskelkrankheiten und zum Einsatz im Affective Computing 31 (z.B. können Muskelverkrampfungen Stress signalisieren Einleitung von Gegenmaßnahmen, wie entspannende Musik aktivieren), integriert. 2.1.6 EKG – Elektrokardiografie Bei der Elektrokardiografie werden Herzströme untersucht, die bei elektrischer Erregung des gesamten Herzmuskels entstehen. Diese messbare elektrische Spannung im mV (Millivolt) Bereich kann mit einem Spannungsmessgerät am Körper abgefasst werden. Aus elektrischer Sicht kann man sich das schlagende Herz als Wechselspannungsquelle im Körper vorstellen, die Wechselströme nach allen Seiten hin fließen lässt. Da der Körper des Menschen elektrisch leitfähig ist, können nun überall an der Körperoberfläche (Brustwand und Extremitäten) diese Potentialschwankungen gemessen werden. Dazu werden verschiedene Elektroden am Körper angebracht, welche die sehr geringen Spannungen aufnehmen und sie nach entsprechender Verstärkung im EKG-Gerät auf ein Oszilloskop abbilden. Anhand der Größe, Richtung und Dauer der elektrischen Spannungsänderungen kann eine Diagnose bzgl. der Herztätigkeit gestellt werden. Herzkrankheiten verändern das charakteristische Schaubild eines gesunden Herzens und werden somit erkennbar. Die Entwicklung der Elektrokardiografie ging aus dem Studium der Elektrizität hervor. Schon in der Antike kannte man 4 Quellen der Elektrizität: den Blitz, den Bernstein, durch Reibung mit weichem, trockenen Stoff, 31 Affective Computing beschreibt eine Mensch-Maschine-Interaktion auf emotionaler Ebene. Dabei sind Mensch-Maschine-Schnittstellen in der Lage auf emotionales Verhalten eines Users zu reagieren, es zu beeinflussen oder hervorzurufen. 39 elektrische Fische und magnetisches Eisenerz. Das eigentliche Studium der Elektrizität wurde ab ca. 1600 systematisch durch verschiedenste Forscher und Wissenschaftler betrieben: William Gilbert betrachtete die Erde als einen Magneten Otto von Guericke beschrieb die Aufladung von gewissen Gegenständen durch Reibung Stephen Gray beschrieb die Eigenschaften von Leiter und Isolator Ewald von Kleist, Abbè Nollet, Pieter van Musschenbroek u.a. erfanden den „ersten Stimulator“, womit zum ersten Mal Stromstöße nach Belieben abgegeben werden konnten. Meilensteine in der Entwicklung der Elektrokardiografie Alles begann 1756 mit der Entdeckung von Leopold Caldani, Professor der Medizin aus Bologna. Er zeigte, dass ein isoliertes Nerven-Muskel-Präparat (meist ein präparierter Froschschenkel) durch einen Stromstoss erregt (zucken) werden kann. Einige Jahre später 1780 entdeckte Luigi Galvani durch Experimente ebenfalls mit präparierten Froschschenkeln, die Kontraktion von Muskeln unter Einfluss statischer Elektrizität. Nach dieser ersten zufälligen Entdeckung stellte Galvani systematische Beobachtungen an und stellte fest, dass die Froschbeine auch zuckten, wenn er sie mit zwei unterschiedlichen Metallen berührte. Galvani zog aus seinen Untersuchen damals jedoch den falschen Schluss. Er vermutete, dass die elektrische Spannung, die die Kontraktion der Froschmuskeln bewirkte, vom Froschgewebe selbst erzeugt worden sei und nannte sie „animalische Elektrizität“. 1799 widerlegte Alessandro Volta aus Padua Galvanis Theorie der „animalischen Elektrizität“. Er erkannte, dass der elektrische Stromfluss in Galvanis Experiment nicht vom Froschbein erzeugt wurde, sondern durch den leitenden Kontakt der zwei unterschiedlichen Metalle (Kupfer und Eisen). Volta war auch der Erfinder der ersten funktionierenden Batterie – der voltaischen Säule. 40 Abb. 29: voltaische Säule Durch die Entdeckung des Elektromagnetismus von Hans Christian Ørsted aus Kopenhagen um 1820, der erstmals magnetische Felder um stromdurchflossene elektrische Leiter beschrieb, und den Forschungsarbeiten von Ampère, Schweigger und Poggendorff konnte das erste elektrische Ladungsmessgerät, der Galvanometer, gebaut werden. In den darauffolgenden Jahren kam es dann zur ständigen Weiterentwicklung dieses Instruments. So konstruierte der Florentiner Physikprofessor Leopold Nobili im Jahre 1825 eine Variante, die er „astatic galvanometer“ nannte und konnte mit ihr verschiedene Ladungsströme in einem Nerven-Muskel-Präparat aufzeigen. Abb. 30: Nobilis „astatic galvanometer“ Im Jahr 1838 bewies Carlo Matteucci, Professor der Physik, bei Forschungsarbeiten ebenfalls mit Froschschenkeln, dass biologisches Gewebe wie Nerven und Muskeln durch willkürliche Kontraktionen geringe elektrische Ströme erzeugen. Schließlich war es Emil Du Bois-Reymond der 1840 die Ursache dieser elektrischen Ströme im Ruhepotential eines Muskels, das sich durch Kontraktion verändert, sah. Die 41 Potentialänderung nannte er Aktionspotential. Im selben Jahr beobachtete Carlo Matteucci bei Tierversuchen mit Taubenherzen, dass auch die Herzmuskeltätigkeit auf elektrischen Strömen basiert. Neun Jahre später leitete Du Bois-Reymond dann als Erster die elektrische Signale von einem menschlichen Muskel ab, um sie mit einem von ihm entwickelten besonders empfindlichen Galvanometer, dem„Multiplikator“, zu messen. Abb. 31: Multiplikator 1873 entwickelte der luxemburgische Physiker Gabriel Lippmann das Kapillarelektrometer. Es bestand aus einer Quecksilber-Schwefelsäule in einem dünnen Glasschlauch (Kapillarröhrchen), der die Veränderungen des elektrischen Potentials durch die Bewegung des Quecksilbermeniskus erkennen lies. Später stellte sich dieses Elektrometer jedoch als unzureichend heraus. 42 Abb. 32: Lippmanns Kapillarelektrometer Eine erste graphische Darstellung elektrischer Ströme, die bei einer Muskelbewegung erzeugt werden – auch beim Herzmuskel - gelang dem Franzosen Etienne Jules Marey im Jahr 1876. Er verwendete dabei das Lippmann’sche Kapillarelektrometer. Den Grundstein für das moderne Galvanometer legten 1880 Arsène d’Arsonval und Marcel Deprez. Sie entwickelten ein Galvanometer mit einem räumlich fixen Magneten und einer beweglichen Spule. Abb. 33: Galvanometer von Deprez und d’Arsonval 43 Zum großen Durchbruch in der Elektrokardiografie kam es 1887, als Augustus Waller das erste menschliche Elektrokardiogramm aufzeichnete. Er benutzte dazu das Lippmann’sche Kapillarelektrometer, um die durch die Herztätigkeit bedingten Spannungsänderungen an der Körperoberfläche zu messen. Zur Ableitung verwendete er zwei Elektroden auf Brust und Rücken. Für Diagnosezwecke waren diese noch recht ungenauen Aufnahmen, die nur Kammerausschläge enthielten, jedoch ungeeignet. Abb. 34: das erste menschliche Elektrokardiogramm 1893 führte der holländische Physiologe Willem Einthoven bei einem Meeting der „Dutch Medical Association“ den Begriff „Elektrokardiogramm“ ein. Später gestand er aber, dass A. Waller ihn als Erster benutzt hatte. Zwei Jahre darauf, 1895 verbesserte Einthoven durch viele mathematische Berechnungen die Kapillarelektrometerkurvenanalyse und beobachtete fünf Phasen der elektrischen Herztätigkeit, die er P, Q, R, S und T nannte. Diese Phasenbezeichnung wird auch noch heute in der modernen Medizin bei der Aufnahme eines EKG verwendet. Abb. 35: 5 Phasen der elektrischen Herztätigkeit Viele große Entdeckungen unserer Zeit wurden oftmals durch zufällige Experimente gemacht und genauso verhielt es sich im Jahre 1897 auf dem Gebiet der Elektrokardiografie. In diesem Jahr entwickelte Clement Ader ein Empfangsgerät für die Überseetelegrafie, welches sich jedoch nicht nur für seinen konstruierten Zweck eignen sollte. Wie sich später herausstellte besaß dieses Gerät ideale Eigenschaften, es in einen Galvanometer zu transformieren. So entstand der sogenannte Fadengalvanometer / Saitengalvanometer. Beim dieser Galvanometervariante wurde der zwischen zwei Elektroden abgenommene Strom durch einen im magnetischen Feld gespannten Faden geleitet, der sich dann je nach Stromrichtung nach 44 rechts oder links bewegte. Der Schatten des Fadens projizierte sich auf eine lichtempfindliche Platte und zeigte das Elektrokardiogramm an. Abb. 36: Fadengalvanometer 1903 baute Einthoven einen verbesserten und empfindlicheren Fadengalvanometer, den er bei der Konstruktion eines Elektrokardiographen verwendete. Dieser Apparat wog etwa 270 kg ermöglichte erstmals die Aufzeichnung verwertbarer Herzstromkurven. Als Elektroden dienten hierbei mit Wasser gefüllte Metalleimer. Willem Einthoven gilt vor allem wegen dieser Erfindung als Erfinder der Elektrokardiografie. Abb. 37: Einthovens Elektrokardiograph 45 Abb. 38: eines der ersten Elektrokardiogramme, aufgezeichnet durch ein Fadengalvanometer In den folgenden Jahren prägte Einthoven mit seinen Forschungsergebnissen und Entwicklungen die Elektrokardiografie. So geschah es auch, dass der erstmals 1905 ein Telekardiogramm aufnahm. Dabei wurden die gemessenen Herzströme eines Mannes, der sich in einem Krankenhaus befand, zu Einthovens 1,5 km entfernten Labor via Telefonkabel übertragen und aufgezeichnet. 1912 beschrieb Einthoven sein „Einthoven-Dreieck“, das die Anordnung und Stückzahl der Leitungen bei der Messung eines EKGs angab. Dazu bestimmte er die drei Standardleitungen I, II und III. Ab 1920 konnten, aufgrund der Erfindung des Röhrenverstärkers um 1906, die ersten fahrbaren Elektrokardiographen konstruiert werden. 1924 erhielt Willem Einthoven den Nobelpreis für die Erfindung des Elektrokardiographen. Ernstine und Levine setzten 1928 erstmals Vakuum-Röhren (Röhrenverstärker) ein, um das vom Körper abgeleitete EKG-Signal zu verstärken. Da der Röhrenverstärker wesentlich leichter zu bedienen und auch billiger war, konnten Diagnosen von nun an in ganz normalen Arztpraxen, anstatt in großen Forschungseinrichtungen oder größeren Kliniken, durchgeführt werden. Außerdem ermöglichte diese Technik eine einfachere und genauere Aufzeichnung der gemessenen elektrischen Potentiale. Im gleichen Jahr baute Frank Sanborn’s Unternehmen (gegründet 1917; 1961 übernommen von Hewlett-Packard und seit 1999 Philips Medical Systems) einen portablen Elektrokardiographen mit einem Gewicht von etwa 23kg, der seinen Strom von einer 6-Volt Autobatterie bezog. 1930 wurden die ersten tragbaren Elektrokardiographen entwickelt, die kurze Zeit später ein fester Bestandteil der medizinischen Diagnostik waren. 1932 entwickelte Frank Wilson eine neue Ableitungsmethodik, die eine Bezugselektrode / Sammelelektrode verwendete. Bei diesem Verfahren wurde von den drei Extremitätenableitungen einzeln gegen die Bezugelektrode abgeleitet (unipolare Ableitung). Nach vielen Experimenten erweiterte er die Elektrodenanzahl um drei und schuf die nach ihm benannte Brustwandableitung. 1934 revolutionierte B.H.C. Matthew mit der Erfindung des Differentialverstärkers die Verstärkertechnik zur Gewinnung von bioelektrischen Signalen. Im Jahr 1938 definierten die “American Heart Association” und die “Cardiac Society of Great Britain” Standardpositionen und –leitungen zum Verdrahten eines Patienten bei einem EKG. Heraus kamen dabei die sechs Brustwandableitungen: V1 – V6; V steht für Volt. 46 Vier Jahre danach, 1942 führte Emanuel Goldberger die drei Extremitätenableitungen aVR, aVL und aVF ein. Zusammen mit Einthovens drei Extremitätenleitungen und den sechs Brustwandableitungen, erhielt er ein EKG mit 12 Leitungen, so wie es auch heute noch zum Einsatz kommt. 1948 konstruierte der Schwede Rune Elmquist den ersten Tintenstrahldrucker zur Aufzeichnung von physiologischen Signalen, mit dem er zur Demonstration beim „First International Congress of Cardiology“ in Paris verschiedene EKGs aufzeichnete. Außerdem gelang in diesem Jahr die Erfindung des Transistors durch William B. Shockley, John Bardeen und Walter Brattain. Der Transistor hatte u.a. auch großen Einfluss auf die Elektrokardiografie. EKG-Geräte waren nun in der Lage das aufgezeichnete Elektrokardiogramm direkt auf Papier auszudrucken. Außerdem ermöglichte der Transistor die Herstellung von wesentlich kleineren und handlicheren Geräten, als zuvor mit der Röhrentechnik. Kurz darauf entwickelte der Physiker Norman Jeff 1949 einen 33 kg schweren tragbaren Elektrokardiografen, integriert in einem Rucksack, der das EKG der Trägers aufzeichnen und als Signal übertragen konnte. Dieses erste System eines „Holter Monitors“ (Langzeit-EKG) gilt als Vorreiter des ambulanten EKGs. Abb. 39: moderner „Holter Monitor“ 1963 waren es Baule und McFee, die als Erste ein Magnetkardiogramm aufzeichneten. Dabei nutzten sie das elektromagnetische Feld, das bei jeder elektrischen Herzaktivität entsteht. Somit gelang die Aufnahme der Herztätigkeit ohne Anbringung von den Hautoberflächenelektroden. Die Firma Schwarzer entwickelte 1956 einen 17 Kilogramm schweren EinkanalDirektschreiber, den „Cardioscript II“. 47 Abb. 40: Einkanal-Direktschreiber der Firma Schwarzer 1993 veröffentlichten Professor Robert Zalenski und Kollegen einen Bericht über die Nutzung eines EKGs mit 15 Ableitungen. Durch die drei zusätzlichen Leitungen (Standard sind 12 Ableitungen) wird die Empfindlichkeit des Elektrokardiographen erhöht, wodurch spezielle Herzkrankheiten, wie z.B. die myokardiale Infarktbildung erkannt werden können. 1999 zeigten Forscher aus Texas, dass EKGs (mit 12 Anschlussleitungen) drahtlos zu einem Handheld-PC übertragen und dann zuverlässig von einem Kardiologen ausgewertet werden können. Heute: Moderne Geräte sind in der Lage ein EKG zu vermessen und die Zeitintervalle der einzelnen Abschnitte anzugeben. Sie drucken vermutliche Diagnosen aus und übertragen die ermittelten Daten über integrierte Schnittstellen zu externen Speichereinheiten. Je Diagnoseverfahren kommen verschiedene Arten von EKGs zu Anwendung; z.B. Ruhe-EKG, Langzeit-EKG (24-Stunden-EKG), Belastungs-EKG, intrakardiales EKG. Bei Langzeituntersuchungen werden kleine tragbare EKGs verwendet. Gegenwärtig sind auch schon EKG-Shirts im Einsatz. Sie enthalten integrierte Sensoren, die den Herzschlag des Trägers messen und die ermittelten Daten via Bluetooth sowie einem speziellen Mobiltelefon an ein medizinisches Service-Center übertragen. Von dort aus erfolgt die Weiterleitung der Daten zu einem Arzt. 32 32 Quelle: http://www.futurenews.at/archives/394-Gesundheits-Handies-und-EKG-Shirts.html 48 Abb. 41: mobiles EKG-Gerät „Cardio24“ Prognose: Durch die Einbindung unsichtbarer, miniaturisierter und intelligenter EKGSensorik in die Alltagskleidung werden neue Wege der Prävention eingeschlagen. EKGSysteme können bei Notfällen ein EKG vermessen und selbstständig den zuständigen Arzt alarmieren. Das EKG kann aber auch zur Selbstkontrolle, z.B. bei sportlicher Aktivität, benutzt werden. 2.1.7 Defibrillatoren Bei lebensbedrohlichen Situationen, wie Herzrhythmusstörungen 33, Kammerflimmern 34, Kammerflattern 35 und plötzlichem Herzstillstand, kann die normale Herzaktivität durch gezielte starke Stromstöße wieder herstellt werden. Dieses Behandlungsmethode nennt sich Defibrillation und das verwendete Gerät dazu Defibrillator. Defibrillatoren werden auf Intensivstationen, in Notfalllaufnahmen, an vielen anderen Orten im Krankenhaus sowie in den Rettungsfahrzeugen und vielen Arztpraxen bereitgehalten. Seit den 90er Jahren des 20. Jahrhunderts werden sie auch zunehmend in vielen öffentlich Gebäuden und Orten für eine Anwendung durch medizinische Laien zugänglich gemacht, um eine schnelle Hilfe zu gewährleisten. Denn das Zeitfenster für eine erfolgreiche Defibrillation und ein erfolgreiches Überleben beträgt insgesamt nur etwa 10 Minuten. 33 Unter einer Herzrhythmusstörung versteht man eine Störung der normalen Herzschlagfolge, verursacht durch nicht regelrechte Vorgänge bei der Erregungsbildung und -leitung im Herzmuskel. 34 Kammerflimmern ist eine ungeordnete Muskeltätigkeit der Herzkammern, bei der eine ausreichende Blutversorgung des Körpers nicht mehr gegeben ist. Im Gegensatz zum häufiger auftretenden Vorhofflimmern, stellt das Kammerflimmern eine sehr bedrohliche Erscheinung dar. 35 Kammerflattern ist die rasche Folge relativ regelmäßiger Herzkammeraktionen mit einer Frequenz von 200 bis 350/Min. Durch außerhalb des Sinusknotens gelegene Strukturen werden Erregungsrückbildungsstörungen ausgelöst. Der Übergang zum Kammerflimmern ist fließend. 49 Der Hauptbestandteil eines Defibrillators ist ein Kondensator, der die vom Benutzer gewählte elektrische Energie speichert, die in einem Bereich zwischen 200 und 360 Joule liegt. Zur Defibrillation werden großflächige Elektroden auf den Brustkorb des Patienten geklebt oder gepresst und die aufgeladene Energie durch Knopfdruck über die Elektroden abgegeben (exponentiale Entladung). Moderne Defibrillatoren arbeiten biphasisch, d.h. das während der Defibrillation die Spannung (Plus/Minus) zwischen beiden Elektrodenplatten gewechselt wird. Dadurch wird weniger Energie für die Defibrillation benötigt, was wiederum schonender für den Patienten ist. Je nach Bauart und Einsatzszenario können verschiedene Defibrillatoren unterschieden werden. Der manuelle Defibrillator stellt die konventionelle Form dar und kann zusätzlich auch als externer Herzschrittmacher, als EKG sowie zur Messung der Sauerstoffsättigung und des Blutdrucks eingesetzt werden. Abb. 42: herkömmlicher manueller Defibrillator Halbautomatische Defibrillatoren (automatisierte externe Defibrillatoren - AED) analysieren mit Hilfe einer Software den Herzrhythmus des Patienten und entscheiden danach selbstständig ob eine Defibrillation notwendig ist. Erst nach dem Entscheid zur Defibrillation wird diese Funktion freigeschaltet und kann vom Anwender ausgelöst werden. AEDs können optional auch mit einem EKG ausgestattet sein und sind für Laien besonders leicht handhabbar. 50 Abb. 43: AED Um eine möglichst frühzeitige Hilfe zu gewährleisten, werden spezielle Defibrillatoren – Public Access Defibrillators (PAD) – in immer mehr öffentlichen Einrichtungen, wie etwa in Einkaufszentren, Flughäfen und Bahnhöfen zur Verfügung gestellt. Bei diesen Geräten handelt es sich um halbautomatische Defibrillatoren, die den Anwender mit Sprachanweisungen führen. Eine besondere Form des Defibrillators ist der implantierbare Kardioverter-Defibrillator (ICD), der bei Patienten mit hohem Risiko für Kammerflimmern, ähnlich einem Herzschrittmacher, eingepflanzt wird. Die Elektroden des Defibrillators haben direkten Kontakt zum Herzmuskel, wodurch bei der Defibrillation viel geringere Energien benötigt werden. Erkennt der ICD beispielsweise eine gefährliche Herzrhythmusstörung gibt er völlig autonom einen Gleichstromimpuls ab, der den regelmäßigen Herzschlag wiederherstellt. Abb. 44: Darstellung eines implantierten Defibrillators 51 Meilensteine in der Entwicklung der Defibrillatoren Die Geschichte der Defibrillatoren begann im Jahre 1774. Aus dieser Zeit stammen Schriften der Royal Human Society worin sich Berichte über eine Wiederbelebung eines 3-jährigen Kindes durch Applikationen von transthorakalen Stromstößen wiederfinden. Zahlreiche Experimente mit der Elektrizität und lebenden Körpern führten immer wieder zu neuen Erkenntnissen auf diesem Gebiet. So gelang es Jean Louis Prevost und Frederic Battelli 1899 erstmals Kammerflimmern am Herzen eines Hundes mittels elektrischen Stroms zu beenden und die zuvor unregelmäßige Herztätigkeit wieder in den normalen Sinusrhythmus zu überführen. Durch weitere Untersuchungen entdeckte M. Hoffa 1849 als Erster, dass durch eine externe elektrische Stimulation Vorhofkammerflimmern hervorgerufen werden konnte. 1930 veröffentlichten William Bennett Kouwenhoven und Kollegen Forschungsberichte eines Experiments, die zeigten, dass Wechselstrom dazu benutzt werden kann, um einer Herzrhythmusstörung bei Hunden entgegenzuwirken. Die erste menschliche Defibrillation am Herzen eines 14 jährigen Jungen gelang Dr. Claude S. Beck im Jahre 1947. Dabei wurde ein 60 Hz Wechselstrom am offenen Thorax direkt an den Herzmuskel abgegeben. Dieses Ereignis brachte der Defibrillation die Akzeptanz in der Medizin, die ihr zuvor verwehrt worden war. Forschungen auf diesem Gebiet wurden nun verstärkt vorangetrieben. Abb. 45: Claude S. Becks erster Defibrillator Im Jahr 1950 suchten W. B. Kouwenhoven und W. Milnor mit Hilfe von externen Defibrillatoren (zur Defibrillation am geschlossenen Thorax), verschiedenen Strömen, Impulsen und Elektroden nach einer idealen Kombination dieser Teile, um bei einer Defibrillation das Herz nach einer Rhythmusstörung oder einem Herzstillstand wieder in den Normalzustand versetzen zu können. Von daher ist es auch nicht verwunderlich, dass 52 Kouwenhoven und Milnor 1954 als Erste eine externe Defibrillation eines Hundes mit einem 60 Hz großen Wechselstrom, über außen am Thorax angebrachte Elektroden, gelang. Drei Jahre danach, 1957, schaffte es Paul Zoll erstmals, auch bedingt durch die Arbeiten von Kouwenhoven und Milnor, eine externe und zudem erfolgreiche Defibrillation eines Patienten, der an Vorhofflimmern litt, durchzuführen. 1958 beauftrage ein Elektrizitätsunternehmen Kouwenhoven und Kollegen einen portablen Defibrillator zum Training des Erste-Hilfe-Personals zu bauen. Daraufhin konstruierten sie den „John Hopkins AC Defibrillator“, der insgesamt über 90 kg wog. Als 1960 der Defibrillator zum weltweit ersten Mal erfolgreich zur Wiederbelebung eines 42 Jahre alten Mannes eingesetzt wurde, stiegen der Stellenwert und die Akzeptanz dieses Instruments sprunghaft an. Der damalige zu behandelnde Arzt war Gottleib Friesinger. Die Forschungen von Professor Frank Pantridge und L. A. Geddes machten es möglich, dass 1965 der erste portable Defibrillator in einem Krankenwagen installiert werden konnte. Er wog ca. 70 kg und bezog seinen Strom von der Autobatterie. Weitere Defibrillatoren dieser Art wurden fortan in Krankenhauszimmern aufgebaut oder mit Hilfe von Rollen durch das Krankenhaus bewegt. Diese neue Art der Mobilität war mit den ersten Geräten, die bis zu über 100 kg wogen nicht möglich. Den Strom für ihre Anwendung bezogen die portablen Defibrillatoren aus Stromnetzen oder über Batterien. Rund 16 Jahre vor der Erstimplantation eines ICDs entwickelte der amerikanische Professor M. Mirowski im Jahr 1966 das Konzept eines implantierbaren Defibrillators. Dessen Realisierung war jedoch aufgrund des damaligen Entwicklungsstandes mit zu hohen Risiken verbunden und konnte somit noch nicht umgesetzt werden. Im Auftrag der amerikanischen Luft- und Raumfahrtbehörde NASA konstruierte Pantrigde 1968 einen nur 3 kg schweren Defibrillator mit einem Minikondensator. Außerdem wurden in den 70er Jahren des 20. Jahrhunderts die ersten internen und externen Defibrillatoren gebaut, die in der Lage waren Herzrhythmusstörungen automatisch zu erkennen. Des Weitern kamen zu dieser Zeit auch die ersten AEDs zum Einsatz. Aufgrund modernerer Technologien konnte 1980 Mirowskis Konzept eines ICDs von 1966 umgesetzt werden. Zum ersten Mal erhielt ein Patient in den USA solch einen ICD zur Überwachung des Herzrhythmus. Im gleichen Jahr wurden auch die ersten transportablen Defibrillatoren konstruiert, die elektronisch Herzkammerflimmern erkennen konnten. Zwei Jahre später, 1982, fand die erste Implantation eines ICDs in Europa statt. Heute: Moderne Defibrillatoren ermöglichen jedem Anwender eine sichere Benutzung durch einfache Handhabung und Sprachanweisungen des Systems. Außerdem sind sie tragbar, praktisch, wartungsfrei, preisgünstig, leicht (etwa 3 kg) und arbeiten biphasisch. Sie sind in der Lage den Herzrhythmus des Patienten zu analysieren und ggf. eine Defibrillation vorzunehmen. Weiterhin übernehmen zusätzliche Funktionen wie beispielsweise EKG- und Blutdruckmessungen. Prognose: Entwicklung neuer Technologien, wie z.B. einer externen Auflademöglichkeit für ICD-Batterien, so dass ein vorsorglicher Einsatz von implantierten Defibrillatoren bei Risikopatienten vorgenommen werden kann. Des Weitern wird es durch die immer kleiner werdende Defibrillationstechnik zukünftig möglich sein, sie in die Alltagskleidung von 53 Risikopatienten und Kranken zu integrieren; siehe LifeVest 36. So kann bei der Erkennung von Herzfehlfunktionen (Kammerflimmern, Rhythmusstörungen etc.) eine Defibrillation ausgelöst werden und es erfolgt eine automatische Alarmierung des Arztes via UMTS sowie die Übertragung der Diagnosedaten. 2.1.8 Pulsmessgeräte Der Puls (Pulsus = Stoß) ist die Dehnung der Schlagaderwände durch die Druckwelle des Blutes. Bei jedem Herzschlag wird Blut in die Aorta gestoßen. Diese Druckwelle breitet sich im gesamten arteriellen Gefäßsystem aus. So gelangt das Blut über die Arterien in die Kapillaren und schließlich bis zu den einzelnen Zellen. An manchen Körperstellen verlaufen die Schlagadern sehr dicht unter der Haut, so dass der Puls durch die Haut hindurch ertastet und gemessen werden kann. Bei der Pulsmessung zählt man die Anzahl der Pulsschläge pro Minute. Der normale Ruhepuls liegt bei etwa 50 bis 80 Schlägen in der Minute. Idealerweise gilt es aber, die Pulsfrequenz für 10 Sekunden zu messen und das Ergebnis mit 6 zu multiplizieren. Grundsätzlich wird zwischen dem arteriellen Puls und dem venösen Puls unterschieden. Die mit dem Blutstrom vorwärts gerichtete Fortleitung der Herzaktionen bestimmt den arteriellen Puls. Die rückwärts gegen den Blutstrom gerichtete Fortleitung der Herzaktionen bestimmt den Venenpuls. In der Medizin findet der arterielle Puls mehr Beachtung als der Venöse. Der gemessene Puls gibt Aufschluss über den Zustand des Kreislaufs, über seine Regelmäßigkeit, über die Druckanstiegsgeschwindigkeit, über den absoluten Druck und über das Füllungsvolumen der Gefäße. Der Puls ist somit ein guter Indikator für den Gesundheitszustand des Blutkreislaufs. Die wichtigsten Punkte an denen der arterielle Puls am menschlichen Körper gemessen werden kann, sind am Hals, beidseitig der Luftröhre, an den Halsschlagadern, an den Handgelenken, an den Leistenbeugen und am Fußrücken. Um die Pulsfrequenz zu ermitteln kommen in der Regel zwei Verfahren zum Einsatz. Entweder wird dazu ein Pulsmessgerät verwendet, oder die Messung erfolgt manuell, durch das Abtasten der o.g. Pulsstellen in einem bestimmten Zeitraum. Die Pulsmessung und die Herstellung entsprechender Instrumente ging eng mit der Entwicklung von Uhren zur Zeitmessung einher sowie mit steigendem medizinischen Wissen über den Puls und dessen Bedeutung. 36 Quelle: http://www.lifecor.com/about_lifevest/about.asp 54 Meilensteine in der Entwicklung der Pulsmessgeräte Schon 300 v. Chr. bestimmte Herophilos von Chalkedon die Pulsfrequenz mit Hilfe einer selbstkonstruierten Wasseruhr „Klepsydra“. Im 2. Jahrhundert ermittelte der römische Arzt und Anatom Galenus von Pergamon (deutsch: Galen) die Pulsgeschwindigkeit ebenfalls mit einer Wasseruhr und konnte somit indirekt Fieber nachweisen, das immer durch ein Ansteigen der Pulsfrequenz charakterisiert ist. Das 16. und 17. Jahrhundert war geprägt von für die Entwicklung von Pulsmessgeräten wichtigen Entdeckungen. So beschrieb der italienische Physiker und Astronom Galileo Galilei als Erster die Gesetze des freien Falls sowie das Trägheitsgesetz und erfand das Pendel. Durch die Pendelgesetze und dem Pendel selbst gelang erstmals die Konstruktion sogenannter Pendeluhren. Galileos erdachte Pendeluhr aus dem Jahr 1640 wurde jedoch erst später von seinem Sohn Vincenzo umgesetzt. Christian Huygens präsentierte dann 1657 die erste genau gehende Pendeluhr, die auf den Pendelgesetzen Galileos basierte. Diese Uhr verbesserte den Gang auf 10 Sekunden pro Tag. Der italienische Arzt und Professor Santorio führte das Pendel 37 in der Medizin zur Messung der Pulsfrequenz ein und entwickelte eine Pendeluhr zur Pulsbestimmung - das Pulsilogium. Es bestand aus einem Faden, an dem eine Bleikugel hing sowie einer kreisrunden Skala zum Ablesen der Pulsfrequenz. Der Faden ließ sich jeweils verlängern oder verkürzen, bis es zu einer Übereinstimmung zwischen Pendelschwingungen und Pulsschlag kam. „Ein Pendel besteht aus einer Masse am Ende eines Seiles oder eines beweglich aufgehängten Stabes. Lenkt man ein Pendel aus seiner vertikalen Ruhelage aus, schwingt es unter dem Einfluss der Schwerkraft zurück und wird ohne den Einfluss von Dämpfung symmetrisch um den zentralen, tiefsten Punkt des Masseschwerpunktes – die Ruheposition – schwingen. Die Pendelfrequenz (Schwingfrequenz) hängt von dessen Länge, nicht jedoch von der Pendelmasse ab. Die regelmäßige Schwingungsperiode eines Pendels wurde bei der Konstruktion der ersten mechanischen Zeitmesser genutzt.“ Quelle: http://de.wikipedia.org/wiki/Pendel 37 55 Abb. 46: Pulsilogium von Santorio 1761 baute John Harrison eine Uhr, die in 161 Tagen nur 5 Sekunden falsch ging. Damit war es also schon zu dieser Zeit möglich, den Puls mit Hilfe dieser Uhr weitestgehend exakt zu ermitteln. 1854 erfand und konstruierte der deutsche Physiologe Karl von Vierordt den ersten indirekten Sphygmographen. Der Sphygmograph ist ein Gerät zur dauerhaften Aufzeichnung von Pulsfrequenzen als Kurven. Abb. 47: Sphygmograph von Karl v. Vierordt 56 Sechszehn Jahre nach der Erfindung des Sphygmographen durch Vierordt um 1862 verbesserte der französische Physiologe und Naturkundeprofessor Etienne Jules Marey diesen so, dass er die ermittelten Pulskurven auf berußten Glasplatten aufzeichnen konnte. Im Jahr 1877 entwickelte Louis Waldenburg entwickelte die erste Pulsuhr. Der Pulskontroller, den Professor Gustav Gärtner 1906 konstruierte, sollte ursprünglich die Pulswerte von Menschen sichtbar machen, die während eines operativen Eingriffs in einer Narkose lagen. Bald wurde dieser Apparat jedoch auch in internen Kliniken zur Beobachtung und Demonstration von Pulsanomalien, Pulsrhythmus, etc. verwendet. Abb. 48: Gustav Gärtners Pulskontroller 1930 entstanden die ersten Quarzuhren, bei denen ein Quarzkristall den Takt vorgibt. Die hervorragenden Schwingungseigenschaften von Quarzkristallen ermöglichten es, eine Genauigkeit von Bruchteilen einer Sekunde im Jahr zu erreichen. Aufgrund dieser exakten Zeitmessung wurde nun auch eine exakte Pulsmessung (Pulsschläge pro Zeiteinheit) machbar. Die Entwicklung des ersten kabellosen Herzfrequenz-Messgerätes (Pulsmesser) der Firma Polar fand 1983 statt. Der Polar PE 2000 Herzfrequenzmesser bestand aus einem Sender, der an der Brust entweder durch Einmal-Elektroden oder durch einen elastischen Elektrodengurt angebracht wurde sowie einem monitorähnlichen Empfänger, der am Handgelenk befestigt werden musste. Heute: Bei modernen Pulsuhren wird ein Brustgurt mit Sender getragen, der den Herzschlag des Trägers aufnimmt und ihn an den Empfänger am Handgelenk funkt. Damit wird eine permanente Anzeige des Herzrhythmus erreicht. Außerdem bieten viele Geräte noch diverse Zusatzfunktionen, wie z.B. Temperaturmessung, Belastungsmessung, Uhrzeitenanzeige und Kalorienberechnung an. 57 Abb. 49: Pulsuhr „Polar F11” Prognose: Pulsmessgeräte werden unsichtbar in Kleidung jeglicher Art (Sport- und Alltagskleidung) oder auch in Alltagsgegenstände (z.B. Computermäuse, Lenkräder in Autos) integriert sein. Dadurch können Messungen zeit- und ortsunabhängig vorgenommen und die Ergebnisse visuell (Uhr, Display) und/oder auditiv (winzige integrierte Lautsprecher in Ohrringen, Brillen) dem Träger mitgeteilt werden. 2.1.9 Blutdruckmessgerät Der Blutdruck ist der Druck, mit dem das Blut durch die Arterien des menschlichen Körpers fließt. Jeder Herzschlag führt zu einem plötzlichen Anstieg des Blutdrucks, der sich auch als Puls fühlen lässt. Der Blutdruck ist höher als der normale Luftdruck. Der Blutdruck ist nicht überall gleich, sondern sinkt von oben nach unten langsam ab, so dass die Strömung vom Ort des höheren Drucks in den des tieferen Drucks erfolgen kann. Bei der Kontraktion des Herzens wird Blut in die Aorta ausgestoßen, womit der Herzinnendruck und damit auch der Blutdruck zunimmt. Bei der Blutdruckmessung ist das der zuerst genannte, höhere Wert. Diese Phase der Herzaktion wird Systole 38 genannt und der gemessene Wert ist der systolische Wert des Blutdrucks. Bei Erschlaffung des Herzens nimmt der Blutdruck wieder ab und sinkt auf einen ganz bestimmten Druck ab. Dieser bei der Blutdrucksmessung zuletzt genannte niedrige Wert, ist der diastolische Wert des Blutdrucks. Diese Herzphase wird als Diastole 39 bezeichnet. Ein genau aufeinander abgestimmtes und kompliziertes Zusammenspiel von Gehirnstrukturen, Nerven und Hormonen steuert die Regulierung des Blutdrucks. Aufgrund dieser hohen Komplexität folgt nur eine vereinfachte Darstellung dieser Zusammenhänge. Der Hypothalamus, eine bestimmte Stelle im Gehirn, lenkt und überwacht alles, was mit dem Blutdruck zusammenhängt. Hauptsächlich steht er in enger Verbindung mit dem vegetativen Nervensystem, das alle lebensnotwendigen Funktionen des Körpers und somit auch den Blutkreislauf überwacht. Das vegetative Nervensystem gliedert sich funktionell in den Sympathikus und den Parasympathikus. Der Sympathikus bewirkt eine Leistungssteigerung des Organismus, regelt die Herztätigkeit und den Blutkreislauf und hemmt die Darmtätigkeit. 38 39 Die Systole ist die Anspannungs- und Blutauswurfphase des Herzens. Die Diastole ist die Füllungsphase des Herzens, im Gegensatz zur Systole, der Leerungsphase. 58 Der Parasympathikus dämpft den Herzschlag und fördert die Verdauung. Die dem Sympathikus zugeordneten Nerven spannen die Blutgefäßmuskeln an, so dass sich der Innenraum verengt, der Druck erhöht und die Blutströmung beschleunigt wird. Da der Parasympathikus der Gegenspieler des Sympathikus ist, sorgt dieser für die Entspannung der Blutgefäßmuskeln, so dass sie sich erweitern können und der Blutdruck gesenkt wird. Nur bei einem perfekten harmonischen Zusammenspiel zwischen Sympathikus und Parasympathikus ist eine gute Blutzirkulation möglich. Andersfalls kommt es zu Gefäßverkrampfungen oder zu überhöhtem Blutdruck. Neben Sympathikus und Parasympathikus haben auch Hormone Einfluss auf die Regulierung des Blutdrucks im menschlichen Körper. Die Hormone Adrenalin und Noradrenalin aus dem Nebennierenmark, die auf Gefäßmuskeln und Herztätigkeit einwirken. Das Schilddrüsenhormon, das ähnlich wie Adrenalin wirkt, das Hormon Insulin, das den Blutdruck herabsetzt, und schließlich die Zellhormone Acetylcholin und Histamin, die in den Kapillaren und Venolen die Blutversorgung und den Blutdruck regulieren. Blutdruckschwankungen Bei einer Veränderung des Blutdrucks können zwei Werte variieren, der systolische und der diastolische Blutdruck. Der Wert des systolischen Blutdrucks steigt an, wenn die aus der linken Herzkammer ausgestoßene Blutmenge ansteigt (das Herz muss kräftiger schlagen, um die größere Blutmenge abtransportieren zu können). die Geschwindigkeit, mit der sich der Herzmuskel zusammenzieht, ansteigt (das Herz schlägt schneller durch z.B. Anstrengung). die Elastizität der herznahen Gefäße geringer wird (d.h. je elastischer die Arterien, desto besser können sie einen plötzlichen Druckanstieg abfangen und desto geringer steigt der systolische Druck; bei Arteriosklerose fehlt die benötigte Elastizität). Der diastolische Wert des Blutdrucks steigt an, wenn der Widerstand, der dem Blutfluss entgegensteht, steigt; z.B. wenn Blutgefässe enger werden. Folglich können ein geweitetes Gefäß zu niedrigem Blutdruck und ein verengtes Gefäß zu hohem Blutdruck führen. Ein optimaler Blutdruck hat die systolischen und diastolischen Werte von 120 : 80. Ein als gut angesehenes Messergebnis ist bei 130 : 85 und als noch normal gelten die Werte von 140 : 90. Liegt der Messwert jedoch zwischen 140 : 90 und 160 : 90, so spricht man von einer Grenzwert-Hypertonie (Bluthochdruck), die - je nach Alter des Patienten - vielleicht noch keiner Behandlung, wohl aber einer regelmäßigen Kontrolle bedarf. Sowohl Bluthochdruck und zu niedriger Blutdruck können zu dauerhaften Schäden (Herzschwäche, Schlaganfall und Durchblutungsstörungen in den Beinen) führen und müssen behandelt werden. 59 Meilensteine in der Entwicklung der Blutdruckmessgeräte Im Jahr 1733 machten Ärzte und gebildete Laien aus England verschiedene Experimente, um die Schwankungen des Blutdrucks in Abhängigkeit des Pulses nachzuweisen. Der Blutdruck konnte dabei jedoch nur direkt, durch das Einführen von Messsonden in große Körperarterien, bestimmt werden. Diese Methode zur Blutdruckmessung – auch blutige Methode genannt wurde noch weit bis in das 19. Jahrhundert praktiziert. Ebenfalls in diesem Jahr entdeckte Stephan Hales ein Hilfspfarrer aus England, dass der menschliche und tierische Blutkreislauf ständig variierte. Bei seinen Experimenten mit Pferden, einem Schaf, einer Damhirschkuh und einer Auswahl von Hunden führte er Glasröhren in die Schenkelarterien der Versuchstiere ein und konnte somit erstmals den Anstieg und Abfall des Drucks in der Blutlaufbahn visualisieren. Anhand dieser Erkenntnisse definierte er den Begriff „Blutdruck“. Er erkannte, dass der Blutdruck die Anstrengungen des kontrahierenden Herzens widerspiegelte und er ein Maß für die Widerstandskraft der Blutgefäße gegen den Blutfluss darstellte. 1828 entwickelte Jean Leonard Marie Poiseuille ein Hämodynamometer. Dabei handelt es sich um eine Art Quecksilbermanometer zur Messung des arteriellen Blutdrucks. Bei der Konstruktion des Hämodynamometers ersetzte Poiseuille die Glasröhren von Hales durch ein U-förmiges Quecksilbermanometer mit einem kurzen Schlauch, der direkt in die Arterien eingeführt werden konnte. Mit diesem Instrument nahm Poiseuille in der nachfolgenden Zeit direkte Blutdruckmessungen bei Hunden und Pferden vor und schätze anhand der Messergebnisse den mittleren arteriellen Blutdruck des Menschen auf etwa 160 mm Hg. Einige Zeit später im Jahr 1834 entwickelte der Pariser Arzt Jules Hèrisson ein Sphygmometer. Damit konnte die Stärke des Pulsschlages gemessen werden, die wiederum Rückschlüsse auf die Höhe des Blutdrucks zuließ. Zur Ermittlung des Blutdrucks wurde dieses Gerät auf die Speichenarterie (arteria radialis) gedrückt. 1854 erfand und konstruierte der deutsche Physiologe Karl von Vierordt den ersten indirekten Sphygmographen (Abbildung 47; Abschnitt 2.1.8). Der Sphygmograph ist ein Gerät zur dauerhaften Aufzeichnung von Pulsfrequenzen als Kurven. Dadurch konnte auf unblutige Art und Weise die ungefähre Blutdruckhöhe bestimmt werden. J. Falvre maß um 1856 während eines chirurgischen Eingriffs als Erster, mit Hilfe von Kathetern und einem Manometer, den genauen Blutdruck der Oberschenkel- und Oberarmarterie eines Menschen. Das war die erste exakte invasive Blutdruckmessung. Vier Jahre später, 1860 entwickelten die französischen Physiologen Auguste Chauveaux und Etienne Jules Marey ein Instrument zur Blutdruckmessung. Es basierte auf dem Quecksilbermanometer von Poiseuille und dem Grundprinzip von Vierordt. Bei den Versuchen mit dem von ihnen konstruierten Instrument mussten Katheter in die linke und rechte Herzkammer geschoben werden. So ermittelten sie unter anderem den systolischen Blutdruck eines Pferdes, welches bei vollem Bewusstsein war. Die Messwerte für die rechte Herzkammer betrugen 27 mm Hg und die der Linken 129 mm Hg. Das Verfahren war für den Einsatz beim Menschen ungeeignet. Im selben Jahr gelang es Frederick Akbar Mahomed Mareys Sphygmographen so zu modifizieren, dass er erstmals zu klinischen Untersuchungen bei Patienten mit „Scarlet Fever“ eingesetzt werden konnte. 60 Aufgrund der Forschungen durch Chauveaux und Marey wird das Jahr 1862 als Beginn der modernen Hämodynamik datiert. Die Hämodynamik beschreibt den Blutfluss in den Blutgefäßen in Abhängigkeit von den dafür verantwortlichen Kräften. Marey und Chauveaux benutzten in diesem Jahr ebenfalls erstmalig eine Apparatur für die Druckmessung von verschiedenen Herzblutgefäßen bei Tieren. Zudem verbesserte Marey den Sphygmographen von Vierordt - seine Variante konnte die Kurven auf berußten Glasplatten aufzeichnen. 1881 konstruierte Samuel Siegfried Karl Ritter von Basch ein mit Pelotte 40 und Manometer versehenes Sphygmomanometer. Damit konnte eine genauere und unblutige Messung der Blutdruckhöhe vorgenommen werden. Seine Messungen des menschlichen systolischen Blutdrucks ergaben 135 – 165 mm Hg. Das von Basch gebaute Gerät ähnelte dem von Hèrisson und wurde bei Messungen direkt an die Speicher- oder Schläfenarterien (arteria temporalis) gepresst. Im Laufe der Zeit verbesserte nicht nur Basch selbst, sondern auch viele andere Wissenschaftler, wie zum Beispiel Pierre Potain, immer wieder sein Sphygmomanometer. 1889 führte Gustav Gärtner sein Tonometer ein. Es maß den Blutdruck zum Zeitpunkt des Wiedereintritts des Blutes in ein zuvor blutleer gemachtes Endglied eines Fingers bei Reduktion des Drucks in einer um den Finger gelegten aufblasbaren Manschette. Dieses Gerät fand speziell im deutschen Raum viel Anwendung und trug maßgeblich zum Fortschreiten klinischer Studien über den Blutdruck bei. Ein großer Nachteil des Tonometers war, dass der Zeitpunkt des Blutrückflusses willkürlich mit dem Auge abgeschätzt werden musste. Dadurch ergaben sich oftmals große Unsicherheiten und Differenzen beim Ablesen der ermittelten Messwerte. Blutdruckmessgeräte in ihrer heutigen Form, mit aufblasbarer zirkulärer Oberarmmanschette, gehen auf ein Instrument des Paduaner Arztes Scipione Riva-Rocci um 1896 zurück. Sein Instrument, das die erste exakte, nicht invasive Blutdruckmessung erlaubte bestand aus einem manschettenähnlichen Fahrradschlauch, der mittels eines Gummiballons aufgeblasen werden konnte, sowie einem Quecksilberbarometer zur Messung des systolischen Drucks in der Armarterie. Zum Gedenken an seine Forschungen und Entwicklungen führte man die Abkürzung „RR“ für den Blutdruckwert ein. 40 Die Pelotte ist ein ballenförmiger, meist halbkugeliger Gegenstand, der in der Regel zu medizinisches Zwecken zur Kompression oder zum Zusammendrücken oder Weghalten von Gewebe genutzt wird. 61 Abb. 50: Riva-Roccis Sphygmomanometer Unabhängig von Riva-Roccis Arbeiten entwickelten die zwei Engländer Leonard Hill und Harold A. Barnard 1897 ein ähnliches Instrument zur systolischen Blutdruckmessung. Sie maßen den Druck jedoch mit einem Federbarometer anstatt des von Riva-Roccis verwendeten Quecksilberbarometers. In den Jahren zwischen 1901 und 1904 publizierten vier Autoren (Janeway, Masing, Sahli und Strasburger) unabhängig voneinander eine einfache unblutige Methode zur Bestimmung des diastolischen Blutdrucks. Lange Zeit maßen Forscher und Kliniker dem diastolischen Druck nämlich nur eine geringe Aussagekraft zu. Ein Grund dafür waren sicherlich auch die komplizierten Methoden seiner Bestimmung. 1905 verbesserte der russische Militärarzt Nikolai Sergejewitsch Korotkow das Riva-RocciMessverfahren, indem er ein Stethoskop (Die Entwicklung des Stethoskops kann in Abschnitt 2.1.3 nachgelesen werden.) zur Bestimmung des Blutdrucks einsetzte. Damit ließ sich nun sowohl der systolische als auch der diastolische Blutdruck bestimmen. Das von Heinrich von Recklinghausen im Jahre 1906 entworfene Blutdruckmessgerät arbeitete nach demselben Prinzip wie Riva-Roccis. Es war jedoch mit einem Federmanometer und einer breiteren Oberarmmanschette von 12 – 13 cm ausgestattet und konnte den systolischen und diastolischen Blutdruck ermitteln. Durch diese Verbesserungen ließen sich nun zuverlässigere Messergebnisse anfertigen. Im Jahr 1968 kamen die ersten vollautomatischen Blutdruckmesser zum Einsatz. Sie waren die Vorläufer der modernen 24-Stunden-Blutdruckmessgeräte. 1976 standen erstmals handliche und leicht zu bedienende elektronische Selbstmessgeräte zur Verfügung. Sie erlaubten eine Blutdruckmessung durch den Patienten selbst. Die ersten Geräte zur Blutdruckmessung am Zeigefinger wurden 1989 entwickelt. Drei Jahre später, 1992 waren dann auch erste elektronische Blutdruckmessgeräte mit Handgelenksmanschetten für Patienten verfügbar. 62 Abb. 51: Blutdruckmessgerät für das Handgelenk Heute: Moderne Blutdruckmessgeräte sind zuverlässig und leicht bedienbar. Sie können zu hause oder unterwegs ohne ärztliche Hilfe benutzt werden. Dies ermöglicht den Trägern eine Selbstkontrolle rund um die Uhr. Außerdem arbeiten sie mit einer digitalen Anzeigeeinheit. Dennoch werden in vielen Kliniken immer noch die üblichen Blutdruckmessgeräte, nach Riva-Rocci benutzt. Prognose: Blutdruckmessgeräte werden zukünftig weiterhin miniaturisiert und in die Alltagsgegenstände, wie zum Beispiel Kleidung oder Uhren integriert. Dadurch kann eine ständige und unsichtbare Überwachung des Blutdrucks gewährleistet werden. 2.1.10 Hörgeräte Ein Hörgerät kann als eine Schnittstelle zwischen dem geschädigtem Ohr und seiner Umgebung aufgefasst werden. Dabei soll es den Höreindruck des geschädigten Ohres so gut wie möglich, an den des Gesunden anpassen. Hörgeräte lassen sich nach vier verschiedenen Entwicklungstechnologien klassifizieren: 1. Analoge Hörgeräte sind auch heute noch am weitesten verbreitet. Sie bestehen aus einem Mikrofon, einem Verstärker incl. Filter und Amplitudenbegrenzer, einem Lautsprecher, Benutzerreglern wie Lautstärkereglung und Funktionsumschalter, Justagereglern wie z.B. Tonregler und Batterien. 2. Digital programmierbare Hörgeräte unterscheiden sich von analogen in der Art der Einstellungskontrolle. Justierungen werden meist durch Programmiergeräte in einen Speicher im Hörgerät übertragen. Der Benutzer kann das Gerät oftmals mit einer Fernbedienung steuern. 3. Werden Hörgeräte mit einem digitalen Pfad ausgestattet, der einen analogen steuert, so spricht man von Hybridgeräten. Der Prozessor wird benutzt, um Schlüsselwerte aus dem Signal zu extrahieren und damit den Verstärker zu beeinflussen. Geräte dieser Art ermöglichen z.B. Rausch- und Rückkopplungsunterdrückung. 63 4. In digitalen Hörgeräten werden Audiosignale durch A/D-Umsetzer in eine digitale Darstellung umgewandelt. Diese werden in einer Prozessoreinheit durch Algorithmen verarbeitet und dann mit Hilfe eines D/A-Umsetzers zurückübersetzt. Digitale Hörgeräte bieten einige Vorteile gegenüber den vorher genannten, wie z.B. größere Zuverlässigkeit durch geringen Verschleiß der Bauteile und bessere Sprachverständlichkeit in lärmbehafteter Umgebung. Des Weiteren werden Hörgeräte nach ihren Bauformen unterschieden: 1. „Hinter-dem-Ohr-Geräte: Diese Hörgeräte werden „Hinter dem Ohr“ getragen, dafür wird neben dem Hörgerät noch eine nach Maß angefertigte Otoplastik (Ohrpassstück) mit einem Schallschlauch benötigt. HdO-Geräte sind in der Lage Hörschäden am Vielfältigsten zu versorgen. Da bei HdO-Geräten mehr Platz für die Elektronik zur Verfügung steht, können bei diesen Geräten vielfältige technische Optionen sowie hohe Verstärkungsleistungen realisiert werden. Die Schallaufnahme geschieht oberhalb der Ohrmuschel. 2. In-dem-Ohr-Geräte: Diese Hörgeräte werden „In dem Ohr“ getragen. Die Elektronik des Hörgerätes ist dabei in eine individuell angefertigte Hohlschale eingearbeitet und wird in den Gehörgang eingeführt. IdO-Hörgeräte können im Gegensatz zu HdOGeräten die anatomischen Vorteile des Außenohres nutzen. Das Mikrofon befindet sich direkt im Ohr und somit am natürlichen Aufnahmeort des Schalls. Ein weiterer Vorteil ist, dass der Schall direkt, d. h. ohne Umweg, vom Hörer auf das Trommelfell trifft. Dadurch ist weniger Verstärkung als bei den HdO-Geräten erforderlich und der Klang wird oftmals als angenehmer empfunden. HdO- und IdO-Geräte unterscheiden sich, abgesehen von der höheren Verstärkung der HdO-Geräte, in der Leistungsfähigkeit kaum noch voneinander. 3. Taschenhörgeräte: Eine heutzutage kaum noch verwendete Bauart sind Taschenhörgeräte. Diese wurden in den 50er und 60er Jahren noch häufig genutzt, durch die Miniaturisierung der Bauteile wurden sie von den HdO- und IdO-Geräten vom Hörgerätemarkt verdrängt. Heute finden diese Geräte selten noch bei Menschen mit an Taubheit grenzender Schwerhörigkeit oder Resthörigkeit Anwendung. Bei einem Taschengerät ist der Hörer an der Otoplastik 41 angebracht. Dieser wird über ein dünnes Kabel mit dem Hörgerät verbunden. Ein Problem bei Taschengeräten ist das Rascheln der Kleidung am Gerät (Körperschall am Mikrofon). 4. Hörbrille: Eine Hörbrille ist eine Brille, in deren dicken Bügeln Hörgeräte untergebracht sind. Hinten am Bügel befinden sich Otoplastik und Batteriefach. 5. Knochenleitungshörgeräte: Bei besonderen Erkrankungen des Ohres wird auf Knochenleitungshörsysteme zurückgegriffen. (Ein Extremfall wäre z.B. ein nicht vorhandener Gehörgang bei ansonsten normalem Aufbau des Gehöres.) Ein Knochenleitungshörgerät wandelt Schallsignale in Vibrationsschwingungen um. Der Hörer dieser Geräte überträgt diese Vibrationen auf den Knochen hinter dem Ohr (Mastoid). Über den Schädelknochen wird das gesamte Mittel- und Innenohr in Schwingung versetzt und der Schwerhörige kann diese Schwingungen als gehörte Informationen wahrnehmen. Üblicherweise werden Knochenleitungshörgeräte in 41 Verbindungsstück zwischen Hörgerät und Ohr, insbesondere zum Gehörgang. 64 Brillenbügeln eingebaut. Ferner gibt es die Möglichkeit ein Taschenhörgerät mit einem Knochenleitungshörer zu tragen, der an einem Kopfbügel oder Stirnband befestigt wird.“ 42 Meilensteine in der Entwicklung von Hörgeräten Schon vor vielen Jahrhunderten setzten Menschen Techniken zur Verbesserung ihres Hörvermögens ein. So beschrieb bereits im 2. Jahrhundert der griechische Arzt Galen von Pergamom ein System zur Hörverbesserung mit ausgehöhlten Tierhörnern. Berichte von Alexander von Tralles aus dem 6. Jahrhundert enthielten Informationen über den Einsatz von sogenannten Hörrohren bei überwiegend schwerhörigen Menschen um deren Hörfähigkeit zu steigern. Im 13. Jahrhundert experimentierten französische Mönche mit schallverstärkenden Tierhörnern. Der Jesuit Leurechon beschrieb 1624 unter dem Decknamen H. van Etten erstmals den Aufbau und die ungefähre Funktionsweise des Hörrohres. Erst 1650 gelang es dem Universalgelehrten und Jesuiten Athanasius Kircher in seinem Werk „Musurgia Universalis“ den exakten Aufbau sowie die Funktion des Hörrohres zu schildern. Daher gilt er als Erfinder des Hörrohres. Hörrohre gab es über viele Jahrhunderte lang in den verschiedensten Formen; sie ließen eine maximale Verstärkung von 8 dB zu. Abb. 52: Hörrohr Etwa 20 Jahre später um 1673 entwickelte Kircher die „Ellipsis Otica“, einen riesigen Hörapparat. Dieses Gerät wurde zwischen zwei Menschen aufgestellt, die an den jeweiligen Enden sprechen und „schallverstärkt“ hören konnten. 42 Quelle: http://de.wikipedia.org/wiki/H%C3%B6rger%C3%A4t 65 Abb. 53: Ellipsis Otica 1706 baute Duguet als Erster anstelle von Armlehnen überdimensionale Hörrohre, die den Schall verstärkt zu seinen Ohren führten, an seinen Fauteuil (Lehnsesssel). Im Jahr 1820 ließ sich Pastor Dunker eine Hörmaschine mit biegsamem Rohr patentieren. Im gleichen Jahr konstruierte W. B. Pine ein teleskopartiges Hörrohr, das zusammengeschoben werden konnte und dadurch in die Tasche passte. Bei Experimenten an Instrumenten für Hörgeschädigte erfand Alexander Graham Bell 1876 das Telefon, welches mit einem Mikrofon aus magnetisiertem Metall ausgestattet war. 1878 stellte David Edward Hughes seine Erfindung – das Kohlemikrofon -, die sich auf den Arbeiten von Edison und Berliner stützte, in der Königlichen Akademie zu London vor. Kohlemikrofone besaßen im Gegensatz zu bisherigen Mikrofonen eine verbesserte Schallübertragung, waren jedoch zur schwer um am Körper getragen werden zu können. Die Erfindung des Hörfächers – „Audiophon“ wird dem Jahr 1879 zugeschrieben. Dieses Instrument überträgt Schallschwingungen über Knochenleitungen, indem man den Fächer gegen die Zähne oder zwischen die Zähne hielt. Außerdem kam es in diesem Jahr zur Patentierung eines Hörstuhls mit gelenkigen beidseitig angebrachten Hörtrichtern. 66 Abb. 54: Hörstuhl von 1879 1892 entwickelte Alonzo E. Miltimore das erste elektrische Hörgerät (elektrisches Audiophon) und ließ es sich patentieren. Es wurde jedoch nie produziert. Abb. 55: elektrisches Hörgerät von Miltimore Vier Jahre später, 1896, baute der Engländer Bertram Thornton das erste Tischhörgerät mit einem Kohlemikrofon, einem magnetischen Hörer (Lautsprecher) und drei Batterien. Es war sehr unhandlich und sehr schwer. 67 Abb. 56: Tischhörgerät von Thornton 1899 produzierte das Unternehmen Acouphone Co. in Alabama, USA, das erste kommerzielle Tischhörgeräte „Akoulallion“. Mit Hilfe der Erfindung des Röhrenverstärkers im Jahr 1906 konnten elektrische Signale in einer bis dahin noch nie erreichten Klangqualität in allen Frequenzbereichen verstärkt werden. Aufgrund der enormen Größe der Röhren und Batterien wurden jedoch meist nur stationäre Hörgeräte gebaut. 1925 entwickelte die Firma Radio Ear ein etwa 84 kg leichtes Tischhörgerät mit Röhrenverstärker. Das wahrscheinlich erste tragbare Hörgerät mit Röhrenverstärker fertigte der Amerikaner Arthur Wengel im Jahre 1937. Die Entwicklung des ersten Hörgerätes mit Röhrenverstärker, welcher das aus nur einem einzigen Stück bestand, fand um 1945 statt. Durch die Entdeckung neuer Konstruktionsmöglichkeiten konnten zunehmend kleinere Bauteile hergestellt werden, die die Fertigung von tragbaren Röhrengeräten ermöglichten. Diese Hörgeräte bestanden aus drei Röhren, einem Kristallmikrofon und einem kristall- oder elektromagnetischen Lautsprecher. Außerdem mussten sie mit zwei großen, schweren und externen Batterien versorgt werden (1,5 V – 4,5 V für die Kathodenheizung und 22,5 V – 45 V für die Anoden). 68 Abb. 57: tragbares Hörgerät mit Röhrenverstärker Auch die Röhrentechnik wurde stetig verbessert, so dass man um 1947 nun auch kleinere und spannungsärmere Röhren produzieren konnte. Damit war es erstmals möglich leichtere und tragbare Hörgeräte zu bauen, in denen die Batterien direkt integriert waren. Im darauf folgenden Jahr erfanden William B. Shockley, John Bardeen und Walter Brattain den Germaniumtransistor, wodurch sich zahlreiche Vorteile, aber auch einige Nachteile für die Hörgeräteentwicklung ergaben: Vorteile von Transistoren benötigten kleinere Spannungen verbrauchten weniger Leistung waren kleiner Nachteile der Transistoren waren anfangs viel teurer als Röhren produzierten mehr Rauschen Die Folge dieser innovativen Technologie waren Hörgeräte mit Hybridfunktionen, bei denen die rauschempfindliche Eingangsstufe mit Röhren und die leistungshungrige Ausgangsstufe mit Transistoren realisiert wurden. Dadurch war die Konstruktion von immer kleineren und leichteren Hörgeräte möglich. In den Jahren nach der Erfindung des Transistors stieg die Massenproduktion dieser Bauteile an, weswegen sie im Laufe der Zeit immer billiger, aber zugleich auch durch verstärkte Forschungsarbeiten rauschärmer wurden. Demzufolge kamen im Jahr 1953 die ersten reinen Transistorhörgeräte auf den Markt, die nur noch eine Verstärkerspannung von 1,5 V benötigten. 69 1954 gab es neue Entwicklungen auf dem Gebiet der Schaltungs- und Lautsprechertechnik. Lautsprecher konnten nun zum Beispiel direkt in das Gerät integriert werden. Außerdem gelang es aufgrund der Miniaturisierung von Hörgeräten, sie in den Haaren zu verstecken oder in Brillen zu integrieren. 1956 kamen die ersten Hörgeräte die hinter dem Ohr getragen werden konnten (HdO = hinter dem Ohr) auf den Markt. Abb. 58: HdO-Hörgerät 1957 eroberten dann die ersten Hörgeräte die im Ohr getragen werden konnten (IdO = in dem Ohr) den Markt. Abb. 59: IdO-Hörgerät Bisherige verfügbare Mikrofone galten als relativ empfindlich gegenüber Vibrationen und begrenzten die Verstärkungsfaktoren wegen der Rückkopplungen durch die Schädelknochen. Erst die Erfindung des Kondensatormikrofons um 1973, dass gegen Vibrationen unempfindlich ist, ließ Verstärkungen bei HdO-Geräten von 70 – 80 dB zu. 70 In den 80er Jahren setzte sich der Trend zur Miniaturisierung von Hörgeräten weiter fort. Mikrofone und Lautsprecher wurden immer kleiner und leistungsfähiger und durch die Zunahme von Erfahrung und Wissen über die Ursachen von Hörbeeinträchtigungen, konnten Hörgeräte hergestellt werden, die auf die speziellen Anforderungen eines jeden Hörgeschädigten eingingen. Durch die Steigerung der Bauteildichte auf dem IC um 1988 war es möglich, Controller von beachtlicher Leistungsfähigkeit zu integrieren, was Einfluss auf die Entwicklung der ersten digital gesteuerten Hörgeräte hatte. Die Entwicklung von Hörgeräten mit digitaler Signalverarbeitung, schritt aufgrund immer kleinerer und leistungsfähigerer Signalprozessoren 1996 soweit voran, dass man in diesem Jahr die ersten 100% digitalen HdO- und IdO-Geräte bauen konnte. 1997 wurde das erste voll digitale CIC-Gerät (Complete in Canal) entwickelt, das vollständig im Gehörgang verschwindet. Heute: Moderne Hörgeräte sind prinzipiell in die in der Einleitung beschriebenen Grundtypen zu unterteilen. Je nach Ohrerkrankung, Budget und Vorlieben des Patienten kommt eine dieser Bauarten zur Anwendung. Der Gebrauch von digitalen Hörgeräten beim Patienten nimmt nur langsam zu, da hochwertige digitale Geräte oftmals sehr teuer und mit einem hohen finanziellen Eigenanteil verbunden sind. Abb. 60: links: IdO-Hörgerät; rechts: HdO-Hörgerät Prognose: Zukünftig benutzen Patienten nur noch digitale Hörgeräte aufgrund ihrer enormen Vorteile gegenüber den Analoggeräten. Außerdem findet eine stetige Verbesserung der Hörgerätetechnologie statt, so dass z.B. Mikrofone ohne Eigenrauschen gebaut werden können. Zudem werden neue Vernetzungsmöglichkeiten von audiologischen Geräten mit Hörgeräten geschaffen. Der Höhepunkt in der Entwicklung von Hörgeräten wird die künstliche Wiederherstellung des Originalhöreindrucks sein, der u.a. mit fähigeren Softwarealgorithmen realisiert werden kann. 2.1.11 Brillen – Augengläser Das Auge ist eines der wichtigsten Sinnesorgane des Menschen. Schon frühzeitig versuchte der Mensch Fehlsichtigkeiten und das nachlassende Sehvermögen im Alter auszugleichen. Die Brille gehört dabei zu den großen Entdeckungen des Mittelalters und ist seit ihrer 71 Erfindung das wohl am häufigsten benutzte optische Instrument. Dennoch ist das Verhältnis des Menschen zur Brille von jeher recht zwiespältig. Einerseits geliebt und vergöttert, macht sie andererseits auf einen Mangel aufmerksam, den man nur ungern zu erkennen gibt. So wird die Brille zum Symbol für Weisheit und Klugheit, Eitelkeit und Dummheit sowie zum Statussymbol und unerlässlichen Modeattribut. Die moderne Brille ist zu einen Teil unseres heutigen Alltags geworden und gerade aufgrund ihrer selbstverständlichen Verfügbarkeit für jeden Menschen, ist ihre lange Geschichte weitestgehend in Vergessenheit geraten. Denn was uns heute manchmal als lästig erscheint und mittlerweile durch Kontaktlinsen oder auch Laseroperationen ersetzt wird, war ein großer kultureller Fortschritt, der insbesondere in der Anfangszeit erheblicher handwerklicher Fähigkeiten in der Herstellung bedurfte. Letztendlich ist die Erfindung der Brille ein Segen für die gesamte Menschheit. Meilensteine in der Entwicklung von Brillen Um 1000 nach Christus veröffentlichte der arabische Mathematiker und Astronom Ibn el Heitam sein Werk „Schatz der Optik“. Dort beschrieb er unter anderem die vergrößernde Wirkung von gläsernen Kugelsegmenten. Etwa 240 Jahre später übersetzte Erazam Golek Vitello den „Schatz der Optik“ ins Lateinische, woraufhin sich das Werk schnell in den Klöstern und bei weltlichen Gelehrten verbreitete. So begannen Mönche des Franziskanerordens mit der praktischen Umsetzung der von Heitam beschriebenen Glaskugel. Sie fertigten erste Lesesteine aus Quarz, Bergkristall oder Beryll 43 an. Der Lesestein ist eine halbkugelförmige, konvexe Linse mit einer glatten Grundfläche, die auf ein Schriftstück zur zeilenweisen Vergrößerung der Buchstaben gelegt werden kann. Abb. 61: Nachbildung eines Lesesteins aus Beryll In den nachfolgenden Jahrhunderten kam es immer wieder zu zahlreichen Neuerungen auf dem Gebiet der Brillenentwicklung. So veränderte sich im 13. Jahrhundert die Herstellung der Lesesteine. Sie wurden kleiner und flacher um sie näher an das menschliche Auge bringen zu können, wodurch ein größeres Gesichtsfeld entstand. Später kam man dann auf die Idee, zwei Linsen zur besseren Handhabung zu nutzen und sie zu ihrem eigenen Schutz jeweils mit einer Fassung zu versehen, die durch einen Niet gelenkartig miteinander verbunden wurden. Diese Konstruktion erhielt den Namen "Nietbrille“. Nietbrillen bestanden entweder aus Metall, Holz oder Tierhorn und besaßen noch keinerlei Befestigungen für den Kopf, so dass 43 Halbedelstein, von dem aus ihm geschliffenen Linsen sich unser heutiges Wort „Brille“ ableitet. 72 sie zur Benutzung einfach vor die Augen gehalten werden mussten. Anklang fand die Nietbrille hauptsächlich bei Gelehrten, Philosophen und Ärzten. In diesem Jahrhundert gab es aber noch viele weitere Entdeckungen. So fand beispielsweise der Franziskanermönch Roger Bacon aus dem englischen Oxford um 1267 bei Forschungsarbeiten mit Linsen heraus, dass sich mit besonders geschliffenem weißem Glas 44 kleine Buchstaben sehr gut vergrößern lassen. Des Weiteren tauchten um 1300 die ersten Brillen für weitsichtige Menschen in Europa auf; vermutlich wurden sie 1280 in einem Kloster in Oberitalien erfunden. Abb. 62: Nachbildung einer Nietbrille um 1350 Im 14. Jahrhundert begann man mit der Herstellung von Brillenrahmen aus Metall, Holz, Leder, Knochen und Tierhorn, die die beiden eingefassten Linsen durch einen Bügel miteinander verbunden. Diese neue Brillenart – die „Bügelbrille“ – zeichnete sich durch eine verbesserte Stabilität aus. Die geschickte Weiterentwicklung der Bügelbrille zur Schlitzbügelbrille (Anbringung eines eingeschlitzten Lederstückes am Bügel selbst) ermöglichte es, sie auf die Nasenwurzel zu setzen, wodurch der Lesende beide Hände für andere Aktivitäten frei zur Verfügung hatte. Zusätzlich sicherte man sie durch eine um den Hals befestigte Kette vor dem Herunterfallen. Aber auch die Weiterentwicklung des Lesesteins wurde unermüdlich vorangetrieben. Mit der Einfassung von kleinen und flachen Linsen in einen Rahmen mit Stiel zum Festhalten entstanden so die ersten Monokel. 44 Weißes Glas wurde zur damaligen Zeit in den Glashütten von Murano (venezianische Insel) hergestellt. Daher gilt Murano auch als Geburtsort der Brille. 73 Abb. 63: Schlitzbügelbrille Bisher war es nur möglich bikonvexe Sehhilfen zur Kompensation der Alterssichtigkeit herzustellen. Dies sollte sich jedoch im 15. Jahrhundert ändern. Von nun an konnten zwei Arten korrigierender Gläser fabriziert werden, nämlich bikonvexe Sammellinsen und bikonkave Zerstreuungslinsen. Außerdem griff man bei der Produktion von Brillengläsern jetzt auf nur noch weißes Kristallglas zurück. In dieser Zeit entstand auch eine neue Brillenart, die „Mützenbrille“. Sie war eine einfache metallische Konstruktion, deren die Brillengläser an einer Mütze befestigt wurden und somit von oben herab über den Augen hing. Ihr großer Vorteil war, dass sie nicht Herunterfallen konnte und auch keine Bügelabdrücke auf der Nase hinterließ. Die Mützenbrille oder auch Stirnfortsatzbrille genannt, fand bis in das 18. Jahrhundert Einsatz und wurde meist von Menschen höherer Stände getragen, die den Hut zur Begrüßung nicht ständig lupfen mussten, da diese Brille dabei störend gewesen wäre. Abb. 64: Mützenbrille Wie schon in den Jahrhunderten zuvor entstanden auch im 16. Jahrhundert viele neuartige Brillentypen. So war es üblich, Monokel ohne Stiel zum Festhalten zwischen Wange und Oberlied einzuklemmen, damit die Hände für andere Sachen frei waren. Eine weitere Entwicklung in diesem Jahrhundert war die „Stirnreifenbrille“. Sie bestand aus einem um die Stirn gelegten Metallreifen, von dem die Gläser herabhingen. 74 Die Verbesserung der Nietbrille führte zu einer neuen Brillenart, der „Gelenkbrille“. Dort ersetzte ein Scharniergelenk die starre Verbindung zwischen den bisherigen Brillengläsereinfassungen. Abb. 65: Stirnreifenbrille Beim, Zwicker einer anderen Neuerung des 16. Jahrhunderts, wurden anfänglich beide Glaseinfassungen mit einem Federbügel aus Eisen oder Kupfer verbunden. Um Druckstellen auf der Nase zu minimieren, versah man die Glaseinfassungen später mit einem leicht austauschbaren Lederpolster. Der Zwicker kam bis in das 19. Jahrhundert zum Einsatz. Abb. 66: Zwicker um 1900 Gegen Ende des dieses Jahrhunderts wurden Brillen mittels eines Fadens an den Ohren befestigt – „die Fadenbrille“. Wahrscheinlich hat die Fadenbrille ihren Ursprung in Spanien und gelang von dort aus nach Asien, wo sie teilweise auch heute noch verwendet wird. Im 17. Jahrhundert sollte die „Nürnberger Drahtbrille“ zum erfolgreichsten Brillenmodell der damaligen Zeit werden. Sie bestand aus einer einfachen Drahteinfassung ohne Bügel, in der die Gläser eingesetzt waren. Die Nürnberger Drahtbrille verkaufte sich bis ins 19. Jahrhundert erfolgreich als Massenprodukt. 75 Abb. 67: Nürnberger Drahtbrille des 18. Jahrhunderts Der Pariser Optiker Thomin fertigte 1746 erstmals ein Brillengestell mit zwei seitlich angebrachten Bügeln zur Fixierung der Brille über den Ohren, an. Diese Brille bekam den Namen „Schläfenbrille“. Abb. 68: Schläfenbrille des 18./19. Jahrhunderts Einige Jahre später, etwa 1752 kam ein Londoner Optiker auf die Idee die Seitenbügel der Schläfenbrille zu verlängern und sie mit einem Gelenk auszustatten, so dass die Brille hinter den Ohren fixiert werden konnte. Die sogenannte „Ohrenbrille“ verbesserte durch die neue Bügelkonstruktion ihren Halt erheblich, konnte sich aber nicht sofort durchsetzen, da die Nürnberger Drahtbrille den Markt in Deutschland eine lange Zeit beherrschte. 76 Abb. 69: Ohrenbrille um 1800 Im Jahr 1784 fertigte Benjamin Franklin die erste Zweistärkenbrille. Sie bestand aus zwei halben Linsen unterschiedlicher Stärke, wodurch es dem Träger möglicht wurde, sowohl nahe als auch entfernte Gegenstände mit nur einer einzigen Brille zu erkennen. Das „Lorgnon“ hielt im 18. Jahrhundert (genaue Daten sind nicht bekannt) Einzug in den deutschsprachigen Raum und erreichte Anfang des 19. Jahrhunderts Frankreich. Seinen Ursprung fand es als umgekehrt gehaltene Nietbrille. Eine wesentliche technische Erneuerung stellte das zusammenklappbare Lorgnon dar, das bei Bedarf mittels einer Feder geöffnet werden konnte. Abb. 70: Lorgnon Mit der Gründung der Brillenmanufaktur im Jahr 1801 im brandenburgischen Rathenow durch J. H. A. Duncker, entwickelte sich Rathenow bis in die Hälfte des 20. Jahrhunderts zu der führenden deutschen Produktionsstätte für Brillen. 1825 ließ sich der französische Arzt Joseph Bressyein eine neue Brillenform patentieren, den „Klemmer“. Dabei handelte es sich um eine Fassung mit stählerner Feder, die in horizontaler Ebene wirkte. Erst 15 Jahre nach seiner Erfindung fand er von Frankreich und England aus eine zunehmende Verbreitung. 77 Zwei Jahre später, 1827, gelang Hawkins die Herstellung von Zweistärkenbrillen / Bifokalgläser aus nur einem einzigen Stück Glas. Moussier und Boulland entwickelten eine Form des Mehrstärkenglases im Jahre 1852, das in ähnlicher Art und Weise bis zum heutigen Tag zur Herstellung von Mehrstärkengläser angewandt wird. Dabei kitteten sie eine kleine Zusatzlinse aus fertigem Brillenglas auf die eigentliche Brille. Erfindung des Nasenhalters durch der Pariser Optiker Poulot um 1857. Zur Standardisierung der Einheit für die Brechkraft optischer Linsen wurde 1875 der Begriff „Dioptrie“ eingeführt. Er definiert die Brechkraft einer Linse, deren Brennweiter einen Meter beträgt. Adolf E. Fick erfindet 1877 die erste Kontaktlinse. 1883 legte der Reichskanzler Otto von Bismarck mit der Einführung der Sozialgesetze auch den Grundstein für die ersten „Kassenbrillen“. Im 20. Jahrhundert konnte durch die Herstellung neuer Werkstoffe die Qualität der Brillen weiter gesteigert werden. Deutschland war zu Beginn des Jahrhunderts weltweit das bedeutendste Produktionsland für Brillen. In den 20er Jahren erhielt die Brille ihr gegenwärtiges Aussehen und ihr anatomisches Design. Die Brillenhersteller „Zeiss und Busch“ sowie „Nitsche und Günther“ hatten dabei großen Einfluss, unter anderem durch die Entwicklung neuer Brillen und innovativer Fassungen. In den 40er Jahren revolutionierten Kunststoffe die Fassungsindustrie und Kunststoffgläser minimierten das Brillengewicht. In den 80er Jahren hielt das Leichtmetall Titan Einzug in die Brillenindustrie, so dass Brillen unter 15 Gramm keine Seltenheit mehr waren. Die Gründung der ersten FielmannNiederlassung in Cuxhaven fand 1972 statt. Günther Fielmann löste als Erster das zeitlose hässliche Einheitsmuster der Kassenbrillen durch modische Vielfalt ab. Aber auch die Weiterentwicklung der Kontaktlinsen wurde ständig vorangetrieben. Heute: Durch die Verwendung von Leichtmetallen können Brillenrahmen immer unauffälliger und dezenter gestaltet werden, so dass sie teilweise ganz verschwinden. Außerdem ermöglichen moderne Kunststoffgläser eine Herstellung von sehr leichten Gläsern, unabhängig von deren Stärke. Brillen sind heutzutage weit mehr als nur Instrumente zur Verbesserung der Sehkraft. Für einige Menschen sind sie zusätzlich Modeartikel, andere wiederum bevorzugen eher unsichtbare Kontaktlinsen zur Sehkraftverbesserung. Es kommen aber auch Brillen, die im eigentlichen Sinne gar keine Sehhilfen mehr sind zum Einsatz. Darunter fallen 3D Brillen, die für verschiedenste Computeranwendungen gebraucht werden, wie z.B. Virtual Reality-Spiele, 3D Simulationen oder Augmented Reality. Abb. 71: moderne Brille von heute 78 Prognose: Zukünftig wird die Entwicklung von Brillengläsern mit hoher Brechzahl bei einer möglichst geringen Dispersion (Streuung) mit gleichzeitiger Gewährleistung einer guten Härte und einer chemischen Beständigkeit forciert. Außerdem werden Brillen viel mehr Funktionen als nur die reine Sehkraftverstärkung aufweisen. Sie dienen dann unter anderem als moderne Ein- und Ausgabeschnittstellen mit Eye-Tracking zur Steuerung von am Körper getragenen Geräten oder Geräten in näherer Umgebung (Smart Home, Smart Car etc.). 2.1.12 Prothesen „Eine Prothese (griechisch: protithenai - voransetzen) bezeichnet in der Medizin den Ersatz von Gliedmaßen, Organen oder Organteilen durch künstlich geschaffene, funktionell ähnliche Produkte. Befindet sich die Prothese außerhalb des Körpers, spricht man von einer Exoprothese (wie z. B. bei künstlichen Gliedmaßen, Arm-, Bein-, oder Handprothese), andernfalls von einer Endoprothese oder einem Implantat. Künstliche Hüftgelenke sind beispielsweise klassische Endoprothesen, gelten aber auch als ein Implantat. Das Besondere an diesem Implantattyp ist, dass es ein geschlossenes Implantat ist und vollständig von Körpergewebe umgeben ist (daher auch die Bezeichnung "Endo-). Es gibt auch Prothesen, die sind zu einem Teil im Körpergewebe und ragen zu einem anderen Teile aus dem Körpergewebe heraus, die sogenannten offenen Implantate. Bekanntestes Beispiel ist das Zahnimplantat. Daneben gibt es offene Implantate, auf denen keine herausnehmbaren oder festsitzenden künstlichen Zähne gesetzt werden, sondern Ohrmuschelimitationen, wenn das Implantat im Ohrbereich im Schädelknochen steckt. Das gleiche gilt für Implantate, die im Gesichtsschädel stecken und an denen zum Beispiel Nasen- oder Augen-Prothesen, Epithesen, befestigt sind. Während mit den ersten Prothesen kaum Funktionen des ursprünglichen Organs oder Körperteils hinreichend ersetzt wurden (man denke an Glasaugen), ermöglichen heute mikroprozessorgesteuerte Arm- oder Bein-Prothesen komplexere Bewegungen und sportliche Betätigung. Meist besteht die Außenhaut heutiger Prothesen aus Silikon, welches robuster ist und der Haut mehr ähnelt als andere Stoffe wie Holz oder Leder-Stahlprothesen. Bei Beinprothesen wird auch häufig eine Kosmetik aus in Form des Körperteils geschliffenem Schaumstoff mit übergezogenem Kosmetikstrumpf verwendet. Derzeit wird daran geforscht, mittels „tissue engineering“ wie zum Beispiel Herzklappen zu züchten.“ 46 45 aus eigenem Gewebe Ersatzteile Meilensteine in der Entwicklung der Prothesen Erste schriftliche Überlieferungen von einer künstlichen Gliedmaße durch Herodotus aus dem Jahre 500 v. Chr. berichteten von einem Gefangenen, der seinen abgeschnittenen Fuß durch ein hölzernes Gegenstück ersetzte. 45 Die Methode des Tissue Engineering - Gewebezüchtung - in Bezug auf die regenerative Medizin beruht darauf, lebende Zellen eines Organismus außerhalb des Zielgewebes zu kultivieren, um diese dann in den meist selben Organismus zu implantieren und so eine Gewebefunktion zu erhalten oder wiederherzustellen. 46 Quelle: http://de.wikipedia.org/wiki/Prothese 79 Der Ritter Götz von Berlichingen ließ sich um 1504 eine Prothese für seine im Krieg verlorene Hand anfertigen. Die Steuerung und Fixierung der Finger erfolgte bei Knopfdruck über verschiedene integrierte Zahnräder. Abb. 72: die Hand des Götz von Berlichingen Eine sehr einfache Art der Prothese nutzte 1517 der Pirat Barbarossa Horuk. Er ersetzte seine verlorene Hand durch einen einfachen Eisenhaken, der selbst nicht bewegt werden konnte. 1529 führte der französische Chirurg Ambroise Parè die Amputation als lebensrettende Maßnahme in der Medizin ein. Dadurch beschäftigten sich von nun an immer mehr Forscher und Mediziner mit der professionellen Herstellung von künstlichen Gliedmaßen (Arme, Hände, Beine und Füße) und trieben somit die Entwicklung der Prothetik entscheidend voran. Abb. 73: Beinprothese nach Parè 80 Der holländische Chirurg Pieter Andriannszoon Verduyn konstruierte 1696 die erste „nonlocking“ Wadenbeinprothese. Abb. 74: Verduyns Wadenbeinprothese Eine der bekanntesten Prothesen aus dem 19. Jahrhundert war die um 1800 vom Londoner James Pott erschaffene Beinprothese mit dem Namen „Anglesey Leg“. Sie bestand aus einem hölzernen Schaft sowie einer hölzernen Einfassung, einer Stahlknieverbindung und einem beweglichen Fuß, der mittels Sehnen zwischen Knie und Fußgelenk gesteuert werden konnte. Abb. 75: „Anglesey Leg“ 81 Bisher waren fast nur starre Hand- und Armprothesen verbreitet, die immer mit der gesunden Hand bewegt werden mussten. Dies änderte sich jedoch mit der Idee von Peter Baliff. Er baute im Jahr 1812 die erste willkürlich bewegbare Handprothese, die durch die noch verbleibende Muskelkraft des Armstumpfes nach einer Amputation gesteuert werden konnte. Finger wurden über gespannte Seilzüge, Riemen und einer starken Feder durch kräftige Ellenbogen- und Schulterbewegungen bewegt. Diese Technik war für den Prothesenträger jedoch sehr kompliziert und anstrengend. Im Jahr 1856 verbesserte A. A. Marks das „Anglesey Leg“ und gab seiner Variante den Namen „American Leg“. Seine Prothese ermöglichte eine willkürliche Bewegung einzelner Prothesenelemente, wie dem Knie, dem Knöchel und den Zehen. 1890 setzte Themistokles Glück in Berlin die ersten künstlichen Kniegelenke ein (Endoprothetik). Die Prothese bestand aus den zwei Komponenten Elfenbein und Nickelstahl. Die englischen Geschwister Marcel und Charles Desoutter konstruierten um 1912 die erste Aluminiumprothese. Außerdem entwickelten sie u.a. eine direkte Kontrolle des Knies sowie die Kniebremse. Ferdinand Sauerbruch revolutionierte 1916 durch die Nutzung der Kraft der Bizepsmuskulatur die Prothesentechnik. Er legte durch den Oberarmmuskel des Patienten einen kleinen Hauttunnel, durch den ein Elfenbeinstift als Überträger der Bewegung des Oberarmmuskels an die Prothese geschoben wurde. Durch Anspannung des Muskels, hob sich der Stift an und löste Finger- und Handbewegungen aus. Abb. 76: Sauerbruch-Armprothese Etwa Mitte des 20. Jahrhunderts 1943 entwickelte Austin Moore die nach ihm benannte Hüftkopfprothese mit gefenstertem Schaft. Hierbei wurde jedoch nur der Hüftkopf ersetzt, 82 was dazu führte, dass die Prothese langsam durch den Beckenknochen hindurch penetrierte. Deshalb musste eine neue Prothesentechnik erfunden werden, bei der sowohl der Hüftkopf als auch die Hüftpfanne ersetzt werden. Abb. 77: Aufbau einer künstlichen Hüftprothese Der hohe Materialverschleiß bei Prothesen führte zum Einsatz ständig neuer Materialen. So verwendeten 1946 die Gebrüder Judet für den Hüftkopf einer Hüftprothese beispielsweise Plexiglas. Doch das Plexiglas stellte sich als ungünstiges Material für Prothesen heraus und wurde deshalb in Folge aufgegeben. Zwei Jahre darauf, 1948, wurden die ersten Fremdkraftprothesen 47 mit Elektromotoren oder Gasdrucksystemen entwickelt. Bei den Elektromotorsystemen bewegten Elektromotoren einzelne Finger und ermöglichten einen einfachen Zangengriff. Eine der bekanntesten Prothesen mit Gasdruck war die des Heidelberger Ingenieurs Otto Häfner und arbeitete mit Kohlendioxid. Ihr großer Vorteil war der feste Zangengriff. Als nachteilig stellte sich die ständige Bereitstellung einer Gasdruckflasche heraus, durch diese die Nutzungsdauer der Prothese stark eingeschränkt wurde. 47 Fremdkraftprothesen nutzen die elektronischen Potentiale der verbliebenden Muskulatur des Stumpfes. 83 Abb. 78: Fremdkraftprothese Die Implantation der ersten brauchbaren Hüfttotalprothese durch G. K. McKee erfolgte im Jahr 1951. Anfangs bestand sie aus rostfreiem Stahl, später aus einer Chrom-KobaltLegierung. Die künstliche Gelenkpfanne wurde mit einem Metallstiftchen im Beckenknochen verankert 1956 meldete van Steenbrugghe das erste Patent für eine funktionserhaltende Bandscheibenprothese an. Darauffolgende Bandscheibenprothesen bestanden aus Materialen wie Stahl, Silikon oder Polyurethan. Diese Behandlungsmethoden wurden jedoch aufgrund mäßiger Ergebnisse schon bald wieder eingestellt. Noch im selben Jahr konstruierten Forscher der Universität von Kalifornien den SACH-Fuß, ein prothetischer Fuß ohne Gelenk. Abb. 79: Sach-Fuß; Version für Damen Sir John Charnley entwickelte 1959 die Urform aller modernen Hüftprothesen mit einem Hüftkopf aus Metall und einer Gelenkpfanne aus Teflon. Wegen der unpassenden Eigenschaften von Teflon wurde es allerdings bald durch Polyethylen ersetzt. Diese Art der Technologie hat sich bis heute durchgesetzt. Heute: Sämtliche Prothesen werden individuell angepasst, um eine optimale Kraftübertragung vom Gewebe zur Prothese zu ermöglichen. Auch der Gebrauch von mikroprozessorgesteuerten Prothesen für spezielle Anwendungen, wie zum Beispiel bei sportlichen Aktivitäten ist heutzutage üblich. Die Prothesen bestehen aus Silikon, Metall (Stahl- und Titanlegierungen), Kunststoff und Keramik. Des Weiteren kommen immer 84 häufiger neuartige Prothesen zum Einsatz, bei denen Luft oder eine Flüssigkeit die schweren Elektromotoren ersetzt. Prognose: Die Funktionalität einer Prothese wird der Funktionalität einer gesunden Gliedmaße gleichen. Es werden Prothesen entwickelt, die das Fühlen (Haptik) wieder ermöglichen und/oder unsere Sinne erweitern, wie zum Beispiel Hörprothesen, die die menschliche Lautstärkewahrnehmung in großem Maße verstärken. Zukünftige Forschungen und Schöpfungen im Bereich der Medizin könnten sogar so weit führen, dass verlorene Gliedmaßen komplett regeneriert werden und somit Prothesen überflüssig machen. 2.2. Zum Stand der Technik Auf Grundlage moderner Forschungen und Entwicklungen auf dem Gebiet der medizinischen Wearable-Technologie wurden bereits zahlreiche Produkte entwickelt. In diesem Abschnitt werden nun einige dieser Produkte näher vorgestellt und erläutert. 2.2.1 SensaTex Smart Shirt Einleitung Das Smart Shirt Projekt, finanziert von der U.S. Navy, startete 1996 an der “School of Textile and Fiber Engineering“ am Georgia Institute of Technology (Atlanta/Georgia). Ziel dieses Projektes war die Entwicklung eines intelligenten Kleidungsstücks, das Soldaten bei einem Militäreinsatz per Satellitennetzwerk exakt lokalisieren sowie deren Gesundheitszustand bestimmen kann. Zur Umsetzung dieser Idee mussten neben den herkömmlichen Materialen, wie Baumwolle und Polyester, Glasfaserfäden und andere elektrischen Leiter sowie verkleinerte Computerchips und Sensoren in Kleidungsstücke integriert werden. Schon nach kurzer Zeit erkannten auch zivile Unternehmen die enormen Vorteile dieser neuartigen Technik und begannen sich schnell dafür zu interessieren. Sie sahen im Smart Shirt ein Monitoring-System, dass beispielsweise Kleinkinder vor dem plötzlichen Kindstod schützen sollte oder gesundheitsgefährdete Menschen in lebensbedrohlichen Situationen. Die SensaTex Incorporation 48 ist ein Textilunternehmen, das auf die Entwicklung von Smart Shirt Systemen ausgerichtet ist. Ihr erstes kommerzielles Produkt ist das SensaTex Smart Shirt. 48 http://www.sensatex.com/ 85 Abb. 80: erster Prototyp eines Smart Shits Aufbau Das Smart Shirt besteht heute je nach Einsatzgebiet aus verschiedensten und voneinander unabhängigen Komponenten, die zum Teil denen eines Computer-Motherboards ähneln. Das ist auch der Grund dafür, dass der Erfinder des Smart Shirts sein Kleidungsstück „Gerogia Tech Wearable Motherboard“ nannte. Aus kommerziellen Vermarktungsgründen entschied man sich jedoch nur für den Namen „Smart Shirt“. Mögliche Komponenten des Smart Shirts sind: das textile Grundgerüst, ein Mikrofon, verschiedene Sensoren (z.B. für Temperaturmessung und Herzschlaganalyse), ein Datenbus (elektrisch leitende Fasern), optische Fasern und ein Multifunktionsprozessor für die Datenverarbeitung/-übertragung (WLAN, Bluetooth). 86 Abb. 81: Aufbau und Grundkomponenten eines Smart Shirts Funktionsweise Das SensaTex Smart Shirt kann jederzeit wie gewöhnliche Alltagskleidung getragen werden. Eingebettete Sensoren überwachen dabei die Herzrate, die Atmung und andere Vitalfunktionen des Trägers. Die dadurch gesammelten Daten werden kontinuierlich via Satellit oder Mobilfunk vom Multifunktionsprozessor des Smart Shirts zum SensaTex Health Center übertragen, in welchem eine ständige Überwachung und Analyse der eingehenden Daten stattfindet. Beim Auffinden von gesundheitsgefährdeten Auffälligkeiten wird sofort ein medizinischer Notfalldienst alarmiert. Die Rettungssanitäter, die vom Health Center sowohl das Krankheitsbild als auch den Standort des Patienten erhalten, wissen dadurch schon vor ihrem Eintreffen beim Patienten über dessen körperliche Verfassung bescheid und können dementsprechend medizinische Hilfemaßnahmen einleiten. Außerdem werden alle aufgezeichneten Vitalfunktionsdaten der Träger eines Smart Shirts auf einer sicheren Internetseite abgelegt, so dass sich jeder Träger dort jederzeit und überall einloggen kann, um den Verlauf seiner Vitalfunktionen zu verfolgen. Anwendungsbereiche Im Gegensatz zu vielen anderen Hilfsmitteln aus dem Bereich des Wearable Computing, zeichnet sich das SensaTex Smart Shirt durch sein unauffälliges Aussehen ohne zusätzlich angebrachte umständliche Apparaturen aus. Das ermöglicht jedem Träger eine selbstverständliche Bewegungsfreiheit und einen uneingeschränkten Handlungsspielraum. Zusätzlich kann es wie jedes andere Kleidungsstück auch gewaschen werden. Gerade aufgrund dieser überaus vorteilhaften Eigenschaften findet das Smart Shirt in vielen Bereichen Anwendung, wie zum Beispiel: 87 im Gesundheits- und Pflegebereich (Überwachung der Vitalfunktionen bei Kranken, Kindern und Schwangeren), beim Sport (Überwachung der Körperfunktionen, Optimierung des Trainings), bei Militär und Polizei (Überwachung der Vitalfunktionen, Meldung über Verletzungen etc.) und bei Feuerwehreinsätzen (Giftstoffalarm durch Sensoren, Ortung etc.). 2.2.2 Bluetooth - EKG-T-Shirt Einleitung Das EKG-T-Shirt ist eine gemeinschaftliche Entwicklung der Firmen Vitaphone GmbH, GEO-VIEW und FALKE AKG. Bei diesem Produkt handelt es sich um eine ShirtMobiltelefon-Kombination, das Freizeit- und Profisportlern sowie kranken Menschen ein gezieltes Herz-Kreislauf-Monitoring unter ärztlicher Aufsicht ermöglicht. Zudem sind die mit dem EKG-T-Shirt erhobenen Daten wesentlich aussagekräftiger als die der herkömmlichen Pulsuhren. Aufbau Das EKG-T-Shirt setzt sich aus 2 Grundkomponenten mit je einer Bluetooth-Schnittstelle zusammen. Die Grundkomponenten sind das FALKE EKG-T-Shirt und das GPSMobiltelefon „Vitaphone 1300“. „Das Vitaphone 1300 unterscheidet sich von herkömmlichen Mobiltelefonen nur durch die Notfall- bzw. Service-Taste. Ansonsten sieht man dem Gerät sein High-Tech Potential nicht an. Bluetooth, GPS, 2 MB Memory und ein sehr leistungsfähiger Akku sind nur ein paar Merkmale des hochwertigen Innenlebens dieses Mobiltelefons. Das EKG-T-Shirt wurde in enger Kooperation mit der Falke KG, - die seit Jahren erfolgreich mit hochwertiger, funktioneller Sportunterwäsche auf dem Markt ist - , entwickelt und baut auf den technologischen Entwicklungen der Vitaphone GmbH auf. Das Gerät, ausgestattet mit einer High-Tech-Folie, misst die Herzfrequenz mit Hilfe von zwei Sensoren über die das EKG abgeleitet wird. Lästige Kabel und Klebeelektroden sind nicht erforderlich. In Verbindung mit einer atmungsaktiven Faser bietet das EKG-Shirt dem Anwender höchsten Tragekomfort. Das Shirt ist atmungsaktiv und garantiert eine schnelle Rücktrocknung bei Belastungen. Das eingearbeitete EKG-Modul kann zum Waschen einfach entfernt werden.“ 49 49 Quelle: http://www.presseportal.de/story.htx?nr=523675&firmaid=28852 88 Abb. 82: EKG-Modul Funktionsweise Während der Nutzung des EKG-T-Shirts wird über das EKG-Modul ein Ein-Kanal-EKG erhoben. Die dadurch aufgezeichneten EKG-Daten werden unmittelbar per Funk über eine Bluetooth-Verbindung zum „Vitaphone 1300“ übertragen. Dort können die Daten entweder gespeichert oder sofort automatisch an das medizinische Service Center zur Auswertung weitergeleitet werden. Umgekehrt kann auch das Service Center automatisch die neusten EKG-Daten innerhalb individuell vereinbarter Zeitpunkte zur Auswertung abrufen. Zusätzlich dazu kann ebenfalls durch manuelles Drücken der Notfall- oder Servicetaste am Mobiltelefon eine sekundenschnelle Verbindung zum medizinischen Service Center aufgebaut werden. Das Service Center ist nun in der Lage, den Mobiltelefonbenutzer mit einem Geoinformationssystem bis auf 15 Meter genau in ganz Europa zu orten und die Daten im Notfall an jede Rettungsleitstelle weiterzuleiten. Wertvolle und eventuell überlebenswichtige Zeit für die Rettung eines Verunglückten wird somit gewonnen. 89 Abb. 83: Kommunikationsablauf Anwendungsbereiche Mit Hilfe des EKG-T-Shirts ist jeder Sportler in der Lage sein Training individuell an die eigene körperliche Leistungsfähigkeit anzupassen. Dadurch wird die Belastungsgrenze frühzeitiger erkannt und deren Überschreitung vermieden. Aber auch im Bereich der Telemedizin zur medizinischen Überwachung des Herzkreislaufsystems ist das Bluetooth – EKG-T-Shirt einsetzbar. Durch die Direktverbindung des GPS-Mobiltelefons zum Vitaphone Service Center kann das Mobiltelefon neben seiner ursprünglichen Funktion auch für weitere Dienstleistungen benutzt werden. Denn aufgrund der genauen Positionsdaten kann der Mobiltelefonnutzer beim Service Center zahlreiche ortsbezogene Informationen abrufen. Ob Hotel, Tankstellen oder die nächstgelegene Apotheke, der Nutzer erhält rund um die Uhr fachkundige Informationen. 2.2.3 LifeVest Wearable Defibrillator Einleitung Der LifeVest Wearable Cardioverter-Defibrillator, eine Entwicklung der LIFECOR Incorporation 50, ist eine neue Behandlungsmöglichkeit um herzkranke Patienten vor einem plötzlichen Herzstillstand zu schützen. Durch eine regelmäßige Überwachung der Herztätigkeit wird ihnen ein ständiger Schutz zuteil, der auch eine verbesserte Lebensqualität für den Patienten bedeutet. 50 http://www.lifecor.com/ 90 Der LifeVest-Defibrillator wird nicht wie ein ICD in den Körper implantiert, sondern außerhalb des Körpers getragen. Mit Hilfe spezieller Elektroden kontrolliert dieses Gerät permanent das Herz des Patienten, um lebensbedrohende anomale Herzrhythmen zu erkennen. Aufbau Die zwei Hauptbestandteile der LifeVest sind ein Kleidungsstück und ein Monitor. Das Kleidungsstück enthält integrierte Elektroden, um das Elektrokardiogramm des Patienten aufzunehmen und wird unter der normalen Alltagskleidung angelegt. Der Monitor, der zur Analyse des EKGs dient, kann um die Taille oder über die Schulter geschnallt werden. Abb. 84: Komponenten der LifeVest Funktionsweise Der Monitor überwacht das durch die Elektroden aufgenommene EKG des Patienten. Wenn er bei einem Patienten einen zu schnellen (ventricular tachycardia) oder einen schnelleren und unregelmäßigen Herzschlag (ventricular fibrillation) feststellt, löst das Gerät eine akustische Warnung in Form eines Pieptons aus. Mit diesem Alarm zeigt die LifeVest eine bevorstehende Elektroschocktherapie gegen den abnormalen Herzrhythmus an. Der Patient muss nun innerhalb eines vorgeschriebenen Zeitintervalls auf die Warnung reagieren, indem er zwei Knöpfe drückt. Dadurch wird die Behandlung abgebrochen, weil eine Defibrillation nur bei Verlust des Bewusstseins notwendig ist. Falls der Patient jedoch nicht auf das Piepen reagiert, warnt das System per Sprachausgabe den Patienten und alle umstehenden Personen erneut vor einem elektrischen Schock. Wenn die arrhythmischen Herztätigkeiten und die Bewusstlosigkeit des Patienten jetzt immer noch andauern, wird ein leitfähiges Gel durch Elektroden auf die Haut abgesondert, um sie für den Elektroschock vorzubereiten. Nach einer erfolgreichen Defibrillation, wenn der Herzschlag des Patienten wieder normal ist, stoppt der Alarm und das System kehrt in den Überwachungsmodus zurück. Die LifeVest kann bis zu fünf Behandlungsstromstöße liefern. 91 Um die aufgezeichneten Informationen der LifeVest dem behandelnden Arzt zukommen zu lassen, wird das System zur Datenübertragung an eine normale Telefonleitung angeschlossen. Die LifeVest überträgt die Daten zu einer sicheren und passwortgeschützten Datenbank innerhalb des LifeVest-Netzwerkes. Ärzte können so jederzeit über das Internet auf das LifeVest-Netzwerk zugreifen und Patientendaten, einschließlich EKG Aufzeichnungen, Geräuschdaten und andere Information über das Gerät selbst erhalten. Anwendungsbereiche Die Wearable LifeVest dient hauptsächlich zur Behandlung von Patienten mit einem mittelfristigen Risiko auf plötzlichen Herzstillstand. Bei lang- oder kurzfristigem Risiko werden häufig andere Lösungen, wie der ICD oder ein einfacher Krankenhausaufenthalt angewandt. Die LifeVest kann zum Beispiel als eine Art Überbrückung vor der Implantation eines ICDs oder einer Herztransplantation benutzt werden. Es wäre nämlich vorstellbar, dass Patienten aus den verschiedensten Gründen (z.B. zusätzliche gesundheitliche Probleme, Wartelisten) zur Zeit nicht operiert werden können, aber dennoch, dank der LifeVest, während dieser Übergangsphase vor tödlichen Herzstörungen geschützt sind. Potenzielle Gruppen, die aus der LifeVest Technologie einen Nutzen ziehen können sind demnach: Post-Myocardial-Infarkt (MI) Patienten mit Komplikationen, Herzchirurgiepatienten mit Komplikationen, Patienten, die auf der Wartelisten für Herztransplantationen stehen, Patienten mit fortgeschrittenem Herzversagen, Patienten, die einen ICD benötigen aber zur Zeit aus vielerlei Gründen nicht für chirurgische Eingriffe zugelassen sind, oder Patienten, die einen operativen Eingriff ablehnen und kein Implantat haben wollen. 3. Empirische Untersuchungen Die vorliegende Untersuchung wurde als schriftliche Befragung mit standardisiertem und strukturiertem Fragebogen konzipiert und durchgeführt. Standardisiert heißt, dass jeder befragten Person dieselben Fragen in derselben Formulierung und in derselben Reihenfolge gestellt werden. Durch diese Art der Erhebung ergeben sich zahlreiche Vorteile aber auch einige Nachteile. Gründe für die Anwendung standardisierter Erhebungsmethoden sind: Vergleichbarkeit von Antworten: Wenn alle Befragten die gleichen Fragen beantworten müssen, dann sind ihre möglicherweise unterschiedlichen Antworten auf die einheitlich formulierten Fragen zurückzuführen und nicht auf unterschiedlich formulierte Fragen. 92 Geringerer Intervieweffekt: Bei der Anwendung standardisierter Formulierungen in einem Interview hängen die Reaktionen der Befragten nicht so sehr von der Persönlichkeit der Interviewer ab, wie bei nicht standardisierten Fragen. Einsatzmöglichkeiten in großen Populationen: Die Erarbeitung eines strukturierten Erhebungsinstrumentes erfordert zwar einige Mühen und Zeit, ermöglicht aber dann den gleichartigen Einsatz bei sehr vielen Personen mit einem überschaubaren zeitlichen Aufwand. Nachteile standardisierter Erhebungen sind: Bedeutungsgehalt der Frage: Eine für alle Befragte gleich formulierte Frage hat für alle Befragten unter Umständen nicht immer den gleichen Bedeutungsinhalt. Unveränderbarkeit während der Untersuchung: Wenn die Frage für alle gleich sein muss, darf sie bei der Datenerhebung auch nicht mehr verändert werden, wenn man erkennt, dass sie wesentlich besser formuliert werden könnte. Denn sonst kann die Vergleichbarkeit nicht gewährleistet werden. Aus diesen Gründen ist gerade bei einem standardisierten Verfahren ein ausführlicher Pretest von größter Bedeutung. Entfremdete Interaktion: Eine standardisierte Befragung stellt immer eine soziale Interaktionssituation dar. Ein standardisierter Fragebogen wirkt jedoch aufgrund der Formulierungsnotwendigkeiten immer gesetzt und künstlich im Vergleich zu einem normalen Gespräch, wie beispielsweise bei einem Interview. Damit ist also immer eine gewisse Entfremdung zum Themenbereich verbunden. Eingrenzung auf Bewusstseinsoberfläche: Durch standardisierte Befragungen können vor allem die Themenbereiche erfragt werden, die nahe der Bewusstseinsoberfläche liegen oder mit einfachen Anreizen ins Bewusstsein gelangen. 3.1. Beschreibung der empirischen Untersuchung 3.1.1 Zielsetzung Die Untersuchung zielt darauf ab, die Akzeptanz von neuartigen medizinischen Technologien im Bereich des Wearable Computing aus Anwendersicht zu erfassen sowie deren Risiken und Chancen für die Zukunft abzuschätzen. Dabei sollen spezielle Befragungen, die mittels eines extra dafür entworfenen Fragebogens durchgeführt werden, helfen. Gegenstand der Untersuchung ist die „Doktor Mouse“ (siehe Abschnitt 3.2.1), das Produkt eines russischen Unternehmens. Mit Hilfe des Fragebogens soll das Produktes „Doktor Mouse“ nach dessen Nutzung durch Versuchspersonen bewerten werden. Aufbauend auf den daraus gewonnenen Erkenntnissen sowie einer kleinen schriftlichen Einführung in die Welt der medizinischen Wearables sollen sich die Versuchspersonen ebenfalls noch zu medizinischer Wearable-Technologie im Allgemeinen äußern. Dies soll dem Befragenden ermöglichen weitere Erkenntnisse auf Anwenderebene bzgl. dieser neuartigen Technik zu sammeln. Dabei dreht sich alles um die 93 folgenden Fragestellungen: Inwieweit findet die heutige medizinische Wearable-Technologie beim Nutzer Anerkennung? Was muss getan werden bzw. welche Bedingungen müssen medizinische Wearables erfüllen, damit sie Vertrauen und die damit verbundene Akzeptanz beim Nutzer hervorrufen? Wo sehen Nutzer Chancen und Risiken dieser Technologie und welche Perspektiven (z.B. evt. Veränderungen im Gesundheitssystem) ergeben sich daraus? Zusätzlich dazu werden verschiedene Selbsttests durch den Befragenden/Untersuchenden mit dem Produkt „Doktor Mouse“ durchgeführt und mit einer verkürzten Variante des genannten Fragebogens dokumentiert (siehe Anhang; Abbildung 3). 3.1.2 Abgrenzung der Untersuchung Da die Grundvorrausetzung für den Einsatz der „Doktor Mouse“ ein PC oder Laptop mit entsprechender Schnittstelle ist und dem Befragenden/Untersuchenden kein Laptop zur Verfügung stand, hätten sämtliche Untersuchungen und Befragungen, die sich auf die „Doktor Mouse“ beziehen am heimischen PC durchgeführt werden müssen. Dies hätte die Anzahl der Untersuchungen und Befragungen natürlich erheblich einschränkt. Fragen zum Produkt „Doktor Mouse“ hätten somit auch nur von Verwandten und Freunden des Befragenden/Untersuchenden beantwortet werden können. Um dieses Problem nun möglichst zu umgehen, wurden die Probanden in 2 verschiedene Personengruppen unterteilt. Gruppe 1 umfasste die Verwandten und Freunde des Befragenden. Diese Gruppe erhielt das Gesamtpaket der Befragung, dass sich aus dem kompletten Fragebogen, mehreren Messungen mit der „Doktor Mouse“ sowie einer kleinen textuellen Einführung zum Thema „medizinische Wearables“ zusammensetzte (siehe Anhang; Abbildung 4). Gruppe 2 beinhaltete alle übrigen Teilnehmer der Befragung, bei denen Messversuche mit der „Doktor Mouse“ nicht möglich waren. Sie bekamen deswegen neben einem abgespeckten Gesamtpaket eine zusätzliche Einführung zum Produkt „Doktor Mouse“, mit der sie in der Lage waren, sämtliche Fragen des Fragebogens, bis auf die in Abschnitt 2 (Fragen zum Messvorgang), zu beantworten (siehe Anhang; Abbildung 5). Entscheidend für die Auswertung der Befragung dieser Gruppe war, dass die Probanden bei Beantwortung der Fragen auf keinerlei Erfahrungen mit dem Gerät zurückgreifen konnten. Sie mussten also auf eine korrekte Funktionalität der „Doktor Mouse“, wie in der Einführung beschrieben, vertrauen. Als kleine Hilfestellung wurde ihnen jedoch das Gerät selbst als Anschauungsobjekt zur Verfügung gestellt. Die Befragung der Gruppe 2 erfolgte grundsätzlich bei einem größeren Panel. Aus wettbewerbstechnischen Gründen konnte die Auswertungssoftware der „Doktor Mouse“ nicht bei potentiellen Nutzern installiert werden. 3.1.3 Angewandte Erhebungsmethoden und Vorgehen Die empirische Untersuchung besteht aus einem Fragebogen für eine Anwenderbefragung, der sowohl geschlossene Fragen als auch offene Fragen beinhaltet. Geschlossene Fragen werden dabei durch einfaches Ankreuzen der vorgegebenen Antwortmöglichkeiten beantwortet. Offenen Fragen dagegen erlauben dem Befragten, aufgrund der fehlenden Vorgabe von Antwortkategorien, eine freie Assoziation innerhalb seiner Antwort. Sie grenzen 94 den Befragten nicht ein, sondern fordern ihn auf, sich inhaltlich und persönlich aktiv mit der Thematik auseinander zu setzen. Dadurch erhofft man sich neue Ideen bzw. Impulse, die der Untersuchende bei der Befragung in dieser Form evt. nicht berücksichtigt hat. Um den o.g. Nachteilen einer standardisierten Erhebung weitestgehend entgegen zu wirken, wurden alle Befragten im Vorfeld dieser Untersuchung mit ausreichend Vorwissen durch eine kleine textuelle Einführung zur Thematik ausgestattet. Zusätzlich war der Befragende während jeder schriftlichen Befragung anwesend, um bei Unklarheiten bzgl. des Fragebogens oder bei allgemeinen Verständnisproblemen auszuhelfen, so dass das Risiko einer Ergebnisverfälschung verringert werden konnte. Der Altersdurchschnitt der Befragten war mit 24,46 Jahren relativ niedrig, da es nur sehr selten gelang ältere Menschen ab 50 für diese neuartige Technologie zu begeistern. Hauptgründe dafür waren mangelndes Vertrauen und Interesse, hervorgerufen durch fehlendes technisches Verständnis. Befragung/Untersuchung der Probanden aus Gruppe 1 Der Fragebogen für diese Gruppe teilt sich in vier Abschnitte und umfasst 25 Fragen auf sechs Seiten, wovon vier offene und 21 geschlossene Fragen sind. Insgesamt wurden hier 10 Personen befragt, von denen 3 weiblich und 7 männlich waren. Die maximale Anzahl der korrekten Messversuche pro Person betrug 5 Durchläufe. Zur Gewährleistung der Korrektheit wurden vor und während jedem Messvorgang die in Abschnitt 3.2.1 aufgezählten Messkriterien auf ihre Einhaltung überprüft. Fehlerhafte Messungen zählten nicht als offizielle Messversuche und mussten wiederholt werden. Befragung der Probanden aus Gruppe 2 Der Fragebogen für diese Gruppe teilt sich in 3 Abschnitte und umfasst 22 Fragen auf 5 Seiten, wovon 4 offene und 18 geschlossene Fragen sind. Insgesamt wurden hier 25 Personen befragt, von denen 11 weiblich und 14 männlich waren. Selbsttests Für die Selbsttests des Untersuchenden wurde bis auf Abschnitt 1 weitestgehend derselbe Fragebogen verwendet. Der Fragebogen für die Selbsttests teilt sich in drei Abschnitte und umfasst 20 Fragen auf 5 Seiten, bei denen es sich nur um geschlossene Fragen handelt. Insgesamt nahm der Untersuchende 5 korrekte Messungen vor, die alle bei einem normalen körperlichen Zustand erfolgten. Zusätzlich dazu kamen noch einige Messversuche, die unter Extremsituationen (z.B. nach körperlicher Anstrengung, Müdigkeit) durchgeführt wurden. Der Untersuchende ist männlich und 26 Jahre alt. 95 3.2. Untersuchungsobjekt 3.2.1 „Doktor Mouse“ Aufbau und Funktionsweise Die „Doktor Mouse“ ist eine Hard- und Softwarekombination des russischen Unternehmens RILA GmbH zum Testen und Überwachen des Herzkreislaufsystems. Dieses Gesamtpaket enthält neben der Software für die Datenverarbeitung einen optischen Infrarotsensorblock, bestehend aus einem verkleinerten Infrarotstrahler und einem Photosensor (optoelektrischer Sensor) zur Erfassung aller relevanten Daten, die für Kontrolle des Herzkreislaufs notwendig sind. Zur Zeit befindet sich dieser Sensorblock in einer getrennt funktionellen Einheit, die über einen seriellen Port (USB, COM) an den PC angeschlossen wird und keine zusätzliche Energiequelle benötigt. In Zukunft soll dieser Sensor jedoch in eine gewöhnliche Computermaus integriert werden, so dass PC-User während ihrer Arbeit am PC die Funktion ihres Herzkreislaufsystems kontrollieren und aufzeichnen können. Das hierbei angewandte Verfahren, um den Zustand des Herzkreislaufsystems zu ermitteln, basiert auf der Pulswellenanalyse. Bei dieser Form der Analyse werden infolge der Blutdruckschwankungen in den Blutgefäßen, die mit der Herztätigkeit (Kontraktion und Entspannung des Herzmuskels) zusammenhängen, bestimmte Parameter erfasst, die als Grundlage für die Analyse des Herzkreislaufsystems dienen. Bei der „Doktor Mouse“ werden speziell Blutdruckschwankungen in den Fingerkapillargefäße gemessen. Dieser Vorgang funktioniert wie folgt: Der IR-Lichtstrom, der von dem Infrarotstrahler zu einem Finger, der auf den Sensorblock gedrückt werden muss, abgestrahlt wird, wird an den Kapillargefäßen des Fingers in verschiedene Richtungen gestreut. Das Streuungsausmaß des Lichtstroms ändert sich dabei proportional zur Menge des Blutes, das sich in den Kapillargefäßen befindet. Da die Blutmenge in den Gefäßen abhängig von der jeweiligen Herzaktivität ist, wird der IRLichtstrom je nach Herzphase unterschiedlich gestreut. Dabei treffen periodisch verschiedene Anteile des gestreuten Lichtstroms auf den Photosensor, der diese Anteile dann registriert, sie transformiert und anschließend zum Computer überträgt. Dort wird das umgeformte, nun elektrische Signal durch die mitgelieferte Software entsprechend weiterverarbeitet und auf dem Bildschirm des PCs als Oszillogramm (Pulskurve/Pulswelle) angezeigt. 96 Entspannung Entspannung des Herzmuskels Kontraktion Gefäß Photosensor IR-Strahler Kontraktion des Herzmuskels und der Gefäße Abb. 85: Pulswellenermittlung Die durch diesen Vorgang gewonnene Pulskurve spiegelt also sämtliche Prozesse, die im menschlichen Herzen stattfinden sowie deren Auswirkungen auf das Gefäßsystem wieder und erlaubt aufgrund ihrer eindeutig visuellen Merkmale die Diagnose verschiedener Basisparameter, die zur Analyse der Herzkreislaufsystems herangezogen werden. Die Merkmale sind: Die Pluskurve zeigt die rhythmischen Schwankungen des kapillaren Blutflusses an, die durch die Bewegung das arteriellen Blutes verursacht werden, die ihrerseits wiederum durch die Muskelkontraktionen der Herzkammern zustande kommt. Anhand der Pulskurve lässt sich der Zeitdauer zwischen der Öffnung und dem Verschluss der Aortenklappe bestimmen. Der Verschlusszeitpunkt der Aortenklappen lässt sich ebenfalls mit Hilfe der Pulskurve ablesen. Außerdem kann man anhand der Pulskurve die Elastizität der Aorta und der Blutgefäße erkennen. Die Basisparameter sind: 1. Pulsschlagrate Die Pulsschlagrate ist die Zahl der Herzkontraktionen pro Minute. Der normale Wert des Pulses liegt bei 60 bis 80 Schlägen in der Minute. Eine Pulsrate von 80 bis 90 Schlägen in der Minute gilt als erhöhter Pulsschlag. Pulsraten mit über 90 Schlägen in der Minute deuten auf eine Tachykardie 51 hin. Eine Tachykardie wird meist nach intensiver 51 Die Tachykardie ist eine stark beschleunigte Herztätigkeit. Sie kann die Vorstufe zu dem hochfrequenten und durch unkoordinierte Herzerregung erzeugten Kammerflimmern sein, das den Blutkreislauf zum Erliegen bringt und unbehandelt zum Tode führt. 97 körperlicher Betätigung sowie nach dem Konsum alkoholischer Getränke, Rauschgift und bei der Einnahme bestimmter Medikamente beobachtet. Eine dauerhafte Tachykardie verlangt jedoch eine ärztliche Behandlung. Eine Pulsrate von 50 bis 60 Schlägen in der Minute wird als erniedrigter Puls angesehen. Bei Pulsraten unter 50 Schlägen in der Minute, deutet dies auf eine Bradykardie 52 hin. Eine Bradykardie ist charakteristisch für Sportler und Kinder sowie für Frauen, die gewöhnlich im Vergleich zu Männern eine etwas niedrigere Pulsschlagrate haben. 2. Schwankung des Herzintervalls Dieser Parameter spiegelt die zeitlichen Unterschiede zwischen dem längsten und dem kürzesten Herzintervalle wider. Beeinflusst wird er durch die Aktivität des sogenannten Sinusknoten, der automatisch elektrische Impulse zur Anregung der Herztätigkeit erzeugt. Der Sinusknoten ist der Hauptherzrhythmusregulator. Normalerweise sollte der Schwankungswert zwischen den Herzintervallen 0,16 Sekunden nicht überschreiten. Falls er es dennoch tut, spricht man von einer Sinusarrhythmie, die jedoch nicht in jedem Fall krankhaft sein muss. So können unterschiedliche Herzfrequenzen durch den Prozess der Atmung hervorgerufen werden. Eine Sinusarrhythmie, die nicht auf den Atmungsvorgang zurückzuschließen ist, kann Vorbote von Extrasystolen sein. Extrasystolen sind Herzschläge, die außerhalb des normalen Herzrhythmus auftreten und von den Betroffenen meist als Herzstolpern oder Pausen empfunden werden. Sie äußern sich zuallererst in Form von verringerten Intervallen zwischen den Herzschlägen und verkleinerten Amplituden. Bei wiederholtem Auftreten von Extrasystolen ist zwingend ein Herzspezialist aufzusuchen. 3. Pulsstabilität Die Pulsstabilität ist ein statistischer Indikator, der die Gleichmäßigkeit der Intervalle zwischen den Herzschlägen charakterisiert. Er wird in Prozent (%) gemessen und drückt das Verhältnis zwischen den Standardabweichungen und der durchschnittlichen Länge der Herzintervalle aus. Der Normwert dieses Parameters liegt zwischen 2 und 5 %. 4. VNS – Spannungsindex Hierbei handelt es sich um einen sehr dynamischen Indikator. Er steht in direkter Verbindung mit der Wirkungsweise des vegetativen Nervensystems (VNS). Das VNS beeinflusst die Gefäß- und Herztätigkeit des Menschen. Während hohe Werte des VNS – Spannungsindex auf einen verstärkten Puls hinweisen, werden niedrige Werte mit einer Sinusarrhythmie verbunden. 5. VNS – Gleichgewichtsindex Der VNS – Gleichgewichtsindex spiegelt das Einsatzverhältnis zwischen dem sympathischen und parasympathsichen Teil des VNS wieder. Berechnungen, die auf der Analyse der Pulskurvenform beruhen, ermöglichen die Bestimmung mehrerer hämodynamsicher Charakteristika des menschlichen Herzkreislaufsystems. Zusätzlich dazu lassen sich die 4 Hauptparameter der Pumpfunktion des Herzens feststellen, die in den Punkten 6 bis 9 beschrieben werden. Dabei repräsentiert jeder Moment der Pulskurve stets eine bestimmte Druckschwankungsrate (dP/dT) in den Gefäßen, die eine Folge der Systole ist. 52 Bei einer Bradykardie schlägt der Herz langsamer als normal. Das führt dazu, dass der Körper nicht mehr mit genügend Sauerstoff und Nährstoffen versorgt wird. 98 6. Intensive Blutinjektionsphase Diese Phase umfasst die Zeit in der die Pulskurve bis zu ihrem Maximum ansteigt. Sie entspricht der Geschwindigkeit der Muskelfaserkontraktion im linken Herzkammermuskel und hängt vom Zustand der Herzkranzgefäße ab, die den Herzmuskel im Normalfall mit ausreichend Blut versorgen. Die normale Dauer dieser Phase liegt zwischen 0,08 und 0,12 Sekunden. 7. Höchste Belastungsphase Die Zeit vom Kurvenmaximum bis zu dem Punkt an dem die Kurve die Null-/Grundlinie durchschneidet ist von besonderer Bedeutung. Denn in dieser Phase erreicht der Herzmuskel seine maximale Spannung. Die Dauer dieses Pulskurvenabschnitts ist direkt mit den biochemischen Prozessen des Herzmuskels verbunden. Demzufolge haben alle Störungen des Metabolismus Auswirkungen auf die Länge dieser Phase. Eine erhebliche Zunahme dieser Phasenlänge (mehr als 0,10 Sekunden) zeigt eine Verschlechterung der Herzmuskelkontraktion an. 8. Entlastungsphase Die Entlastungsphase beschreibt das Zeitintervall zwischen dem Punkt, an dem die Kurve die Null-/Grundlinie durchschneidet bis zum Punkt, an dem sie am Niedrigsten ist (Kurvenminimum). Dieser recht schnelle Vorgang hängt mit der Entspannung des Herzmuskels zusammen und dauert gewöhnlich nicht länger als 0,09 Sekunden. 9. Beendigung der Systolenphase Während dieser Phase findet der Verschluss der Aortenklappe statt. Deshalb ist sie auch als Schlussphase der Herzkontraktion anzusehen. Die Dauer dieser Phase hängt direkt mit von der Elastizität der Aortenwand zusammen. In der Regel überschreitet sie die 0,15 Sekunden nicht. Überschreitungen treten häufig infolge hormonaler Störungen oder Vergiftungen (Alkohol/Drogen) auf. 10. Gefäßwiderstand Als Gefäßwiderstand bezeichnet man den Strömungswiderstand, den ein Gefäß dem Herzen entgegensetzt. Je höher der Gefäßwiderstand ist, desto langsamer ist der kapillare Blutfluss und umso höher die Möglichkeit einer Hypertonie (Blutdruck). 11. Gefäßspannung Die Gefäßspannung entspricht der Gefäßelastizität. Je größer dieser Parameter ist, desto größer ist die Belastung des Herzens während der Kontraktion. Die „Doktor Mouse“ nutzt nun diese elf ermittelten Parameter um das Herzkreislaufsystem des Anwenders zu beurteilen. Die Beurteilung enthält neben einer grafischen Darstellung (Abbildung 86) auch eine dazugehörige textuelle Beschreibung der Messergebnisse (Abbildung 87) und umfasst insgesamt 8 physiologische Größen, die den Zustand des Herzkreislaufs widerspiegeln. Die 8 Größen sind: die Pulsschlagrate, die Variationsbreite, die maßgebend für den Herzrhythmus ist, der Variationskoeffizient, der Unregelmäßigkeiten während der Herzaktivität aufdeckt, 99 der Gefäßwiderstand, der Gefäßtonus, der der Gefäßelastizität entspricht, der Blutdruck, der Cholesterinwert und die „Zeit der maximalen Belastung“, die mit der Herzmuskelkontraktion einhergeht. Der gesamte Prozess des Messens sowie die Auswertung und Betrachtung der Messergebnisse beansprucht ca. 2 – 3 Minuten. Zudem verursacht dieses Messverfahren keinerlei unangenehme und schmerzhafte Empfindungen und ist leicht handhabbar. Damit die Korrektheit des Messvorgangs gewährleistet werden kann, müssen folgende Kriterien während der Messung erfüllt sein: warme, trockene Hände von etwa 28 – 30°C, eine gleichmäßige Druckbelastung des Sensors mit dem Finger, keine Bewegungen des Arms und der Hand (links) ausführen, an der die Messung vorgenommen wird (sämtliche Einstellungen mit der rechten Hand vornehmen), ein stabiler Atem, ein entspannter körperlicher Zustand und die Pulskurve sollte etwa ein Drittel des Bildschirms einnehmen. Abb. 86: grafische Darstellung der Messergebnisse 100 Abb. 87: textuelle Auswertung und Erklärung der Messergebnisse Einsatzmöglichkeiten Vor dem Einsatz der „Doktor Mouse“ sollte jedem Anwender bewusst sein, zu welchem Zweck er die Messungen vornimmt. Denn je nach Einsatzziel müssen die Messergebnisse differenziert betrachtet und bewertet werden. Einsatzziele der „Doktor Mouse“ sind: regelmäßige und systematische Beobachtungen des Herzkreislaufsystems, um Unregelmäßigkeiten aufzudecken und entsprechende Gegenmaßnahmen einzuleiten, damit eventuell auftretende schwerwiegende Komplikationen vermieden werden können. Benutzer des Systems bekommen so ebenfalls die Möglichkeit, ihre zu unterschiedlichen Zeiten genommenen Messergebnisse miteinander zu vergleichen und dadurch Abhängigkeiten zwischen der Herztätigkeit und äußeren Einflüssen (physische und nervliche Belastungen) aufzuspüren. Dadurch können sie dann den zulässigen Grad der äußeren Einflüsse einwandfrei bestimmen und entsprechend, durch Abbau der negativen äußeren Einflüsse, gesundheitsfördernd auf ihre Herzaktivität Einfluss nehmen. regelmäßige und systematische Beobachtungen des Herzkreislaufsystems, um die Wirksamkeit von Medikamenten zu bestimmen. In diesem Fall erlaubt das System die Überwachung von Behandlungsprozessen mit medizinischen Präparaten, die sich direkt auf die Herz- und Gefäßtätigkeit auswirken und somit den Erfolg oder Misserfolg einer medikamentösen Behandlung anzeigen. die regelmäßige Überwachung des Herzkreislaufsystems während sportlicher Aktivitäten/Training. 101 die Kontrolle der Herztätigkeit nach einer Drogen- oder Alkoholvergiftung. die Kontrolle des Herzkreislaufsystems während einer Erkältung oder bei Infektionskrankheiten. die Kontrolle der Herztätigkeit während einer Entspannungs-/Ruhephase etc. 3.3. Ergebnisse Der komplette Fragebogen besteht aus vier Teilen. Der erste Teil des Fragebogens enthält allgemeine Fragen zu Wearables bzw. medizinischen Wearables und soll über den Bekanntheitsgrad dieser Technik Auskunft geben. Außerdem werden in diesem Zusammenhang Probleme, Chancen und Risiken von medizinischen Wearables erörtert, um Rückschlüsse auf eventuelle Akzeptanzprobleme zu ziehen. Der zweite Teil umfasst ausschließlich Fragen zu dem Messvorgang mit der „Doktor Mouse“ und soll die korrekte Funktionsweise dieses Produktes testen. Im dritten Teil sollen die Akzeptanz des Produktes „Doktor Mouse“ untersucht und speziell Probleme des Gerätes bei dessen Nutzung aufgedeckt werden. Anhand dieser Erkenntnisse können dann mögliche Verbesserungsvorschläge gemacht werden, um die Anerkennung bzw. Akzeptanz derartiger Technik in der Bevölkerung zu steigern. Der letzte und vierte Teil des Fragebogens dient der Sammlung von Daten über persönliche Informationen der Teilnehmer, wie Geschlecht, Alter, körperlicher Zustand usw. In Abhängigkeit von den Befragten variiert der Umfang des Fragebogens, wie in Abschnitt 3.1. beschrieben. Die nach der Untersuchung/Befragung statistische Auswertung der quantitativen Daten erfolgte mit dem Softwareprogramm GrafStat. Die Freitextantworten wurden vom Untersuchenden/Befragenden entsprechend kategorisiert und mit Hilfe der Software MS Excel tabellarisch dargestellt. 3.3.1 Ergebnisse der Anwenderbefragung – Allgemein In diesem Abschnitt wird nur der erste Teil des Fragebogens sowohl von Gruppe 1 als auch von Gruppe 2 ausgewertet, da beide diesen unter gleichen Voraussetzungen bearbeiten konnten. Unterstützt wurde die Auswertung dabei mit den Antworten der Probanden aus dem vierten Teil des Fragebogens. 3.3.1.1 Stand des Wissens aller Befragten über „Wearables“ Obwohl die Technik des Wearable Computing schon in viele Bereiche Einzug gehalten hat und gar nicht mehr so innovativ ist, kennen nur etwa 34% der Befragten den Begriff des „Wearables“, von denen ein Großteil - 75% - Schüler bzw. Studenten sind (Abbildung 88). Gründe hierfür scheinen fehlende Informationsnetzwerke der Hersteller zu sein, die potentielle Nutzer über diese Technik und ihre enormen Vorteile aufklären. Denn diese 34% kamen meist in einer Lehrveranstaltung oder über private Gespräche mit Mitmenschen erstmals mit diesem Begriff in Berührung. Ein nur verschwindend geringer Prozentsatz erhielt seine Informationen über TV und Rundfunk. Durch diese mangelhafte Aufklärung seitens der 102 Industrie kann und wird in Zukunft das bisher geringe Vertrauen der Öffentlichkeit in diese Technologie nicht wachsen, sondern stagnieren, so dass „Wearables“ weiterhin mit Akzeptanzproblemen zu kämpfen haben werden, obwohl das nicht so sein muss. Denn nach der kleinen textuellen Einführung über Wearables zu Beginn des Fragebogens, stellte sich im nachhinein bei der Auswertung der Befragung heraus, dass ein Großteil der Befragten gute bis sehr gute Chancen in der Technologie sehen und deren Einsatz im alltäglichen Leben begrüßen würden (Abbildung 89). Abb. 88: Ergebnisse und Zusammenhänge über den Kenntnisstand von Wearables und der Berufsgruppe 103 Abb. 89: Akzeptanz und Einsatzchancen von medizinischen Wearables aus Sicht der Befragten 3.3.1.2 Ergebnisse der Freitextbefragung Die Antworten aus der Freitextbefragung wurden kategorisiert und hinsichtlich der Häufigkeit der Nennung geordnet (Tabelle A). 104 Antworten Anzahl der Nennungen Prozent (%) Frage 1: "Welche Probleme sehen Sie bei der Einführung von medizinischen Wearables auf dem Markt?" zu hohe Kosten 19 42,2 mangelndes Vertrauen der Patienten/Berührungsängste 15 33,3 fehlende Alltagstauglichkeit 6 13,4 mangelndes Vertrauen der Ärzte/Berührungsängste 3 6,7 Umschulungen von Medizinern/Ärzten notwendig 1 2,2 Informationsüberflutung 1 2,2 bessere und schnellere Diagnose/Hilfe/Früherkennung 22 44,9 Unterstützung des Arztes bei Behandlung/ Unterschungen/Überwachungen 11 22,4 Alltagstauglichkeit (praktisch, nicht einschränkend) 5 10,2 Verbesserung der Lebensqualität (gesunderes Leben, längeres Leben) 4 8,3 Zeitaufwand für Arztbesuche minimieren 3 6,1 Arztkosten sparen 2 4,1 Sicherheitsgefühl beim Patienten 1 2 gezieltere Behandlungen möglich 1 2 Fehldiagnosen durch Mensch und/oder Technik 13 24,1 fehlende Zuverlässigkeit der Technik 11 20,4 Datensicherheit/Missbrauch von Daten 9 16,7 übersteigertes Vertrauen in die Technik 5 9,2 Überwachung von Patienten 5 9,2 gesundheitliche Risiken, wie Strahlung etc. 4 7,4 Lösen unnötige Panik bei Fehldiagnosen aus 4 7,4 zwanghafte Kontrolle des Gesundheitszustandes 2 3,7 verschwindende Arzt-Patienten-Beziehung Tabelle A: Ergebnisse der Freitextbefragung 1 1,9 Frage 2: "Welche Chancen sehen Sie in medizinischen Wearables?" Frage 3: "Welche Risiken sehen Sie in medizinischen Wearables?" Aus Tabelle A wird sichtbar, welche Probleme, Chancen und Risiken die Befragten bei der Einführung und Nutzung von medizinischen Wearables sehen. Die meisten Schwierigkeiten bei der Einführung von medizinischen Wearables sehen die Probanden in dem fehlenden Vertrauen der Patienten in diese relativ neue Technologie (33,3%) und vor allem aber befürchten sie zu hohe Anschaffungskosten (42,2%). Weniger problematisch ist dagegen die fehlende Alltagstauglichkeit von Wearables, da sich hierzu nur 13,4% der Befragten kritisch äußerten. 105 Für einen Großteil der Befragten ergeben sich durch den Einsatz von medizinischen Wearables klare Vorteile in der Diagnose von Krankheiten und der allgemeinen medizinischen Versorgung. 44,9 % der Antworten beziehen sich hierbei auf bessere und schnellere Diagnose- und Behandlungsmöglichkeiten und auf eine frühzeitige Erkennung von auftretenden Erkrankungen. Die Unterstützung des Arztes bei Behandlungen, Untersuchungen und Überwachungen der menschlichen Vitalfunktionen ist mit 22,4% ebenfalls als hoher Nutzen von medizinischen Wearables erkannt worden. Dem gegenüber stehen natürlich Risiken und Ängste, die die Befragten in medizinischen Wearables sehen. Hier stehen evt. auftretende Fehldiagnosen durch den Menschen und/oder die Technik mit 24,1% an erster Stelle. Nachfolgend mit 20,4% wird an der Zuverlässigkeit der Technik gezweifelt. Ist sie immer funktionsbereit, wenn sie benötigt wird? Ein weiterer wichtiger Punkt der von den Befragten nicht vernachlässigt wurde, ist die Datensicherheit bzw. der aus dem Verlust der Datensicherheit resultierende Missbrauch der Daten. 16,7% sehen hier bei dem Einsatz von medizinischen Wearables große Risiken, da bei einigen Wearable-Anwendungen der Datenversand oftmals mittels Funkübertragungen umgesetzt wird (siehe Abschnitt 2.2). 3.3.2 Ergebnisse der Anwenderbefragung – Gruppe 1 3.3.2.1 Messungen mit der „Doktor Mouse“ Insgesamt wurden mit jedem der zehn Probanden fünf direkt aufeinander folgende Messungen durchgeführt. Die Messergebnisse katalogisierten die Probanden selbstständig, aber unter Aufsicht, in ihren Fragebögen, damit es dem Untersuchenden sowie den Untersuchten nachträglich möglich sein würde, Rückschlüsse auf die Verlässlichkeit des Gerätes zu ziehen. Jeder der zehn Probanden gaben in ihrem Fragebogen an, dass sie keinerlei Krankheiten, die die „Doktor Mouse“ erkennen kann, haben bzw. ihnen nicht bekannt ist, dass sie an derartigen Erkrankungen leiden. Die körperliche Verfassung aller Probanden war zum Zeitpunkt der Messungen weitestgehend normal. Grundsätzlich attestierte die „Doktor Mouse“ jedem Teilnehmer mehrere gesundheitliche Probleme, wie in Abbildung 90 dargestellt. Führend dabei waren ein erhöhter bzw. erniedrigter Puls und Rhythmusstörungen. Die Messergebnisse sollten jedoch unter Berücksichtigung der entsprechenden textuellen Beschreibung (Abschnitt 3.2.1; Abbildung 88) betrachtet werden. Zusätzlich dazu gelang es dem Gerät bei allen fünf Messungen nie die gleichen Messergebnisse zu erzielen. So unterschieden sich die gesundheitlichen Probleme aller Probanden bei fast jeder Messung voneinander, obwohl dennoch eine grundsätzliche Tendenz zu bestimmten vermeidlichen Krankheitsbildern erkennbar war. Beispielsweise bescheinigte die „Doktor Mouse“ einem Probanden bei jeder der fünf Messungen, neben Variationen zwischen Rhythmusstörungen und Problemen mit dem Gefäßwiderstand, einen konstant erhöhten Plusschlag (Abbildung 91). 106 Abb. 90: Attestierte gesundheitliche Probleme Messung: 1 2 3 4 5 erhöhter/niedriger Pulsschlag Herzmuskelschwäche Rhythmusstörungen Unregelmäßigkeiten während der Herzaktivität Probleme mit dem Gefäßwiderstand Probleme mit dem Gefäßtonus hohe/niedrige Cholesterinwerte hoher/niedriger Blutdruck Abb. 91: Messergebnisse eines männlichen Probanden Mit denen bei der Nutzung der „Doktor Mouse“ gewonnenen Erfahrungen stellten sich die Befragten nun dem dritten Teil des Fragebogens. Dort nahmen sie Stellung zum Gerät selbst und ließen ihr Akzeptanzverhalten bzgl. der „Doktor Mouse“ und ähnlichen Geräten für den Befragenden/Untersuchenden sichtbar werden. 107 3.3.2.2 Akzeptanz Aufgrund der gesammelten Erkenntnisse bei dem Umgang mit der „Doktor Mouse“ fallen sämtliche Beurteilungen der Probanden bzgl. der „Doktor Mouse“ und der medizinischen Wearable-Technologie im Allgemeinen negativ aus. So schätzen alle Befragten die Untersuchungsergebnisse, die die „Doktor Mouse“ liefert, als unzuverlässig ein und können sich demnach nicht vorstellen, dass dieses und/oder ähnliche Produkte ihre regelmäßigen ärztlichen Untersuchungen in diesem Bereich ersetzen. Gründe dafür sind in Tabelle B sichtbar. Alle zehn Probanden beantworteten die Fragen. Antworten Anzahl der Nennungen Prozent (%) Frage 4: "Warum halten Sie die Ergebnisse der "Doktor Mouse" für nicht zuverlässig?" das Gerät ist zu sensibel 6 60 Messungen sind zu ungenau 4 40 Frage 5: "Warum können die "Doktor Mouse" und/oder ähnliche Produkte ihre regelmäßigen ärztlichen Untersuchungen nicht ersetzen?" Unzuverlässigkeit 6 54,5 mehr Vertrauen in die Ärzte 3 27,3 2 18,2 Kontakt zum Arzt fehlt Tabelle B: Gründe für die fehlende Akzeptanz 60% der Probanden finden, dass das Gerät zu sensibel auf äußere Einflüsse, wie Bewegung, Lachen, Sprechen, Körpertemperatur etc. reagiert und somit korrekte Messungen sehr erschwert. Zusätzlich dazu basiert das richtige Verhalten während einer Messung, um negative äußere Einflüsse zu minimieren, auf einer reinen subjektiven Bewertung des Probanden, da man diesbezüglich vom Gerät keinerlei Feedback erhält. Die restlichen 40% halten die Messungen für zu ungenau, weil sich die Messergebnisse bei fast jeder der fünf Messungen stetig unterschieden haben. Hinzu kommt die hohe Sensibilität des Gerätes, die u.U. zu ungenauen bzw. falschen Messresultaten führen kann. Unzuverlässigkeit ist einer der Hauptgründe, weshalb sich 54,5% der Probanden nicht vorstellen können, dass die „Doktor Mouse“ und/oder ähnliche Produkte in der Lage sind, Vorsorgeuntersuchungen beim Arzt zu ersetzen. Dies wird wahrscheinlich auch der Anlass dafür sein, dass 27,3% der Befragten zurzeit immer noch mehr Vertrauen in die Fähigkeiten der Ärzte haben, als in die der Computertechnik. Dennoch können sich einige der Befragten gut vorstellen, dass sie in Zukunft, bei 100% Zuverlässigkeit der Technik, derartige Geräte für Vorsorgeuntersuchungen dem Arzt vorziehen. 18,2% hingegen würde durch den Einsatz von medizinischen Wearables der persönliche Kontakt zum Arzt fehlen, der ihnen ein gewisses zusätzliches Sicherheitsgefühl gibt. Letztendlich würde sich keiner der Befragten mit dem Produkt „Doktor Mouse“ sicherer fühlen und deshalb wäre ein Erwerb dieses Gerätes für 80% der Befragten ausgeschlossen. Die übrigen 20% wären aus unerkenntlichen Gründen dennoch bereit, sich trotz aller zuvor aufgezählten Mängel und Probleme zum Kauf dieses Produktes hinreißen zu lassen. 108 3.3.2.3 Nutzen Unabhängig von den bisherigen Akzeptanzproblemen bzgl. der Funktionalität der „Doktor Mouse“ soll hier nun der Nutzen dieser Technologie in den Punkten Kostensparendes Verfahren, Zeitsparendes Verfahren, Räumliche Flexibilität, Zeitliche Flexibilität und Zuverlässigkeit durch die Probanden bewertet werden (Tabelle C). Durch das Einfügen des Punktes „Zuverlässigkeit“ wollte der Untersuchende die Widerspruchsfreiheit aller Befragten prüfen, die die „Doktor Mouse“ zuvor noch als unzuverlässig beschrieben haben. Alle zehn Befragten wählten dabei je eine der vorgegebenen Antwortmöglichkeiten aus. Punkte hoch / % mittel / % niedrig / % ich weiß nicht / % Frage 6: "Wie hoch schätzen Sie den Nutzern der "Doktor Mouse in folgenden Punkten ein?" kostensparendes Verfahren 3 / 30 4 / 40 1 / 10 2 / 20 zeitsparendes Verfahren 6 / 60 2 / 20 1 / 10 1 / 10 Zuverlässigkeit 1 / 10 1 / 10 7 / 70 1 / 10 räumliche Flexibilität 5 / 50 4 / 40 1 / 10 0/0 2 / 20 0/0 zeitliche Flexibilität 7 / 70 1 / 10 Tabelle C: Nutzen der „Doktor Mouse“ Grundsätzlich schätzen die meisten Befragten die „Doktor Mouse“ als recht kostensparendes und zeitsparendes Verfahren ein und erkennen den Wert ihrer flexiblen Einsatzmöglichkeiten sowohl in räumlicher als auch in zeitlicher Hinsicht. Wie schon im Abschnitt 3.3.2.2 sind auch hier leichte Widersprüche der Befragten hinsichtlich ihrer Antworten zu erkennen. So wird von 2 Befragten die Zuverlässigkeit des Gerätes auf einmal als hoch bzw. mittel eingestuft. 3.3.2.4 Zielgruppen Die Ergebnisse zu der Frage nach den Zielgruppen für den Einsatz der „Doktor Mouse“ ergaben, dass die Befragten die Anwendung dieses Gerätes hauptsächlich bei älteren Menschen (27,6%), Kranken (27,6%) und Sportlern (24,1%) sehen (Abbildung 92). Nur 6 (20,7%) der insgesamt 29 Nennungen bezogen sich auf Kinder, Jugendliche, Erwachsene und sonstige Personen. 109 Abbildung 92: Zielgruppen der “Doktor Mouse” 3.3.2.4 Bewertung Abschließend sollten die Befragten noch einmal in kurzer Art und Weise das Produkt „Doktor Mouse” hinsichtlich sämtlicher gesammelter Erkenntnisse und mit Hilfe ihrer Antworten auf die Fragen des Fragebogens bewerten, damit der Untersuchende einen groben Überblick über das Akzeptanzverhalten der Probanden gegenüber dem Produkt selbst erlangt. Die Resultate sind in Abbildung 93 dargestellt. 80% der Teilnehmer halten das Produkt für ausbau- und verbesserungsfähig. Nur jeweils 10% halten es für sinnvoll bzw. für nicht sinnvoll. Dieses Ergebnis lässt erkennen, dass die Befragten durchaus den Zweck und auch die Vorteile dieser Technologie begreifen, sie jedoch für noch nicht ausgereift und anwendungsfähig halten. 110 Abbildung 93: abschließende Beurteilung der “Doktor Mouse” 3.3.3 Ergebnisse der Anwenderbefragung – Gruppe 2 In der zweiten Gruppe der Untersuchung wurden, wie schon im Vorfeld beschrieben, sämtliche Personen eingestuft mit denen es nicht möglich war, Messungen mit der „Doktor Mouse“ durchzuführen. Deshalb erhielten sie als Ausgleich vor Beantwortung des Fragebogens eine kleine Einführung zum Produkt selbst. Dieser doch entscheidende Nachteil wirkte sich stark auf die Ergebnisse der Befragung aus, wie im Folgenden festzustellen sein wird. 3.3.3.1 Akzeptanz Erste Anzeichen der unterschiedlichen Sichtweisen zwischen Gruppe 1 und Gruppe 2 werden schon bei der Frage nach der Zuverlässigkeit sichtbar (Tabelle D). Allein hier schätzen 69,6% der Befragten das Produkt „Doktor Mouse“ als zuverlässig ein und 52% könnten sich sogar vorstellen, dass dieses oder ähnliche Geräte ihre regelmäßigen Vorsorgeuntersuchungen bzgl. des Herzkreislaufsystems ersetzen (Tabelle E). Auf die Frage nach der Zuverlässigkeit antworteten nur 23 von 25 Personen. Die restlichen zwei fühlten sich nicht in der Lage, diese Frage ohne praktische Tests zu beantworten. Auf die Frage 2 in der Tabelle E antworteten alle 25 Befragten. 111 Antworten Anzahl der Nennungen Prozent (%) Frage 1: "Schätzen Sie die Ergebnisse der "Doktor Mouse" als zuverlässig ein?" Nein 7 30,4 16 69,6 Anzahl der Nennungen Prozent (%) Ja Tabelle D: Zuverlässigkeit der „Doktor Mouse“ Antworten Frage 2: "Können Sie sich vorstellen, dass die "Doktor Mouse und/oder ähnliche Produkte ihre regelmäßigen ärztlichen Untersuchungen ersetzen können?" Nein Ja 12 48 13 Tabelle E: Ersatzpotential von medizinischen Wearables 52 Die 69,6% der Befragten, die die Ergebnisse der „Doktor Mouse“ als zuverlässig einschätzen, geben allesamt als Grund ihr generelles Vertrauen in diese Technik und deren Funktionsweise an, da das Gerät ihrer Meinung nach vertrauenswürdige und sehr detailreiche Informationen liefert. Die übrigen 30,4% die das Produkt „Doktor Mouse“ für nicht zuverlässig halten, bilden bis auf eine Ausnahme, den kompletten Gegenpart zu den 69,6%. Sie zweifeln an der technischen Funktionsweise des Apparates und können sich nicht vorstellen, dass man über eine Fingerkuppenanalyse korrekte Informationen zum Herzkreislaufsystem erhält (Tabelle F). Antworten Anzahl der Nennungen Prozent (%) Frage 3: "Warum halten Sie die Ergebnisse der "Doktor Mouse" für nicht zuverlässig?" Zweifel an der technischen Funktionsweise 6 85,7 Zweifel an der korrekten Auswertung der Messergebnisse 1 14,3 Frage 4: "Warum können die "Doktor Mouse" und/oder ähnliche Produkte ihre regelmäßigen ärztlichen Untersuchungen nicht ersetzen?" fehlender persönlicher Kontakt zum Arzt 7 43,8 zu geringe Funktionsweise 4 25 Zweifel an der korrekten Auswertung der Messergebnisse 2 12,5 grundsätzlich vernachlässigte Gesundheitskontrolle 2 12,5 fehlendes Vertrauen in die Technik Tabelle F: Gründe für die fehlende Akzeptanz 1 6,2 Gründe für das Vertrauen, dass die „Doktor Mouse“ und/oder ähnliche Produkte medizinische Vorsorgeuntersuchungen ersetzen kann sind sicherlich mit dem Vertrauen der Befragen in die technische Zuverlässigkeit des Gerätes zu erklären. Die Gründe, die jedoch gegen dieses 112 Vertrauen sprechen, sind weit aus vielschichtiger und umfangreicher (Tabelle F). So würde 43,8% der Befragten der persönliche Kontakt zum Arzt fehlen, welcher mit seiner Erfahrung und seinen Beratungsmöglichkeiten jederzeit beruhigend auf den Patienten einwirken kann. Außerdem ist ein Arzt in der Lage weitaus umfangreichere und vor allem für Laien verständliche Informationen zu einem Krankheitsbild zu liefern als ein technisches Gerät. 25% attestierten der „Doktor Mouse“ eine zu geringe Funktionsweise, da sie einzig und allein nur Diagnosezwecke besitzt und der Patient bei Krankheitssymptomen sowieso den Arzt aufsuchen muss. 12,5% setzen in die Fähigkeiten des Arztes mehr Vertrauen als in die der Technik, weil beispielsweise ähnliche Symptome verschiedene Krankheitsbilder haben können, die das Gerät bei der Auswertung der Messergebnisse nicht berücksichtigt. Weitere 12,5% der Befragten sehen gar keinen Bedarf in Vorsorgeuntersuchungen, egal ob von Mensch oder Technik. Nur eine einzige Person gibt als Grund fehlendes Vertrauen an. 16 (64%) der 25 Befragten würden sich mit der „Doktor Mouse“ als technisches Gerät zur Überwachung ihres Herzkreislaufsystems sicherer fühlen und 13 davon (81,3%) würden es sogar in Betracht ziehen, sich dieses Produkt für den privaten Gebrauch zu zulegen. 3.3.3.2 Nutzen Wie schon zuvor bei der Ergebnisauswertung der Gruppe 1 mussten sich die Befragten der Gruppe 2 auch zum Nutzen der „Doktor Mouse“ in den nachfolgenden fünf Punkten äußern. Auch die Frage nach der Zuverlässigkeit des Gerätes wurde erneut gestellt, um die Widerspruchsfreiheit der hier Befragten zu prüfen. Die Ergebnisse dazu sind in Tabelle E dargestellt. Alle 25 Befragten wählten dabei je eine der vorgegebenen Antwortmöglichkeiten aus. 1. Kostensparendes Verfahren 2. Zeitsparendes Verfahren 3. Räumliche Flexibilität 4. Zeitliche Flexibilität 5. Zuverlässigkeit Punkte hoch / % mittel / % niedrig / % ich weiß nicht / % Frage 5: „Wie hoch schätzen Sie den Nutzern der „Doktor Mouse in folgenden Punkten ein?“ kostensparendes Verfahren zeitsparendes Verfahren Zuverlässigkeit räumliche Flexibilität zeitliche Flexibilität 2/8 14 / 56 5 / 20 4 / 16 17 / 68 5 / 20 1/4 2/8 4 / 16 13 / 52 3 / 15 5 / 20 15 / 60 9 / 36 1/4 0/0 21 / 84 4 / 16 0/0 Tabelle G: Nutzen der “Doktor Mouse” 0/0 Wie anhand der Tabelle F deutlich zu erkennen ist, schätzt ein Großteil der 25 Probanden – jeweils über 60% - die „Doktor Mouse“ in allen fünf Punkten als sehr nützlich ein. Die Werte 113 bzgl. der Zuverlässigkeit stimmen bis auf zwei Abweichungen mit den zuvor gegebenen Antworten der Befragten überein. Die Widerspruchsfreiheit ist dementsprechend hoch. 3.3.3.3 Zielgruppen Die Befragten der Gruppe 2 sehen den Einsatz der „Doktor Mouse“ ähnlich wie die der Gruppe 1. Hauptzielgruppen sind wieder ältere Menschen (22,5%), Kranke (27%) und Sportler (22,5%). Die übrigen 4 Kategorien sind mit einem Prozentsatz von 28% vertreten (Abbildung 94). Abb. 94: Zielgruppen der „Doktor Mouse“ 3.3.3.4 Bewertung Eine abschließende kurze Bewertung der „Doktor Mouse“ durch die Befragten soll nochmals einen zusammenfassenden und komprimierten Überblick bzgl. des Akzeptanzverhalten der Probanden gegenüber dem Produkt geben. Die in Abbildung 95 grafisch dargestellten Ergebnisse zeigen, dass alle Befragten die „Doktor Mouse“ für ausbaufähig bis sehr sinnvoll halten. Keiner der Befragten reagierte mit strikter Ablehnung oder stufte das Gerät als sinnlos ein. Prinzipiell ist das Akzeptanzverhalten bzgl. medizinischer Wearable-Technologie Teilnehmer der Gruppe 2 also wesentlich höher, als das der Gruppe 1, auch wenn es hier scheinbar einige unüberwindbare Faktoren (fehlender persönlicher Kontakt zum Arzt) gibt, die die Akzeptanz und die Verbreitung dieser Technik bisher hemmen. Dennoch zeigt dieses 114 Ergebnis auch, dass die Menschen die Vorteile und Chancen von medizinischen Wearables erkannt haben und ihnen bei einwandfreier Funktionsweise, die mit ein Hauptgrund für die Akzeptanz darstellt, durchaus Vertrauen schenken würden. Abb. 95: abschließende Beurteilung der “Doktor Mouse” 3.3.4 Ergebnisse der Selbsttests Die bei den Selbsttests durchgeführten Messungen mit der „Doktor Mouse“ ergaben ein ähnliches Bild, wie das der Gruppe 1. Bei jeder der fünf direkt aufeinander folgenden Messungen attestierte die „Doktor Mouse“ dem Untersuchenden immer einen erniedrigten Puls, Rhythmusstörungen und Probleme mit dem Gefäßwiderstand. Um den von der „Doktor Mouse“ analysierten Pulsschlagwert zu verifizieren, ermittelte der Untersuchende während der Messungen durch „Puls fühlen“ noch zusätzlich seinen eigenen Pulsschlag. Beide gemessenen Werte stimmten in etwa überein und unterschieden sich im Schnitt um ca. 1-5 Pulsschläge pro Minute. Ob dieses Ergebnis nun der Beleg dafür ist, dass die „Doktor Mouse“ korrekt funktioniert, ist dennoch anzuzweifeln. Denn dazu müssten aufwändigere Tests, wie z.B. das parallele Messen mit einem EKG-Gerät vorgenommen werden. Die Messergebnisse nach Extremsituationen wie Müdigkeit oder nach körperlicher Anstrengung oder nach dem Gebrauch von Suchtmitteln (Alkohol) zeigten leicht bis stark erhöhte Werte, wiesen aber grundsätzlich dieselben gesundheitlichen Probleme mit ein paar wenigen Schwankungen wie bei den Messungen im Normalzustand auf. 115 Während der umfangreichen Testphase (weit mehr als 50 Messungen), die der Untersuchende vor den offiziellen Messversuchen durchgeführt hat, bescheinigte die „Doktor Mouse“ dem Untersuchenden nur zwei mal ein gesundes Herzkreislaufsystem. Aufgrund der gemachten Erfahrungen mit dem Produkt „Doktor Mouse“ schätzt der Untersuchende das Gerät bzw. die gelieferten Messergebnisse als nicht zuverlässig ein und könnte sich zum jetzigen Zeitpunkt nicht vorstellen, dass dieses und/oder ähnliche Geräte in der Lage wären, ärztliche Vorsorgeuntersuchungen zu ersetzen. Die Gründe hierfür stimmen mit den der Gruppe 1 weitestgehend überein. Erst bei einer entsprechenden Weiterentwicklung/Verbesserung des Gerätes, so dass dem Nutzer eine 100% Zuverlässigkeit garantiert werden kann, könnte sich der Untersuchende vorstellen, dieses Gerät für den Eigenbedarf einzusetzen. Prinzipiell sieht der Untersuchende jedoch große Zukunftschancen in derartiger Technologie und gibt als mögliche Zielgruppen alle auf dem Fragebogen genannten Kategorien als potentielle Käufer an. Den Nutzen der „Doktor Mouse“ beurteilt der Untersuchende wie in Abbildung 96 dargestellt. Abschließend stuft der Untersuchende das Gerät „Doktor Mouse“, so wie es ihm während der Messungen zur Verfügung stand, konsequenterweise als ausbaufähig ein. hoch mittel niedrig ich weiß nicht kostensparendes Verfahren zeitsparendes Verfahren Zuverlässigkeit räumliche Flexibilität zeitliche Flexibilität Abb. 96: Nutzen der „Doktor Mouse“ 3.4 Schlussfolgerungen der empirischen Untersuchung Nach hinreichender Betrachtung der Ergebnisse wird sichtbar, dass sich die Meinungen beider Untersuchungsgruppen bzgl. der „Doktor Mouse“ in einigen Punkten sehr stark voneinander unterscheiden. Verantwortlich dafür ist, dass eine der beiden Gruppen – Gruppe 1 – beim Umgang mit dem Gerät „Doktor Mouse“ praktische Erfahrungen sammeln konnte, die ihre Ansichten beim Ausfüllen des Fragebogens enorm beeinflussten. Die zweite Gruppe hingegen arbeitete bei der Beantwortung des Fragebogens nur mit einer kleinen textuellen Einführung, in der kurz die Funktionsweise und die Möglichkeiten der „Doktor Mouse“ näher erläutert werden. Diese unterschiedlichen Voraussetzungen und die daraus resultierenden verschiedenen Ansichten beider Gruppen über die „Doktor Mouse“ lassen ganz leicht erkennen, wie stark das Akzeptanzverhalten der Öffentlichkeit gegenüber neuer Technologie von dem Vertrauen in diese beeinflusst wird. Besonders der Punkt der technischen Zuverlässigkeit bzw. korrekten Funktionalität kristallisierte sich bei den Probanden der Gruppe 1 als ausschlaggebend für die sehr schlechte Bewertung der „Doktor Mouse“ heraus. Sie bemängelten die zu hohe Sensibilität des Gerätes und die ständig variierenden (ungenauen) Messergebnisse. Für diese Probanden ist es demnach zurzeit unvorstellbar, 116 diesem Gerät ihren Gesundheitszustand anzuvertrauen. Die Akzeptanz der Probanden der Gruppe 1 in diese Technik unterlag somit einer erheblichen Abschwächung. Die Probanden der Gruppe 2 hingegen beurteilen die „Doktor Mouse“ weitaus positiver, weil ihnen die praktische Erfahrung mit dem Gerät fehlte und sie der Funktionsweise der „Doktor Mouse“, so wie sie in der textuellen Einführung beschrieben ist, größtenteils vertrauten. Die Akzeptanz und somit das gesteigerte Vertrauen in diese Technologie fiel bei den Probanden der Gruppe 2 deutlich höher aus, als bei denen in der Gruppe 1. Trotz dieses zum Teil sehr unterschiedlichen Ergebnisses, gibt es auch gemeinsame Ansichten zwischen beiden Gruppen. Beide erkennen die sich bietenden Vorteile und die vielfältigen Einsatzmöglichkeiten der „Doktor Mouse“, immer vorausgesetzt, dass sie zu 100% zuverlässig und richtig funktioniert. Dann und nur dann wäre sie in der Lage zeit- und kostenaufwändige Vorsorgeuntersuchungen des Herzkreislaufsystems zu ersetzen und somit viele Krankheiten, wie bspw. Symptome für Herzinfarkte, die von den Betroffenen im Vorfeld selbst kaum bis gar nicht wahrgenommen oder komplett falsch interpretiert werden, frühzeitig zu erkennen. Sie könnte also zur Diagnose, Früherkennung von Krankheiten des Herzkreislaufsystems und für eine allgemeine Überwachung von Patienten benutzt werden. Die „Doktor Mouse“ fände somit bei fast allen Menschen Anwendung, auch wenn die Probanden beider Gruppen ihren Einsatz nahezu ausschließlich bei älteren Menschen, Kranken und Sportlern sehen. Um langfristig bei allen Menschen Einsatz zu finden, müsste die „Doktor Mouse“ die typischen Merkmale eines Wearables aufweisen, welche sie zum jetzigen Zeitpunkt noch nicht besitzt. Sie müsste unauffällig in Gebrauchsgegenstände integriert werden und dürfte keinerlei zusätzlicher Handhabung/Bedienung benötigen. Sie würde den Menschen quasi „ganz nebenbei“ überwachen. Ein weiterer Vorteil, der sich durch die Nutzung der „Doktor Mouse“ ergibt, jedoch von den Probanden nicht berücksichtigt wurde, und für die Anwendung in einer breiten Masse spricht, ist der immer ungesunder werdende Lebenswandel der Menschen. Mangelhafte Ernährung und zu wenig körperliche Betätigung verursachen immer mehr Krankheiten, die auch das Herzkreislaufsystem betreffen können. Die Idee hinter der „Doktor Mouse“, diese künftig in eine Computermaus zu integrieren und laut Herstellerangaben später sogar in noch andere Technik, wie Mobilfunktelefone, PDAs etc., ist gut und wird von allen Probanden als positiv bewertet, auch wenn es derzeit noch an der technischen Ausführung scheitert. Grundlagen für diese Integration sind jedenfalls vorhanden, weil heutzutage, wie die Umfrage ergab, fast jeder Mensch in den Industrieländern mindestens einmal am Tag für mindestens eine Stunde einen PC mit angeschlossener Maus benutzt oder Mobiltelefone, PDAs etc besitzt (Tabelle H). Zumal eine Messung mit diesem Gerät nur ca. eine Minute andauert. Der Untersuchende sieht diesen Entwicklungstrend jedoch etwas skeptischer als die Probanden beider Gruppen, weil die Tendenz dorthin geht, dass Mobiltelefone, PDAs etc. in Kleidung oder andere Alltagsgegenstände eingebunden werden und somit diese Idee der Integration hinfällig wird. Angemessener wäre hier eine Integration dieser Technik in beispielsweise Autos. 117 Antworten Anzahl der Nennungen Prozent (%) beruflich 29 53,7 privat 25 46,3 gar nicht 0 0 0-2 11 31,4 0-5 10 28,6 5 - 10 10 28,6 10 und mehr 4 11,4 Frage 1: "Wann nutzen Sie einen Computer?" Frage 2: "Wie viel Stunden am Tag nutzen Sie den Computer?" Tabelle H: Nutzung des Computers Mit Hilfe dieser gewonnenen Schlussfolgerungen bzgl. der „Doktor Mouse“ und den beantworteten Fragen der Probanden über medizinische Wearable-Technologie im Allgemeinen (1. Abschnitt des Fragebogens), können nun auch Rückschlüsse auf die Akzeptanz der Öffentlichkeit bzgl. medizinischer Wearables gezogen werden. Grundsätzlich sehen beide Gruppen in dieser Technologie große Chancen für die Zukunft, die jedoch erst noch am Anfang ihrer Entwicklung steht und in vielen Bereichen wachsen muss. Vor allem aber in der Zuverlässigkeit der Funktionalität, die wiederum die Akzeptanz dieser Technik stark beeinflusst, besteht großer Nachholbedarf. Denn gerade weil die Gesundheit das höchste Gut des Menschen ist, kann sich kein Unternehmen leisten, ein unzuverlässiges, nicht korrekt funktionierendes Produkt auf den Markt zu bringen, dem der Mensch seine Gesundheit anvertraut. Gerade in diesen Bereich reagiert der Mensch auf technische Unzulänglichkeiten noch empfindlicher, als beispielsweise in der Personalcomputertechnik, in der vor allem Software häufig mit Problemen verschiedenster Art (siehe Windows) zu kämpfen hat. Generell werden Menschen aber immer an allen Dingen interessiert sein, die ihr Leben sicherer und länger machen, auch wenn damit einige Nachteile verbunden sein sollten. So gaben die Probanden bei der Befragung, neben dem fehlenden Vertrauen in die Technik, als Problem oder Risiko von medizinischen Wearables, zu hohe Kosten, mangelnde Datensicherheit (evt. Missbrauch der Daten bei Versicherungsabschlüssen oder Arbeitsverträgen) und Privatsphäre („gläserner Patient“) etc. an. Doch bei 100% Funktionalität der Technik steigt die Akzeptanz und das Vertrauen der Menschen und sie werden sich an die weniger bedeutsamen Nachteile, der evt. zu hohen Kosten, der Datensicherheit, dem fehlenden Kontakt zum Arzt etc. gewöhnen, weil sie entweder den höheren Nutzen schätzen lernen oder sich einfach mit diesen Problemen abfinden. Bestes Beispiel dafür ist das Mobilfunktelefon, das wahrscheinlich gesundheitsschädliche Funkstrahlung aussendet (verlässliche Studien, die diese Theorie bestätigten bzw. widerlegen stehen noch aus) sowie eine Überwachung der Telefonbesitzer ermöglicht, aber dennoch reißenden und wachsenden Absatz findet. Damit sich ein Trend zu den medizinischen Wearables entwickelt muss also eine zuverlässige Funktionsweise gewährleistet werden und parallel ein umfangreiches Marketing, um potentielle Nutzer über die Vorteile und die enormen Chancen von Wearables aufzuklären und somit ihr Vertrauen in diese zu wecken, stattfinden. Dadurch können die Berührungsängste mit dieser Technologie sowohl bei den Patienten als auch bei den Ärzten genommen werden. Letztendlich müssten, um einen Erfolg von medizinischen Wearables garantieren zu können, alle in Tabelle A des Abschnitts 3.3.1.2 118 aufgezählten Risiken und Probleme beseitigt werden, damit medizinische Wearables auf jeder Ebene unseres Alltags Einzug halten. 4. Ausblick, Visionen und Perspektiven Mit fortschreitender Technik werden sich immer neuere Möglichkeiten für tragbare medizintechnische Anwendungen eröffnen. In 15 oder 20 Jahren werden wir über hochintelligente Hemden, Hosen und Jacken verfügen, die uns selbsttätig kühlen oder wärmen, bei Unfällen schützen und unsere Körperfunktionen überwachen. Dabei wird es sich um Textilien handeln, die über eine eigene elektronische, chemische, physikalische und biotechnische Intelligenz verfügen. Vor allem das Interesse des Militärs gibt der Entwicklung von Hightech-Outfits einen starken Schub. Entwürfe von hochintelligenten Kampfanzügen, die ähnlich intelligent wie ein moderner Computer sind und die vitalen Funktionen des Soldaten (Atmung, Körpertemperatur, Puls, Blutdruck etc.) mit eingebetteten Sensoren messen und zur Kontrolle an die Einsatzzentrale funken, liegen schon längst vor. Die Kleidung wird trotz ihrer außergewöhnlichen Fähigkeiten leicht und komfortabel sein, weil alle elektronischen Geräte und Batterien als Mikrokomponenten direkt in die Bekleidung eingebaut werden und Kabel überflüssig machen. Neue Fasern sind selbst in der Lage, Strom zu leiten. Irgendwann ist es vielleicht auch möglich, wie in der Science-Fiction Serie „Star Trek“ mit einem Tricorder und anderen von dem medizinischen Personal verwendeten tragbaren Geräten zu arbeiten. Der Tricorder kann den Körper durchleuchten, Diagnosedaten zum Rechner des Hauptschiffes übertragen und von dort Behandlungshinweise für den behandelnden Arzt empfangen. Die Firma Blue Fire arbeitet auf eine Anwendung hin, die für die der Medizin zuarbeitenden Industrie bestimmt ist. Diese Anwendung soll in der Lage sein die beschriebenen Funktionen des Tricorders zu nutzen, indem sie von Krankenhäusern und Ärzten Audio- und Videodateien, für lebensrettende Maßnahmen vor Ort, empfängt und an diese überträgt. Auch durch den Einsatz elektronischer Implantate, die Körperteile oder Organe ersetzen (Prothetik) eröffnen sich auf diesem Gebiet vielfältige Einsatzmöglichkeiten. So könnte beispielsweise durch die Integration von Sensoren in das menschliche Gewebe die Zusammensetzung des Blutes bestimmt werden. Paniken und Ängste vor Spritzen bei Blutuntersuchungen würden damit der Vergangenheit angehören. Trotz der enormen sich bietenden Vorteile müssen auch Bedenken, vor allem aus ethischer Sicht angesprochen werden. Denn durch die Nutzung derartiger Technologie besteht die Gefahr des Missbrauchs. Menschen wären imstande die Grenzen des eigenen Körpers auszureizen sowie die eigenen Fähigkeiten (z.B. durch zusätzliche oder verbesserte Sinnesorgane) zu erweitern um sich dadurch Wettbewerbsvorteile zu verschaffen. Bei allen Hightech-Ambitionen greifen die Textilforscher jetzt neuerdings immer öfter auf das Vorbild Natur zurück. Sie haben Ideen, zukünftig Biomasse zu nutzen, um z.B. künstliches Spinnengewebe oder Designer-Muskeln zu erschaffen, die wie eine zweite Haut über unserer echten Haut liegen und sich der Umwelt beliebig anpassen können. Die TU München forscht bereits mit Muschel-Muskeln, die die Poren der Kleidung je nach Bedarf öffnen und schließen, um einen optimalen Wärme- und Kälteschutz (Luftzirkulation) zu gewährleisten. Gesteuert werden soll dieser Mechanismus direkt von unserem Nervensystem. 119 Letztendlich steht die Entwicklung für tragbare Elektronik zur Überwachung des menschlichen Gesundheitszustandes jedoch noch ganz am Anfang und wird in Zukunft der Medizin sicher noch zu dem einen oder anderen Durchbruch verhelfen. „Bald werden wir Schuhe haben, die mehr über uns wissen als jeder Arzt.“ (Quelle: Bass TA. Die Kleiderordnung des 21. Jahrhunderts. In: Monitor, Mai 1998) 5. Fazit Hier möchte ich stichpunktartig zusammenfassen, welche Probleme während der Arbeit auftraten, aber auch, was besonders positiv zu erwähnen ist. Probleme: Das Auffinden und Bearbeiten von Quellen für die Erstellung der Genesis beanspruchte sehr viel Zeit, da u.a. auch englische Texte verwendet werden mussten. Es stand nur eine russische und sehr stark gekürzte englische Version des Handbuchs der „Doktor Mouse“ zur Verfügung. Dadurch hatte ich bei dem Umgang mit der „Doktor Mouse“, aufgrund fehlender Informationen, einige Probleme. Das Finden von Probanden, die bei einer gewissenhaften Bearbeitung des Fragebogens ca. 30 - 45 Minuten ihrer Zeit opfern mussten. Positives: Hohe Motivation, da das Thema Wearables für mich sehr interessant ist. Sammeln von Erfahrungen bzgl. Umfragetechniken und den daraus entstehenden Problemen. Die Möglichkeit der Nutzung eines Prototyps für medizinische Wearables. Ich sah diese Bachelorarbeit als logische Konsequenz zu meinen bisherigen Arbeiten, die ich im Rahmen meines Studiums bisher absolvierte. So beschäftigte ich mich bei Seminaren, Hausarbeiten etc. (z.B. Ambient Intelligence) fast ausschließlich mit Themen zu medizinischen Wearables, solange sie zur jeweiligen Veranstaltung passten. Außerdem hoffe ich, die bei der Bachelorarbeit gemachten Erfahrungen für spätere Projekte oder Arbeiten wie der folgenden Masterarbeit mitzunehmen. 120 Eidesstattliche Erklärung Ich versichere hiermit, alle im Zusammenhang mit dieser Bachelorarbeit erstellten Dokumente ohne fremde Hilfe und ausschließlich mit den aufgeführten Hilfsmitteln und Quellen angefertigt zu haben. 121 Literaturverzeichnis 1. Geschichte der Medizin – Band II; Charles Lichtenthaeler; Deutscher Ärzte –Verlag GmbH; 1974; Kölm-Lövenich 2. Medizin und Technik – 3000 Jahre ärztliche Hilfsmittel für Diagnostik und Therapie; Heinz Goerke; Verlag Georg D. W. Callwey; 1988; München 3. Die Geschichte der Medizin – von der Antike bis zur Gegenwart; Bernt KargerDecker; Patmos Verlag GmbH & Co. KG, Albatros Verlag; 2001; Düsseldorf 4. http://www.media.mit.edu/wearables/lizzy/timeline.html#1665 5. http://de.wikipedia.org/wiki/Memex 6. http://gonzo.uni-weimar.de/~lobers/Wearable/Wearable_Computing.html 7. http://www.tzi.de/~ruegge/PDF-Dateien/THEALIT_01_Ohne_Bilder.pdf 8. http://www.cs.albany.edu/~maniatty/teaching/ubicomp/class02/lectnotes.pdf 9. http://www.teco.edu/~cdecker/onhandpc/ 10. http://www.voltaicsystems.com/bag_backpack.shtml 11. http://www.golem.de/0204/19543.html 12. http://www.spiegel.de/wissenschaft/mensch/0,1518,323079,00.html 13. http://www.heise.de/tp/r4/artikel/8/8555/1.html 14. http://www.xybernaut.de/downloads/daten/anwendungen/uniregensburg_noahweste_e. pdf#search=%22NOAH%20Vest%22 15. http://www.sensatex.com/ 16. http://www.primidi.com/2006/05/13.html 17. http://net.informatik.unituebingen.de/fileadmin/RI/teaching/seminar_mobil/ws0304/slides/slidesbunoza.pdf#search=%22SensaTex%20Smart%20Shirt%22 18. http://www.ifi.unizh.ch/ddis/fileadmin/teaching/current/sem_context_SS06/20060612 1_wearable_Tiefe.pdf#search=%22SensaTex%20Smart%20Shirt%2 19. http://www.lifecor.com/about_lifevest/when_to_use.asp 20. http://www.clevelandclinic.org/heartcenter/pub/guide/tests/procedures/lifevest.htm 21. http://www.presseportal.de/story.htx?nr=523675&firmaid=28852 22. http://www.geo-view.net/index_SPORT_sport-ekg-shirt.php 23. http://archiv.chip.de/news/c1_archiv_news_17199457.html 24. http://www.aerztezeitung.de/docs/2004/03/02/039a1301.asp 25. http://www.ifeas.uni-mainz.de/FriedPein/AbsPein4.html 26. http://paedpsych.jk.unilinz.ac.at/internet/arbeitsblaetterord/Erzwissenschaftempirisch/empirischfragebogenko nstr.html 27. http://arbeitsblaetter.stangl-taller.at/FORSCHUNGSMETHODEN/Fragebogen.shtml 28. http://www.h-wie-herz.de/broschueren_ordner/brosch_SM.html 29. http://www.cardiologe.de/index_extern.html?/patient/info/aktuell/schrittmacher_40j.ht ml 30. http://www.herzschrittmacher.info/ 31. http://www.hdz-nrw.de/de/kardiologie/wir_ueber_uns/herzschrittmachertherapie.php 32. http://www.onmeda.de/arztbesuch/behandlung/herzschrittmacher.html?p=2 33. http://www.elektroauto-tipp.de/modules.php?name=Battlithium 34. http://www.wikipedia.org 35. http://members.aol.com/drrknur/icd.htm 36. http://www.medsana.ch/artikel.php?id=1998&page_no=3 37. http://www.grundkurs-ekg.de/schrittmacher/schrittmacher.htm 38. http://www.biotronik.com/content/detail.php?id=1445 122 39. http://www.uni-heidelberg.de/presse/news/2307gleich.html 40. http://deposit.ddb.de/cgibin/dokserv?idn=969077408&dok_var=d1&dok_ext=pdf&filename=969077408.pdf 41. http://www.microvalue.ch/downloads/Cardiac_Rhythm_Management.pdf 42. http://www.freidok.uni-freiburg.de/volltexte/1570/pdf/Endfassung.pdf 43. http://www.freunde-alter-wetterinstrumente.de/22theges.htm 44. http://www.greiner-glasinstrumente.de/thermometer/thermometrie/tp-geschichte.html 45. http://www.temp-web.de/modules.php?name=Content&pa=showpage&pid=145 46. http://www.4teachers.de/?action=material&id=15359 47. http://www.norbertschnitzler.de/Surftipps/2001_40.htm#Temperatur 48. http://www.wikiweise.de/wiki/Thermometer 49. http://cc.uni-paderborn.de/lehrveranstaltungen/_testpt/kap_2/s18/temperatur.html 50. http://www.thermometermuseum.de/Neu/Seiten/start1024.htm 51. http://kugener.com/abfrage.php?id=0222&show=1 52. http://www7.nationalacademies.org/germanbeyonddiscovery/Stickoxid__2.html 53. http://www.madeasy.de/4/herzhist.htm 54. http://de.wikipedia.org/wiki/Blutdruckmessung 55. http://de.wikipedia.org/wiki/Sphygmograph#Geschichte_und_Entwicklung 56. http://www.heilpraktikerverband.de/heilv/natur_220.php?sid=&s_von=para 57. http://www.freewebs.com/scientific_anti_vivisectionism7/equipment2.htm 58. http://www.tk-logo.de/lexikon/s/rmenue.php3?li=./stethoskop.html 59. http://de.wikipedia.org/wiki/Kardiologie 60. http://www.onmeda.de/lexika/persoenlichkeiten/meilensteine_medizingeschichte.html 61. http://www.johann-winter-heilkundemuseum.de/album/Seiten/auskultation.htm 62. http://www.wdr5.de/sendungen/leonardo/dossiers/dossier_geschichte_der_medizin/die _geschichte_der_medizin/689455.phtml http://www.welt.de/data/2003/02/06/39276.html 63. http://www.aerztewoche.at/viewArticleDetails.do?articleId=4264 64. http://www.geocities.com/stethoskope/ 65. http://www.grg23-alterlaa.ac.at/allerlei_arznei/medizin.html 66. http://hns.pvs-bw.de/mod.php?mod=userpage&page_id=30 67. http://www.3m-pressnet.info/pressnet/de/prnews_detail.html?id=876 68. http://images.google.de/imgres?imgurl=http://www.antiquemed.com/binauralstethosco peimg/schreiberphonendoscopes.jpg&imgrefurl=http://www.antiquemed.com/binaural_stethoscope.htm&h=140&w= 100&sz=3&tbnid=DQvv38DRFFY1UM:&tbnh=88&tbnw=62&hl=de&start=3&prev =/images%3Fq%3Dbinaural%2BStethoskop%26svnum%3D10%26hl%3Dde%26lr%3 D 69. http://de.wikipedia.org/wiki/Elektrokardiogramm#Geschichte 70. http://www.grundkurs-ekg.de/geschichte/geschichte.htm 71. http://www.cardiologe.de/index_extern.html?/common/koro_geschichte.html 72. http://www.vobs.at/bio/spezial/x-hist29.htm 73. http://wwwalt.med-rz.unikliniksaarland.de/andere/hkh/medizin/fachbeitraege/fach_geschkard/body_fach_geschkard.h tml 74. http://www.ecglibrary.com/ecghist.html 75. http://www.uihealthcare.com/depts/medmuseum/galleryexhibits/beatgoesonhistory/05 ekgmachine.html 76. http://leifi.physik.uni-muenchen.de/web_ph10/geschichte/03galvani/galvani.htm 77. http://www.onmeda.de/lexika/persoenlichkeiten/einthoven.html 78. http://www.kugener.com/abfrage.php?id=0229 123 79. http://butler.cc.tut.fi/~malmivuo/bem/bembook/01/01.htm 80. http://de.wikipedia.org/wiki/Vektorkardiogramm 81. http://www.aeksh.de/shae/200107/h017023a.htm 82. http://www.itiv.unikarlsruhe.de/opencms/opencms/de/research/workgroups/MST_Optik/wear_comp/inde x.html 83. http://www.futurenews.at/archives/394-Gesundheits-Handies-und-EKG-Shirts.html 84. http://www.geo-view.net/de_Sport_sport-ekg-shirt.php 85. http://archiv.chip.de/news/c1_archiv_news_17199457.html 86. http://www.lrz-muenchen.de/~jmd/geschichte.htm 87. Projektarbeit; Fachbereich: Medizintechnik; Thema: Aufbau eines Biosignalverstärkers mit Computeranbindung; Projektteam: Marcel Dittmann, Patrick Falkenberg, Andreas Redlin, Matthias Rosenkranz; Hannover 88. http://www.freewebs.com/scientific_anti_vivisectionism7/equipment2.htm 89. http://www.durm-therapie.de/html/ganzheit/indukt.htm 90. http://www.vobs.at/bio/spezial/x-hist29.htm 91. http://www.ecglibrary.com/ecghist.html 92. http://translate.google.com/translate?hl=de&sl=en&u=http://butler.cc.tut.fi/~malmivu o/bem/bembook/01/01.htm&prev=/search%3Fq%3D%2522Leopold%2BNobili%252 2%26start%3D10%26hl%3Dde%26lr%3D%26sa%3DN 93. http://www.psychologie.unizh.ch/neuropsy/Forschung/eeg.html 94. http://torque.oncloud8.com/archives/cat_history_of_eeg.html 95. http://fc.units.it/ppb/NeuroBiol/Neuroscienze%20per%20tutti/hist.html 96. http://chem.ch.huji.ac.il/~eugeniik/history/berger.html 97. http://www.cerebromente.org.br/n03/tecnologia/historia.htm 98. http://www.ibl.uni-bremen.de/lehre/lui/user/ag02/GeschichteH.htm 99. http://en.wikipedia.org/wiki/EEG_topography 100. http://www.ub.uni-konstanz.de/kops/volltexte/1999/248/index.html 100. http://www.eetimes.de/at/news/showArticle.jhtml?articleID=19502700 101. http://www.file-commander.de/projektarbeit.htm 102. http://www.futurehealth.org/wireless_eeg.htm 103. http://www.bio-medical.com/product_info.cfm?inventory__imodel=PETEEG 104. http://www.schwarzer.net/wir/deutsch/wirset.htm 105. http://deposit.ddb.de/cgibin/dokserv?idn=971281726&dok_var=d1&dok_ext=pdf&filename=971281726.pdf 106. http://www.imse.med.tu-muenchen.de/mi/lectures/msv/msv-09elektroenzephalogramm-051205.pdf 107. http://nmrc.bu.edu/technology/history.html 108. http://sundoc.bibliothek.uni-halle.de/diss-online/04/05H018/t2.pdf 109. https://eldorado.uni-dortmund.de/bitstream/2003/2976/1/KozakHauptteil.pdf 110. http://vts.uni-ulm.de/docs/1999/341/vts_341.pdf 111. http://list.feat.org/scripts/wa.exe?A2=ind9903e&L=featnews&D=1&O=D&F=&S=& P=400 112. http://www.drjamesgolseth.com/index.html 113. http://www.acsu.buffalo.edu/~dfine/Hist.%20EMG4.ppt 114. http://www.dhi-online.de/DhiNeu/12_Fachtec/FtHgTec/Ftht_00.html 115. http://www.forumbesserhoeren.de/index.php?id=52 116. http://www.german.hear-it.org/page.dsp?page=2010 117. http://home.schule.at/teaching/Hoeren_und_Hoerprobleme/hilfen/history.htm 118. http://www.typolis.de/hear/go.htm?www.oticon.de/ 124 119. http://www.beckerhoerakustik.de/unternehmenbeckerhoerakustik/rundumsohr/vomhoe rrohrzumhoersystem/index.html 120. http://www.dhi-online.de/DhiNeu/DHIIndex.html 121. http://www.akustiker.at/museum/geschichte/index.html 122. http://steiermark.orf.at/magazin/immergutdrauf/tipps/stories/27367/ 123. http://www.propatient.info/content/i20.pdf 124. http://www.hoerforum.de/501.html 125 125. http://www.zelger.it/assets/images/content/AudioN.2003dt.pdf 126. Dissertation: Messung von sechs verschiedenen modernen digitalen Hörgeräten mit fünf Audiogrammen am 2 cm³-Kuppler; Christiane Barbara Rau; medizinische Fakultät der Bayerischen Julius-Maximillian-Unversität zu Würzburg 126. http://www.geschichte-der-brille.de/index.html 127. http://www.optiker.at/archiv/brillengeschichte/brilleng.htm 128. http://www.sov.ch/german/Dokumentation/Themen/3-1-1_GeschichtederBrille.htm 129. http://www.gesundheit.de/wissen/medizingeschichte/brillen/index.html 130. http://www.diekmann.de/geschichte%20brille/geschichte.htm 131. http://www.igaoptic.de/besucher/mainseiten/rundumsB/dieGeschichte.html 132. http://www.gallati.com/Infos/Geschichte.htm 133. http://www.thueringen.info/session/saaletal/optmus2.html 134. http://www.fielmann.ch/rund_ums_sehen/2051,2407,geschichte_19.php 135. http://www.tomshardware.de/lexikon/Brille#Geschichte 136. http://archiv.ub.uni-marburg.de/diss/z2002/0109/pdf/z2002-0109.pdf 137. http://www.univie.ac.at/medizingeschichte/instrumente.htm 138. http://de.wikipedia.org/wiki/Kardiologie#Geschichte_der_Kardiologie 139. http://www.madeasy.de/4/herzhist.htm 140. http://de.wikipedia.org/wiki/Pulsmesser 141. Medizin und Technik – 3000 Jahre ärztliche Hilfsmittel für Diagnostik und Therapie; Heinz Goerke; Verlag Georg D. W. Callwey; 1988; München; Seite 17 142. http://vlp.mpiwg-berlin.mpg.de/technology/search?-max=10&Op_lit.reference=eq&lit.reference=lit13659 143. http://www.arndt-bruenner.de/mathe/Allgemein/bios.htm http://leifi.physik.unimuenchen.de/web_ph11/geschichte/08zeitmessung/g_zeitmessung.htm 144. http://www.scientific.at/2005/roe_0503.htm 145. http://www.uhrenaktuell.de/uak_mnews20.htm 146. http://www.anr.de/anr_online/cbt/inhalt/t_2/t_2_3/t_01.htm 147. http://efimov.wustl.edu/defibrillation/history/defibrillation_history.htm 148. http://en.wikipedia.org/wiki/Defibrillation#History 149. http://www.musc.edu/bmt737/Spr_1999/Kelly/eads.htm 150. http://www.sjab.org.sg/AED.pdf 151. http://www.baylorhealth.edu/proceedings/16_4/16_4_hyland.pdf 152. http://de.wikipedia.org/wiki/Defibrillator 153. http://www.biotronik.com/content/detail.php?id=1416 154. http://www.uni-duisburg-essen.de/herz/html/defibrillator.html 155. http://www.stadtkoeln.de/feuerwehr/rettung/ifn/wissenschaft/artikel/00418/index.html 156. http://www.ecglibrary.com/ecghist.html 157. http://www.medsana.ch/artikel.php?id=1998&page_no=3 158. http://www.medsana.ch/artikel.php?eid=3308&page_no=1 159. http://butler.cc.tut.fi/~malmivuo/bem/bembook/01/01.htm 160. http://www.geocities.com/neveyaakov/electro_science/kouwenhoven.html 125 161. 162. 163. 164. 165. 166. 167. 168. 169. 170. 171. 172. 173. http://en.wikipedia.org/wiki/Frank_Pantridge http://www.madehow.com/Volume-7/External-Defibrillator.html http://www.bvmed.de/stepone/data/downloads/ed/9a/00/geschichte_web.pdf http://www.archaeologisch.de/forschung/prothese1.html http://inventors.about.com/library/inventors/blprosthetic.htm/ http://de.wikipedia.org/wiki/Prothese http://www.visionm.de/visionM-0105.pdf http://people.bath.ac.uk/en3tm/Report/history.html http://klinik.qualimedic.de/Bandscheibe_prothese_geschichte.html http://www.orthopoint.de/basics/armaktiv2.htm http://www.medschool.northwestern.edu/depts/nupoc/proshistory.html http://www.quarks.de/dyn/7405.phtml http://edoc.hu-berlin.de/oa/books/rezuzIE9APXxc/PDF/24QdYloQEVLM.pdf 126 Abbildungsverzeichnis Abbildung 1: Signalflüsse zwischen Mensch und Maschine nch Steve Mann ..................... 8 Quelle: http://www.cs.albany.edu/~maniatty/teaching/ubicomp/class02/lectnotes.pdf Abbildung 2: erster externer Herzschrittmacher ................................................................. 16 Quelle: http://www.medtronic.com/corporate/images/patient.jpg Abbildung 3: Earl Bakkens Herzschrittmacher ................................................................... 16 Quelle: http://www.medtronic.de/cmsimages/batt_herzschr_nr1.jpg Abbildung 4: erster implantierbarer Herzschrittmacher ...................................................... 17 Quelle: http://www.deutsches-museum.de/dmznt/images/ersatzteile/1/schrittmachergruen.jpg Abbildung 5: Medtronic Chardack-Greatbatch Herzschrittmacher .................................... 17 Quelle: http://www.nlm.nih.gov/share/image/frank11.gif Abbildung 6: moderne interne Herzschrittmacher .............................................................. 19 Quelle: http://www.lkh-wo.at/Medizin/schritt_fr.jpg Abbildung 7: Thermoskop von Heron von Alexandria ....................................................... 21 Quelle: http://www.wundersamessammelsurium.de/Heron/BuchPneu/Pneu2-08.html Abbildung 8: Galileis Thermoskop ..................................................................................... 21 Quelle: http://www.temp-web.de/modules.php?name=Content&pa=showpage&pid=148 Abbildung 9: 50-teiliges Thermometer „Florentine Little“ ................................................ 22 Quelle: http://www.freunde-alter-wetterinstrumente.de/22theges03.htm Abbildung 10: frühes Quecksilberthermometer .................................................................. 23 Quelle: http://inventors.about.com/library/inventors/blthermometer.htm Abbildung 11: Thermometer mit Réaumur-Skala .............................................................. 24 Quelle: http://www.amuseum.de/physik/alwami/exponate/kelvin/Reaumur.jpg Abbildung 12: modernes digitales Fieberthermometer ....................................................... 25 Quelle: http://alatkesehatan.com/components/com_phpshop/shop_image/product/1d68240cf8601a730 307f687f5439ba4.jpg Abbildung 13: Nachbildung des Stethoskops von Laennec ................................................ 26 Quelle: http://www.antiquemed.com/monoauralstethimg/laennec01.jpg Abbildung 14: binaurales Stethoskop von Camman ........................................................... 27 Quelle: http://www.antiquemed.com/binauralstethoscopeimg/camm_1852.jpg Abbildung 15: Alisons Differentialstethoskop .................................................................... 28 Quelle: http://www.antiquemed.com/binauralstethoscopeimg/alison1.jpg Abbildung 16: Stethoskop nach Littmann ........................................................................... 29 127 Quelle: http://www.nofamed.de/assets/images/Littmann_Select.jpg Abbildung 17: elektronisches Stethoskop ........................................................................... 29 Quelle: http://www.medical-econet.com/bilder/soundplus.jpg Abbildung 18: modernes digitales EEG-System mit 32 Kanälen ....................................... 30 Quelle: http://www.hospimedicaintl.com/Products.aspx?CatID=5&SubCatID=37 Abbildung 19: das erste von H. Berger aufgenommene Elektroenzephalogramm ............. 32 Quelle: http://chem.ch.huji.ac.il/~eugeniik/history/berger_eeg2.jpg Abbildung 20: Bergers EEG-Aufnahmesystem um 1926 ................................................... 32 Quelle: http://chem.ch.huji.ac.il/~eugeniik/history/berger.html Abbildung 21: direkt schreibendes Multikanal-EEG-Gerät ................................................ 33 Quelle: http://www.mediawars.ne.jp/~yukisss/EEG%20room.jpg Abbildung 22: modernes Computer-EEG ........................................................................... 34 Quelle: http://www.lutin.utc.fr/documents/eeg.jpg Abbildung 23: Wireless-EEG.............................................................................................. 35 Quelle: http://www.futurehealth.org/wireless_eeg.htm Abbildung 24: Oberflächenelektroden ................................................................................ 37 Quelle: http://www.emsbiomed.com/img/acc/large/surf_elec.jpg Abbildung 25: Braunsche Röhre ......................................................................................... 37 Quelle: http://de.wikipedia.org/wiki/Kathodenstrahlr%C3%B6hre Abbildung 26: konzentrische Nadelelektrode ..................................................................... 38 Quelle: http://www.ambu.de/ambude/final.nsf/(pubid)/iD74852620AB39A6FC1256F6900373BFDi5 25E1C663CA6E100C1256F78004704F8i564CC67C3618A84DC1256ED6004D4FE1?Open &SubName=%5C&ParentName=Nadelelektroden Abbildung 27: Elektromyograph von Huddleston & Golseth ............................................. 38 Quelle: http://www.acsu.buffalo.edu/~dfine/Hist.%20EMG4.ppt; Seite 21 Abbildung 28: tragbares EMG-Gerät .................................................................................. 39 Quelle: http://www.medgadget.com/archives/2005/01/advances_in_ele_1.html Abbildung 29: voltaische Säule .......................................................................................... 41 Quelle: http://www.emb-akku.com/index.html?/main-d/glossar/voltaische-saeule.html Abbildung 30: Nobilis „astatic galvanometer“ ................................................................... 41 Quelle: http://www.na.infn.it/Museum/schede/jpg/88.jpg Abbildung 31: Multiplikator ............................................................................................... 42 Quelle: http://www.bmm.charite.de/aktuelles/besonderes_objekt/som05.htm Abbildung 32: Lippmanns Kapillarelektrometer ................................................................ 43 128 Quelle: http://chem.ch.huji.ac.il/~eugeniik/history/lippmann_electrometer1.jpg Abbildung 33: Galvanometer von Deprez und d’Arsonval................................................. 43 Quelle: http://www.sidis.net/galvandeprez2.jpg Abbildung 34: der erste menschliche Elektrokardiogramm von A. Waller ........................ 44 Quelle: http://www.grundkurs-ekg.de/geschichte/wallerekg.gif Abbildung 35: 5 Phasen der elektrischen Herztätigkeit ...................................................... 44 Quelle: http://www.einthoven.nl/index_einthoven_menu.html Abbildung 36: Fadengalvanometer ..................................................................................... 45 Quelle: http://www.einthoven.nl/images/historicalphotos/eh008.jpg Abbildung 37: Einthovens Elektrokardiograph ................................................................... 45 Quelle: Projektarbeit; Fachbereich: Medizintechnik; Thema: Aufbau eines Biosignalverstärkers mit Computeranbindung; Projektteam: Marcel Dittmann, Patrick Falkenberg, Andreas Redlin, Matthias Rosenkranz; Hannover; Seite 3 Abbildung 38: eines der ersten Elektrokardiogramme, aufgezeichnet durch einen Fadengalvanometer ............................................................................................................. 46 Quelle: http://www.einthoven.nl/index_einthoven_menu.html Abbildung 39: moderner “Holter Monitor” ........................................................................ 47 Quelle: http://www.merck.com/media/mmhe2/figures/fg021_2.gif Abbildung 40: Einkanal-Direktschreiber der Firma Schwarzer .......................................... 48 Quelle: http://www.kugener.com/abfrage.php?id=0229 Abbildung 41: mobiles EKG-Gerät „Cardio24“ ................................................................. 49 Quelle: http://www.de.wellnessshop.com/cardio24.html?PHPSESSID=b44f5fe48b9b1bc2e609003acf24d9e0#details Abbildung 42: herkömmlicher manueller Defibrillator ...................................................... 50 Quelle: PDF; “The Heart, Defibrillation & Automated External Defibrillation”; Seite 19 Abbildung 43: AED ............................................................................................................ 51 Quelle: http://www.ci.glendora.ca.us/images/aed.jpg Abbildung 44: Darstellung eines implantierten Defibrillators ............................................ 51 Quelle: http://www.sjm.com/assets/popups/icd.gif Abbildung 45: Claude S. Becks erster Defibrillator ........................................................... 52 Quelle: http://efimov.wustl.edu/defibrillation/history/defibrillation_history.htm Abbildung 46: Pulsilogium von Santorio ............................................................................ 56 Quelle: http://clendening.kumc.edu/dc/rm/17_04p.jpg Abbildung 47: Sphygmograph von Karl v. Vierordt........................................................... 56 Quelle: http://clendening.kumc.edu/dc/rm/19_03p1.jpg 129 Abbildung 48: Gustav Gärtners Pulskontroller ................................................................... 57 Quelle: http://vlp.mpiwg-berlin.mpg.de/vlpimages/images/img3816.jpg Abbildung 49: Pulsuhr „Polar F11“ .................................................................................... 58 Quelle: http://www.bstaendig.at/OSCommerce/images/F11_GRY_front.jpg Abbildung 50: Riva-Roccis Sphygmomanometer ............................................................... 62 Quelle: http://pacs.unica.it/biblio/fig47e.jpg Abbildung 51: Blutdruckmessgerät für das Handgelenk .................................................... 63 Quelle: http://www.sanitaetshaus-48.de/images/sanicare/ibp/10084.jpg Abbildung 52: Hörröhr ........................................................................................................ 65 Quelle: http://gaia.oticon.de/eprise/main/Oticon/DE_de/SEC_AboutHearing/LearnAboutHearing/Pro ducts/SEC_Gaia/GaiaMagazine/PDFs/TheHistoryOfHearingAids Abbildung 53: Ellipsis Otica ............................................................................................... 66 Quelle: http://beckerexhibits.wustl.edu/did/rarebks/index.htm Abbildung 54: Hörstuhl von 1879 ....................................................................................... 67 Quelle: http://www.bis.uni-oldenburg.de/mirror/presse/einblick/22/geraete.gif Abbildung 55: elektronisches Hörgerät von Miltimore ...................................................... 67 Quelle: http://beckerexhibits.wustl.edu/did/win_19th/magneto.htm Abbildung 56: Tischhörgerät von Thornton ........................................................................ 68 Quelle: http://www.mauderli-hno.ch/Lexikon/Lex_baha.html Abbildung 57: tragbares Hörgerät mit Röhrenverstärker .................................................... 69 Quelle: http://www.ollmann.de/bilder/alt_standart.JPG Abbildung 58: HdO-Hörgerät ............................................................................................. 70 Quelle: http://www.hoergeraete-zieglmaier.de/Bilder/HdO_hoergeraet.jpg Abbildung 59: IdO-Hörgerät ............................................................................................... 70 Quelle: http://www.jaeckel.optiker.at/hoergeraet_ite.jpg Abbildung 60: IdO und HdO-Hörgeräte ............................................................................. 71 Quelle: http://republic.cap.ru/2002_61/34.HTM Abbildung 61: Nachbildung eines Lesesteins aus Beryll .................................................... 72 Quelle: http://www.zeiss.de/4125680F0055C122/GraphikTitelIntern/A39_1b/$File/A39_1b.jpg Abbildung 62: Nachbildung einer Nietbrille um 1350........................................................ 73 Quelle: http://www.amuseum.de/physik/brillen/exh98_99/20.jpg Abbildung 63: Schlitzbügelbrillet ....................................................................................... 74 Quelle: http://www.optiker.at/archiv/brillengeschichte/schlitzb.gif 130 Abbildung 64: Mützenbrille ................................................................................................ 74 Quelle: http://www.geschichte-der-brille.de/img/muetze.jpg Abbildung 65: Stirnreifenbrille ........................................................................................... 75 Quelle: http://www.optiker.at/archiv/brillengeschichte/stirn.jpg Abbildung 66: Zwicker um 1900 ........................................................................................ 75 Quelle: http://www.antik-optik.de/brillen/brille4.1.jpg Abbildung 67: Nürnberger Drahtbrille des 18. Jahrhunderts .............................................. 76 Quelle: http://www.fielmann.ch/images/geschichte/pic_gesch_17jh.jpg Abbildung 68: Schläfenbrille des 18./19. Jahrhunderts ...................................................... 76 Quelle: http://www.amuseum.de/physik/brillen/exh98_99/19.jpg Abbildung 69: Ohrenbrille um 1800 ................................................................................... 77 Quelle: http://www.schlossmuseum.de/bilder/brille.gif Abbildung 70: Lorgnon ....................................................................................................... 77 Quelle: http://www.thueringen.info/session/saaletal/saaletal010s.jpg Abbildung 71: moderne Brille von heute ............................................................................ 78 Quelle: http://www.ehleroptik.de/Bilder/brille1.jpg Abbildung 72: die Hand des Götz von Berlichingen .......................................................... 80 Quelle: http://www.quarks.de/dyn/pics/7405-7678-2-kap8_1.jpg Abbildung 73: Beinprothese nach Parè ............................................................................... 80 Quelle: http://www.medschool.northwestern.edu/bin/z/n/PareLeg.JPG Abbildung 74: Verduyns Wadenbeinprothese .................................................................... 81 Quelle: http://www.medschool.northwestern.edu/bin/f/t/VerduinLeg.JPG Abbildung 75: „Anglesey Leg“ ........................................................................................... 81 Quelle: http://www.medschool.northwestern.edu/bin/v/n/PalmerLeg.JPG Abbildung 76: Sauerbruch-Armprothese ............................................................................ 82 Quelle: http://www2.hu-berlin.de/kulturtechnik/kabinette/gross/SauerbruchArmprothese.jpg Abbildung 77: Aufbau einer künstlichen Hüftprothese ...................................................... 83 Quelle: http://media.gek.de/tnet/medizin/c_hueftprothese.jpg Abbildung 78: Fremdkraftprothese ..................................................................................... 84 Quelle: http://www.quarks.de/dyn/pics/7405-7682-2-kap8_4.jpg Abbildung 79: Sach-Fuß; Version für Damen .................................................................... 84 Quelle: http://www.teufel-international.com/uploads/pics/21419226.jpg Abbildung 80: erster Prototyp eines Smart Shirts ............................................................... 86 Quelle: http://static.howstuffworks.com/gif/computer-clothing-prototype.gif 131 Abbildung 81: Aufbau und Grundkomponenten eines Smart Shirts................................... 87 Quelle: http://ldt.stanford.edu/~jeepark/jeepark+portfolio/smartshirt_closer_large.jpg Abbildung 82: EKG-Modul ................................................................................................ 89 Quelle: http://www.innovations-report.de/bilder_neu/25389_ekg_tshirt.jpg Abbildung 83: Kommunikationsablauf ............................................................................... 90 Quelle: http://www.geo-view.net/dateien/schaubildekg.jpg Abbildung 84: Komponenten der LifeVest ......................................................................... 91 Quelle: http://www.lifecor.com/images/secondary/mouseovers/what_is_image_1.jpg Abbildung 85: Pulswellenermittlung .................................................................................. 97 Quelle: Handbuch der „Doktor Mouse“ Abbildung 86: grafische Darstellung der Messergebnisse ................................................ 100 Quelle: Screenshot Abbildung 87: textuelle Auswertung und Erklärung der Messergebnisse ........................ 101 Quelle: Screenshot Abbildung 88: Ergebnisse und Zusammenhänge über den Kenntnisstand von Wearables und der Berufsgruppe ............................................................................................................... 103 Abbildung 89: Akzeptanz und Einsatzchancen von medizinischen Wearables aus Sicht der Befragten ........................................................................................................................... 104 Abbildung 90: Attestierte gesundheitliche Probleme........................................................ 107 Abbildung 91: Messergebnisse eines männlichen Probanden .......................................... 107 Abbildung 92: Zielgruppen der „Doktor Mouse ............................................................... 110 Abbildung 93: abschließende Beurteilung der „Doktor Mouse“ ...................................... 111 Abbildung 94: Zielgruppen der „Doktor Mouse ............................................................... 114 Abbildung 95: abschließende Beurteilung der „Doktor Mouse“ ...................................... 115 Abbildung 96: Nutzen der „Doktor Mouse“ ..................................................................... 116 Tabelle A: Ergebnisse der Freitextbefragung .................................................................... 105 Tabelle B: Gründe für die fehlende Akzeptanz ................................................................. 108 Tabelle C: Nutzen der „Doktor Mouse“ ............................................................................ 109 Tabelle D: Zuverlässigkeit der „Doktor Mouse“ .............................................................. 112 132 Tabelle E: Ersatzpotential von medizinischen Wearables ................................................ 112 Tabelle F: Gründe für die fehlende Akzeptanz ................................................................. 112 Tabelle G: Nutzen der „Doktor Mouse“ ........................................................................... 113 Tabelle H: Nutzung des Computers .................................................................................. 118 133 Anhang Abbildung 1 134 Abbildung 2 135 Abbildung 3 (Seite 1/5) Bitte geben sie vor dem Ausfüllen des Fragebogens die aktuelle Uhrzeit an: 2. Fragen zum Messvorgang mit der „Doktor Mouse“ 2.1 Wie viele Messungen haben Sie vorgenommen? (max. 5) 2.2 Attestierte Ihnen „Doktor Mouse“ gesundheitliche Probleme? Wenn ja, welche? Mehrfachkreuzungen sind möglich. Nein Ja erhöhten/niedrigen Pulsschlag Herzmuskelschwäche Rhythmusstörungen Unregelmäßigkeiten während der Herzaktivität Probleme mit dem Gefäßwiderstand Probleme mit dem Gefäßtonus hohe/niedrige Cholesterinwerte erhöhten/niedrigen Blutdruck 2.3 Waren die Messergebnisse bei jeder Messung immer gleich? Wenn nein, wo traten Unterschiede auf? Mehrfachkreuzungen sind möglich. Nein Ja Messung: 1 2 3 4 5 erhöhter/niedriger Pulsschlag Herzmuskelschwäche Rhythmusstörungen Unregelmäßigkeiten während der Herzaktivität Probleme mit dem Gefäßwiderstand Probleme mit dem Gefäßtonus hohe/niedrige Cholesterinwerte hoher/niedriger Blutdruck Seite 1 136 Abbildung 3 (Seite 2/5) 3. Fragen zum Produkt „Doktor Mouse“ 3.1 Kannten Sie das Produkt „Doktor Mouse“ schon vorher? Wenn ja, woher? Nein Ja _______________________________ 3.2 Hatten Sie zuvor schon einmal Kontakt zu ähnlichen Produkten? Wenn ja, wie heiß es und welchen Zweck erfüllte es? Nein Ja _______________________________ _______________________________ _______________________________ _______________________________ 3.3 Würden Sie sich die „Doktor Mouse“ für den privaten Gebrauch zulegen? Nein 3.4 Ja Bei welchen Personengruppen halten Sie den Einsatz der „Doktor Mouse“ für sinnvoll? Mehrfachkreuzungen sind möglich. Kindern Kranken Jugendlichen Sportlern Erwachsenen Sonstige ________________________________________ älteren Menschen 3.5 Würden Sie sich mit diesem Produkt sicherer fühlen? Nein Ja Seite 2 137 Abbildung 3 (Seite 3/5) 3.6 Schätzen Sie die Untersuchungsergebnisse mit der „Doktor Mouse“ als zuverlässig ein? Wenn nein, warum nicht? Wenn ja, warum? Nein Ja ____________________________________________________ ____________________________________________________ ____________________________________________________ 3.7 Könnten Sie sich vorstellen, dass dieses und/oder ähnliche Produkte Ihre regelmäßigen ärztlichen Untersuchungen ersetzen? Wenn nein, warum nicht? Nein Ja ____________________________________________________ ____________________________________________________ ____________________________________________________ 3.8 Wie hoch schätzen Sie den Nutzen der „Doktor Mouse“ in den folgenden Punkten ein? hoch mittel niedrig ich weiß nicht kostensparendes Verfahren zeitsparendes Verfahren Zuverlässigkeit räumliche Flexibilität zeitliche Flexibilität 3.9 Bewerten Sie abschließend dazu, anhand Ihrer bisherigen Erkenntnisse das Produkt „Doktor Mouse“ ! sehr sinnvoll sinnvoll ausbaufähig nicht sinnvoll ich weiß nicht Seite 3 138 Abbildung 3 (Seite 4/5): 3.10 Anmerkungen 4. Allgemeine Fragen zur Person 4.1 Wie alt sind Sie? 4.2 Geben Sie Ihr Geschlecht an! männlich 4.3 weiblich Leiden Sie an einer der folgenden Krankheiten? Mehrfachkreuzungen sind möglich. Bluthochdruck Blutgefäßerkrankungen (z.B. mangelnde Gefäßelastizität) Blutunterdruck Erkrankungen im Zusammenhang mit schlechten Cholesterinwerten (z.B. Arteriosklerose) Herzrhythmusstörungen Pulsunregelmäßigkeiten hohem Puls Nein Nicht bekannt niedrigem Puls 4.4 In welcher körperlichen Verfassung befinden Sie sich? müde erschöpft krank normal 4.5 In welchem Umfeld arbeiten Sie hauptberuflich? Büro Bau zu hause Sonstiges _____________________________________ Seite 4 139 Abbildung 3 (Seite 5/5): 4.6 Wann nutzen Sie einen Computer? Mehrfachkreuzungen sind möglich. beruflich privat gar nicht 4.7 Wie viel Stunden am Tag nutzen Sie den Computer? 0-2 2-5 5 - 10 10 und mehr Bitte geben Sie die aktuelle Uhrzeit an: Seite 5 140 Abbildung 4 (Seite 1/8) Bitte geben sie jetzt die aktuelle Uhrzeit an: Umfrage zum Thema „Medizintechnische Wearables“ Einleitung Ursprünglich stammt das Wort „Wearable“ aus dem Englischen und bezeichnet streng genommen nichts weiter, als am Körper getragene Technik (auch: Wearable Electronics). Diese körpernahe Integration von miniaturisierter Computertechnik in beispielsweise Kleidung unterscheidet sich von der Verwendung anderer mobiler Computersysteme dadurch, dass die Tätigkeit des Benutzers nicht die Benutzung des Computers selbst ist, sondern eine durch den Computer unterstützte Tätigkeit in der realen Welt ist. Wearables stellen dem Nutzer demnach weitaus mehr als nur einen mobilen Arbeitsplatz zu Verfügung – sie übernehmen die Aufgabe eines unsichtbaren, intelligenten und persönlichen Assistenten, der nach dem „anytime, anything, anywhere“ – Prinzip arbeitet. Damit ein System als tragbar/wearable bezeichnet werden darf, muss es jedoch konkrete Charakteristika aufweisen: Wearables müssen aus der Bewegung heraus benutzt werden können. Wearables können durch gesprochene Sprache o.ä. kontrolliert werden, so dass beide Hände frei für andere Aufgaben sind. Wearables sind mit Sensoren zur Wahrnehmung der physikalischen Umwelt ausgestattet. Wearables sind immer funktionsbereit und versorgen den Benutzer autonom mit Informationen. Wearables nehmen kontinuierlich Daten auf und sind permanent im Einsatz. Wegen ihrer vielfältigen Einsatzmöglichkeiten eröffnen Wearables neue Perspektiven in der Anwendung. So finden sie sich schon heute in verschiedensten Bereichen, wie z.B. Militär, Medizin und Logistik wieder. Vor allem im medizinischen Sektor übernehmen Wearables erfolgreich die unterschiedlichsten Aufgaben. Dort dienen sie als Überwachungssysteme für die medizinische Vor- und Nachsorge oder Übernehmen gar Aufgaben defekter Körperfunktionen (Implantate als Extrem-Wearables). Derartige Systeme werden von den Patienten ständig am/im Körper getragen oder sind direkt unsichtbar in die Alltagskleidung integriert. Dadurch ermöglichen sie eine allgegenwärtige Kontrolle der Vitalfunktionen (Puls, Blutdruck, Körpertemperatur etc.) und können bei Notfällen völlig autonom Hilfe alarmieren oder selbst lebensrettende Maßnahmen einleiten. Seite 1 141 Abbildung 4 (Seite 2/8) Um die Möglichkeiten von medizinischen Wearables nochmals zu verdeutlichen, wird im Folgenden kurz das „Smart Shirt“ des amerikanischen Textilunternehmens SensaTex vorgestellt, dass auf die Entwicklung von intelligenten Kleidungsstücken spezialisiert ist. Das SensaTex Smart Shirt ist ein intelligentes T-Shirt, ausgestattet mit diverser Computertechnik und kann jederzeit wie gewöhnliche Alltagskleidung getragen werden. Eingebettete Sensoren überwachen dabei die Herzrate, die Atmung und andere Vitalfunktionen des Trägers. Die dadurch gesammelten Informationen werden dann kontinuierlich via Satellit oder Mobilfunk zu dem SensaTex Health Center übertragen, in welchem eine ständige Überwachung und Analyse der eingehenden Daten stattfindet. Beim Auffinden von gesundheitsgefährdeten Auffälligkeiten wird sofort ein medizinischer Notfalldienst alarmiert. Die Rettungssanitäter erhalten vom Health Center sowohl das Krankheitsbild als auch den Standort des Patienten und wissen dadurch schon vor ihrem Eintreffen beim Patienten über dessen körperliche Verfassung bescheid und können dementsprechend schnell medizinische Hilfemaßnahmen einleiten. Außerdem werden alle aufgezeichneten Vitaldaten der Träger eines Smart Shirts auf einer sicheren Internetseite abgelegt, so dass sich jeder Träger dort jederzeit und überall einloggen kann, um den Verlauf seiner Vitalfunktionen zu verfolgen. Das SensaTex Smart Shirt ermöglicht jedem Träger eine selbstverständliche Bewegungsfreiheit und einen uneingeschränkten Handlungsspielraum. Zusätzlich kann es wie jedes andere Kleidungsstück auch, gewaschen werden. Gerade aufgrund dieser überaus vorteilhaften Eigenschaften kann das Smart Shirt in sehr vielen Bereichen (z.B. beim Militär und Polizei zur Überwachung der Vitalfunktionen und zur Meldung von Verletzungen) eingesetzt werden. Seite 2 142 Abbildung 4 (Seite 3/8) 1. Allgemeine Fragen zu medizinischen Wearables 1.1 Kannten Sie den Begriff „Wearables“ und dessen Inhalt schon vor dieser Befragung? Wenn ja, woher? Nein Ja _______________________________ _______________________________ _______________________________ 1.2 Für wie wichtig halten Sie den Einsatz von Wearables im medizinischen Sektor? sehr wichtig wichtig nicht so wichtig unwichtig ich weiß nicht 1.3 Welche Probleme sehen Sie bei der Einführung von medizinischen Wearables auf dem Markt? 1.4 Welche Chancen sehen Sie in medizinischen Wearables? 1.5 Welche Risiken sehen Sie in medizinischen Wearables? Seite 3 143 Abbildung 4 (Seite 4/8) 2. Fragen zum Messvorgang mit der „Doktor Mouse“ 2.1 Wie viele Messungen haben Sie vorgenommen? (max. 5) 2.2 Attestierte Ihnen „Doktor Mouse“ gesundheitliche Probleme? Wenn ja, welche? Mehrfachkreuzungen sind möglich. Nein Ja erhöhten/niedrigen Pulsschlag Herzmuskelschwäche Rhythmusstörungen Unregelmäßigkeiten während der Herzaktivität Probleme mit dem Gefäßwiderstand Probleme mit dem Gefäßtonus hohe/niedrige Cholesterinwerte erhöhten/niedrigen Blutdruck 2.3 Waren die Messergebnisse bei jeder Messung immer gleich? Wenn nein, wo traten Unterschiede auf? Mehrfachkreuzungen sind möglich. Nein Ja Messung: 1 2 3 4 5 erhöhter/niedriger Pulsschlag Herzmuskelschwäche Rhythmusstörungen Unregelmäßigkeiten während der Herzaktivität Probleme mit dem Gefäßwiderstand Probleme mit dem Gefäßtonus hohe/niedrige Cholesterinwerte hoher/niedriger Blutdruck Seite 4 144 Abbildung 4 (Seite 5/8 ) 3. Fragen zum Produkt „Doktor Mouse“ 3.1 Kannten Sie das Produkt „Doktor Mouse“ schon vorher? Wenn ja, woher? Nein Ja _______________________________ 3.2 Hatten Sie zuvor schon einmal Kontakt zu ähnlichen Produkten? Wenn ja, wie heiß es und welchen Zweck erfüllte es? Nein Ja _______________________________ _______________________________ _______________________________ _______________________________ 3.3 Würden Sie sich die „Doktor Mouse“ für den privaten Gebrauch zulegen? Nein 3.4 Ja Bei welchen Personengruppen halten Sie den Einsatz der „Doktor Mouse“ für sinnvoll? Mehrfachkreuzungen sind möglich. Kindern Kranken Jugendlichen Sportlern Erwachsenen Sonstige ________________________________________ älteren Menschen 3.5 Würden Sie sich mit diesem Produkt sicherer fühlen? Nein Ja Seite 5 145 Abbildung 4 (Seite 6/8) 3.6 Schätzen Sie die Untersuchungsergebnisse mit der „Doktor Mouse“ als zuverlässig ein? Wenn nein, warum nicht? Wenn ja, warum? Nein Ja ____________________________________________________ ____________________________________________________ ____________________________________________________ 3.7 Könnten Sie sich vorstellen, dass dieses und/oder ähnliche Produkte Ihre regelmäßigen ärztlichen Untersuchungen ersetzen? Wenn nein, warum nicht? Nein Ja ____________________________________________________ ____________________________________________________ ____________________________________________________ 3.8 Wie hoch schätzen Sie den Nutzen der „Doktor Mouse“ in den folgenden Punkten ein? hoch mittel niedrig ich weiß nicht kostensparendes Verfahren zeitsparendes Verfahren Zuverlässigkeit räumliche Flexibilität zeitliche Flexibilität 3.9 Bewerten Sie abschließend dazu, anhand Ihrer bisherigen Erkenntnisse das Produkt „Doktor Mouse“ ! sehr sinnvoll sinnvoll ausbaufähig nicht sinnvoll ich weiß nicht Seite 6 146 Abbildung 4 (Seite 7/8): 3.10 Anmerkungen 4. Allgemeine Fragen zur Person 4.1 Wie alt sind Sie? 4.2 Geben Sie Ihr Geschlecht an! männlich 4.3 weiblich Leiden Sie an einer der folgenden Krankheiten? Mehrfachkreuzungen sind möglich. Bluthochdruck Blutgefäßerkrankungen (z.B. mangelnde Gefäßelastizität) Blutunterdruck Erkrankungen im Zusammenhang mit schlechten Cholesterinwerten (z.B. Arteriosklerose) Herzrhythmusstörungen Pulsunregelmäßigkeiten hohem Puls Nein Nicht bekannt niedrigem Puls 4.4 In welcher körperlichen Verfassung befinden Sie sich? müde erschöpft krank normal 4.5 In welchem Umfeld arbeiten Sie hauptberuflich? Büro Bau zu hause Sonstiges _____________________________________ Seite 7 147 Abbildung 4 (Seite 8/8): 4.6 Wann nutzen Sie einen Computer? Mehrfachkreuzungen sind möglich. beruflich privat gar nicht 4.7 Wie viel Stunden am Tag nutzen Sie den Computer? 0-2 2-5 5 - 10 10 und mehr Bitte geben Sie die aktuelle Uhrzeit an: Seite 8 148 Abbildung 5 (Seite 1/8) Bitte geben sie jetzt die aktuelle Uhrzeit an: Umfrage zum Thema „Medizintechnische Wearables“ Einleitung Ursprünglich stammt das Wort „Wearable“ aus dem Englischen und bezeichnet streng genommen nichts weiter, als am Körper getragene Technik (auch: Wearable Electronics). Diese körpernahe Integration von miniaturisierter Computertechnik in beispielsweise Kleidung unterscheidet sich von der Verwendung anderer mobiler Computersysteme dadurch, dass die Tätigkeit des Benutzers nicht die Benutzung des Computers selbst ist, sondern eine durch den Computer unterstützte Tätigkeit in der realen Welt ist. Wearables stellen dem Nutzer demnach weitaus mehr als nur einen mobilen Arbeitsplatz zu Verfügung – sie übernehmen die Aufgabe eines unsichtbaren, intelligenten und persönlichen Assistenten, der nach dem „anytime, anything, anywhere“ – Prinzip arbeitet. Damit ein System als tragbar/wearable bezeichnet werden darf, muss es jedoch konkrete Charakteristika aufweisen: Wearables müssen aus der Bewegung heraus benutzt werden können. Wearables können durch gesprochene Sprache o.ä. kontrolliert werden, so dass beide Hände frei für andere Aufgaben sind. Wearables sind mit Sensoren zur Wahrnehmung der physikalischen Umwelt ausgestattet. Wearables sind immer funktionsbereit und versorgen den Benutzer autonom mit Informationen. Wearables nehmen kontinuierlich Daten auf und sind permanent im Einsatz. Wegen ihrer vielfältigen Einsatzmöglichkeiten eröffnen Wearables neue Perspektiven in der Anwendung. So finden sie sich schon heute in verschiedensten Bereichen, wie z.B. Militär, Medizin und Logistik wieder. Vor allem im medizinischen Sektor übernehmen Wearables erfolgreich die unterschiedlichsten Aufgaben. Dort dienen sie als Überwachungssysteme für die medizinische Vor- und Nachsorge oder Übernehmen gar Aufgaben defekter Körperfunktionen (Implantate als Extrem-Wearables). Derartige Systeme werden von den Patienten ständig am/im Körper getragen oder sind direkt unsichtbar in die Alltagskleidung integriert. Dadurch ermöglichen sie eine allgegenwärtige Kontrolle der Vitalfunktionen (Puls, Blutdruck, Körpertemperatur etc.) und können bei Notfällen völlig autonom Hilfe alarmieren oder selbst lebensrettende Maßnahmen einleiten. Seite 1 149 Abbildung 5 (Seite 2/8) Um die Möglichkeiten von medizinischen Wearables nochmals zu verdeutlichen, wird im Folgenden kurz das „Smart Shirt“ des amerikanischen Textilunternehmens SensaTex vorgestellt, dass auf die Entwicklung von intelligenten Kleidungsstücken spezialisiert ist. Das SensaTex Smart Shirt ist ein intelligentes T-Shirt, ausgestattet mit diverser Computertechnik und kann jederzeit wie gewöhnliche Alltagskleidung getragen werden. Eingebettete Sensoren überwachen dabei die Herzrate, die Atmung und andere Vitalfunktionen des Trägers. Die dadurch gesammelten Informationen werden dann kontinuierlich via Satellit oder Mobilfunk zu dem SensaTex Health Center übertragen, in welchem eine ständige Überwachung und Analyse der eingehenden Daten stattfindet. Beim Auffinden von gesundheitsgefährdeten Auffälligkeiten wird sofort ein medizinischer Notfalldienst alarmiert. Die Rettungssanitäter erhalten vom Health Center sowohl das Krankheitsbild als auch den Standort des Patienten und wissen dadurch schon vor ihrem Eintreffen beim Patienten über dessen körperliche Verfassung bescheid und können dementsprechend schnell medizinische Hilfemaßnahmen einleiten. Außerdem werden alle aufgezeichneten Vitaldaten der Träger eines Smart Shirts auf einer sicheren Internetseite abgelegt, so dass sich jeder Träger dort jederzeit und überall einloggen kann, um den Verlauf seiner Vitalfunktionen zu verfolgen. Das SensaTex Smart Shirt ermöglicht jedem Träger eine selbstverständliche Bewegungsfreiheit und einen uneingeschränkten Handlungsspielraum. Zusätzlich kann es wie jedes andere Kleidungsstück auch, gewaschen werden. Gerade aufgrund dieser überaus vorteilhaften Eigenschaften kann das Smart Shirt in sehr vielen Bereichen (z.B. beim Militär und Polizei zur Überwachung der Vitalfunktionen und zur Meldung von Verletzungen) eingesetzt werden. Informationen zum Produkt „Doktor Mouse“ Um die Fragen zu Abschnitt 3 beantworten zu können, muss der nachfolgende kurze Text zum Produkt „Doktor Mouse“ durchgelesen werden. Bei der Beantwortung der Fragen, sollte vorausgesetzt werden, dass das Gerät korrekt funktioniert und so arbeitet wie anschließend beschrieben. Die „Doktor Mouse“ ist eine Hard- und Softwarekombination, des russischen Unternehmens RILA GmbH, zum Testen und Überwachen des Herzkreislaufsystems. Dieses Gesamtpaket enthält neben der Software für die Datenverarbeitung einen optischen Infrarotsensorblock, bestehend aus einem verkleinerten Infrarotstrahler und einem Photosensor (optoelektrischer Sensor), zur Erfassung aller relevanten Daten, die für Kontrolle des Herzkreislaufs notwendig sind. Zurzeit befindet sich dieser Sensorblock in einer getrennt funktionellen Einheit, die über einen seriellen Port (USB, COM) an den PC angeschlossen wird und keine zusätzliche Energiequelle benötigt. In Zukunft soll dieser Sensor jedoch in eine gewöhnliche Computermaus integriert werden, so dass PC-User während ihrer Arbeit am PC ihr Herzkreislaufsystem kontrollieren und aufzeichnen können. Seite 2 150 Abbildung 5 (Seite 3/8) Die „Doktor Mouse“ nutzt eine spezielle Analysetechnik, die Pulswellenanalyse, um das Herzkreislaufsystem des Anwenders zu beurteilen. Als Ergebnis werden dem Anwender insgesamt 8 physiologische Größen, die den Zustand des Herzkreislaufs widerspiegeln, präsentiert. Diese 8 Größen sind: die Pulsschlagrate; die Variationsbreite, die maßgebend für den Herzrhythmus ist; der Variationskoeffizient, der Unregelmäßigkeiten während der Herzaktivität aufdeckt; der Gefäßwiderstand; der Gefäßtonus, der der Gefäßelastizität entspricht; der Blutdruck; der Cholesterinwert und die „Zeit der maximalen Belastung“, die mit der Herzmuskelkontraktion einhergeht. Der gesamte Prozess des Messens sowie die Auswertung und Betrachtung der Messergebnisse beansprucht 2 – 3 Minuten. Zudem verursacht dieses Messverfahren keinerlei unangenehme und schmerzhafte Empfindungen und ist leicht handhabbar. Die Einsatzziele der „Doktor Mouse“ sind: regelmäßige und systematische Beobachtungen des Herzkreislaufsystems, um Unregelmäßigkeiten aufzudecken und entsprechende Gegenmaßnahmen einzuleiten, damit eventuell auftretende schwerwiegende Komplikationen vermieden werden können. Benutzer des Systems bekommen so ebenfalls die Möglichkeit, ihre, zu unterschiedlichen Zeiten, genommenen Messergebnisse miteinander zu vergleichen und dadurch Abhängigkeiten zwischen der Herztätigkeit und äußeren Einflüssen (physische und nervliche Belastungen) aufzuspüren. Dadurch können sie dann den zulässigen Grad der äußeren Einflüsse einwandfrei bestimmen und entsprechend, durch Abbau der negativen äußeren Einflüsse, gesundheitsfördernd auf ihre Herzaktivität Einfluss nehmen. regelmäßige und systematische Beobachtungen des Herzkreislaufsystems, um die Wirksamkeit von Medikamenten zu bestimmen. In diesem Fall erlaubt das System die Überwachung von Behandlungsprozessen mit medizinischen Präparaten, die sich direkt auf die Herz- und Gefäßtätigkeit auswirken und somit den Erfolg oder Misserfolg einer medikamentösen Behandlung anzeigen. die regelmäßige Überwachung des Herzkreislaufsystems während sportlicher Aktivitäten/Training. die Kontrolle der Herztätigkeit nach einer Drogen- oder Alkoholvergiftung. die Kontrolle des Herzkreislaufsystems während einer Erkältung oder bei Infektionskrankheiten. die Kontrolle der Herztätigkeit während einer Entspannungs-/Ruhephase. Dies ist nur ein Teil einer Liste von Situationen, bei denen die „Doktor Mouse“ verwendet werden kann. Seite 3 151 Abbildung 5 (Seite 4/8) 1. Allgemeine Fragen zu medizinischen Wearables 1.1 Kannten Sie den Begriff „Wearables“ und dessen Inhalt schon vor dieser Befragung? Wenn ja, woher? Nein Ja _______________________________ _______________________________ _______________________________ 1.2 Für wie wichtig halten Sie den Einsatz von Wearables im medizinischen Sektor? sehr wichtig wichtig nicht so wichtig unwichtig ich weiß nicht 1.3 Welche Probleme sehen Sie bei der Einführung von medizinischen Wearables auf dem Markt? 1.4 Welche Chancen sehen Sie in medizinischen Wearables? 1.5 Welche Risiken sehen Sie in medizinischen Wearables? Seite 4 152 Abbildung 5 (Seite 5/8 ) 3. Fragen zum Produkt „Doktor Mouse“ 3.1 Kannten Sie das Produkt „Doktor Mouse“ schon vorher? Wenn ja, woher? Nein Ja _______________________________ 3.2 Hatten Sie zuvor schon einmal Kontakt zu ähnlichen Produkten? Wenn ja, wie heiß es und welchen Zweck erfüllte es? Nein Ja _______________________________ _______________________________ _______________________________ _______________________________ 3.3 Würden Sie sich die „Doktor Mouse“ für den privaten Gebrauch zulegen? Nein 3.4 Ja Bei welchen Personengruppen halten Sie den Einsatz der „Doktor Mouse“ für sinnvoll? Mehrfachkreuzungen sind möglich. Kindern Kranken Jugendlichen Sportlern Erwachsenen Sonstige ________________________________________ älteren Menschen 3.5 Würden Sie sich mit diesem Produkt sicherer fühlen? Nein Ja Seite 5 153 Abbildung 5 (Seite 6/8) 3.6 Schätzen Sie die Untersuchungsergebnisse mit der „Doktor Mouse“ als zuverlässig ein? Wenn nein, warum nicht? Wenn ja, warum? Nein Ja ____________________________________________________ ____________________________________________________ ____________________________________________________ 3.7 Könnten Sie sich vorstellen, dass dieses und/oder ähnliche Produkte Ihre regelmäßigen ärztlichen Untersuchungen ersetzen? Wenn nein, warum nicht? Nein Ja ____________________________________________________ ____________________________________________________ ____________________________________________________ 3.8 Wie hoch schätzen Sie den Nutzen der „Doktor Mouse“ in den folgenden Punkten ein? hoch mittel niedrig ich weiß nicht kostensparendes Verfahren zeitsparendes Verfahren Zuverlässigkeit räumliche Flexibilität zeitliche Flexibilität 3.9 Bewerten Sie abschließend dazu, anhand Ihrer bisherigen Erkenntnisse das Produkt „Doktor Mouse“ ! sehr sinnvoll sinnvoll ausbaufähig nicht sinnvoll ich weiß nicht Seite 6 154 Abbildung 5 (Seite 7/8): 3.10 Anmerkungen 4. Allgemeine Fragen zur Person 4.1 Wie alt sind Sie? 4.2 Geben Sie Ihr Geschlecht an! männlich 4.3 weiblich Leiden Sie an einer der folgenden Krankheiten? Mehrfachkreuzungen sind möglich. Bluthochdruck Blutgefäßerkrankungen (z.B. mangelnde Gefäßelastizität) Blutunterdruck Erkrankungen im Zusammenhang mit schlechten Cholesterinwerten (z.B. Arteriosklerose) Herzrhythmusstörungen Pulsunregelmäßigkeiten hohem Puls Nein Nicht bekannt niedrigem Puls 4.4 In welcher körperlichen Verfassung befinden Sie sich? müde erschöpft krank normal 4.5 In welchem Umfeld arbeiten Sie hauptberuflich? Büro Bau zu hause Sonstiges _____________________________________ Seite 7 155 Abbildung 5 (Seite 8/8): 4.6 Wann nutzen Sie einen Computer? Mehrfachkreuzungen sind möglich. beruflich privat gar nicht 4.7 Wie viel Stunden am Tag nutzen Sie den Computer? 0-2 2-5 5 - 10 10 und mehr Bitte geben Sie die aktuelle Uhrzeit an: Seite 8 156
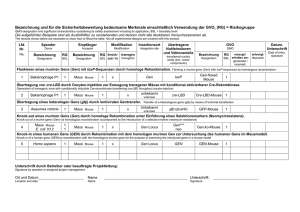










![Update autologe Stammzelltransplantation [Schreibgeschützt]](http://s1.studylibde.com/store/data/001930173_1-7b08e1fb1ce1458cbe1706c7479edd48-300x300.png)