Kapitel 12 (bis zum 12.6.)
Werbung

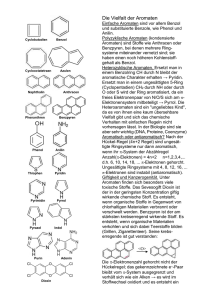
12. Aromaten 12.1 Einleitung: der aromatische Zustand Tafelbild: Vergleiche - Hexatrien / Cyclohexatrien - Butadien / Cyclobutadien Cyclisch, planar, konjugiert, 4n + 2 -Elektronen Tafelbilder: diverse Aromaten (Cyclopropanyl-Kation, Cyclopentadienyl-Anion, ...) Video: Salomons: -Orbitale des Benzene Tafelbild: Berechnung der Resonanzenergie: Hydrierung von Cyclohexen, Cyclohexadien, Benzol 1-1 Kriterien der Aromatizität: - konjugiertes -System - cyclisch - planar - Hückelregel 4n+2 -Elektronen - Resonanzenergie - Diamagnetismus, Ringstrom Chemische Eigenschaften - Geruch und Brennverhalten - Substitution statt Addition Physikalische Eigenschaften Diamagnetismus besondere optische Eigenschaften - hoher Brechungsindex, Dispersion, .. - Farben, Photoleiter besondere elektronische Eigenschaften - UV Spektrum, .. Biologische Eigenschaften - nicht-bindende Wechselwirkungen (u.a. -Stacking) 1-2 -Molekülorbitale des Benzols 1-3 Zeichnungen nach Frost und Musulin - Kreis mit Radius 2 - regelmäßiges Vieleck mit Spitze nach unten einzeichnen - Schnittpunkt der Ecken mit dem Kreis ergibt die Energie-Niveaus Cyclopropenylium Cyclobutadien Benzol Zeichnungen: J. Voß 1-4 UV Spektrum des Benzols Quelle: J. Voß Siehe auch: H.-H. Perkampus, „UV-VIS Atlas of Organic Compounds“, 2nd Ed. 1992: Part 2, Spectra D1/1 1-5 1 H-NMR der Aromaten B0 H H Abb.: Aromatischer Ringstrom H H H H H H H H H H H H H H H H H H ( H außen) = 9.28 (H innen) = -2.99 H H H CH3 (Ring) = 7.27; 6.95 (CH2) = -0.51 (Ring) = 8.14-8.64 (CH3) = -4.25 1-6 12.2 Geschichte, Vorkommen der Aromaten Geruch, chemische Verwandtschaft bei Reaktionen Aromastoffe, Farbstoffe, Holz, Graphit, Teer (Extrafolie: Struktur der Steinkohle) (Extrafolie: Struktur des Lignin) Abb.: Huminstoffmodell (G. Eisenbrand, M. Metzler, Toxikologie für Chemiker) 1-7 Struktur des Lignins H. Nimz, Angew. Chem. 86, 336 (1974) 1-8 Struktur der Steinkohle Shinn, zitiert in Nachr. Chem. Tech. Lab. 34, 968 (1986) 1-9 Typische aromatische Verbindungen Aldehyde gehören zu den ersten isolierten und synthetisierten aromatischen Verbindungen. OH O MeO O O H H MeO HO H (1) O (2) (3) H (4) O O O O H (5) (6) H Abb.: Benzaldehyd (1); Anisaldehyd (2); Salicylaldehyd (3); Vanillin (4); Piperonal (5); Zimtaldehyd (6) Benzaldehyd wurde 1837 von Liebig und Wöhler aus Bittermandelöl isoliert. Zimtaldehyd wurde 1834 von Dumas und Péligot aus Zimtöl isoliert und 1856 von Chiozza synthetisiert. 1-10 Die ersten Farbstoffe: Me N Me HN N NH 2 Me Mauvein, 1856 von Perkin durch Ox. von unreinem Anilin dargestellt O OH OH O Alizarin, technische Synthese ab 1869 O HN NH O Indigo, technische Synthese ab 1890 1-11 Das aromatische Zeitalter: Bis ca. 1950 war die organische Chemie größtenteils durch die Chemie der Aromaten bestimmt. Alte Syntheseroute für Nylon und Perlon (links, aus Aromaten) und moderner Zugang (rechts, aus Aliphaten). Kohle Erdol Pyrolyse Teer Destillation Destillation Extraktion Phenol Benzin Reformierung Benzol Platforming + 3 H2 1. Cl 2, 2. NaOH Cyclohexan + 3 H2 Cl-NO / h Cyclohexanol - HCl - H2 NH 2OH Cyclohexanon Cyclohexanonoxim BeckmannUmlagerung Adipinsaure -Caprolactam Nylon Perlon 1-12 Geschichte des Benzols Ursprung des Namens Benzol: Benzoeharz Benzin Benzol (Öl) Phen (gr.: phainein = ans Licht bringen) [6] Annulen / engl.: benzene 1825 isolierte Faraday 3 g Benzol aus dem Pyrolysat von Walöl (Leuchtöl). 1834 erhielt Mitscherlich Benzol durch Decarboxylierung von Benzoesäure. 1845 wies Hofmann Benzol im Steinkohlenteer nach. 1865 erstellte Kekulé das Modell der alternierenden Einfach- und Doppelbindungen. Es ließen sich jedoch keine zwei Isomere nachweisen. Cl Cl Cl Cl Abb. 1: Mögliche Isomere bei alternierender Einfach- und Doppelbindung 1-13 1872 Kekulé formulierte die Oszillations-Hypothese Abb. 2: Kekulé's Oszillationshypothese Alternative Formulierungen: (1) (2) (3) (4) (5) Abb. 3: Verschiedene elektronische Formulierungen des Benzols: Claus (1867) 1; Dewar (1867) 2, Ladenburg (1869) 3; Armstrong (1887) Bayer (1888) 4; Thiele (1899) 5 Einige dieser Strukturisomere konnten in neuerer Zeit synthetisiert werden, z.B.: hv hv oder hv Benzvalen oder hv Fulven hv hv oder hv Bicyclo[2.2.0]-hexa-2,5-dien Prisman Abb.: Bicyclo[2.2.0]hexa-2,5-dien: van Tamelen (1963); Prisman: Katz (1973); Benzvalen: Viehe (1964). 1-14 Nachweis der Struktur des Benzols: Es existiert nur ein monosubstituiertes Produkt (alle 6 C’s sind gleichwertig): R mono Es gibt nur drei disubstituierte Produkte: R R R R R di R Bei fixierten Einfach- und Doppelbindungen wären 5 Produkte zu erwarten: R R R R R R R R R* R Bei fixierten Doppelbindungen eines reinen Isomers würden zwei Produkte erwartet. Die Ozonolyse von o-Xylol ergibt jedoch drei Produkte: (OHC-CHO, OHC-CO-Me, Me-CO-CO-Me) Me Me Me Me Me Me O O O O O O Me O O Me O O O O 1-15 Nicht-benzoide aromatische Systeme Cyclopropyliumkation Cyclobutenyliumdikation Cyclopentadienyliumanion Tropyliumkation Cycloheptatrienyliumdikation Anti-Aromaten: (a) (b) Abb. : Molekülorbitalenergiediagramm des Cyclopentadienylanions (a) und des planaren Cyclooctatetraens (b) 1-16 12.3. Elektrophile Substitution der Aromaten Beispiele: Cyclohexen + Br2: Add. des Elektrophils + Add. des Nukleophils Benzen: Add. des Elektrophils + Eli. eines Elektrophils + E H E H+ Energie E X H + X X E + E+ H+ + X X Reaktionskoordinate 1-17 Arenium-Ion Mechanismus, SE1 X X +Y langsam Y Y -X schnell + Abb.: Arenium-Mechanismus: -Komplex, Wheland Zwischenverbindung, Arenium-Ion H EtF BF3, - 80°C Et + BF4 + (1) Abb. 2: 2-Ethylmesityltetrafluoroborat 1 V.A. Koptyug, „Topics in Current Chemistry 3: Arenium Ions - Structure and Reactivity“, Top. Curr. Chem. 122, 1-245 (1984) Benzol in SbF5 - HSO3F, -120°C : Benzenium-Kation sichtbar im 1H-NMR. Achtung: Diese -Komplexe sind Zwischenprodukten der SE-Reaktion . 1-18 nicht identisch mit den echten -Komplex X X Y+ + Y+ Abb.: -Komplex G. A. Olah, „Mechanism of Electrophilic Aromatic Substitutions“, Acc. Chem. Res. 4, 240-248 (1971). Ferner: -Komlexe zwischen Aromaten und I2, Pikrin-Säure etc. Achtung: diese -Komplexe sind Übergangszuständen der SE-Reaktion nicht identisch mit den echten -Komplexe als Zwischenprodukte der SE-Reaktion werden heute nicht mehr formuliert. Wichtige Reaktionen: - Nitrierung - Sulfonierung - Halogenierung - Alkylierung / Acylierung nach Friedel-Crafts 1-19 Nitrierung und Nitrosierung ArH + NO2+ ArNO2 + H+ Weniger reaktive Aromaten können mit konz. Salpetersäure und Schwefelsäure nitriert werden: HNO3 + NO2+ + H3O+ + 2 HSO4- 2 H2SO4 Reaktive Aromaten lassen sich mit Salpetersäure allein nitrieren. Meist in Wasser, Essigsäure oder Essigsäureanhydrid: NO2+ + NO3- + H2O 2 HNO3 Mit N2O5 in Tetrachlorkohlenstoff in Gegenwart von P 2O5 kann unter wasserfreien Bedingungen nitriert werden: NO2+ + NO3- N2O5 J.W. Fischer, in H. Feuer, A.T. Nielsen, „Nitro Compounds, Recent Advances in Synthesis and Chemistry“, VCH, New York, 1990, 267-365. ArH + NO+ ArNO + H+ H3O+ + 2 NO3- + NO+ HNO2 + 2 HNO3 Das NO+ ist 1014 mal reaktiver als NO2+ OH OH OH NO3- NO+ OH + HNO3 - HNO2 H NO NO NO2 Abb. Selbstkatalyse von Spuren an salpetriger Säure in Salpetersäure 1-20 Sulfonierung Das elektrophile Agenz ist SO3: 2 H2SO4 SO3 + H3O+ + HSO4Ar-H Ar-SO3H Sulfonierungsreaktionen sind oft reversibel. Halogenierung Aktivierung durch Lewis-Säuren: Br2 + AlBr3 Alkylierung / Acylierungen nach Friedel-Crafts Mehrfach Alkylierungen, oft Umlagerung zum stabileren Carbenium vor der Substitution Ph-H + CH3-CH2-CH2-Br Ph-CH(CH3)2 (Hauptprodukt) + Ph-CH2-CH2CH3 1-21 Zweit-Substitution Ortho, Meta, Para, Ipso Dirigierende Wirkung von Substituenten Reaktivität Substituenten, die die Reaktivität des Aromaten erhöhen: +I +M>-I + M; +I Alkylgruppen -OH < -NH2 < -NHR < R2(-SR), (-SH) -O-, (-S-) Substituenten, die die Reaktivität des Aromaten vermindern - M; - I +M<-I -I -CHO, -COR, -COOH, -COOR, -CN, NO2, CONR2, -CONHR, -CONH2, -SO3H Halogene NR3+, -CF3, -CCl3, NH3+, SR2+, -PR3+ 1-22 Z Z Z H H E E Z Z E Z H H E H E Z E H E Z H E Z H E H Abb.: Mesomere Grenzstrukturen des -Komplexes bei einem elektronenziehenden Substituenten; metadirigierend 1-23