Diest ist ein Test - UK-Online
Werbung

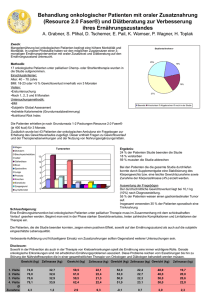
Wirksamkeit und Verträglichkeit rezeptfreier Nasensprays: Eine vergleichende Untersuchung von Medizinprodukten und Pharmaka bei Patienten mit saisonaler allergischer Rhinokonjunktivitis L. A. Weston, R. Mösges Institut für Medizinische Statistik, Informatik und Epidemiologie der Universität zu Köln 1 Einleitung 2 Über 20% der europäischen Bevölkerung leidet an allergischer Rhinokonjunktivitis [2, 4]. Da eine Allergenkarenz schwer einzuhalten ist und die spezifische Immuntherapie mit dem Risiko systemischer Nebenwirkungen einhergeht [2, 5], kommt der symptomatischen Therapie eine wichtige Rolle zu. Mehrere Studien konnten zeigen, dass nasal applizierte Liposomen zu einer Symptomreduktion bei Patienten mit saisonaler allergischer Rhinokonjunktivitis führen [1, 10]. Eine Vorläuferstudie (MeyerGutknecht 2008) schrieb dem liposomalen Nasenspray LipoNasal eine solche Wirkung zu [7]. Im Rahmen der vorliegenden Studie wurden die Eigenschaften des Medizinprodukts LipoNasal bei der Therapie einer saisonalen allergischen Rhinokonjunktivitis durch Baumpollen genauer untersucht. Neben der Wirksamkeit wurden auch die Verträglichkeit sowie der Einfluss auf die Lebensqualität dokumentiert. Für eine vergleichende Einordnung der Ergebnisse wurden dieselben Parameter parallel für das Zellulosespray Nasaleze und die leitliniengemäße Therapie, eine Kombination aus nasalem Antihistaminikum und Glucocorticosteroid [6] (Livocab und Livocab mit Beclomethason), erhoben. 3 Material und Methoden Diese prospektive, kontrollierte, offene Beobachtungsstudie (AWB) fand monozentrisch statt. 64 Patienten mit saisonaler allergischer Rhinokonjunktivitis durch Baumpollen wurden nach Maßgabe ihrer Beschwerden vom Prüfarzt auf drei Behandlungsarme verteilt: LipoNasal: N = 24; Nasaleze: N = 24; Livocab + LivocabBeclo: N = 16 Die AWB umfasste einen Beobachtungszeitraum von einer Woche mit jeweils einer Visite am ersten und am letzten Tag. Die Wirksamkeit wurde anhand des bei den beiden Visiten und täglich vom Patienten im Tagebuch dokumentierten nasalen und konjunktivalen Symptomscores ermittelt. Zur Untersuchung der Verträglichkeit diente die Nasenspray-Sensorik-Skala [8]. Die Lebensqualität wurde mittels der RHINASTHMA-Lebensqualitätsskala [9] untersucht. Ergebnisse 3.1 Wirksamkeit LipoNasal führte zu einer signifikanten Verbesserung der nasalen (p = 0,003) und konjunktivalen (p = 0,005) Symptome. Daraus resultierte eine ebenfalls signifikante Verbesserung des rhinokonjunktivalen Symptomscores (p = 0,002) (s. Tabelle 2) von 7,54±3,064 auf 4,42±3,092 (s. Tabelle 1). Gleichermaßen signifikant war die Symptomverbesserung durch die Kombination von Livocab und LivocabBeclo wie auch durch das andere Medizinprodukt. Beobachtet man den rhinokonjunktivalen Symptomscore im Verlauf des Behandlungszeitraums von einer Woche, so wird auch hier der ähnliche Behandlungserfolg deutlich. Sowohl die beiden Medizinprodukte, als auch das Pharmakotherapeutikum führten innerhalb von zwei Behandlungstagen zu einem relativ konstanten Symptomscore und pendelten ab Tag 3 morgens um den Wert 4,0 (s. Abbildung 1). Betrachtet man allerdings die Symptomreduktion, so zeigen sich Unterschiede (s. Abbildung 2), da die Behandlungsgruppen verschiedene Ausgangsscores hatten. Patienten, die LipoNasal erhielten, hatten den niedrigsten Symptomscore bei Visite 1 und verzeichneten somit auch die geringste Symptomreduktion. Dieser Unterschied erwies sich allerdings beim Area under the curve-Vergleich des baseline-adjustierten Wochenverlaufs als nicht signifikant (p = 0,127) (s. Tabelle 3 und 4). 8 LipoNasal Wilcoxon-Test: Vergleich der Mi ttelwerte des rhinokonjunktivalen Symptomscores bei Visite 1 und Visite 2 fr die drei Behandlungsgruppen -1 Wilcoxon-Test p-Wert Tabe l e 2: LipoNasal 0,002 Nasaleze 0,001 Livocab + LivocabBeclo 4 2 Statistik Gruppe Area under the curve MW SD Tabe l e 3: Ta g Vi si te 1 1 m or Ta ge g ns 1 ab Ta en g ds 2 m or Ta ge g ns 2 ab Ta en g ds 3 m or Ta ge g ns 3 ab Ta en g ds 4 m or Ta ge ns g 4 ab Ta en g ds 5 m or Ta ge g ns 5 ab Ta en g ds 6 m or Ta ge g ns 6 ab Ta en g ds 7 m or Ta ge g ns 7 ab Ta en g ds 8 m or ge ns Vi si te 2 0 Beobachtungstage LipoNasal -3,0664 3,36824 Nasaleze -5,2122 4,44603 Livocab + LivocabBeclo -4,5039 1,92952 Mittelwert (MW) und Standardabweichung (SD) der Area under the curve des baseline-adjustierten Verlauf des rhinokonjunktivalen Symptomscores fr die drei Behandlungsgruppen Kruskal-Wallis-H-Test Tabe l e 4: p-Wert 0,127 m or 1 0 Gruppe Nasaleze 6 Livocab + LivocabBeclo -4 4,22 x 10 Statistik 1 10 Mittelwert (MW ) und Standardabweichung (SD) des rhinokonjunktivalen Symptomscores (RKS) bei Visite 1 und Visite 2 fr die drei Behandlungsgruppen ge ns ab Ta en g ds 2 m Ta or ge g 2 ns ab Ta en g ds 3 m Ta or ge g 3 ns ab Ta en g ds 4 m Ta or ge g 4 ns ab Ta en g ds 5 m Ta or ge g 5 ns ab Ta en g ds 6 m Ta or ge g 6 ns ab Ta en g ds 7 m Ta or ge g 7 ns ab Ta en g ds 8 m Vi or si te gen s 2 rhinokonjunktivaler Symptomscore Tabe l e 1: 10,0 3,800 5,30 4,172 Abbildung 2: Verlauf des rhinokonjunktivalen Symptomscores (baseline-adjustiert) 1 RKS Visite 2 7,54 3,064 4,42 3,092 Livocab + LivocabBeclo 8,94 2,645 3,31 2,024 Ta g MW SD MW SD Nasaleze Ta g RKS Visite 1 LipoNasal Vi si te 12 Gruppe rhinokonjunktivaler Symptomscore (baseline-adjustiert) Abbildung 1: Verlauf des rhinokonjunktivalen Symptomscores Statistik -2 -3 LipoNasal Nasaleze -4 Livocab + LivocabBeclo -5 -6 -7 Kruskal-Wallis-H-Test: Vergleich der Area under the c urve des baselineadjustierten Verlaufs des rhinokonjunkt ivalen Sympt omscores der drei Behandlungsgruppen 3.2 Verträglichkeit Die Verträglichkeit aller drei Behandlungsarten war gut. Es kam zu keinerlei Nebenwirkungen. Bei der Auswertung der Nasenspray-Sensorik-Skala zeigten sich Unterschiede zwischen den drei Behandlungsarten. In Bezug auf Geruch und Geschmack schnitt LipoNasal schlechter ab als die beiden anderen Produkte. Bei der Einschätzung der Nasenbefeuchtung erhielt es dagegen die beste Beurteilung. (s. Tabelle 5). Da die Nasenspray-Sensorik-Skala jedoch nur bei Visite 1 erhoben wurde und mehrere Patienten initiativ im Nachgespräch äußerten, dass sie sich an den Geruch und den Geschmack von LipoNasal gewöhnt und diese Parameter am Ende der Beobachtungswoche besser bewertet hätten, müssen die Ergebnisse zur Verträglichkeit als vorläufig angesehen werden. In eine Folgestudie 2009 wird die Sensorik der Nasensprays über einen längeren Zeitraum hinweg untersucht. 3.3 Lebensqualität Der Globalscore der RHINASTHMA-Lebensqualitätsskala verbesserte sich bei den Patienten aller Behandlungsgruppen signifikant (s. Tabelle 6 und 7). Zu keinem der Erhebungszeitpunkte trat eines der drei Behandlungsmittel durch eine signifikant bessere Lebensqualität im Vergleich zu den anderen Therapeutika hervor (s. Tabelle 8) Beobachtungstage Statistik Gruppe Geruchsintensit t MW SD MW SD MW SD Geschmacksintensitt Einsch t z ung der Nasenbefeuchtung LipoNasal Nasaleze 38 30,8 69 31,8 63 19,4 71 30,1 78 27,9 24 21,3 Livocab + LivocabBeclo 76 20,1 80 19,4 57 19,2 Tabelle 5: Ergebnisse von drei der 14 items aus der Nasenspray-Sensorik-Skala Statistik Gruppe Globalscore Visite 1 MW SD MW SD Globalscore Visite 2 LipoNasal Nasaleze 1,38 0,476 1,23 0,493 1,50 0,569 1,20 0,677 Livocab + Licocab Beclo 1,45 0,458 1,12 0,416 Tabe lle 6: Mittelwert (MW) und Standardabweichung (SD) des Globalscores RHINASTHMA-Lebensqualittsskala fr die drei Behandlungsgruppen Statistik Gruppe LipoNasal Nasaleze -4 der Livocab + Licocab Beclo 0,002 Globalscore Visite 2 Š p-Wert 0,002 1,06x10 Globalscore Visite 1 Tabelle 7: Wilcoxon-Test: Vergleich der Globalscores der RHINASTHMA-Lebensqualittsskala bei Visite 1 und 2 fr die drei Behandlungsgruppen Kruskal-Wallis-H-Test Visite 1 Kruskal-Wallis-H-Test Visite 2 p- Wert 0,826 0,750 Tabe lle 8: Kruskal-Wallis-H-Test: Vergleich der Globalscores der Lebensqualittsskala bei Visite 1 und Visite 2 frdie drei Behandlingsgruppen 4 RHINASTHMA- Zusammenfassung Die Behandlung der Baumpollenallergie mit LipoNasal führt zu signifikanter Symptomreduktion und signifikanter Verbesserung der Lebensqualität. Darin unterscheidet es sich darin nicht signifikant von der leitliniengemäßen Therapie mit einem Antihistamin- und Glucocoticosteroid-Spray. Die Verträglichkeit von LipoNasal ist gut. 5 Literatur 1 Andersson M, Greiff L, Wollmer P. Nasal treatment with microemulsion reduces allergen challenge-induced symptoms and signs of allergic rhinitis. Acto Oto-Laryngologica 2008; 128(6):666-669 2 Bauchau V, Durham SR. Prevalence and rate of diagnosis of allergic rhinitis in Europe. European Respiratory Journal 2004; 24(5):758-764 3 Bousquet J et al. Allergic rhinitis and its impact on asthma (ARIA) 2008 update. Allergy 2008; 63(Suppl.86):8-160 4 Heinrich J, Richter K, Frye C, Meyer I, Wölke G, Wjst M, Nowak D, Magnussen H, Wichmann HE. Die Europäische Studie zu Atemwegserkrankungen bei Erwachsenen (ECRHS): Bisherige Ergebnisse und der Beitrag der beiden deutschen Studienzentren. Pneumologie 2002; 56:297-303 5 Frew AJ, Powell RJ, Corrigan CJ, Durham SR. Efficacy and safety of specific immunotherapy with SQ allergen extract in treatment resistant seasonal allergic rhinoconjunctivitis. Journal of Allergy and Clinical Immunology 2006; 117:319-325 6 Kaliner MA. A novel and effective approach to treating rhinitis with nasal antihistamines. Annals of Allergy, Asthma and Immunology 2007; 99(5):383-390 7 Meyer-Gutknecht H, Mösges R. Wirkung eines neuartigen liposomalen Nasensprays auf die Symptome der saisonalen allergischen Rhinitis. HNO Kompakt 2008; Suppl.1:1-5 8 Mösges R, Pasch N, Sayar A, Schmalz P, Vent J. Erhebung der sensorischen Wahrnehmung und subjektiven Patienteneinschätzung bei der Verabreichung von Nasenspray Die Nasenspray-Sensorik-Skala. Larynogo-Rhino-Otologie 2009 9 Mösges R, Schmalz P, Köberlein J, Kaciran M, Baiardini I. RHINASTHMA-Lebensqualitätsskala German Adapted Version - Validierung einer neuartigen krankheitsspezifischen Lebensqualitätsskala für Patienten mit allergischer Rhinitis und bronchialer Hyperreaktivität. HNO 2007; 55:357-364 10 Schwetz S, Olze H, Melchtsedech S, Grigorov A, Latza R. Efficacy of pollen blocker cream in the treatment of allergic rhinitis. Archives of Otolaryngology – Head and Neck Surgery 2004; 140:979-984