Pathologie und moderne Diagnostik des Ovarialkarzinoms
Werbung
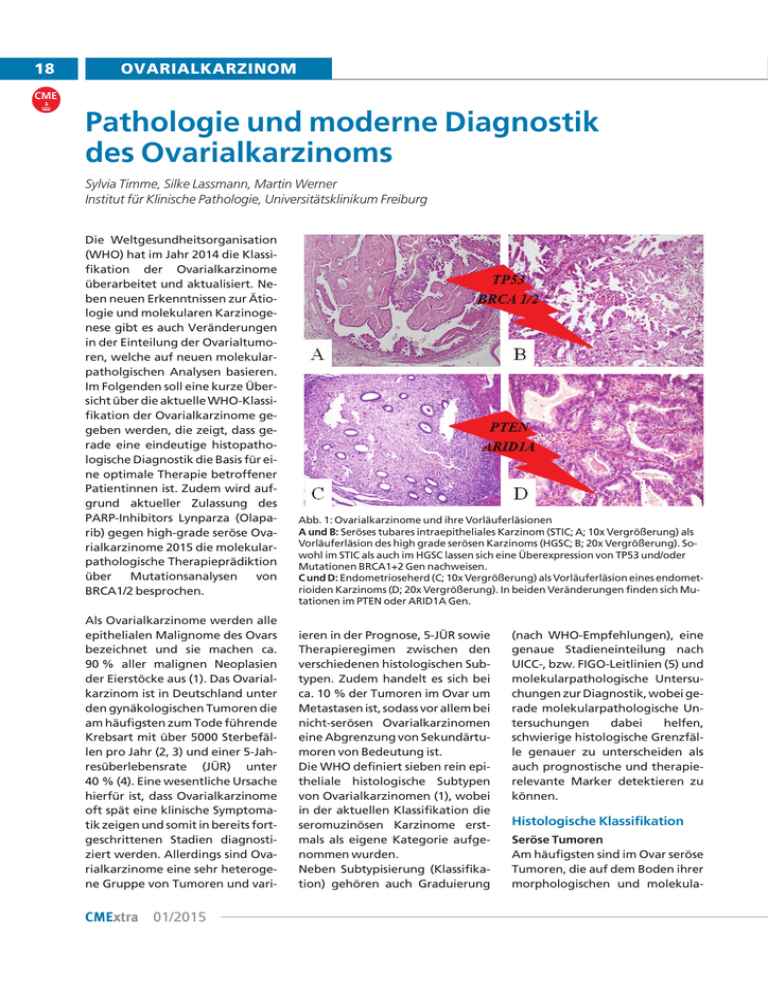
18 OVARIALKARZINOM CME Pathologie und moderne Diagnostik des Ovarialkarzinoms Sylvia Timme, Silke Lassmann, Martin Werner Institut für Klinische Pathologie, Universitätsklinikum Freiburg Die Weltgesundheitsorganisation (WHO) hat im Jahr 2014 die Klassifikation der Ovarialkarzinome überarbeitet und aktualisiert. Neben neuen Erkenntnissen zur Ätiologie und molekularen Karzinogenese gibt es auch Veränderungen in der Einteilung der Ovarialtumoren, welche auf neuen molekularpatholgischen Analysen basieren. Im Folgenden soll eine kurze Übersicht über die aktuelle WHO-Klassifikation der Ovarialkarzinome gegeben werden, die zeigt, dass gerade eine eindeutige histopathologische Diagnostik die Basis für eine optimale Therapie betroffener Patientinnen ist. Zudem wird aufgrund aktueller Zulassung des PARP-Inhibitors Lynparza (Olaparib) gegen high-grade seröse Ovarialkarzinome 2015 die molekularpathologische Therapieprädiktion über Mutationsanalysen von BRCA1/2 besprochen. Als Ovarialkarzinome werden alle epithelialen Malignome des Ovars bezeichnet und sie machen ca. 90 % aller malignen Neoplasien der Eierstöcke aus (1). Das Ovarialkarzinom ist in Deutschland unter den gynäkologischen Tumoren die am häufigsten zum Tode führende Krebsart mit über 5000 Sterbefällen pro Jahr (2, 3) und einer 5-Jahresüberlebensrate (JÜR) unter 40 % (4). Eine wesentliche Ursache hierfür ist, dass Ovarialkarzinome oft spät eine klinische Symptomatik zeigen und somit in bereits fortgeschrittenen Stadien diagnostiziert werden. Allerdings sind Ovarialkarzinome eine sehr heterogene Gruppe von Tumoren und vari- CMExtra 01/2015 Abb. 1: Ovarialkarzinome und ihre Vorläuferläsionen A und B: Seröses tubares intraepitheliales Karzinom (STIC; A; 10x Vergrößerung) als Vorläuferläsion des high grade serösen Karzinoms (HGSC; B; 20x Vergrößerung). Sowohl im STIC als auch im HGSC lassen sich eine Überexpression von TP53 und/oder Mutationen BRCA1+2 Gen nachweisen. C und D: Endometrioseherd (C; 10x Vergrößerung) als Vorläuferläsion eines endometrioiden Karzinoms (D; 20x Vergrößerung). In beiden Veränderungen finden sich Mutationen im PTEN oder ARID1A Gen. ieren in der Prognose, 5-JÜR sowie Therapieregimen zwischen den verschiedenen histologischen Subtypen. Zudem handelt es sich bei ca. 10 % der Tumoren im Ovar um Metastasen ist, sodass vor allem bei nicht-serösen Ovarialkarzinomen eine Abgrenzung von Sekundärtumoren von Bedeutung ist. Die WHO definiert sieben rein epitheliale histologische Subtypen von Ovarialkarzinomen (1), wobei in der aktuellen Klassifikation die seromuzinösen Karzinome erstmals als eigene Kategorie aufgenommen wurden. Neben Subtypisierung (Klassifikation) gehören auch Graduierung (nach WHO-Empfehlungen), eine genaue Stadieneinteilung nach UICC-, bzw. FIGO-Leitlinien (5) und molekularpathologische Untersuchungen zur Diagnostik, wobei gerade molekularpathologische Untersuchungen dabei helfen, schwierige histologische Grenzfälle genauer zu unterscheiden als auch prognostische und therapierelevante Marker detektieren zu können. Histologische Klassifikation Seröse Tumoren Am häufigsten sind im Ovar seröse Tumoren, die auf dem Boden ihrer morphologischen und molekula- OVARIALKARZINOM ren Eigenschaften in invasive Lowgrade seröse Karzinome (LGSC) und High-grade Karzinome (HGSC) sowie die nichtinvasiven serösen Borderlinetumoren (SBT) unterteilt werden (1). Eine Differenzierung zwischen LGSC und HGSC basiert auf der histologischen Beurteilung der Tumoren bezüglich Ihrer Kernatypien (Primärkriterium) und ihrer Mitosezahl (Sekundärkriterium) (6, 7). Diese Subklassifikation ist zunächst bezüglich der Prognose wichtig, da LGSC weitaus weniger aggressiv sind und häufiger einen besseren Verlauf im Vergleich zu HGSC aufweisen. Auf molekularer Ebene finden sich bei LGSC häufiger Mutationen im KRAS- und BRAF-Gen (8), während das HGSC therapeutisch wichtige Mutationen im BRCA1/2-Gen oder eine Überexpression von TP53 zeigt (4). Heutzutage geht man davon aus, dass die serösen Neoplasien nicht nur aus metaplastisch verändertem mesothelialen Oberflächenepithel des Ovars entstehen, sondern in vielen Fällen im Bereich der distalen Tube bzw. Fimbrientrichter ihren Ursprung haben. Dafür sprechen identische molekularpathologische Veränderungen, wie Mutationen im BRCA1/2-Gen oder eine Überexpression von TP53 (9), die sich auch in Vorläuferläsionen wie serösen tubaren intraepithelialen Karzinomen (STIC) nachweisen lassen (E Abb. 1A und B, Seite 18). Da diese charakteristischen Veränderungen ebenfalls in primären peritonealen serösen Karzinomen vorzufinden sind, wird von einigen Autoren und der WHO inzwischen der Oberbegriff der „pelvinen serösen Neoplasien/Karzinome“ vorgeschlagen (1, 10). Zu den serösen Ovarialtumoren gehören zudem die nichtinvasiven serösen Borderlinetumoren (SBT), die mit extraovariellen nichtinvasiven, aber auch invasiven „Implants“ vergesellschaftet sein können. „Implants“ entsprechen serösen Epithelproliferaten, die zytologisch „low grade“ Kriterien aufweisen, per Definition allerdings noch kein invasives Verhalten zeigen, wobei sich in einigen Fällen auch bei SBT ein mikroinvasives Wachstum nachweisen lässt. Die diagnostische Abgrenzung eines SBT gegenüber einem invasiven LGSC ist von besonderer Bedeutung, da bei Patientinnen mit einem nichtinvasiven SBT z. B. von einer Chemotherapie abgesehen werden kann. Daher wird bei großen und ausgedehnt wachsenden SBT ein ausgedehntes Tumorsampling zur Diagnosesicherung empfohlen. Endometrioide und klarzellige Karzinome Endometrioide Karzinome des Ovars ähneln in ihrem Wachstum dem Korpusendometrium. Mit einer Häufigkeit von 10−15 % aller Ovarialkarzinome, bilden sie die zweitgrößte Tumorgruppe. Sie imponieren oft als pelvine durchschnittlich 15 cm große Masse, wachsen allerdings meist nur unilateral ohne Kapseldurchbruch und werden eher in einem frühen Stadium diagnostiziert, was wiederum mit einer besseren Prognose verbunden ist (5-JÜR 78 % bei einer Erstdiagnose in Stadium 1). In bis zu 20 % der Fälle sind endometrioide Ovarialkarzinome assoziiert mit endometrioiden Karzinomen des Corpus uteri (1), weswegen sich auch eine genaue Inspektion des Uterus empfiehlt. Zusätzlich können bei ca. 40% der endometrioiden Ovarialtumoren im Becken zusätzlich Endometrioseherde gefunden werden (Abb. 1C und D), die entsprechend als Vorläuferläsionen zählen. Klarzellige Karzinome machen 10% der ovarialen Karzinome aus. Glykogen-haltige Tumorzellen mit tubulozystischem bis zu solidem Wachstum sind ein charakteristisches histologisches Merkmal. Wie auch die endometrioiden Karzinome wachsen sie meist unilateral. Bei fortgeschrittenen klarzelligen Ovarialkarzinomen ist allerdings zu beachten, dass sie ein schlechtes Ansprechen auf eine Platin-basierte Chemotherapie und somit auch eine moderate bis schlechte Prognose aufweisen (1). Als wichtigste Vorläuferläsion gilt auch bei klarzelligen Ovarialkarzinomen die Endometriose, während nichtinvasive Borderline-Läsionen nur eine geringe Rolle spielen. In bis zu 38 % der endometrioiden Ovarialkarzinome lassen sich Mutationen im beta-Catenin-Gen (CTNNB1) nachweisen, was mit einer besseren Prognose vergesellschaftet ist (1). Zudem finden sich auf molekularer Ebene PTEN-Deletionen (bis zu 20%), die auch in Kombination mit PIK3CA-Mutationen auftreten können, sowie in ca. 30 % inaktivierende Mutationen im AT-rich interactive domaine 1A (ARID1A)-Gen (1.) Bis zu 20 % der endometrioiden Ovarialkarzinome zeigen Mikrosatelliteninstabilitäten und sind gehören damit zu einer Tumorentität, die bei einem HNPCC-Syndrom auftreten kann (11). Bei klarzelligen Karzinomen finden sich ebenfalls PIK3CA-akivierende Mutationen und Deletionen im PTEN-Gen, wobei hier die Mutation im ARID1A-Gen in mehr als 50 % der Fälle, die mit einem Verlust des BAF250a Proteins gekoppelt sein kann, im Vordergrund steht. Muzinöse Karzinome Muzinöse Karzinome zeigen charakteristischerweise zytoplasmati- 01/2015 CMExtra 19 20 OVARIALKARZINOM sches Muzin und machen nur etwa 3−4 % der primären Ovarialkarzinome aus (12). Primäre muzinöse Ovarialkarzinome sind überwiegend große (>13 cm), unilateral lokalisierten (multi-) zystische Tumoren, die oft in frühen FIGO Stadien diagnostiziert werden und dann auch eine gute Prognose haben (1). Obwohl muzinöse Karzinome eine bessere Prognose aufweisen als HGSC, sprechen sie meist nicht optimal auf eine bei serösen Ovarialkarzinomen üblicherweise angewendete Chemotherapieregime an. Bei der Diagnose eines bilateralen Tumors oder extraovariellem Befall sollte differentialdiagnostisch immer eine Metastase eines anderen Primärtumors ausgeschlossen werden, allen voran eines gastrointestinalen Karzinoms (Kolo-Rektum oder Magen). Insbesondere immunhistochemische Untersuchungen, etwa für Zytokeratin 7 und 20, aber auch PAX8, welches von gastointestinalen Tumoren in der Regel nicht exprimiert wird (13), sind hier bei der Differentialdiagnostik hilfreich. Da invasive muzinöse Ovarialkarzinome auf dem Boden nichtinvasiver muzinöser Borderlinetumoren entstehen können, sollte bei muzinösen Borderline-Tumoren eine genaue makroskopische Inspektion und umfassendes histologisches Sampling durch den Pathologen erfolgen, um einen Übergang in ein invasives Karzinom auszuschließen. Molekularpathologisch finden sich bei muzinösen Karzinomen des Ovars häufig KRAS, HER2/neu und EGFR Mutationen sowie Veränderungen im PI3K-pAKT Signalweg (14, 15, 16). Seromuzinöse Karzinome Bisher wurde innerhalb der Gruppe der muzinösen Ovarialkarzinome ein intestinaler und ein endo- CMExtra 01/2015 zervikaler Wachstumstyp unterschieden. Molekularpatholgische Analysen zeigten jedoch häufig bei muzinösen Tumoren mit einem endozervikalen Wachstumsmuster Verluste des ARID1A-Gens, wie auch bei endometrioiden und klarzelligen Ovarialkarzinomen (17). In der Folge wurden sie von der WHO als eigene Kategorie gelistet. Neben endozervikalen finden sich auch seröse Wachstumsmuster oder endometrioid bzw. plattenepithelial differenzierte Areale. Insgesamt sind diese Tumoren selten, sodass die Datenlage zur Ätiologie, prognostischen und prädiktiven Marken noch gering ist. Sofern sie jedoch in einem frühen Stadium diagnostiziert werden, ist auch hier die Prognose gut (1). Maligne Brenner-Tumoren und undifferenzierte Karzinome Neben den oben beschriebenen Adenokarzinomen definiert die WHO noch die malignen BrennerTumoren und die undifferenzierten Karzinome (1). Maligne Brenner-Tumore sind selten, imponieren als Karzinome vom Transitionalzelltyp und imitieren mit ihrem Wachstum invasive Urothelkarzinome, wobei sie sich gut durch ihr divergentes immunhistochemisches Profil von Metastasen eines primären Urothelkarzinoms differenzieren lassen. Undifferenzierte Karzinome lassen sich durch ihr Wachstum keinem speziellen oben beschriebenen Tumortyp zuteilen, wachsen oft solide mit zentralen Nekrosen und vielen Mitosen und haben somit ein aggressives Verhalten. Beide seltenen Tumortypen haben gemein, dass sie − wie auch die high grade serösen Karzinomeüberwiegend in einem fortgeschrittenen Tumorstadium diagnostiziert werden und eine schlechte Prognose und niedrige 5JÜR haben (1). Prognostische und Prädiktive Marker Tumorstaging bei Erstdiagnose Einer der wichtigsten prognostischen Marker für Ovarialkarzinome ist das Staging, die lokale Tumorausdehnung. Im histopathologischen Befund wird es durch die UICC-Klassifikation für Ovarialkarzinome angegeben (6), die wiederum in die auf klinischer Ebene weithin verbreitete FIGO-Klassifikation übertragen wird. Aktuell wurde auf Grund neuer Erkenntnisse zum Ovarialkarzinom, aber auch zu prognostischen Faktoren wie Nodalstatus und Kapselrupturursachen, 2012 nach fast 24 Jahren eine neue FIGO Klassifikation beschlossen und final 2014 mit der UICC und AJCC Klassifikation abgeglichen (18). Zudem gilt die neue FIGO-Klassifikation nicht nur für Malignome des Ovars, sondern ebenso für Tubenkarzinome und primäre Peritonealkarzinome. Grundlegende diagnostische Parameter für das Staging sind Tumorausdehnung auf ein oder beide Ovarien, Kapseldurchbrüche und Oberflächenbefall des Tumors, Befund der Asziteszytologie, Tumorausbreitung im bzw. jenseits des Beckens, Größe extrapelviner Absiedelungen und Lymphknotenbzw. Fernmetastasen. Neu dazu gekommen ist eine Beurteilung der Kapselruptur: ist diese iatrogen/artefiziell oder durch den Tumor spontan bedingt. In jedem Fall gilt es, die Operationspräparate der Ovarialkarzinome inkl. der pelvinen und extrapelvinen Gewebe makround mikroskopisch genau aufzuarbeiten, um eine korrekte Stadieneinteilung zu gewährleisten. Tumorrest Die postoperative residuelle Tumormasse ist ebenfalls ein bedeu- OVARIALKARZINOM Histol. Typ (Häufigkeit %) Molekulare Eigenschaften Vorläuferläsion Genetisches Risiko Prognose CTX Ansprechen Targeted Therapy Serös; high grade (-60 %) BRCA/TP53 Seröses Carcinoma in situ der Tube BRCA 1/2 schlecht gut PARP-Inhibitor Serös; low grade (-10 %) KRAS, BRAF Seröser Borderlinetumor moderat moderat BRAF-Inhibitor Muzinös (-5 %) KRAS, HER2, EGFR Muzinöser Borderlinetumor günstig gering HER2/neu Antagonisten Endometrioid (-10 %) PTEN, ARID1A, ȕCatenin, Pl3K-pAKT Endometriose günstig gut x Klarzellig (-10 %) ARID1A, PTEN, Pl3K-pAKT Endometriose moderat gering PlK-3CA-Inhibitor HNPCC Tab. 1: Übersicht über die wichtigsten Typen der Ovarialkarzinome [nach 1] tender Prognosefaktor für das Überleben, weswegen diese bei der primären Operation optimal reduziert werden sollte (sog. „Debulking“). Doch eine große Anzahl von Ovarialkarzinomen wird nicht nur in fortgeschrittenem Stadium erstdiagnostiziert, sondern ist primär inoperabel (z. B. durch enterale Verwachsungen oder durch Ummauerung/Einwachsen in größere Gefäße). In solchen Fällen besteht die Möglichkeit, durch neoadjuvante Chemotherapie den Tumor zu verkleinern, um eine anschließende Debulkingoperation ggf. zu ermöglichen. Molekulare Marker Bei serösen Ovarialkarzinomen konnte gezeigt werden, dass Mutationen im BRCA1/2 Gen auch ein Ansprechen auf Platin-basierte Chemotherapien begünstigt, da bei durch BRCA1/2 Mutationen veränderten Tumorzellen die durch Platin-basierte Chemotherapien verursachten DNS Schäden nicht mehr korrigiert werden können, was zu einem Absterben speziell BRCA1/2-mutierter Tumorzellen führt. Dieser Effekt kann durch weitere chemotherapeutische Substanzen, wie etwa PARP- Inhibitoren verstärkt werden (19,20). Die Zulassung für den PARP-Inhibitor Olaparib erfolgte 2015, so dass zum aktuellen Zeitpunkt in der molekularpathologischen Diagnostik beim Ovarialkarzinom die BRCA1/2 Untersuchungen im Vordergrund stehen. Hierfür wird die Technik des „targeted Next-Generation Sequencing“ (tNGS) aus mikrodissektierten Tumorgewebe angewandt. Diese ermöglicht eine umfassende, zeitnahe und kostengünstige Analytik, insbesondere da für die Olaparib Therapieprädiktion bislang keine „Hotspot“ Sequenzregionen für Einzelanalysen eingegrenzt werden konnten. Diese spezielle Analytik des tNGS ist in den Pathologien der Universitätsklinika bereits im Einsatz. Zudem können auch bei anderen Tumorarten (z. B. Mamma- oder Kolonkarzinom) bereits etablierte Inhibitoren gegen Tumorzell-spezifische Oberflächenproteine wie etwa EGFR, HER2 bei der Therapie von Ovarialkarzinomen zukünftig genutzt werden; entsprechend des jeweiligen histologischen Subtypen (Tab. 1). Auch die vor allem bei Malignen Melanomen etablierten BRAF-Inhibitoren können bei BRAF-mutierten Ovarialkarzinomen (LGSC) zukünftig in der Therapie eine Rolle spielen. Fazit Bei der Diagnose Ovarialkarzinom werden heutzutage viele verschiedene Anforderungen an den Pathologen gestellt. Neben der exakten Klassifikation eines der von der WHO definierten Subtypen, mit Hilfe von immunhistologischen als auch molekularpathologischen Analysen, und der Bestimmung des Tumorstadiums nach UICC/FIGO, sollte in jedem Fall eine Metastase eines extraovariellen Karzinoms ausgeschlossen werden. Da Ovarialkarzinome eine sehr unterschiedliche Prognose aufweisen, können eine eindeutige histopathologische Diagnostik und Klassifikation des Tumors eine optimale Therapie ermöglichen. Zudem ist mit Zulassung von Olaparib die molekularpathologische Analyse von BRCA1/2 als Grundlage für die Therapieprädiktion von Bedeutung und stellt einen ersten Schritt in die zukünftige molekularpathologische Stratifizierung von Patientinnen mit Ovarialkarzinomen für zielgerichtete Therapien („targeted therapy“) dar. 01/2015 CMExtra 21 22 OVARIALKARZINOM Literatur 1. Longacre T.A. and Wells M (2014) Tumours of the ovary In: Kurman RJ, Carcangiu ML, Herrington CS and Young RH (eds) World Health Organization Classification of Tumours of Female Reproductive Organs.IARC Press, Lyon, pp 11-43. 2. Jemal A, Bray F, Center MM. et al. Global cancer statistics. CA Cancer J Clin. 2011;61(2):69-90. 3. Krebs in Deutschland 2003 – 2004. Häufigkeiten und Trends. 6th revised edition. Robert-Koch-Institut (ed.) und die Gesellschaft der epidemiologischen Krebsregister in Deutschland e. V. (ed.). Berlin 2008. 4. Runnebaum IB, Stickeler E. Epidemiological and molecular aspects of ovarian cancer risk. J Cancer Res Clin Oncol. 2001;127(2):73-9. Review. 5. Odicino F.. (2010) UICC Klassifikation Ovar-Gynäkologische Tumoren. In: Wittekind C. Meyer H.J..TNM Klassifikation maligner Tumoren. Siebente Auflage. WILEY-VCH GmbH & Co. KGaA, Weinheim, pp 208-212. 6. Bodurka DC, Deavers MT, Tian C et al. Reclassification of serous ovarian carcinoma by a 2-tier system: a Gynecologic Oncology Group Study. Cancer 2012;118:3087-3094 7. Malpica A, Deavers MT, Lu K et al. Grading ovarian serous carcinoma using a two-tier system. Am J Surg Pathol. 2004 28:496-504. 8. Singer G, Oldt R 3rd, Cohen Y et al. Mutations in BRAF and KRAS characterize the development of low-grade ovarian serous carcinoma. J Natl Cancer Inst. 2003;19;95(6):484-6. 9. Piek JM, van Diest PJ, Zweemer RP et al. Dysplastic changes in prophylactically removed Fallopian tubes of women predisposed to developing ovarian cancer. J Pathol. 2001;195(4):451-6. 10. Nik NN, Vang R, Shih I, Kurman R Origin and Pathogenesis of pelvic (Ovarian, Tubal, and Primary Peritoneal) Se- w w .d w e CME .c me .m go -f ac h v er la ge CMExtra 01/2015 rous Carcinoma. Annu. Rev. Pathol. Mech. Dis. 2014 ;9:27-45. 11. Prat J. Ovarian Carcinomas: five distinct diseases with different origins, genetic alterations, and clinicopathological features. Virchows Arch. 2012;460(3):237-49. 12. Kobel M, Kalloger SE, Hunsman DG et al. Differences in tumor type in lowstage versus high-stage ovarian carcinomas. Int J Gynecol Pathol. 2010;31:546-554. 13. Laury AR, Perets R, Piao H et al. A comprehensive analysis of PAX8 expression in human epithelial tumors. Am J Surg Pathol 2011;35:816-826. 14. Cuatrecasas M, Villanueva A, Matias-Guiu X et al. K-ras mutations in mucinous ovarian tumors: a clinicopathologic and molecular study of 95 cases. Cancer. 1997;15;79(8):1581-6. 15. McAlpine JN, Wiegand KC, Vang R et al. HER2 overexpression and amplification is present in a subset of ovarian mucinous carcinomas and can be targeted with trastuzumab therapy. BMC Cancer. 2009;10;9:433. 16. Alshenawy HA. Immunohistochemical expression of epidermal growth factor receptor, E-cadherin, and matrix metalloproteinase-9 in ovarian epithelial cancer and relation to patient deaths. Ann Diagn Pathol. 2010;14(6):387-95. 17. Wu CH, Mao TL, Vang R et al. Endocervical-type mucinous Borderlinetumors are related to endometrioid tumors based on mutation and loss of expression of ARID1A. Int J Gynecol Pathol. 2012;31:297-303. 18. Prat J, FIGO Committee on Gynecologic Oncology Staging classification for cancer of the ovary, fallopian tube, and peritoneum. Int J Gynaecol Obstet 2014;124:1-5. 19. Ignatov T, Eggemann H, Costa SD et al. BRCA1 promotor methylation is a marker of better response to platinumtaxane-based therapy in sporadic epi- thelial ovarian cancer. J Cancer Res Clin Oncology. 2014 (epub ahead of print). 20. Gelmon KA, Tischkowitz M, Mackay H et al. Olaparib in patients with recurrent high grade serous or poorly differentiated ovarian carcinoma or triplenegative breast cancer: a phase 2, multicentre, open-lable, non-randomised study. Lancet Oncol 2011;12:852-61. Korrespondenzadresse: Prof.Dr. med. Martin Werner Department für Pathologie - Ludwig-Aschoff-Haus Institut für Klinische Pathologie UniversitätsklinikumFreiburg Breisacher Str. 115a, 79106 Freiburg E-Mail: [email protected] Prof. Martin Werner Prof.Dr. Silke Laßmann BEQUEM UND EINFACH Alle CME Artikel finden Sie online auf unserem neuen CME-Portal unter www.cme.mgo-fachverlage.de!











