in situ - Ruhr-Universität Bochum
Werbung

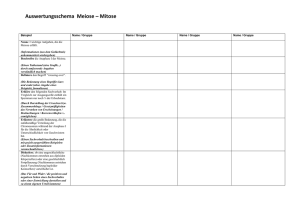
(Molekulare-) Zytogenetik numerische Chromosomenaberrationen • autosomale Aneuploidien – Trisomie 13: Pätau-Syndrom (47,XX+13) – Trisomie 18: Edwards-Syndrom (47,XY+18) – Trisomie 21: Down-Syndrom (47,XX+21) • gonosomale Aneuploidien Trisomie-Risiko steigt(45,X0) mit ↑ mütterl. Alter - Turner-Syndrom - nicht für 45,X0 und(47,XXY) Triploidie - Klinefelter-Syndrom Mikrodeletions-Syndrome DiGeorgeSyndrom Mikrodeletions-Syndrome Prader-WilliSyndrom WilliamsBeuren-S. AngelmanSyndrom reziproke Translokation Symptome bei Chromosomen-Aberrationen • körperliche + geistige Entwicklung • Fehlbildungen innerer Organe • Dysmorphien Kopf, Hand, Fuß (Skelett) • weitere neurologische Symptome whole chromosome painting Stammbäume Warum sind Stammbäume wichtig? • Stammbaum über 3 Generationen als Bestandteil jeder genetischen Beratung • (genetische) Erkrankungen in der Familie • Rückschlüsse auf Erbgang • Berechnung des Wiederholungsrisikos Stammbaum-Symbole männlich (Mann, Sohn) Probandin (für die eine Analyse erstellt wird) weiblich (Frau, Tochter) verstorben phänotypische Merkmalsträger genotypisch homozygot Heterozygotie oder oder Geschlecht unbekannt (bzw. ohne Bedeutung) schwanger (Geschlecht unbekannt) Elternpaar außereheliche Verbindung Zweieiige Zwillinge geschiedenes Paar Verwandtenehe Eineiige Zwillinge kinderloses Paar Geschwister (älterer Bruder und Schwester) Paar mit zwei Kindern, das erste Kind ein Sohn Abort, weiblich Totgeburt, weiblich Konduktorin (heterozygot für X-chr. rez. Erbgang) autosomal-dominanter Erbgang • Morbus Huntington • Neurofibromatose Penetranz Anteil betroffener Mutationsträger an der Gesamtheit der Mutationsträger • vollständige Penetranz: 100% der Träger erkrankt • reduzierte Penetranz: klinisch gesunde Träger bekannt variable Expressivität Erkrankung manifestiert sich unterschiedlich schwer bei Betroffenen derselben Familie oder verschiedener Familien variable Expressivität: NF1 Neumutation Neumutationsrate sehr unterschiedlich Achondroplasie 90% Neurofibromatose 1 50% Morbus Huntington sehr selten Wiederholungsrisiko gering; cave Keimzellmosaik autosomal-rezessiver Erbgang • Stoffwechselerkrankungen – Cystische Fibrose, CF – Phenylketonurie – Sichelzellanämie etc. • angeb. Schwerhörigkeit/Taubheit • spinale Muskelatrophie autosomal-rezessiver Erbgang • 1 oder mehrere erkrankte Kinder bei gesunden Eltern • häufiger bei Verwandtenehen • Risikoberechnung für Verwandte, Anlageträger zu sein heterozygot heterozygot ? Erkrankungsrisiko: 1/4 Risiko für Anlageträgerschaft: 2/3 Anlageträger gesund 1/4 Anlageträger Anlageträger 2/4 krank 1/4 X-chromosomal-rezessiver Erbgang • Muskeldystrophie Duchenne • Hämophilie A • Fragiles X-Syndrom X-chromosomal rezessiver Erbgang XY XX XX XY XX XY X X-Chromosom mit Wildtyp-Gen X X-Chromosom mit mutiertem Gen hemizygot XX-Frau ist (gesunde) Konduktorin für X-chromosomale Mutation • 50% Erkrankungsrisiko für jeden Sohn • statistisch 50% der Töchter erneut Konduktorinnen • Kinder eines erkrankten Mannes: alle Söhne gesund, alle Töchter Konduktorinnen Zusammenfassung • Stammbaum: Dokumentation der Familienanamnese • Hinweis auf Mendel‘ Erbgang ? • Beurteilung des Wiederholungsrisikos Mitose - Meiose - Zellzyklus - Mitose - Meiose - Gametogenese - Polkörper-Diagnostik - PID Definitionen Eukaryonten: 2 Formen der Zellteilung Mitose: Zellteilung der somatischen Zellen Chromosomensatz diploid (2n) Meiose: Reduktionsteilung Keimbahnzellen Chromosomensatz haploid (1n) Zellzyklus M-Phase Interphase S-Phase G1-Phase G2-Phase Mitose DNA-Synthese zw. M und S zw. S und M G0-Phase Zellen ohne Zellteilung neue Zelle geht in Zellzyklus ruhende Zellen Zellzyklus sich teilender Zellen Interphase G1- bzw. G0-Phase: 1 Chromatide/ 1 DNA-Helix gestreckt, diffus Genexpression ↑ diploider Chromosomensatz (2n, 2C) S-Phase: Replikation 46 Chromosomen mit 2 Chromatiden (Endzustand: 2n, 4C) neue Zelle geht in Zellzyklus ruhen -de Zelle Zyklus teilender Zellen Mitose Dauer: 5 Stadien: 60min Prophase Prometaphase Metaphase Anaphase Telophase Metaphase-Chromosomen 2 Chromatiden stark kondensiert Genexpression lichtmikroskopisch sichtbar neue Zelle geht in Zellzyklus ruhen -de Zelle Zyklus teilender Zellen Centromer • • • • primäre Chromosomen-Einschnürung Chromatiden hängen zusammen Anheftung an Mitosespindel Bildung der Kinetochore (Multiprotein-Komplexe) steuern Auf- + Abbau der Mikrotubuli Chromosomen-Bewegung • bestehen aus hochrepetitiven DNA-Sequenzen Chromatide Telomer Centromer Kinetochor Mitosespindel 3 versch. Mikrotubuli, MT - Pol-MT Kinetochor MT - Kinetochor-MT - Astral-MT Kinetochor Aster MT Spindelpol: Centrosom (2 Centriolen, Mikrotubuli) Pol (CenPol-MTs Aster Chromosom Spindel trosom) Aster Meiose = Reduktionsteilung 2 aufeinander folgende Zellteilungen, (Meiose I, Meiose II Mitose) aber nur eine Phase der DNA-Replikation in Meiose I (Ziel: 1n, 1C) genetische Diversität: Rekombination, unabhängige Verteilung der väterlichen und mütterlichen Chromosomen asymmetrische Zellteilung: 1 Oocyte, 3 Polkörperchen Meiose I Ziel: haploider Chromsomensatz (1n, 2C) Bivalent: mütterliches und väterliches Homolog gepaart (Tetrade) Chromosomen (2 Chromatiden) werden zu einem Pol gezogen unabhängige Verteilung der Chromosomen 223 (8,4x106) mögliche Kombinationen Rekombination DNA-Austausch zwischen homologen Chromosomen Synaptonemaler Komplex: räumliche Nähe der Homologen, Trennung durch Proteinkomplex Rekombination: DNA-Bruch, Neuverknüpfung der Enden zwischen Chromatiden homologer Chromosomen Chiasmata: Verbindungsstellen der Homologen - wichtig für Segregation der Chromosomen Gametogenese primordiale Keimzellen wandern ein in embryonale Gonaden (Mitose) Oogonien prim. Oocyten Spermatogonien prim. Spermatozyten Meiose/Reduktionsteilung Spermatogenese Oogenese Gametogenese • Spermatogenese: – kontinuierlich ablaufend – symmetrische Teilung • Oogenese: Meiose I Meiose I Meiose II – Beginn vor der Geburt, arretiert in Meiose I, Prophase – asymmetrische Teilung Meiose II reife Spermatozoen Oogonien Spermatogenese Oogenese 2n2C 2n2C Meiose I Meiose I 2n4C 2n4C 1n2C Meiose II 1n1C 1n2C Meiose II reife Spermatozoen Oogonien 1n1C Vergleich Mitose-Meiose Mitose Meiose Vorkommen alle Gewebe Hoden, Ovarien Ergebnis diploide somatische haploide Eizellen, Zellen haploide Samenzellen Dauer kurz, 30 min Meiose I: bis zu Jahren Homologenpaarung nein ja Rekombination selten, anomal mind. 1/Chromosomenarm Tochterzellen genetisch identisch genetisch verschieden In welchen meiotischen Teilungen kann nondisjunction zu Aneuploidien führen? • autosomale Trisomien: – 1. oder 2. meiotische Teilung bei ♀ oder ♂ • Klinefelter-Syndrom: – 1. meiotische Teilung bei ♂ oder ♀ – 2. meiotische Teilung bei ♀♀ Polkörper-Diagnostik Analyse im Vorkernstadium (18-20h nach ICSI) Polkörper-Absaugen mit Glaspipette Untersuchen durch FISH, PCR Polkörper-Diagnostik Indikationen - Ausschluss von Chromosomenfehlverteilung - monogene Erbkrankheiten (M. Huntington, z.B. heterozygote Trägerinnen bei M. Duchenne) - maternale Translokation PI rä D mplantations iagnostik Indikation - monogen bedingte Leiden; erbliche Chromosomenstörungen -- z.B. Muskeldystrophie Duchenne, M. Huntington -- z.B. Translokation Konventionelle Zytogenetik optimal 5-10 Megabasen Chromosomenanalysen inhärente Limitierungen • Chromosomen nur bei Zellteilung darstellbar • submikroskopische Mutationen nicht erkennbar • schwierige Interpretation komplexer Veränderungen (mehrere Chromosomen) Pränataldiagnostik - Amniocentese Zentrifuge Plazenta Amnionhöhle Amnionflüssigkeit Biochemie Zellen Uteruswand Zellkultur Biochemie Chromosomen Kultivieren: Amnionzellen Dauer bis zum Befund ͠ 10 Tage Chorionzotten-Biopsie Bauchdecke Uterus Amnionhöhle Decidua Nabelschnur Placenta Fet trans-vaginal FISH (Fluoreszenz in situ-Hybridisierung) G C G A T A T A T T T C T A T T A T A A A T A C G C A G C G T T A T T G C A FISH (Fluoreszenz in situ-Hybridisierung) A C G C A T T A T T A A T A T C G G C T A C Chromosomen nicht-teilungsaktiver Zellen Diagnostik in unkultiv. Zellen ( Zellteilung): sog. Interphase-FISH limitiert auf Sondenkomplementäre DNA, kein komplettes Karyogramm