mikroRNAs – Feinregulatoren der synaptischen Übertragung
Werbung

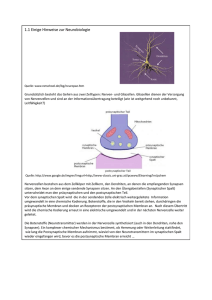
402_448_BIOsp_0408.qxd 430 13.06.2008 8:11 Uhr Seite 430 KA R R IE R E , KÖP FE & KON Z EPTE Gerhard Schratt Jahrgang 1972. 1992–1998 Biochemiestudium an der Universität Tübingen. 1998–2002 Promotion am Institut für Zellbiologie, Abteilung Molekularbiologie der Universität Tübingen, Doktorvater Prof. A. Nordheim. 2002– 2006 Postdoc im Labor von Prof. M. Greenberg, Children’s Hospital und Harvard Medical School, Boston, USA. Seit 2006 Nachwuchsgruppenleiter (SFB488) am Interdisziplinären Zentrum für Neurowissenschaften der Universität Heidelberg. ó Mehr als hundert Milliarden Nervenzellen sind im Gehirn eines Erwachsenen auf engstem Raum gedrängt. Die korrekte Verschaltung dieser Nervenzellen ist maßgebend für höhere kognitive Leistungen wie Lernen und Gedächtnis. Defekte in ihrer Verschaltung sind die Grundlage einer Reihe neurologischer Erkrankungen, wie z. B. Autismus, Demenz und Epilepsie. Einzelne Nervenzellen kommunizieren über Synapsen, hoch spezialisierte Kontaktstellen, an denen Botenstoffe freigesetzt werden, die als Vermittler an nachgeschaltete Nervenzellen docken und dadurch Signale weitergeben können. Synapsen ketten nicht nur Nervenzellen aneinander, sie können vielmehr auch als Informationsspeicher fungieren: Die Zahl und die Stärke dieser Verknüpfungen bestimmen, wie effizient Informationen im Gehirn durchlaufen und abgefragt werden können[1]. Unsere Forschung beschäftigt sich mit den molekularen Mechanismen, die für die Veränderung (Plastizität) von Synapsen, und damit für Lern- und Gedächtnisvorgänge, von Bedeutung sind. Es ist seit längerem bekannt, dass die Proteinmaschinerie an den Synapsen dabei eine zentrale Rolle spielt. Plastizität erfordert eine dynamische Regulation der Proteinausstattung von Synapsen, sowohl durch Proteinsynthese als auch durch Pro- Analytica Forschungspreis I mikroRNAs – Feinregulatoren der synaptischen Übertragung GERHARD SCHRATT INTERDISZIPLINÄRES ZENTRUM FÜR NEUROWISSENSCHAFTEN (IZN), UNIVERSITÄT HEIDELBERG teinabbau[2]. Welche Moleküle für diese Regulation wichtig sind, ist jedoch weitestgehend unklar. Auf der Suche nach solchen regulatorischen Faktoren wurden wir kürzlich auf eine neue Molekülklasse aufmerksam, die so genannten mikroRNAs (Mikro-Ribonukleinsäuren, miRNAs). Die miRNAs sind winzige, 19–23 Nukleotide lange Ribonukleinsäuren, die im Gegensatz zu Boten-RNA (messenger-RNA, mRNA) nicht in Protein umgeschrieben werden, sondern rein regulatorische Funktionen übernehmen. Die miRNA bindet hierbei an einen partiell komplementären Bereich im 3’untranslatierten Bereich (3’-UTR) so genannter „Ziel-mRNA”, wodurch die Proteinsynthese des Zielgens gehemmt wird. Der exakte Wirkmechanismus ist noch nicht vollständig aufgeklärt[3]. miRNAs finden sich in allen Zelltypen des Körpers. Sie sind an der Steuerung einer Vielzahl biologischer Prozesse beteiligt, unter anderem bei Herzentwicklung, Insulinstoffwechsel und Krebsentstehung[4]. Auffallend viele miRNAs wurden spezifisch im Gehirn identifiziert. Eine wichtige Funktion von miRNAs im Säugerhirn scheint die Steuerung von Zelldifferenzierung und -überleben zu sein, die genaue Funktion der meisten dieser winzigen „RNA-Schnipsel” ist bislang jedoch unbekannt[5]. ¯ Abb. 1: Funktion neuronaler miRNAs bei der Regulation des Wachstums dendritischer Dornfortsätze. Siehe Text für weitere Details (verändert nach [6]). Die ersten experimentellen Belege, dass miRNAs in der Tat eine wesentliche Rolle bei der synaptischen Entwicklung und Plastizität spielen können, lieferten unsere Untersuchungen an aus Rattenembryonen isolierten Nervenzellen[6]. Wir machten die Beobachtung, dass die gehirnspezifische miRNA miR134, im Gegensatz zu einer Vielzahl anderer neuronaler miRNAs, an hoch spezialisierten synaptischen Kontaktstellen der Empfängerzelle, den so genannten dendritischen Dornfortsätzen, lokalisiert ist. Dort hemmt sie die lokale Synthese wichtiger synaptischer Strukturproteine, wie beispielsweise Lim-domain containing protein kinase 1 (Limk1), und verhindert dadurch ein übermäßiges Wachstum der dendritischen Dornfortsätze (Abb. 1). Interessanterweise kann diese Hemmung durch die Applikation von Faktoren, welche auch bei erhöhter neuronaler Aktivität ausgeschüttet werden (z. B. brain derived neurotrophic factor, BDNF), überwunden werden. Diese dynamische Kontrolle der synaptischen Proteinsynthese durch miR-134 könnte von wesentlicher Bedeutung für eine reizabhängige plastische Veränderung spezifischer synaptischer Verknüpfungen sein, z. B. während Lern- und Gedächtnisvorgängen. Wir erforschen derzeit intensiv, ob und wie sich diese miRNA-vermittelten morphologischen Veränderungen auf die synaptische Übertragung auswirken. Eine Frage, die sich uns unmittelbar aufdrängte, war die folgende: Ist miR-134 eine Ausnahme oder kommen auch anderen miRNAs wichtige Funktionen an der Synapse zu? Unsere neuesten Forschungsergebnisse deuten in der Tat darauf hin, dass eine ganze Gruppe neuronaler miRNAs wesentlich zur Plastizität synaptischer Verknüpfungen beiträgt (Siegel et al., eingereicht). Diese Gruppe dendritischer miRNAs scheint parallel eine Vielzahl von Proteinen zu regulieren, welche die Struktur und Funktion von Synapsen beeinflussen. Beispiele sind miR-132, eine miRNA, die ähnlich wie miR-134 die Bildung BIOspektrum | 04.08 | 14. Jahrgang 402_448_BIOsp_0408.qxd 13.06.2008 8:11 Uhr zentraler Komponenten des Aktin-Mikrofilamentsystems reguliert, und miR-138, eine miRNA, die mittels Inhibition eines Depalmitoylierungs-Enzyms die Lokalisation von Signalproteinen an der synaptischen Membran beeinflusst. Insgesamt sprechen diese Ergebnisse für die Existenz eines Netzwerks aus dendritischen miRNAs, welches die lokale Synthese einer Reihe von Schlüsselproteinen an der Synapse koordiniert und dadurch entscheidend zur synaptischen Plastizität beiträgt. Es ist zu erwarten, dass mithilfe biochemischer, genetischer und systembiologischer Ansätze in den kommenden Jahren die Charakterisierung des „mikroRNANetzwerks” an der Synapse weiter voranschreiten wird. Im Moment beschäftigen wir uns ausgehend von unseren ursprünglichen Beobachtungen mit einer Vielzahl von Fragen, wie z. B.: Wie gelangen miRNAs und ihre Ziel-mRNAs an die Synapse? Wie wird die Expression und Funktion der miRNAs aktivitätsabhängig reguliert? Welchen Einfluss haben miRNAs auf die Nervenleitung und letztendlich kognitive Leistungen? Kann durch die Manipulation von miRNAs im Tiermodell die Fähigkeit zur synaptischen Plastizität und damit die Lernfähigkeit beeinflusst werden? Letztendlich stellt sich auch die Frage nach den therapeutischen Möglichkeiten von neuronalen miRNAs. Prinzipiell stellen kleine Nukleinsäuren ideale drug targets dar: Aufgrund der Möglichkeit, diese Moleküle effizient und spezifisch mit Nukleinsäuren komplementärer Sequenz (antisense) zu blockieren, entfällt die langwierige Suche nach pharmakologischen Inhibitoren, wie z. B. bei Rezeptoren oder Enzymen. Wir beschreiten im Moment zwei unterschiedliche Wege, um miRNAs oder deren Blocker effizient ins Säugerhirn zu transportieren. Zum einen benutzen wir ein virales System (Adeno-assoziierte Viren, AAV), das bereits im Rahmen der Gentherapie vielfältigste Anwendung findet. Zum anderen untersuchen wir, inwiefern synthetische Nukleinsäuren, die kovalent an membrangängige Peptide gekoppelt wurden, die Blut-Hirn-Schranke passieren und miRNA-Aktivität im Gehirn modulieren können. Mittlerweile werden miRNAs im Zusammenhang mit der Entstehung einer Vielzahl schwer wiegender neurologischer Erkrankungen diskutiert, darunter Alzheimer, Parkinson und Schizophrenie[7]. Die effiziente BloBIOspektrum | 04.08 | 14. Jahrgang Seite 431 ckade von neuronalen miRNAs im Tiermodell sollte somit nicht nur für die Grundlagenforschung, sondern auch für die pharmazeutische Industrie von erheblichem Interesse sein. Die Erforschung dieser faszinierenden Molekülklasse steht sicherlich erst am Anfang. Man kann jedoch erwarten, dass künftige Ergebnisse wesentlich zu unserem Verständnis der molekularen Vorgänge während Lernvorgängen und Gedächtnisbildung beitragen. So könnten miRNAs auch von klinischem Interesse sein für die Behandlung neurologischer Erkrankungen, die mit Störungen der synaptischen Übertragung einhergehen. Danksagung Mein besonderer Dank gilt Gabriele Siegel für das Korrekturlesen und die Erstellung der Abbildung, sowie allen Mitgliedern meines Labors für die hervorragende Zusammenarbeit. Unsere Forschung wird durch die DFG und HFSP unterstützt. ó Literatur [1] Kandel, E. R. (2001): The molecular biology of memory storage: a dialogue between genes and synapses. Science 294: 1030–1038. [2] Sutton, M. A., Schuman, E. M. (2006): Dendritic protein synthesis, synaptic plasticity, and memory. Cell 127: 49–58. [3] Filipowicz, W., Bhattacharyya, S. N., Sonenberg, N. (2008): Mechanisms of post-transcriptional regulation by microRNAs: are the answers in sight? Nat. Rev. Genet. 9: 102–114. [4] Kloosterman, W. P., Plasterk, R. H. (2006): The Diverse Functions of MicroRNAs in Animal Development and Disease. Dev. Cell 11: 441–450. [5] Kosik, K. S. (2006): The neuronal microRNA system. Nat. Rev. Neurosci. 7: 911–920. [6] Schratt, G. M., Tuebing, F., Nigh, E. A., Kane, C. G., Sabatini, M. E., Kiebler, M., Greenberg, M. E. (2006): A brain-specific microRNA regulates dendritic spine development. Nature 439: 283–289. [7] Fiore, R., Siegel, G., Schratt, G. (2008): MicroRNA function in neuronal development, plasticity and disease. Biochim. Biophys. Acta. doi:10.1016/j.bbagrm.2007.12.006. (Siehe auch GBM-Beitrag zur Preisverleihung auf S. 406) Korrespondenzadresse: Dr. Gerhard Schratt Universität Heidelberg Interdisziplinäres Zentrum für Neurowissenschaften (IZN) SFB488 Nachwuchsgruppe Im Neuenheimer Feld 345 D-69120 Heidelberg Tel.: 06221-566210 Fax: 06221-567897 [email protected]