der Alpha-1-Blocker - Deutsches Ärzteblatt
Werbung

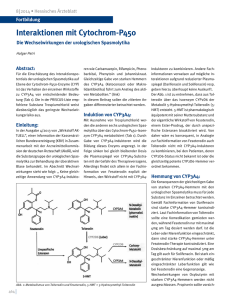
ARZNEIMITTEL-WECHSELWIRKUNGEN ... der Alpha-1-Blocker Bei der symptomatischen Behandlung des benignen Prostatasyndroms spielen neben Phytotherapeutika und dem 5a-Reduktasehemmer Finasterid die selektiven Alpha-1-Adrenozeptorantagonisten (α1-Blocker) eine Rolle. ls „benignes Prostatasyndrom“ (BPS) wird bei Männern über 40 Jahre die variable Trias aus Symptomen des unteren Harntraktes, ● Prostatavolumen und ● Blasenauslassobstruktion bezeichnet (1). Alpha-1-Adrenozeptorantagonisten (α1-Blocker) sind die am häufigsten verwendeten Medikamente zur Behandlung von BPS-Symptomen (2). α-Blocker führen via kompetitiver Inhibition von α1-Adrenozeptoren an der postsynaptischen Membran (insbesondere α1A-Subtyp) zur Relaxation der glatten Muskulatur in Prostata, Prostatakapsel und im Blasenhals, was den Blasenauslasswiderstand reduziert (3). Zusätzlich wird für die Wirkung auch die Inhibition von α1-Adrenozeptoren im Detrusor und im Rückenmark vermutet (3). In Deutschland sind die α1-Blocker Alfuzosin, Doxazosin, Silodosin, Tamsulosin und Terazosin zugelassen. Sie reduzieren den International Prostata Symptom Score (IPSS) im Vergleich zu Placebo in den einzelnen Studien um 1–4 Punkte (1). Vergleichende Untersuchungen zwischen den einzelnen α1-Blockern ergaben keine signifikanten Unterschiede beim IPSS. Sie sind bei adäquater Dosierung vergleichbar effektiv und in dieser Hinsicht austauschbar (1). Müdigkeit, Abgeschlagenheit, Schwindel, Kopfschmerzen, Diarrhö, Schwellung der Nasenschleimhaut, grippale Symptome, hypotone Dysregulation und Synkopen sind mögliche, dosisabhängige Nebenwirkungen (3). Ein erhöhtes Risiko für Schwindel, hypotone Dysregulation oder Synkopen wurde insbesondere für Doxazosin und Terazosin beobachtet (relatives Risiko 3,71–5,53), weniger ausgeprägt und selten für Silodosin oder Tamsulosin, die eine hohe Selektivität für α1A-Adrenorezeptoren besitzen (1). Alfuzosin und Silodosin Pharmakokinetische Wechselwirkungen können Wirksamkeit und Verträglichkeit der einzelnen α1-Blocker beeinflussen. Alfuzosin und Silodosin werden primär über CYP3A4 abgebaut (4, 5). CYP3A4 ist das prominenteste Isoenzym der CYP-Familie. Es ist für etwa 40 % aller Phase-I-Reaktionen verantwortlich. Modulatoren von CYP3A4 führen zu Änderungen der Konzentrations-Zeit-Profile: CYP3A4-Hemmer erhöhen die Plasmaspiegel und das Risiko für Nebenwirkungen ist erhöht, während CYP3A4-Induktoren die AUC-(Area under the Curve-)Werte erniedrigen und zu einem Wirkungsverlust führen können (6). Die maximale Plasmakonzentration und die AUC von Alfuzosin steigen bei gleichzeitiger Anwendung des hochwirksamen CYP3A4-Hemmers Ketoconazol um das 2,3- beziehungsweise 3,0-Fache (4). Cmax und die Exposition von Silodosin sind durch Ketoconazol um das 3,7- beziehungsweise 3,0-Fache erhöht. Mittelstarke CYP3A4-Hemmer lassen die AUC von Silodosin um 30 % ansteigen (5). Die Fachinformationen empfehlen, starke CYP3A4-Hemmer nur mit Vorsicht anzuwenden (Alfuzosin) oder zu vermeiden (Silodosin). Wechselwirkungen mit moderaten CYP3A4-Hemmern besitzen keine klinische Relevanz (4, 5). Eine Wirkungsabschwächung durch erniedrigte Plasmaspiegel von Alfuzosin und Silodosin ist mög- Foto: Steve Gschmeissner SPL Agentur Focus A ● 18 GRAFIK Inhibitoren von CYP3A4 Grapefruit Indinavir Idelalisib Itraconazol Ketoconazol Lopinavir-Ritonavir Nelfinavir Posaconazol Saquinavir-Ritonavir Ritonavir Telaprevir Verapamil Voriconazol } Induktoren von CYP3A4 CYP3A4 } Bosentan Carbamazepin Efavirenz Johanniskraut Nevirapin Phenobarbital Phenytoin Primidon Rifampicin Auswahl von modulierenden Substanzen (stark wirkende fettgedruckt) mit klinisch relevanter Wirkung auf die Cytochrom-P450-(CYP-)Isoenzyme 2D6 und 3A4 (Stand 06/2016) lich bei Komedikation mit starken CYP3A4-Induktoren wie Carbamazepin (Grafik). Diesbezügliche Hinweise fehlen jedoch in den Fachinformationen. Doxazosin und Terazosin Die aus der Hypertoniebehandlung stammenden Alpha-1-Adrenozeptorantagonisten Doxazosin und Terazosin wirken weniger spezifisch am Blasenhals und können besonders zu Beginn der Therapie zu erheblichem Blutdruckabfall („first dose phenomenon“) führen. In-vitro-Daten deuten darauf hin, dass CYP3A4 auch beim Abbau von Doxazosin von Bedeutung ist (7). Aus diesem Grund wird die Kombination des starken CYP3A4-Hemmers Boceprevir mit Doxazosin nicht empfohlen (8). Terazosin wird umfangreich metabolisiert. Die genauen Mechanismen sind unbekannt, eine Beteiligung von CYP-Isoenzymen ist nicht auszuschließen (9). Die klinischen Konsequenzen für den Menschen sind bei jetzigem Kenntnisstand bei gleichzeitiger Gabe von CYP-Modulatoren schwer abzuschätzen. Tamsulosin Tamsulosin ist die Leitsubstanz der Kassenärztlichen Bundesvereinigung zur Behandlung des BPS. Tamsulosin ist Substrat von CYP3A4. Daneben wird der α1-Blocker über das polymorphe Isoenzym CYP2D6 verstoffwechselt (10). Die größere Bedeutung hat aber der Abbau über CYP3A4, da die Inhibition des CYP3A4-abhängigen Metabolismus zu einem stärkeren Anstieg der AUC führt (11). Die gleichzeitige Anwendung von Ketoconazol erhöht die AUC um das 2,8-Fache. Der starke CYP2D6-Hemmer Paroxetin steigert die Tamsulosin-Exposition um das 1,6-Fache, was als klinisch nicht relevant angesehen wird (10). Tamsulosin sollte mit Vorsicht in Kombination mit starken und moderaten CYP3A4-Inhibitoren gegeben werden. Bei Patienten vom CYP2D6-Poor-Metabolizer-(PM-)Phänotyp sollte der α1-Blocker nicht in Kombination mit starken CYP3A4-Inhibitoren gegeben werden (10). Diese Personen besitzen zwei nicht funktionelle Allele und können kein CYP2D6 bilden. Der Quelle: mediQ-Interaktionsprogramm Amiodaron Atazanavir-Ritonavir Boceprevir Ciprofloxacin Clarithromycin Cobicistat Darunavir-Ritonavir Diltiazem Dronedaron Erythromycin Fluconazol Fluvoxamin Fosamprenavir Metabolismus von CYP2D6-Substraten wie Tamsulosin verläuft extrem langsam (12, 13). Medikamentös können starke CYP2D6-Hemmer wie Bupropion, Fluoxetin und Paroxetin einen vergleichbaren PM-Status bewirken. Das sollte besonders bei Anwendung starker CYP3A4-Hemmer beachtet werden, weil in dieser Situation beide Abbauwege blockiert sind. Für Tamsulosin besteht in den ersten acht Tagen nach Therapiebeginn ein zwar nicht sehr großes, aber signifikant erhöhtes Risiko für eine klinisch bedeutsame Hypotension (14). Erhöhte Plasmaspiegel von Tamsulosin können zu dieser unerwünschten Arzneimittelwirkung beitragen. Eine erniedrigte Tamsulosin-Exposition ist bei Komedikation mit CYP3A4-Induktoren zu beachten. Die Wahrscheinlichkeit einer klinisch relevanten Plasmaspiegelsenkung ist besonders erhöht bei Patienten mit einem CYP2D6-Ultrarapid-Metabolizer(UM-)Phänotyp. Bei diesen Personen werden durch Genamplifikation vermehrt CYP2D6-Enzyme gebildet und die Verstoffwechslung von CYP2D6Substraten ist stark beschleunigt (12). Es gibt große ethnische Unterschiede in der Häufigkeit des Auftretens von CYP2D6-Polymorphismen. 7–10 % der Mitteleuropäer sind langsamer Metabolisierer (PM) und 1–10 % ultraschnelle Metabolisierer (UM). Asiaten haben zu 1–2 % PM-Status, Nordafrikaner und Orientalen zu 10–29 % UM-Status (15). In der täglichen Praxis ist ein Genotyp-/Phänotyp-Screening nicht durchführbar. Reagiert der Patient besonders unter Komedikation mit CYP3A4-Modulatoren unerwartet, sollte auch an die interindividuellen Unterschiede in der Metabolisierungskapazität von CYP2D6 gedacht werden. DOI: 10.3238/PersUro.2016.08.22.04 Holger Petri Fachapotheker für Arzneimittelinformation und Klinische Pharmazie Werner Wicker Klinik, Bad Wildungen-Reinhardshausen Interessenkonflikt: Der Autor erklärt, dass kein Interessenkonflikt vorliegt. @ Literatur im Internet: www.aerzteblatt.de/lit3316 Perspektiven der Urologie und Nephrologie 2016 | Deutsches Ärzteblatt 19 ARZNEIMITTEL-WECHSELWIRKUNGEN ... der Alpha-1-Blocker Bei der symptomatischen Behandlung des benignen Prostatasyndroms spielen neben Phytotherapeutika und dem 5a-Reduktasehemmer Finasterid die selektiven Alpha-1-Adrenozeptorantagonisten (α1-Blocker) eine Rolle. LITERATUR 1. Höfner K, Bach T, Berges R, et al.: S2e-Leitlinie der Deutschen Urologen: konservative und medikamentöse Therapie des benignen Prostatasyndroms. Urologe 2015; 55: 184–94. 2. Cornu JN, Cussenot O, Haab F, Lukacs B: A widespread population study of actual medical management of lower urinary tract symptoms related to benign prostatic hyperplasia across Europe and beyond official clinical guidelines. Eur Urol 2010; 58: 450–6. 3. Oelke M, Martinelli E: Medikamentöse Therapie des benignen Prostatasyndroms. Urologe 2016; 55: 81–96. ® 4. Fachinformation UroXatral . Stand: März 2014. ® 5. Fachinformation Urorec . Stand: Februar 2015. 6. Böhm R, Reinecke K, Haen E, et al.: Interaktionen mit CYP3A4. Dtsch Apo Ztg 2012; 152: 4840–9. ® 7. Prescribing information Cardura XL . Stand: Juni 2015. ® 8. Fachinformation Victrelis . Stand: Februar 2015. 9. Oh EY, Bae SK, Kwon JW, et al.: Pharmacokinetic and pharmacodynamic consequences of inhibition of terazosin metabolism via CYP3A1 and/or 3A2 by DA-8159, an erectogenic, in rats. Br J Pharmaco 2007; 151: 24–34. ® 10. Fachinformation Alna . Stand: Dezember 2013. 11. Troost J, Tatami S, Tsuda Y, et al.: Effects of strong CYP2D6 and 3A4 inhibitors, paroxetine and ketoconazole, on the pharmacokinetics and cardiovascular safety of tamsulosin. Br J Clin Pharmacol 2011; 72: 247–56. 12. Reinecke K, Böhm R, Haen E, et al.: Arzneimittel und CYP2D6. Dtsch Apo Ztg 2012; 152: 5762–8. 13. Choi CK, Bae JW, Jang CG, et al.: Tamsulosin exposure is significantly increased by the CYP2D6*10/*10 genotype. J Clin Pharmacol 2012; 52: 1934–8. 14. AMB: Benigne Prostatahyperplasie: Bei Beginn der Behandlung mit Alphablockern kann es zu starkem Blutdruckabfall kommen. Arzneimittelbrief 2014; 48: 22. 15. Benkert O, Hippius H, et al.: Kompendium der Psychiatrischen Pharmakotherapie, 10. Aufl. Heidelberg: Springer Medizin 2014. 3 Perspektiven der Urologie und Nephrologie 2016 | Deutsches Ärzteblatt