13 Aufbau der Materie Teil I
Werbung

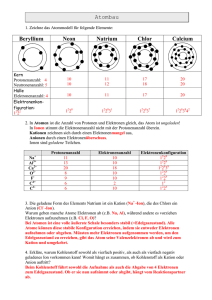
LZ F13.5 /B13.5 Physik des Aufbaus der Materie Inhaltsverzeichnis 13 Physik des Aufbaus der Materie 13.1 Physik der Atomhülle 13.1.1 Das Atommodell von Rutherford – Streuversuch 13.1.2 Bohrsches Atommodell 13.1.2.1 Postulate 13.1.2.2 Energiestufen des Wasserstoffatoms 13.1.2.3 Rydberg-Konstanten 13.1.2.4 Die Spektralserien des Wasserstoffatom 13.1.2.5 Erweiterung auf andere Einelektronensysteme 13.1.3 Franck-Hertz-Versuch 13.1.4 Quantenhafte Absorption und Emission 13.1.5 Röntgenstrahlung 13.2 Physik der Atomkerne 13.2.1 Kernaufbau und -zerfall 13.2.2 Die α-, β- und γ-Strahlung 13.2.2.1 Die α-Strahlung 13.2.2.2 Die β-Strahlung 13.2.2.3 Die γ-Strahlung 13.2.2.4 Eigenschaften radioaktiver Strahlung 13.2.2.5 Zerfallsreihen 13.2.3 Künstliche Kernumwandlungen und Energiebilanzen 13.2.4 Kernspaltung und –fusion 13.2.5 Das Zerfallsgesetz, Halbwertszeit und Aktivität 13.2.6 Nachweisgeräte 13.2.6.1 Ionisationskammer 13.2.6.2 Geiger-Müller-Zählrohr 13.2.6.3 Nebelkammer 13.2.7 Wechselwirkung von Strahlung mit Materie 13.2.7.1 Absorptionsgesetz 13.2.7.2 Dosimetrie und biologische Wirkung ENDE ........... ........... ........... ........... ........... ........... ........... ........... ........... ........... ........... ........... 1 1 1 2 2 3 6 7 10 12 14 16 Folie 1 Folie 2 Folie 3 Folie 4 Folie 5 Folie 6 Folie 7 Folie 8 Folie 9 Folie 10 Folie 11 Folie 12 Folie 13 Folie 14 Folie 15 Folie 16 Folie 17 Folie 18 Folie 19 Folie 20 Folie 21 Folie 22 Folie 23 Folie 24 Folie 25 Folie 26 Folie 27 Folie 28 Folie 29 Folie 30 LZ F13.5 /B13.5 Physik des Aufbaus der Materie Folienverzeichnis Atommodell 1 Atommodell 2 Streuversuch von Rutherford Größenverhältnisse am Atom Größen von Atomen Energieniveauschema des Wasserstoffatoms Lymann - Serie Balmer - Serie Wasserstoff - Termschema Bohrsches Atommodell Natrium-Termschema Franck-Hertz-Versuch - Versuchsaufbau Die Frauenhoferschen Linien Quantenhafte Absorption/ Emission von Licht Gesetz von Moseley – Untersuchung der Kα–Linien verschiedener Atome Gesetz von Moseley Röntgenspektrum Drehkristallmethode Nuklidkarte - gesamt Nuklidkarte Teil 1 Nuklidkarte Teil 2 Mittlere Bindungsenergie pro Nukleon Stabilität der Atomkerne C-14 Methode Ionisationskammer Geiger-Müller Zählrohr Geiger-Müller Zählrohr LZ F13.5 /B13.5 Physik des Aufbaus der Materie 1 13 Physik des Aufbaus der Materie 13.1 Physik der Atomhülle 13.1.1 Das Atommodell von Rutherford1 - Streuversuch Versuchsanordnung und –durchführung: Ein radioaktives Präparat (Radium) mit Bleimantel zur Abschirmung sendet einen α-Teilchenstrahl aus. Dieser trifft um Punkt auf eine Goldfolie . Der Teilchenstrahl durchdringt die Folie und wird nur teilweise gestreut/reflektiert. Auf einem Leuchtschirm bzw. Fotografieschirm wird der Teilchenstrahl registriert. (Animation: http://groups.uni-paderborn.de/cc/arbeitsgebiete/rutherford/video/makro_12.avi) Ergebnis: Die meisten α-Teilchen durchdringen die Folie ohne wesentliche Ablenkung, nur wenige erfahren eine starke Richtungsänderung und sogar Rückstreuung. (Animation: http://groups.uni-paderborn.de/cc/arbeitsgebiete/rutherford/video/mikro_12.avi) Aussagen des Modells 1. Atome haben einen Durchmesser von ca. 10-10 m in deren Zentrum der Atomkern mit einem Durchmesser von 10-14 m nahezu die gesamte Masse konzentriert 2. Der Atomkern ist positiv geladen. 3. Die Elektronen der Atomhülle sind negativ geladen. Problem - Stabilität des Atoms 1. Elektronen können auf jeder möglichen Bahn um den Atomkern kreisen. (vgl. Planeten) – Emissions- und Absorptionsspektren nicht erklärbar 2. Bewegte Ladungen geben (analog Dipolschwingung) Energie in Form von elektromagnetischer Strahlung ab – Folge: stetige Annäherung an Atomkern 1 Ernest Rutherford, 1871 – 1937, neuseeländischer Physiker, 1908 Nobelpreis Chemie LZ F13.5 /B13.5 Physik des Aufbaus der Materie 2 13.1.2 Bohrsches2 Atommodell 13.1.2.1 Postulate3 Bohr ergänzte das Rutherfordsche Atommodell durch Annahmen, die später durch 2 Postulate formuliert wurden. 1. Postulat - Quantenbedingung: Der Bahndrehimpuls L = r · me · v nimmt nur Vielfache von h ( n = 1, 2, ...) 2π 2 π rn me v = n h Ln bzw. h an: 2π FS S. 86 rn – Radius der n-ten Elektronenbahn v – Bahngeschwindigkeit Die Elektronen bewegen sich strahlungsfrei. n ist die Quantenzahl, die die Bahn bestimmt. In atomaren Dimensionen hat allein die wellenmechanische Auffassung Gültigkeit. Das Elektron umläuft den Atomkern in Form einer Welle mit der Wellenlänge h h λ.Einstationärer Zustand p me v ergibt sich nur dann, wenn der Kreisumfang u = 2πr ein ganzzahliges Vielfaches der de-Broglie-Wellenlänge des Elektrons ist. Es gilt: 2. nλ (aus Fendt Appletu1999) 2 πr nh 2 πrm e v nh mev Postulat - Frequenzbedingung: Elektronen geben beim Übergang von einer Bahn hoher Energie Em zu einer Bahn niedriger Energie En Energie in Form eines Photons ab, bzw. umgekehrt wird ein Photon aufgenommen: ΔE = En – Em = h·f FS S. 86 Mängel des Bohrschen Atommodells - Anwendbarkeit beschränkt auf - Bewegung in einer Ebene – Widerspruch zur Kugelsymmetrie der kinetischen Gastheorie - können (Alkalimetalle) Fälle, die auf Einelektronensysteme reduziert werden richtige Energieniveaus, aber falscher Elektronendrehimpuls Elektronen als Punktmassen mit vorgeschriebenen Bahnen und genau angebbarer Geschwindigkeit (Widerspruch zur Quantenmechanik vmin = 7,3·106ms-1) ... Die Bohrschen Postulate sind willkürliche Annahmen, die es ermöglichen, Spektrallinien vorauszuberechnen. 2 3 Niels Henrik David Bohr, 1885 – 1962, dänischer Physiker, 1922 Nobelpreis Physik Ein Postulat (lat.: postulatum = „Forderung“) ist eine plausibel erscheinende These, ohne Beweis. LZ F13.5 /B13.5 Physik des Aufbaus der Materie 3 13.1.2.2 Energiestufen des Wasserstoffatoms Für die Gesamtenergie auf der Bahn gilt En = Epot,n + Ekin,n Potentielle Energie: E pot, n 1 Q1Q 2 4 πε 0 rn E pot,n E pot,n Bahngeschwindigkeit vn (Atomkern als ruhend im Mittelpunkt gedacht: mKern→∞) FZ FC mit Q1 = – Q2 = – e m e v 2n e2 rn 4 πε 0 rn2 e2 2 rn m e v n 4 πε 0 e2 h Lv n mit L n 4 πε 0 2π 2 e v Bahnradius rnn 2 ε 0 hn e2 e 2 πme 4 πε 0 ε 0 h 2 n 2 me e4 4 ε 02 h 2 n 2 Kinetische Energie e2 e2 mit v n 4 πε 0 2 ε 0 hn 4 2 e e rn m e 2 2 2 4 ε0h n 4 πε 0 ε h2 2 rn 2 0 n e πme rn m e v 2n me 2 vn 2 me e4 2 4 ε 02 h 2 n 2 m ee 4 2 2 2 8 ε0h n E kin, n E kin, n Gesamtenergie En E n E kin,n E pot, n me e4 me e 4 8 ε 02 h 2n 2 4 ε 02 h 2 n 2 m e4 2 m e4 2 e 2 2 2 e2 2 8ε0h n 8ε0h n En me e 4 1 8 ε 02 h 2 n 2 FS S. 87 Zusammenfassung: Für den Grundzustand (n = 1) ergeben sich r1 = 5,29·10-11m der Bohrsche Radius. Es gilt rn = r1 · n2. 1 n2 rn und En hängen damit nur von Naturkonstanten und der Quantenzahl n ab. E1 = -2,18·10-18 J = -13,6 eV. Es gilt E n 13,6eV LZ F13.5 /B13.5 Physik des Aufbaus der Materie 4 Gesamtenergien für verschiedene Quantenzahlen - Energiestufen Mit E n 13,6eV 1 ergeben sich für n2 verschiedene Quantenzahlen die verschiedenen Energiestufen des Wasserstoffatoms. 1 13,6 eV 12 1 E 2 13,6 eV 2 3,4 eV 2 1 E3 13,6 eV 2 1,51eV 3 1 E 4 13,6 eV 2 0,85 eV 4 1 E5 13,6eV 2 0,544 eV 5 ... E 0 E1 13,6 eV n→∞ n=4 n=3 freie Elektronen gebundene Elektronen n=2 n=1 Damit können Elektronen und Aufnahme/Abgabe von bestimmten Energiemengen auf verschiedene Energiestufen (mit den Quantenzahlen n oder m) „springen“. z.B. von m = 2 auf n = 3: ΔE = E3 – E2 = –1,51 eV – (–3,4 eV) = 1,89 eV Ionisierungsenergie Wird eine Elektron aus dem Zustand mit der Quantenzahl n auf den Energiezustand mit n → ∞ gehoben, so wird das Elektron vom Kern gelöst, das Atom wird ionisiert (vgl. Photoeffekt). Die Ionisierungsenergie des Wasserstoffatoms (aus dem Grundzustand) beträgt Ei = 13,6 eV. In dieser Größenordnung liegen auch die Ionisierungsenergien anderer Atome. LZ F13.5 /B13.5 Physik des Aufbaus der Materie AP 2004/I 5 LZ F13.5 /B13.5 Physik des Aufbaus der Materie 6 13.1.2.3 Rydberg4-Konstanten Rydberg-Konstante5 R∞ für Einelektronensysteme Für die Energie eines emittierten Photons ergibt sich entsprechend dem 2. Bohrschen Postulat folgender Zusammenhang: me e 4 1 m ee 4 1 m ee 4 1 1 ΔE 2 2 2 2 2 2 2 2 2 2 8 ε0h n 8 ε0h m 8 ε0h m n und mit ΔE hf h f c0 λ mee 4 1 1 2 2 2 3 8 ε0h m n bzw. 1 m e4 1 1 2e 3 2 2 λ 8 ε 0 h c0 m n mit c 0 λf me e 4 R mit 8 ε 02 h 3c0 FS S. 87 Rydberg-Konstante R∞ = 1,0973731568527 ·107 m-1 mee4 R R c 3,2898 1015 Hz . f 0 Nicht zu verwechseln ist diese mit der Rydberg-Frequenz 2 3 8 ε0h Modifizierte Rydberg-Konstante R Die bisherigen Formeln und deren Herleitungen betrachten den Atomkern als ruhend im Zentrum - Atomkern mit unendlich großer Masse. Da aber der Atomkern und das Elektron (wie auch Erde und Mond) um einen gemeinsamen Schwerpunkt kreisen, muss eine Korrektur vorgenommen werden - die r sogenannte reduzierte Masse r1 m me m 1 e wird eingeführt. mK r2 Für die modifizierte Rydberg-Konstante ergibt sich demnach jeweilige Ruhemasse des Atomkerns ist. R R m 1 e , wobei mK die mK Rydberg-Konstante RH des Wasserstoffatoms Für die Rydberg-Konstante RH des Wasserstoffatoms ergibt sich mit mK = mP: RH = 1,09677583·107 m-1. 4 5 12 Johannes Robert Rydberg, 1854 – 1919, schwedischer Physiker, 1900 genaueste zu ermittelnde Naturkonstante mit einer relativen Standardabweichung von 6,6·10- LZ F13.5 /B13.5 Physik des Aufbaus der Materie 7 13.1.2.4 Die Spektralserien des Wasserstoffatom allgemeine Serienformel des Wasserstoffatoms 1 Die gewonnene Formel für kann auch für das Wasserstoffatom mit der modifizierten λ Rydbergkonstanten RH für das Wasserstoffatom verwendet werden. 1 1 1 RH 2 2 λ m n 1 ... Wellenzahl λ n,m = 1; 2; 3 ...; m > n Damit konnte nun auch die auffälligste Erscheinung, die von Atomen ausgeht – die Ausstrahlung von Licht, gedeutet werden. Zerlegt man dieses Licht durch ein Gitter oder Prisma in seine Bestandteile, so erhält man das für dieses Atom charakteristische Spektrum Das einfachste Spektrum sendet Wasserstoff aus. Balmer6 ist es 1885 gelungen, die Frequenzen der Spektrallinien des Wasserstoffatoms durch die empirische7 Formel 1 1 f R H, f 2 2 m 2 zu beschreiben. bzw. Frequenzen der Balmer-Serie mit RH,f ... Rydberg-Frequenz 1 1 1 RH 2 2 λ m 2 390 400 410 H ζ H ε Hδ 430 Wellenlänge der Balmer-Serie 480 490 Hγ Wellenlänge in nm 650 660 Hβ Hα Später fand man nach Vervollkommnung der Geräte zum spektrographischen Nachweis auch Linienserien im nichtsichtbaren Bereich: Lyman-Serie Paschen-Serie Brackett-Serie Pfund-Serie neu: 6 7 1 λ 1 λ 1 λ 1 λ 1 λ 1 1 RH 2 2 m 1 1 1 RH 2 2 m 3 1 1 RH 2 2 m 4 1 1 RH 2 2 m 5 1 1 RH 2 2 m 6 im ultravioletten Bereich (1906) im infraroten Bereich (1908) im infraroten Bereich (1922) im infraroten Bereich (1924) mit der ersten Linie bei λ = 11,7 μm Johann Jakob Balmer,1825-1898, schweizer Mathematiker und Physiker auf Erfahrung beruhend LZ F13.5 /B13.5 Physik des Aufbaus der Materie 8 Diese Linien gelten nicht nur für die Emission, sondern auch für die Absorption von Licht, das von außen auf das Atom trifft. Stimmt die Energie des Lichtquants mit der Energie überein, die das Atom selbst aussenden kann, so wird die Energie des Lichtquants absorbiert, in dem das Atom aus seinem energieärmsten Zustand n = 1, dem Grundzustand, in einem energiehöheren angeregten Zustand übergeht – Resonanzabsorption. freie Elektronen gebundene Elektronen Emission, Absorption von Lichtquanten Termschema des Wasserstoffatoms LZ F13.5 /B13.5 Physik des Aufbaus der Materie AP 1994/II AP 1992/I AP 2002/II 9 LZ F13.5 /B13.5 Physik des Aufbaus der Materie 13.1.2.5 10 Erweiterung auf andere Einelektronensysteme Ein Atom, das aus einem mehrfach geladenen Kern und einer entsprechenden Anzahl von Elektronen besteht, ist in der Lage, eine größere Anzahl von Spektralserien zu emittieren als das Wasserstoffatom. Diese Spektren sind kompliziert und schwer mit einem Modell zu beschreiben. Mit einfachen Annahmen gelingt es in Einzelfällen diese dennoch zu beschreiben - Einelektronensysteme. Ze2 F Mit el 4 0 r 2 für einen Z-fach geladenen Atomkern folgt für die Frequenzen der 1 1 2 emittierten Spektrallinien f Z R f 2 2 . m n Mit Z = 1 ist diese Beziehung identisch mit der Serienformel für das Wasserstoffatom. Mit Z = 2 erhält man das Spektrum des einfach ionisierten He+-Atoms. Mit höherer Ordnungszahl sind nur noch die Spektren der Alkalimetalle einfach darstellbar. Hier spielt sich die Emission und Absorption im optischen Bereich ohne Beteiligung der niedrigen Niveaus ab, da diese schon voll mit Elektronen besetzt sind. Jedoch sind bei Mehrelektronensystemen aufgrund der vier Quantenzahlen n (Hauptquantenzahl), l (Nebenquantenzahl: l ≤ n-1), m (magnetische Quantenzahl: -l ≤ m ≤ +l) und s (Spinquantenzahl: +1/2 und -1/2) viele Zustände möglich, zwischen denen eine Vielzahl optischer Übergänge auftreten können (bestimmte Auswahlregeln, auf die hier nicht eingegangen wird, schließen einige Übergänge aus – Beispiele gestrichelt gezeichnet). Auch ist die Kernladungszahl Z durch die effektive Kernladungszahl Zeff zu ersetzen, da nicht alle Elektronen vom Atomkern gleich stark angezogen werden. Die bekannteste Linie im dargestellten Energieniveauschema ist die Natrium-D-Linie (λ ≈ 589nm), die eine gelbe Färbung der Flamme hervorruft, wenn man Kochsalz hineinstreut. Bei genügend hoher Auflösung des Spektrometers ist diese als Dublett – zwei eng benachbarte Linien - zu sehen. Animation Gasentladung: http://phet.colorado.edu/sims/discharge-lamps/discharge-lamps_de.jnlp LZ F13.5 /B13.5 Physik des Aufbaus der Materie AP 2000/III 11 LZ F13.5 /B13.5 Physik des Aufbaus der Materie 12 13.1.3 Franck-Hertz8-Versuch Aufbau und Funktionsweise einer Vakuum-Triode Glühkatode Vakuum-Röhre Gitteranode UH Auffangelektrode A IA UA UG Eine Gitterspannung UG regelt den Anodenstrom IA. Einsatzgebiet: Audio-Verstärker Untersuchung der Energieaufnahme von Atomen durch beschleunigte Elektronen Versuchsaufbau: mit HG-Dampf gefüllte Röhre Glühkatode Gitteranode Auffangelektrode UH 6,3V IA A in pA UB 0..60V Versuchsdurchführung: UA 1,5 V In einer mit Quecksilberdampf gefüllten Vakuumröhre ( 200 C ) werden mittels einer Glühkatode Elektronen erzeugt und durch die regelbare Spannung UB zwischen Katode und Gitteranode beschleunigt. Im Anodenstromkreis wird der Anodenstrom IA gemessen. Versuchsergebnis: (vereinfacht) IA 4,9 V 0 8 U1 4,9 V U2 4,9 V UB James Franck, 1882-1964, Gustav Ludwig Hertz, 1887-1975, deutsche Physiker, 1911-1914 LZ F13.5 /B13.5 Physik des Aufbaus der Materie 13 Erklärung: 0..U1: ab U1: ab U2: Durch die Beschleunigungsspannung UB erhalten die Elektronen kinetische Energie und sind in der Lage gegen die Anodenspannung anzulaufen. Je größer die Beschleunigungsspannung UB desto großer ist der messbare Anodenstrom IA. Die Elektronen geben bei einer Spannung über U1 den Energiebetrag ∆E = 4,9eV = 7,85·10-19J an die Quecksilberatome ab. Dies entspricht der Anhebung der HGAtome auf eine bestimmte Anregungsstufe und wird beim Übergang in den Grundzustand durch Anregungsleuchten (λ = 253,6 nm - ultraviolett) wieder ausgestrahlt. Die restliche Energie der Elektronen wird wieder zum Anlaufen gegen die Anodenspannung genutzt und erhöht somit wieder die Anodenstromstärke IA. Die Elektronen können nun mehrmals den Energiebetrag von ∆E = 4,9eV an die Quecksilberatome abgeben, so dass bei Vielfachen von 4,9V ein wiederholtes Absinken der Anodenstromstärke IA zu beobachten ist. (Video Anregungszonen: http://www.leifiphysik.de/web_ph12/versuche/10frankherz/franck_hertz.wmv) (einfache Animation zum Versuch: http://www.leifiphysik.de/web_ph12/versuche/10frankherz/animation.htm) (aufwendige Animation zum Versuch: http://www.thomasunkelbach.de/p/a/fhv/FranckHertz/FranckHertz.html) Anregungszonen der Quecksilberatome durch Stöße der Elektronen verschiedener Energien. Ergebnis: Atome absorbieren Energie nur in bestimmten Beträgen (quantenhafte Absorption), deren Größe charakteristisch für das entsprechende Atom ist. LZ F13.5 /B13.5 Physik des Aufbaus der Materie 14 13.1.4 Quantenhafte Absorption und Emission Quantenhafte Emission von Licht Durch Energiezufuhr kann man die Atome eines Gases zum Leuchten anregen. Dabei wird nur Licht mit für das Atom spezifischen Frequenzen emittiert, d.h. Quanten Energie E = h·f der charakteristischen Quantenhafte Absorption von Licht – Resonanzfluoreszenz Atome absorbieren genau das Licht, das sie bei geeigneter Anregung auch emittieren. Die Fluoreszenz ist eine charakteristische Leuchterscheinung von festen Körpern, Flüssigkeiten oder Gasen nach Bestrahlung mit Licht, Röntgen- oder Korpuskularstrahlen. Die Atome des Fluoreszenzstoffes absorbieren Energiequanten (z.B. Photonen geeigneter Energie) der einfallenden Strahlung, befinden sich also im angeregten Zustand. Durch spontane Emission des charakteristischen Fluoreszenzlichtes geben sie diese Energie ab und gelangen so in den Grundzustand. (© Sebastian Stumpf: http://sebastianstumpf.ilo.de/refph2/refph2.html) Versuch: Schickt man durch eine Bunsenflamme Licht einer Na-Dampflampe, so lässt die Flamme das Licht ungehindert durch. Bringt man Kochsalz NaCl in die Bunsenflamme, so sendet sie das charakteristische gelbe Natriumlicht aus und wirft einen kräftigen Schatten. Erklärung: Die Na-Atome in der Flamme absorbieren die Photonen der Na-Dampflampe und emittieren sie anschließend nach allen Richtungen. LZ F13.5 /B13.5 Physik des Aufbaus der Materie 15 Die Fraunhoferschen9 Linien Im Jahre 1814 entdeckte J. Fraunhofer die Absorptionslinien im kontinuierlichen Spektrum des Sonnenlichtes. Wie im Versuch gezeigt wurde, wird das gelbe Licht einer Na-Dampflampe von Na-Dampf absorbiert, d.h. dass man mit Hilfe von den Absorptionslinien im Spektrum des Sonnenlichtes feststellen kann, welche Elemente auf der Sonne vorkommen. Ein Teil von den Ursprungs Linien ist (Absorption Erdatmosphäre), irdischen in während der der größte Teil durch Absorption des Sonnenlichts in der "Chromosphäre" entsteht. A (äußerstes Rot) Terrestrischer Sauerstoff B (Rot) Terrestrischer Sauerstoff C (Rot) Solarer Wasserstoff F (Blau) Solarer Wasserstoff G (Violett) Solares Eisen und solares Calcium H (äußerstes Violett) Solares Calcium D1 (Gelb) Solares Natrium D2 (Gelb) Solares Natrium E (Grün) Solares Eisen Kontrollfragen 1.0 Beim Franck-Hertz-Versuch wird eine mit Quecksilberdampf gefüllte Dreielektrodenröhre verwendet. Diese emittiert ultraviolettes Licht mit der Wellenlänge 254 nm. 1.1 Berechnen Sie die zugehörige Anregungsenergie der Hg-Atome in eV. 1.2 Skizzieren Sie die Versuchsanordnung zum Franck~Hertz-Versuch und benennen Sie die wesentlichen Teile, auch die der Triode. 1.3 Beschreiben Sie die Durchführung des Versuchs sowie sein Ergebnis anhand eines IA(UG)-Diagramms. 1.4 Erklären Sie mit Hilfe des Bohrschen Atommodell den Verlauf der Stromstärkekurve im Diagramm von 1.2. Warum ist der Verlauf mit dem Rutherfordschen Atommodell nicht erklärbar. 1.5 Welche wesentliche Aussage des Bohrschen Atommodells wird durch den Franck-HertzVersuch gestützt ? 9 Fraunhofer, Joseph v., 1787 – 1826, deutscher Physiker LZ F13.5 /B13.5 Physik des Aufbaus der Materie 16 13.1.5 Röntgenstrahlung 10 Erzeugung von Röntgenstrahlung Kühlkopf Lässt man energiereiche Elektronen, die vorher im Vakuum Cu-Anode beschleunigt wurden, auf Materie aufprallen, so entsteht eine elektromagnetische Wellenstrahlung – Röntgenstrahlung bzw. X-Strahlung. UA Röntgenstrahlung Die Intensität dieser Strahlung kann durch die Anzahl der aus der Glühkatode austretenden Elektronen bestimmt werden – Regelung des Heizstromes. Die Härte (Durchdringungsfähigkeit) der Strahlung wird durch die Beschleunigungsspannung, also der kinetischen Energie der Elektronen, bestimmt. UH Rund 5% der kinetischen Energie der Elektronen wird in Strahlung umgesetzt, der Rest wird als Wärmeenergie an die Anode abgegeben. Je nach Erregungsprozess unterscheidet man zwischen der kontinuierlichen Röntgenstrahlung oder Bremsstrahlung und der charakteristischen Röntgenstrahlung oder Eigenstrahlung. Spektrum der Röntgenstrahlung Das kontinuierliche Spektrum Elektronen werden durch den Atomkern infolge der Coulomb-Kräfte abgebremst. Dabei wird die kinetische Energie des Elektrons verringert und diese Energiedifferenz in Form von Strahlung abgegeben: ΔEkin = EQ = h∙f. Die Geschwindigkeit der Elektronen kann zwischen 0 und der Anfangsgeschwindigkeit variieren, so dass ein kontinuierliches Spektrum entsteht. Bei Abbremsung auf v = 0 (ΔEkin,max = Wel) wird eine Höchstfrequenz fG erreicht. Es gilt dann: h∙fG = eUB Conrad Wilhelm Röntgen, 1845 - 1923, deutscher Physiker,1985 – Entdeckung der Röntgenstrahlung 10 LZ F13.5 /B13.5 Physik des Aufbaus der Materie Das charakteristische Spektrum Bei genügend hoher 17 Beschleunigungsspannung entsteht zusätzliche eine Linienstruktur, die für das jeweilige Material charakteristisch ist und der Bremsstrahlung überlagert ist. Diese Linien entstehen, indem die Elektronen der inneren Elektronenschalen durch die aufprallenden energiereichen Elektronen „herausgeschlagen“ werden und Elektronen der äußeren Schalen in diese „Löcher nachrutschen“. Entsprechend der Frequenzbedingung für die einzelnen Übergänge werden diskrete Spektrallinien emittiert. Je nach Elektronenschale auf der der Quantensprung endet, wird die Strahlung mit K, L ... bezeichnet und mit α, β ... von welcher dieser Sprung beginnt. Energieniveauschema zur Entstehung der charakteristischen Kα- und Kβ-Strahlung Spektren bei verschiedenen Beschleunigungsspannungen Bremsspektrum mit charakteristischer Kα- und KβStrahlung einer Molybdän-Anode LZ F13.5 /B13.5 Physik des Aufbaus der Materie 18 Gesetz von Moseley11 für die Kα-Linie Moseley untersuchte mit einer braggschen Anordnung das Röntgenspektrum. Er fand einen Zusammenhang zwischen der das Element bestimmenden Ordnungszahl Z und der Wurzel der f der jeweiligen cha- Frequenz rakteristischen Strahlung: Z ~ f. Für die Kα-Linie stellte er fest, dass eine auftretende Konstante QK stets um 1 kleiner war als die Ordnungszahl Z. Mit QK = Z – 1 ergibt sich: 1 λKα Z 1 3 R 4 QK 1 3 1 1 1 λKα 1 2 3 Z 1 R und mit 1 2 2 4 4 1 2 3 λKα 4 R 4 1 2 3 Z 1 R λKα 4 Gesetz von Moseley für die Kα-Linie Deutung der Formel Die positive Kernladung Z·e wird durch die eine negative Ladung des verbleibenden K-Elektrons teilweise abgeschirmt wird. Die effektive Kernladungszahl Zeff ist dann Z - 1. Die Formel entspricht zudem der Serienformel mit effektiver Kernladungszahl Zeff = Z – 1 für den Übergang von von der L- zur K-Schale aus der bohrschen Theorie, denn 1 λK α Z–1 2 R ∞ 1 12 Weitere Formeln: Kβ-Linie: Lα-Linie: 11 Moseley 1 - 22 ist die Serienformel für n = 1 und m = 2. 1 λK β 1 λ Lα Z–1,8 2 R ∞ Z–7,4 2 R ∞ 1 12 1 - - 1 32 1 22 32 Z–1,8 2 R ∞ Z–1,8 2 R ∞ Moseley, Henry Georges Jeffreys, 1887 – 1915, englischer Physiker, 1914 – Gesetz von LZ F13.5 /B13.5 Physik des Aufbaus der Materie AP 2003/III 19 LZ F13.5 /B13.5 Physik des Aufbaus der Materie 20 Drehkristallmethode – Messung der Wellenlänge durch Interferenz am Kristallgitter (aus http://de.wikipedia.org/wiki/Drehkristallmethode) Die Drehkristallmethode ist ein Analyseverfahren in der Kristallographie zur Bestimmung von Kristallstrukturen auf der Basis von Röntgenbeugung. Sie wurde 1913 entwickelt von William Henry Bragg gemeinsam mit seinem Sohn William Lawrence Bragg. Ein Kristallgitter wird mit monochromatischer Röntgenstrahlung bestrahlt, wobei der Glanzwinkel α (Winkel zwischen Oberfläche und Strahl, im Gegensatz zum Einfallswinkel = Winkel zwischen Strahl und Einfallslot) von 0° aus gesteigert wird. Die Impulsrate wird jeweils unter dem Winkel 2α durch ein Geiger-Müller-Zählrohr gemessen, da am Kristall Reflexion nach dem Reflexionsgesetz auftritt (Huygenssches Prinzip). Bei den Winkeln, die der BraggGleichung genügen, tritt konstruktive Interferenz auf: Hier ist der Gangunterschied zwischen den jeweils an der ersten bzw. zweiten Strahlen Netzebene ein reflektieren ganzzahliges Vielfaches der Wellenlänge, die Impulsrate hat dort also ein lokales Maximum. Aus der Bragg-Gleichung lassen sich bei bekannter Wellenlänge der Röntgenstrahlung die Netzebenenabstände berechnen. Daraus kann man auf die Struktur des jeweiligen Kristalls schließen. LZ F13.5 /B13.5 Physik des Aufbaus der Materie AP 2006/II AP 2000/III 21