12 Elektrophile Addition +
Werbung
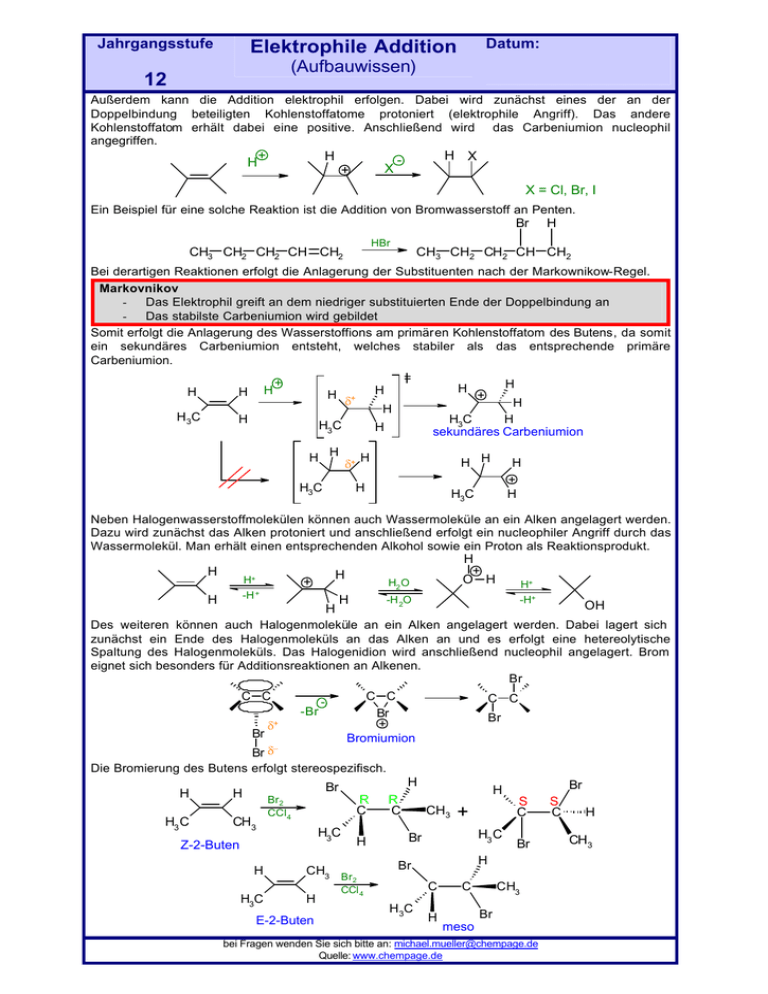
Jahrgangsstufe Datum: Elektrophile Addition (Aufbauwissen) 12 Außerdem kann die Addition elektrophil erfolgen. Dabei wird zunächst eines der an der Doppelbindung beteiligten Kohlenstoffatome protoniert (elektrophile Angriff). Das andere Kohlenstoffatom erhält dabei eine positive. Anschließend wird das Carbeniumion nucleophil angegriffen. H + H X + H X - X = Cl, Br, I Ein Beispiel für eine solche Reaktion ist die Addition von Bromwasserstoff an Penten. Br HBr CH3 CH2 CH2 CH CH2 H CH3 CH2 CH2 CH CH2 Bei derartigen Reaktionen erfolgt die Anlagerung der Substituenten nach der Markownikow-Regel. Markovnikov Das Elektrophil greift an dem niedriger substituierten Ende der Doppelbindung an Das stabilste Carbeniumion wird gebildet Somit erfolgt die Anlagerung des Wasserstoffions am primären Kohlenstoffatom des Butens, da somit ein sekundäres Carbeniumion entsteht, welches stabiler als das entsprechende primäre Carbeniumion. H H H 3C H H = + H δ+ H H δ+ H3C H + H H3C H sekundäres Carbeniumion H H3C H H H H H H H H + H H3C Neben Halogenwasserstoffmolekülen können auch Wassermoleküle an ein Alken angelagert werden. Dazu wird zunächst das Alken protoniert und anschließend erfolgt ein nucleophiler Angriff durch das Wassermolekül. Man erhält einen entsprechenden Alkohol sowie ein Proton als Reaktionsprodukt. H H+ -H + H H + H H + O H H2 O H H+ -H+ -H 2O OH Des weiteren können auch Halogenmoleküle an ein Alken angelagert werden. Dabei lagert sich zunächst ein Ende des Halogenmoleküls an das Alken an und es erfolgt eine hetereolytische Spaltung des Halogenmoleküls. Das Halogenidion wird anschließend nucleophil angelagert. Brom eignet sich besonders für Additionsreaktionen an Alkenen. Br C C Br δ+ -Br C C Br + Bromiumion - C C Br Br δ Die Bromierung des Butens erfolgt stereospezifisch. − H H3 C H Br H CH3 R C Br2 CCl4 H3C Z-2-Buten H H3C H CH3 Br 2 H E-2-Buten R C CH3 H3 C Br H Br C H 3C S C + Br CCl 4 Br H H C CH3 Br meso bei Fragen wenden Sie sich bitte an: [email protected] Quelle: www.chempage.de S C H CH3
![6.3.1 1-Oxa-spiro[2.5]octan - Institut für Organische Chemie](http://s1.studylibde.com/store/data/001356875_1-96e669e5c88ad586db9f9f199d424d05-300x300.png)